三种抗菌药物微生物限度检查方法学验证研究
蒋天逖,曹聪聪
(长沙医学院,湖南长沙 410219)
对于非规定灭菌制剂及其原料、辅料的微生物污染程度的检查,《中国药典》制定了微生物限度检查法[1],主要检查项目有需氧菌总数、霉菌数和酵母菌总数及控制菌(指药品中特定的菌体)检查[2]。药品微生物限度检查的主要目的是通过微生物数量的定量检测以准确反映药品侵蚀程度,继而确定样品微生物具体含量[3]。
微生物在日常生活中不可或缺,可参与大自然循环,分解有机物,产生代谢产物,其中部分代谢产物会导致人畜疾病、食物腐败或霉烂等,具有分布广、种类多、繁殖快的特点[4]。在药品中,可造成药物污染的微生物种类繁多,如生活中随处可见的细菌、酵母菌和霉菌,其中绝大部分是致病菌。由于药物在生产过程中原料、辅料和生产工艺的差异,不同种类药物受到微生物污染程度也不尽相同。而药品在生产过程中受污染的微生物越多,其变质越快,有效期越短,甚至将导致服药者产生发热、感染、中毒、过敏等不良反应,从而造成各种临床疾病的可能性就越多[5-6]。
研究表明,导致药物活性降低的原因一般有两种:(1)部分微生物存在于药品中,继而导致部分药品效果缺失或完全丧失;(2)样品存储年限较久而导致其部分失效[7-8]。因此,药品生产、流通、储存等环节均需严格遵循相应的质量把控、管理规范,从而最大限度降低药品受到微生物污染的风险及污染程度。为实现上述目标,验证不同抗菌药物的微生物限度检查方法有效性,改善相关检测技术也非常必要。
1 材料与方法
1.1 仪器与试剂
BSC-1500IIA2 生物安全柜,上海中庸检验设备有限公司;SW-CJ-2D 超净工作台,苏州净化设备有限公司;HTY 无菌隔离器,浙江泰林生物技术股份有限公司;HR 封闭式/开放式两用无菌检查薄膜过滤器,北京恒瑞天创机电设备有限公司;标准型PH 计PB-10/C,上海精密科学仪器有限公司;移液枪,上海精密科学仪器有限公司;FC104 电子天平,上海民桥精密科学仪器有限公司;智能高压蒸汽灭菌器,艾德生仪器有限公司;25℃SPX-250B-Z 型生化培养箱、35℃SPX-250B-Z 型生化培养箱,上海博讯实业有限公司医疗设备厂;匀浆仪,杭州高得医疗器械有限公司。
大肠埃希菌(Escherichiacoli)[CMCC(B)44102]、金黄色葡萄球菌(Staphylococcusaureus)[CMCC(B)26003]、白色念珠菌(Candidaalbicans)[CMCC(F)98001],0.5 ~1.0×103cfu/颗,中国食品药品检定研究院。营养琼脂培养基、玫瑰红钠琼脂培养基、BL增菌培养基、沙氏培养基,中国药品生物制品检定所;培养基所用蛋白胨、氯化钠等其他试剂均由广东翁江化学试剂有限公司提供。盐酸莫西沙星(批号:180304)、诺氟沙星(批号:180210)、阿奇霉素(批号:180401),湖南迪诺制药有限公司。
1.2 实验方法
1.2.1 冲洗剂制备
配置0.9%氯化钠溶液和0.1%蛋白胨氯化钠缓冲液,高压灭菌后备用。
1.2.2 菌液制备
取两种新鲜培养物(金黄色葡萄球菌、大肠埃希氏菌)同时分别接种到营养肉汤培养基,而后取白色念珠菌新鲜培养物接种到沙氏液体培养基,按《中国药典》描述的具体方法,将其制备成50 ~100 个/mL水平,分为一式三份待用。
1.2.3 供试液制备
取10 g 药物样品到100 mL 无菌氯化钠溶液(浓度0.9%),制成供试液(1 ∶10),若存在不溶性颗粒,则可500 r/min 离心处理5 min,而后取上层液体,确保供试液均匀。
1.2.4 试验方法
1.2.4.1 平皿菌落计数法(平皿法)
采用常规平皿倾注法进行试验。分别取1 ∶10的供试品溶液9.9 mL,加入试验菌液各0.1 mL,充分混匀后吸取混合溶液1 mL 至无菌平皿中,倾注胰酪胨大豆琼脂培养基,先后经过混匀、凝固等操作步骤,平行制备2 组。将大肠埃希氏菌、金黄色葡萄球菌在30~35 ℃培养3 d,白色念珠菌在30~35 ℃培养5 d。计数,计算各组的平均菌落数。
1.2.4.2 洗脱法
取供试液使用直径为50 mm、孔径0.45 μm 的滤膜进行减压抽滤,而后取出滤膜使用100 mL灭菌生理盐水缓慢流动冲洗,总用量不超过1 000 mL。取1 mL冲洗液放入双碟中,先后加入等量的营养琼脂和玫瑰红钠琼脂培养基,并先后在35 ℃培养48 h、27 ℃培养72 h 后取出计算菌数。
1.2.4.3 薄膜过滤法(薄膜法)
分别取1 ∶10 的供试品溶液1.0 mL 至薄膜过滤器中,用0.7%氯化钠蛋白胨溶液冲洗3 次,每次用量100 mL,在最后一次冲洗前加入0.1 mL 菌液进行过滤,转移滤膜,将细菌表面贴于胰蛋白酶琼脂培养基上,按规定培养计数。
1.2.4.4 回收率测定
分别取前述步骤中制备的菌液,将其稀释至指定浓度(30 ~100 cfu/mL),而后将其加入至供试液中,并取1 mL 溶液进行培养基计数,计算回收率。
1.2.5 数据分析
实验过程中的数据收集整理采用Excel 2010软件。
2 结果与分析
2.1 样品检出情况
使用三种药物重复实验3 次,平皿菌落计数法细菌数、洗脱法细菌数、薄膜过滤法细菌数具体见表1。可以看到,3 种药物供试样品中薄膜过滤法检出细菌数均最多。
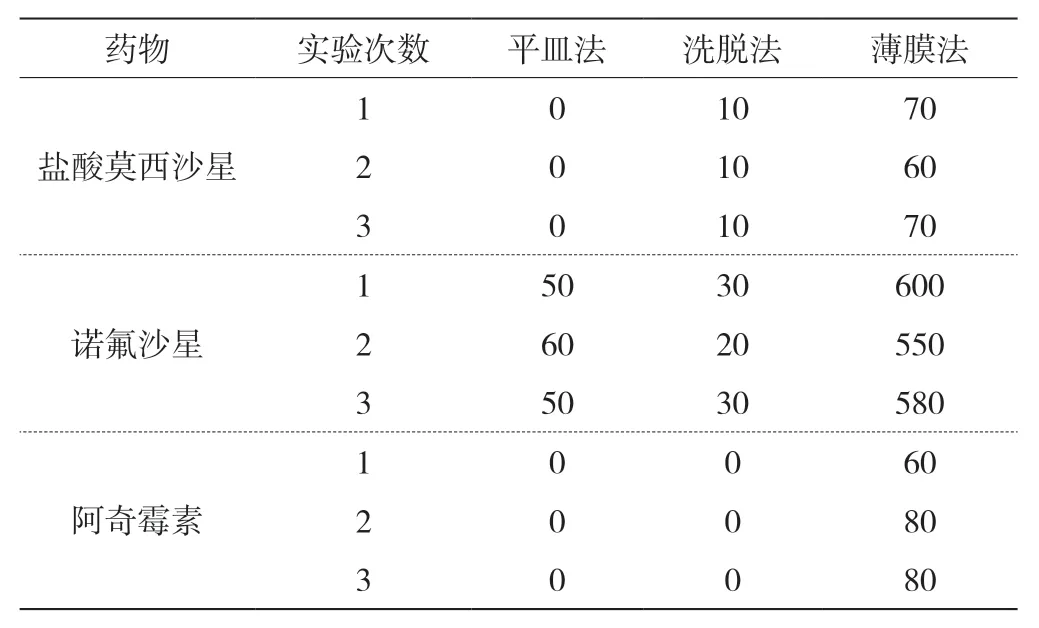
表1 三种方法样品检出细菌数(单位:个/g)
2.2 回收率
如表2 所示,3 种药物使用薄膜过滤法检测细菌回收率均最高,盐酸莫西沙星中金黄色葡萄球菌、大肠埃希氏菌和白色念珠菌的回收率分别为78.00%、81.25%、75.38%,诺氟沙星中的回收率分别为70.00%、72.50%、84.62%,阿奇霉素中的回收率分别为72.00%、75.00%、80.00%。

表2 三种验证方法对菌种的回收率
2.3 讨论
需氧菌总数、霉菌数、酵母菌总数及控制菌(指药品中特定的菌体)等是非规定的灭菌制剂(及其原料)、辅料等药品组分中微生物存在情况及具体污染程度的主要检查项目。本试验研究中采取薄膜过滤法检查盐酸莫西沙星、阿奇霉素和诺氟沙星的需氧菌总数、控制菌(大肠埃希菌)总数和盐酸莫西沙星的霉菌数,所得结果均符合《中国药典》规定。三种抗菌药物微生物限度检查结果比较,莫西沙星的抑菌活性强于其余两者,通过不同稀释级供试液和不同检查方法得出薄膜过滤法适用于盐酸莫西沙星、阿奇霉素和诺氟沙星的微生物限度检查[9]。
本研究发现薄膜法样品中菌数测定结果和回收率显著高于平皿法和洗脱法,可能与以下原因有关。(1)平皿菌落计数法是将供试液按照设定程度予以稀释后直接接种于平皿并进行菌数测定的方法,虽然稀释剂和培养基会对抗菌药物中的抑菌成分进行稀释,其抑菌能力有所降低,但是不至于完全消失,因此会影响细菌的生长过程,同时降低其检出率和回收率。(2)洗脱法的操作过程中细菌会吸附在滤膜表面或镶嵌在纤维膜的间隙中,很难通过冲洗洗脱下来,因此会出现检出率和回收率低。(3)薄膜法在具体操作过程中则会使用稀释液对滤膜进行反复冲洗,该处理方式会极大降低抑菌成分浓度,甚至在微生物限度检查层面会降低原有成分的抑菌效果。需要注意的是,在具体操作过程中,薄膜过滤法必须首先将供试液加入滤罐中,先混匀冲洗液再进行减压抽滤,否则抑菌成分不能彻底去除,将直接影响测定结果[10]。
3 结论
薄膜法在过滤样品过程中,将微生物留在滤膜表面,药品中的抑菌成分则在无菌冲洗液的反复冲洗下有效去除,培养过程中其营养成分和代谢物也可以通过滤膜上的微孔不断进行交换。总的来说,薄膜法不仅能增大取样量,实验结果更具代表性,还可以有效减少外部环境或操作因素的干扰,操作过程更为方便实用,简化了微生物的检测程序,可在相关领域推广应用。

