齐墩果酸盐的选择及理化性质研究
王路,施斌,孙晨,尹民,关凯琳,贺敦伟,*
(1.中国海洋大学 医药学院,山东青岛 266003;2.则正(上海)生物科技有限公司,上海 201807)
处方前研究旨在提供药品研究中所需的必要数据(特别是原辅料和包装材料的物理化学、物理机械力学和生物药剂学特性),这些数据可能会影响处方设计、原料药和药品的生产方法,最终影响产品的药代动力学、生物药剂学特性以及产品的包装稳定性。
在大型制药公司,有许多指导方针和标准来确定化合物的物理化学性质是否良好。在所有重要的物理化学性质中,熔点、分解起始温度、颗粒的形态和粒径、晶癖、结晶度、吸湿性、固体稳定性、溶解度和渗透性是最重要的因素。
为了更好地了解预配方在药物开发中发挥的作用,本研究选择了齐墩果酸(OA)作为候选药物进行物理和化学表征。齐墩果酸广泛存在于多种植物中,OA 及其衍生物具有抗真菌、抗病毒、利尿、降血糖和抗肿瘤以及护肝和抗炎等药理作用[1-4]。根据团队前期观测结果(未发表),在X 射线粉末衍射(XRPD)中原料药表现了较差的结晶性,在差示扫描热量法(DSC)中出现了冷结晶,在热重分析(TGA)中,从环境温度到120 ℃重量损失为1.593%,这可能是由于晶格中的溶剂或者水的损失导致。经动态水蒸气吸附(DVS)试验证实,在相对湿度为95%的条件下,该化合物的吸湿率为4.43%。OA 在pH 值为1 ~6的缓冲液中的溶解度小于0.001 mg/mL,在模拟胃液(SGF)、禁食状态小肠液(FaSSIEF)和饱食状态小肠液(FeSSIF)中的溶解度分别为0.081 mg/mL、0.001 mg/mL 和0.038 mg/mL。在人结直肠腺癌细胞(Caco-2)模型中测得的表观渗透率为1.2×10-6cm/s。油水分配系数(LogP)和药物解离常数(pKa)分别为4.67 和2.52。在临床上使用的剂量是30 ~50 mg。根据溶解度、剂量(40 mg)和渗透率数据,计算出溶解度数(Dn)为1.510 9,剂量数(Do)为4.210 5,渗透性数(An)为1.340 0。根据生物制药分类系统(BCS)的定义,OA 为BCS Ⅱ(高渗透性和低溶解性)化合物。对于这种化合物,溶解度和溶解性可能限制其吸收。此外,在晶型筛选中,OA 可以形成水合物、甲醇溶剂化物、乙醇溶剂化物和异丙醇溶剂化物。根据以上表征结果,发现OA 存在结晶度差、水合物和溶剂化物形成能力强以及溶解度较低等问题。
为了改善OA 的物理化学性质,计划对化合物进行重结晶和成盐反应,并对所有盐的理化性质进行表征;采用Johnson 法和Gastroplus 软件,以渗透性、溶解度、溶出系数、粒径及其logP 和pKa 为输入数据,计算最大吸收剂量(MAD)。
1 材料与方法
1.1 材料
齐墩果酸,纯度99.0%,成都超人植物化工发展有限公司;氢氧化钠(NaOH)、甲乙酮,分析纯,上海润捷化学试剂有限公司;胆碱,分析纯,郑州浩力化工有限公司;氢氧化钾(KOH),85%,美国Alfa Aesar公司;无水哌嗪,99%,美国Alfa Aesar 公司;异丙醇(IPA)、甲醇,色谱级,美国Sigma-Aldrich 公司;乙腈(ACN),色谱级,美国Burdick & Jackson 公司;乙酸乙酯,分析纯,美国Fisher 公司;乙二胺,分析纯,比利时Acros 公司。
Q1000 DSC 仪、Q500 热重分析仪,美国TA 公司;S40K 型pH 计、MX5 电子天平,瑞士Mettler Toledo 公司;水冷ZX98-1 型旋转蒸发仪,上海鲁伊工贸有限公司;SHB-S ⅢA 型循环水式多用真空泵,上海豫康科教仪器设备有限公司;DMLP 偏振光显微镜,德国Leica 公司;labquaker 三维旋转振荡器,美国Thermo Scientific 公司;1200 高效液相色谱(配备DAD 检测器)、XDB-d C18色谱柱(4.6 mm×150 mm,粒径 5μm),美国Agilent 公司。
1.2 OA 的重结晶
称量99.1 mg 齐墩果酸至20 mL 容量瓶中,加入4.0 mL 水饱和乙酸乙酯。将样品在大约55 ℃下搅拌,缓慢加入7 mL 乙腈作为反溶剂直至昙点。样品慢慢冷却至大约25 ℃后,通过真空过滤将固体分离,在真空干燥箱中45 ℃干燥过夜,收率为74.97%。其中,收率=目的产物实际生成量/目的产物理论生成量×100%=生成目的产物的原料量/原料进料量×100%(下同)。
1.3 OA 盐的合成
取5 个20 mL 容量瓶,分别加入169.2 mg、115.0 mg、112.1 mg、114.8 mg、210.9 mg 重结晶齐墩果酸,然后分别加入5.885 mL 甲乙酮、4.000 mL 甲乙酮、4.000 mL异丙醇、3.000 mL 水饱和乙酸乙酯、8.000 mL 异丙醇。将5 份样品在55 ℃下搅拌,分别加入370 μL 的1 mol/L NaOH水溶液、250 μL的1 mol/L KOH水溶液、1 000 μL 的0.25 mol/L 哌嗪甲醇溶液、500 μL 的0.25 mol/L 乙二胺甲醇溶液、460 μL 的1mol/L 胆碱水溶液。晶体逐渐析出形成悬浮液,将5 份样品55 ℃继续搅拌3 h,然后慢慢冷却到25 ℃。通过真空过滤分离固体,并在真空干燥箱中45 ℃干燥过夜,分别得到OA 的钠盐、钾盐、哌嗪盐、乙二胺盐、胆碱盐,收率依次为85.22%、87.74%、76.40%、45.52%、81.24%。
1.4 结构表征
1.4.1 X 射线粉末衍射(XRPD)分析
工作电压:40 kV;工作电流强度:40 mA;检测器:LynxEye 检测器;扫描角度(2θ):4°~40°;步长值为0.05°;扫描速度为0.05°/s;分析软件:MDI Jade 软件。
1.4.2 偏光显微镜
显微照片通过佳能Power Shot S80 数码相机连接偏振光显微镜获得,其中目镜放大10 倍,物镜放大20 倍。粒径用徕卡有限公司的测微尺(每格10 μm)测量。
1.5 理化性质表征
1.5.1 DSC/TGA 分析
(1)差示扫描量热:样品(2 ~3 mg)在非密封铝锅中以5 ℃/min 的速率从25 ℃加热到300 ℃。(2)热重分析:样品(约10 mg)在开放式铝盘中以5 ℃/min 的速率从25 ℃加热到300 ℃,氮气流速为60 mL/min。
1.5.2 溶解度测定
在25 ℃下测定化合物在SGF、FaSSIF 和FeSSIF中的溶解度。过量的活性药用成分(API,2 mg)悬浮在液体(1 mL)中,在三维旋转振荡器上恒温旋转(250 r/min)16 h,样品用0.45 μm 孔径滤膜过滤,并记录滤液/上清液的pH 值。用高效液相色谱法分析滤液浓度。
1.5.3 DVS 分析
水分吸附-解吸等温线采用动态蒸汽吸附仪测定。称取约10 mg 样品在25 ℃下用干燥氮气进行预干燥。相对湿度按照5%/min 的速度由0 升至95%或75%再降回到0%;增重平衡标准:设定每步相对湿度5 min 内达到重量变化率(dm/dt)小于0.01%即为平衡;最长平衡时间:120 min。
1.5.4 水/水-有机相混悬平衡实验
每个10 mL 容量瓶中分别放入约25 mg 的化合物,分别加入400 μL 水、乙酸乙酯-水(体积比97.06 ∶2.94)和异丙醇-水(体积比4 ∶1)溶液。将小瓶密封并在旋转仪上以250 r/min 的转速25 ℃旋转70 h,样品经过干燥后为固体粉末,进行XRD分析。
1.5.5 固体稳定性研究
将样品在40 ℃、50 ℃、70 ℃、40 ℃/75%RH、50 ℃/75%RH 条件下分别存放7 d 和14 d,进行稳定性研究。保存结束后放置于-20 ℃的冰箱中,用高效液相色谱仪进行含量、溶解度测定,以评估化学稳定性。在不同的时间间隔测定DSC 和XRPD 以确定药物的化学和物理稳定性。
1.5.6 色谱条件
进样量10 μL,EZchromElite 软件控制色谱系统。流动相A 为0.025%三氟乙酸乙腈溶液,流动相B 为0.025%三氟乙酸水溶液,流动相组成为A∶B=80∶20。流速为1 mL/min,检测波长为215 nm。
样品制备:精密称定25 mg 样品,置100 mL 容量瓶,加入适量乙醇溶解样品后稀释定容,摇匀后得样品溶液。
1.5.7 最大吸收剂量计算
本研究采用一种相对简单的方法(Johnson 模型)来计算最大吸收剂量,如公式(1)~(3)所示[5-6]。
式中,MAD为最大吸收量,mg;S为pH=6.5(FaSSIE)或5.5(FeSSIE)时的溶解度,mg/mL;Ka为经肠吸收速率常数,min-1;VSIW为小肠水容量,取250 mL;TSIT为小肠转运时间,取270 min;Peff为人体有效渗透率;R为人体小肠半径,取1.5 cm;PCaco-2是Caco-2模型中的表观渗透系数。为对比不同模型的计算差异,另外采用本团队开发的基于生理的药代动力学(BSPK)模型对MAD进行模拟,其中小肠转运时间取值为1 440 min,包括胃排空时间15 min,小肠通过时间200 min,大肠通过时间1 225 min。
2 结果与分析
2.1 重结晶OA 及其盐的结构和基础理化特性
OA 及其盐的结晶形式见表1 和图1 ~图4。对于OA 重结晶样品,此晶型有某种不明晶癖,粒径为10 ~50 μm,从25 ℃升温到127 ℃时失重为0.28%;该晶型在311.51 ℃开始熔化;吸湿性强,在0 ~75%相对湿度范围吸湿增重为0.501 3%,在0 ~95%相对湿度范围吸湿增重为0.601 8%。5 种OA 盐晶体中哌嗪盐吸湿情况较为乐观(低于重结晶样品),因此选择OA 哌嗪盐进行后续表征分析。OA 哌嗪盐从25 ℃升温到187 ℃失重1.469%。在219.35 ℃时出现明显的吸热峰,此时TGA 失重10.23%。在311.90 ℃出现另一个吸热峰,该峰可能是失去哌嗪后的游离OA 熔化产生。
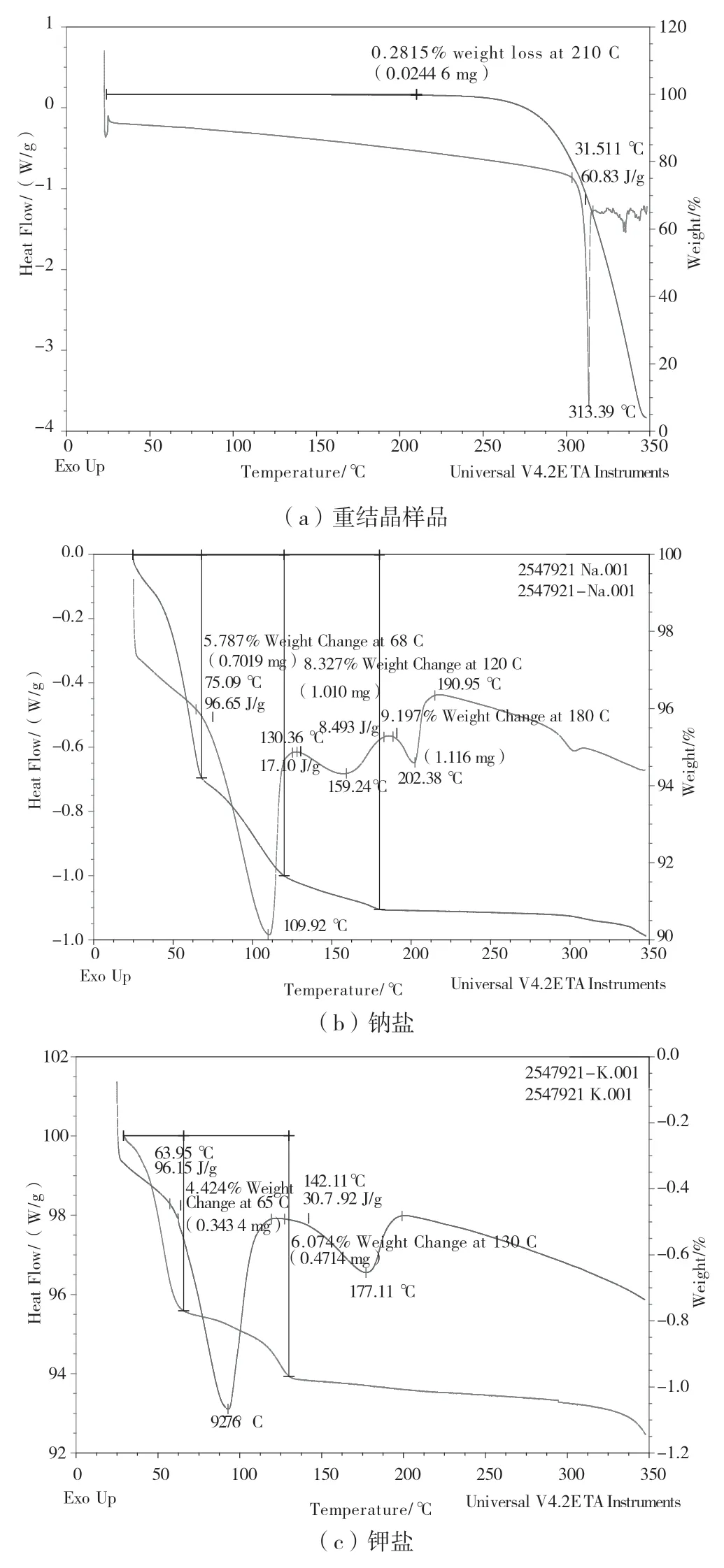
图2 样品的DSC/TGA 热图
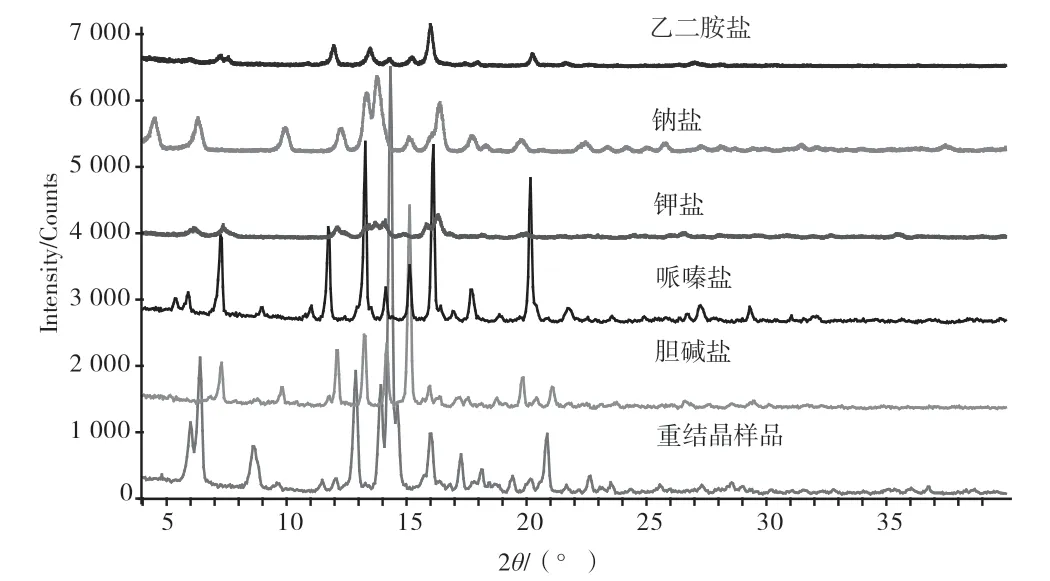
图3 样品的XRPD 图

图4 样品的DVS 等温线
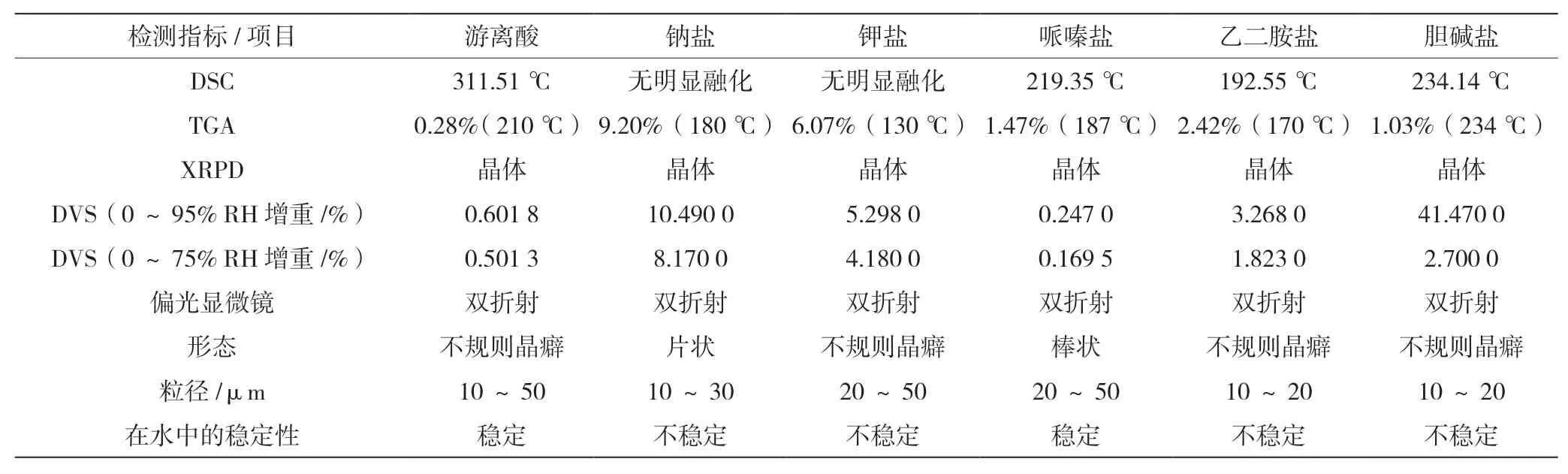
表1 OA 及其盐类的结构和基础理化特性
2.2 溶解度
如图5 所示,OA 在SGF、FaSSIF 中的溶解度很差;虽然是游离酸,但OA 在SGF 中的溶解度高于FaSSIF 和FeSSIF,说明十二烷基硫酸钠的加入比卵磷脂和牛磺胆酸等表面活性剂更能显著提高OA 的溶解度。在SGF 中,OA 钠盐、哌嗪盐、乙二胺盐和胆碱盐的溶解度也有所提高。在FaSSIF 中,OA 钠盐和乙二胺盐的溶解度分别大幅提高了约562 倍和318倍。在FeSSIF 中,OA 钠盐、钾盐、哌嗪盐、乙二胺盐和胆碱盐的溶解度分别提高了16.76、0.37、4.55、4.50、10.97 倍。就溶解度而言,OA 钠盐、OA 胆碱盐是最佳的候选盐型。

图5 OA 哌嗪盐的水/水-有机混合物混悬平衡XRPD 图

图6 OA 不同盐型的溶解度
2.3 OA 哌嗪盐的水/水-有机混合物混悬平衡试验
原始样品和水/水有机混合物浆体样品之间的XRPD 图谱无显著差异,表明该化合物在浆料(83%~100%水活度)中相当稳定,见图5。
2.4 OA 哌嗪盐的固体稳定性
OA 哌嗪盐在所选实验条件下均表现出很好的稳定性(见表2),含量没有明显下降,HPLC 图谱显示有关物质总量没有明显增加,即杂质未明显增加。在极端条件下(包括70℃和50℃/75%RH)暴露的样品的DSC 图也基本没有变化(未展示)。

表2 OA 哌嗪盐的固体稳定性
2.5 OA 哌嗪盐的最大吸收量
采用Johnson 模型和BSPK 模型计算的MAD,如表3 所示。Johnson 模型中,粒径设置为10 μm;扩散常数为0.000 005 cm2/s;当颗粒半径小于30 μm 时,扩散层厚度等于颗粒半径;若颗粒半径不小于30 μm,则扩散层厚度为30 μm;固体药物浓度为1 200 mg/cm3[6]。BSPK 模型中,不考虑颗粒半径范围,固定扩散层厚度等于颗粒半径;其余条件与Johnson 模型一致。
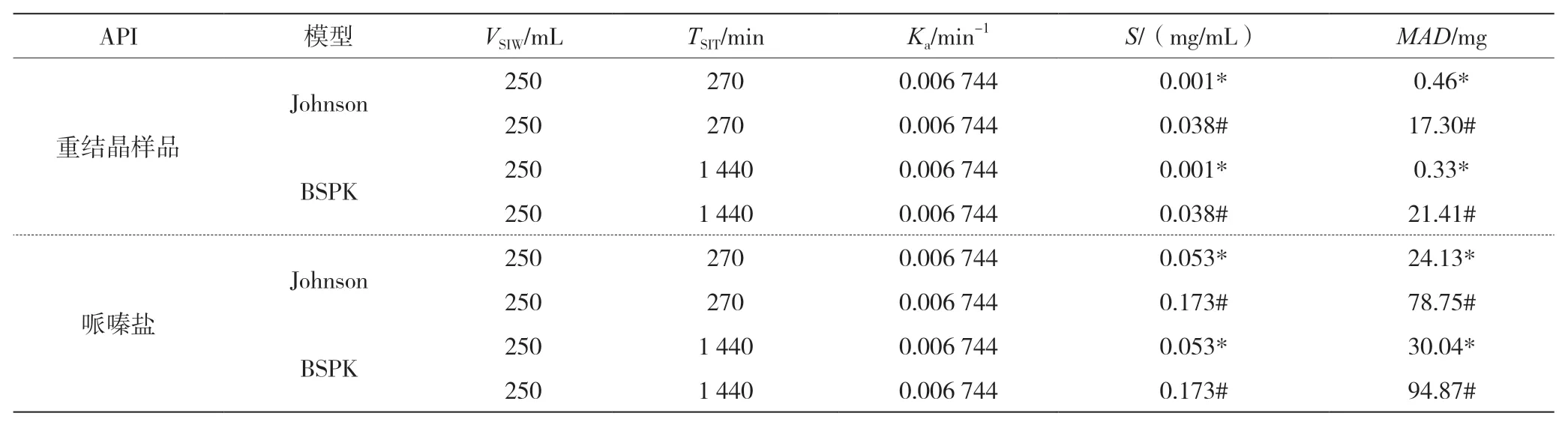
表3 根据临床所需剂量(40 mg)计算MAD
结果表明,Johnson 模型和BSPK 模型计算的禁食状态下的重结晶样品MAD分别为0.46 mg 和0.33 mg,远低于临床给药剂量40 mg。然而,摄食后MAD显著升高,分别达到17.30 mg 和21.41 mg。但该MAD仍不能满足临床平均40 mg 的需求。而OA 哌嗪盐的MAD在Johnson 模型模拟的空腹和饱腹状态下分别达到24.13 mg 和78.75 mg,在BSPK 模型模拟的空腹和饱腹状态下分别达到30.04 mg 和94.87 mg。因此,随着饱腹状态下溶解度的提高,OA 哌嗪盐可应用于临床,40 mg 时吸收率可达91%。
3 结论
本文以OA 为模型药物,合成了钠、钾、哌嗪、乙二胺和胆碱的OA 盐,在五种盐类中,哌嗪盐具有较低的吸水性,在95% RH 环境下,其吸水率为0.247 4%,其他盐类在5%~80% RH 环境下可形成水合物。与游离酸相比,哌嗪盐在SGF、FaSSIF 和FeSSIF 中的溶解度分别提高了6.80 倍、53.00 倍和4.55 倍。在BSPK 模型模拟的饱腹状态下,10 μm 粒径下OA 哌嗪盐的MAD达到94.87 mg。OA 可用于临床使用剂量为40 mg,吸收率高达91%。这为进一步开发OA哌嗪盐的制剂奠定了基础。

