T1-T2双模纳米磁共振造影剂的研究进展
李雅辉,罗怡杰,吴籽萱,姜文沛,李拓欢,曹众
磁共振成像(magnetic resonance imaging,MRI)是利用核磁共振原理,通过收集和分析水分子中氢质子的弛豫信号来对生物体内部结构进行成像的技术。与其他医学成像技术如荧光成像、超声成像、计算机断层扫描、单电子发射计算机断层扫描等相比,MRI 具有许多独特的优势。由于没有电离辐射的危害,且具有无创性,MRI 被认为是一种相对比较安全的检查方法。MRI 信号主要来自于水的氢核,与脂肪、蛋白质等组织中的氢质子信号强度不同,所以磁共振成像具有出色的组织对比度。MRI 设备具备获取任意方向断层的能力,可以获得不同角度和不同断面的信号。此外,磁共振成像不受骨伪影的干扰,可以进行病变部位组织化学、结构、功能方面的研究。因此,MRI 已成为目前临床诊断中最有用的医学成像技术之一。
MRI 有纵向(T1加权)和横向(T2加权)两种弛豫模式,每种成像模式都有其独特的优缺点。例如,T1加权MRI 可以显示正常的软组织解剖结构,具有良好的分辨率,而 T2加权 MRI 对软组织病变的检测则表现出更高的敏感性。此外,MRI 造影剂能够减少水质子的 T1和 T2弛豫时间,进一步提升 MRI 的灵敏度和检测能力,提供更准确的图像。T1造影剂能够产生明亮的 MR 图像,更有利于解剖结构的观察。通常 T1造影剂由金属钆和锰制成,由于它们的离子分别含 7 个和 5 个未配对的电子,使其具有高的电子自旋。Fe3+有 5 个不成对的电子,也使其成为 T1造影剂的潜在候选者[1-2]。T2造影剂主要是铁基材料,如超顺磁性氧化铁纳米颗粒,产生暗的 MR 信号,但灵敏度及特异性更高,能够更好地鉴别良性与恶性肿瘤。其中 Fe3O4纳米颗粒的研究已经较为成熟,科研人员可以通过调节其尺寸、形貌,并利用合金化和外壳包覆等手段来增强氧化铁纳米颗粒的造影效果;镝(Dy3+)和钬(Ho3+)最近也被报道用于超高场强 MRI 的 T2成像,它们具有镧系金属中最大的磁矩以及较短的弛豫时间,在超高场强下也能保持良好的成像性能。尽管 T2造影剂能带来异常强烈的对比度增强效果,但阴性造影可能与 MR 图像中其他因素导致的黑暗区域混淆,这无疑极大地制约了 T2造影剂的应用。
T1成像具有较高的组织分辨率,而 T2成像在检测疾病方面则具有更高的灵敏度[3]。然而,单独使用 T1或 T2造影剂,很难同时获得同一组织区域两种类型的图像。此外,由于脂肪酸、出血、血栓、空气、钙化、金属沉积等因素的干扰,单模 T1或 T2磁共振成像可能会产生伪影,造成歧义,严重限制对病变组织的准确诊断。T1和 T2双模 MRI的结合可以弥补彼此的不足,为了获取更全面、准确的信息,赋予其应用于临床诊断的巨大潜力,需要开发一种 T1-T2双模造影剂,可以在一台仪器上同步收集不同的诊断信息,并实现时空成像的精确匹配。由于结合了两种成像模式的优点,具有 T1-T2双模 MRI 效应的造影剂在提高疾病诊断准确性方面显示出巨大的潜力,引起了相当大的关注。截至目前,已经开发了多种方法来制备 T1-T2双模磁共振成像造影剂。本文将对目前 T1-T2双模磁共振成像造影剂的设计思路和研究进展进行综述。
1 化学合成偶联法
Chou 等[4]采用一锅法合成了具有 T1-T2双模对比度的磁性纳米材料 FeGdPt 纳米颗粒(FeGdPt NPs)。三合金纳米粒子中的 Pt 可以保护 Gd 和 Fe 元素免受氧化。FeGdPt NPs 在体内外同时表现出正负对比度,成功地展示了其在 T1-T2双模成像中的潜力。Li 等[5]通过水热合成的方法制备了一种新型的氧化铁和氧化钆(IO/GdO)纳米复合材料作为 T1-T2双模磁共振造影剂,进一步将肿瘤靶向配体(PDGFB-PEG)连接到 IO/GdO 纳米复合材料表面(PDGFB-pIO/GdO),成功制备了肿瘤靶向 MRI 探针用于原位前列腺癌的准确诊断。Zhu 等[6]通过溶剂热法构建了一种靶向 Fe/Gd 纳米平台(ipGdIO-Dox),用于化疗和铁死亡协同治疗癌症,并且表现出较强的 T1-T2双模 MRI 能力。全身给药 ipGdIO-Dox 可显著增强肿瘤内 T1加权成像(T1W1)和 T2加权成像(T2W1)的信噪比(ΔSNR),进而提高 MR 图像质量,获得更详细的肿瘤病变病理信息。Zhao 等[7]首次报道了聚丙烯酸修饰的可清除的 MnCo2O4纳米点(MnCo2O4@PAA)。由于 Mn 和 Co 的固有磁性,MnCo2O4@PAA 可以作为 T1-T2双模 MRI 造影剂,为诊断和指导治疗提供更全面的信息。Gu 和 Cao 等[8-9]采用电沉积法制备了一维二氧化硅包覆的铁/锰多层纳米线(NWS)。随着 Mn 浓度的增加,T1加权 MR 图像中的信号强度逐渐增强;随着 Fe 浓度的增加,T2加权 MR 信号强度逐渐减弱。Lv 等[10]制备了蜂窝状的 MnO2,并同时负载光敏剂 Ce6 和超小超顺磁性氧化铁(USPIO),构建的USPIO@MnO2@Ce6(UMC)纳米探针具有 pH/H2O2双重响应性,可以实现多模式成像引导的光动力疗法(图1)。

图1 多功能纳米探针 USPIO@MnO2@Ce6 的合成及其在 pH/H2O2 触发多模态成像的指导下自补氧 PDT 抗肿瘤治疗作用机制示意图[10]
2 两种金属元素掺杂法
Wang 等[11]将脱镁叶绿素 a-顺磁性 Mn2+螯合物(P-Mn)(T1造影剂)和超顺磁性氧化铁(SPIO)纳米颗粒(T2造影剂)同时包载到具有稳定性和刺激响应性的胶束中,构建出一种可激活 T1和 T2信号的新型双向磁共振(t-MRET)纳米造影剂(图2)。该策略还可以应用于不同的胶束纳米结构,并设计成响应其他生物标记物以应对不同疾病的靶向需求。Lu 等[12]也设计并合成了一种 pH 激活的T1-T2双模磁共振造影剂 SPIO@SiO2@MnO2。在正常组织中,MnO2作为一种非活性的 T1造影剂前体,可以有效地猝灭 SPIO 的 T2加权信号。然而,在肿瘤或炎症组织的酸性环境下,MnO2分解为 Mn2+,进而逐步增加 T1和 T2加权信号。

图2 t-MRET 纳米技术和 DESI 在 pH 响应型 POP@P-Mn-SPIO 中的应用[11]
受距离相关磁共振调谐(MRET)现象的启发,Zhang等[13]利用血小板衍生生长因子(PDGFB)偶联的包覆氧化铁且掺杂锰的二氧化硅(FMS)核-壳纳米结构(PDGFB-FM)设计了一种新型的肿瘤微环境响应的 T1和 T2双模式MRI 纳米开关(图3)。该纳米开关在肿瘤微环境中具有明显的关闭-开启(Off-On)T1-T2双模协同成像效果,且具有超快的响应速度、高灵敏度和特异性。

图3 PDGFB-FMS 的合成工艺示意图(A)及其作为智能双模磁共振造影剂的作用机制(B)[13]
Liang 等[14]通过将顺磁性的 Mn2+离子和 Fe3O4纳米颗粒组装到 pH 和谷胱甘肽(GSH)敏感的锌沸石咪唑骨架(ZIF-8)基质中,构建了一种成分简单的 pH 和 GSH 响应型 T1-T2双模造影剂 Fe3O4@ZIF-8-Zn-Mn 纳米颗粒。在酸性环境(pH 6.5~5.5)和 GSH(0~4 mmol/L)中,Fe3O4@ZIF-8-Zn-Mn 纳米粒子可以分解并释放 Fe3O4纳米粒子和顺磁性的 Mn2+离子,使 T1和 T2成像性能同时恢复,r1和 r2弛豫率分别提高 6.9 倍和 9.9 倍。Liu 等[15]将 Fe3O4和 BMS-202(Pd-L1 抑制剂)负载到聚丙交酯-乙交酯基纳米粒子核中,开发了一种多功能的金属-有机多模式热疗纳米平台(FMN-BMS@HA + AMD),铁/锰复合结构使其具有良好的 T1-T2双模磁共振成像能力,并在乳腺癌动物模型中显示了显著的肿瘤生长和转移抑制作用。
3 单一顺磁性金属元素掺杂法
T1和 T2双模态造影剂的开发和应用已取得了显著进展。然而,双金属基造影剂还存在一些缺陷,包括金属负载率低、金属浸出和毒性,以及由于两种金属靠近引起的磁耦合导致金属的干扰,进而使 MRI 信号猝灭。因此,使用具有单金属基的试剂可能有助于克服上述两种金属之间相互作用的限制。
在此基础上,我们课题组采用聚合前掺杂的方法制备了锰螯合介孔聚多巴胺纳米粒(Mn-MPDA),负载一氧化氮(NO)前体药物 BNN6 和免疫激动剂 R848,构建了一种T1-T2双模 MRI 可视化纳米诊疗体系(RBMM)(图4)。在酸性 pH 和高 GSH 含量的条件下载体材料会发生降解,释放出 Mn2+和 R848,释放的 R848 可作用于肿瘤相关巨噬细胞,使其由 M2 型向 M1 型极化,近红外激光照射下 RBMM 可释放大量 NO 气体,从而实现了高效协同抗肿瘤作用;聚合前掺杂策略使得 Mn2+在 MPDA 内部的掺杂效率显著升高,几何约束构象作用可使 Mn-MPDA 附近水分子的自由旋转及近端水分子的扩散受限,因此显著提高了 T1-T2双模态 MRI 造影剂的灵敏度[16]。在这一基础上,我们通过在介孔聚多巴胺中掺杂精氨酸(Arg)和锰离子(Mn2+),赋予其优异的抗 ROS 和 MRI 可视化探针功能,进一步负载临床抗炎药物皮质类固醇地塞米松(DEX)构建 DEX@Arg-Mn-MPDA(DAMM)纳米诊疗探针,该探针不仅能够抑制滑膜巨噬细胞极化炎性反应和关节软骨细胞凋亡,有效延缓骨关节炎发展;同时该探针具有 T1-T2双模磁共振(MRI)造影能力,有望实现 MRI 可视化关节内药物递送,对病理微环境药物浓度进行有效监控,并实现对骨关节炎发展进程的精准诊断[17]。
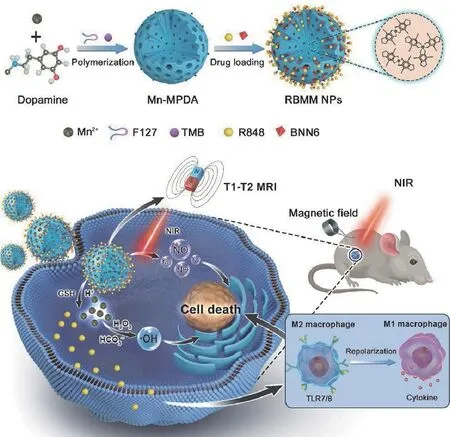
图4 T1-T2 双模 MRI 可视化纳米诊疗体系及作用机制[16]
具有顺磁特性的钆是一种非常经典的能同时发生横向弛豫和纵向弛豫的材料。Zhou 等[18]设计了氧化还原二茂铁硒化合物(FcSe)修饰的顺磁性 Gd3+基上转换纳米颗粒(UCNPs),用于调节 T1-T2弛豫时间,以实现多模态成像和 H2O2响应光-化学动力学治疗。氧化钆纳米颗粒(Gd2O3NPs)由于具有更好的安全性、功能性和弛豫性,已成为 Gd造影剂的有效替代品。Kadria-Vili 等[19]报道了聚乙二醇化的 Gd2O3-介孔二氧化硅/金核/壳纳米颗粒(Gd2O3-MS NSs)的合成,该纳米颗粒的 r1 弛豫率是传统 T1造影剂的三倍以上,r2弛豫率与现有 T2造影剂相当。Gholibegloo 等[20]在其研究中合成了 pH 敏感的 Gd2O3/CS-TPP@5-ALA 纳米颗粒,除了 Gd2O3固有的 T1效应外,通过 5-氨基乙酰丙酸(5-ALA)和柠檬酸铁铵(FAC)诱导细胞内铁蛋白增加的强磁化率,影响邻近质子的 T2。因此,细胞 T1加权成像加代谢 T2加权成像可以为多形性胶质母细胞瘤的准确诊断提供更详细的信息。另有学者采用仿生合成方法,以牛血清白蛋白(BSA)为模板,在水中一步制备出具有T1-T2双模态成像功能的 KMnF3@BSA 探针。该探针只含有一种顺磁元素,可避免 T1和 T2组分之间的相互干扰和复杂的多步合成步骤,呈现出双高的 r1和 r2弛豫性能。这种简单的仿生方法还可用于制备 KCoF3、KGdF4和KEuF4等金属氟化物[21]。与元素周期表中的 Gd 一样,铒(Er)因其磁性而引起了研究人员的兴趣,有研究者研究了PEO/Er2O3作为诊断性纳米纤维的潜在用途[22]。
另外,铁氧体磁性纳米颗粒 MFe2O4(其中 M = Fe、Mn、Zn、Co、Ni)由于具有独特的尺寸和可调节的物理性质而备受关注,成为肿瘤疾病诊断或治疗中前景广阔的药物。Shabalkin 等[23]团队首次提出 ZnFe2O4@MnFe2O4纳米粒子(MNPs)可以同时进行磁热疗、放疗和磁共振成像,并验证了其 T1-T2双模 MRI 对比能力是通过超顺磁特性以及化学和结构组成来确定的。Wang 等[24]提出一种超高场T1-T2双模态磁共振血管成像策略,并设计合成了基于超小氧化铁纳米粒子的 T1-T2双模态超高场磁共振造影剂(UDIOC)。如图5 所示,UDIOC 的超小尺寸使其在超高场下具有适当的 T2对比效果,同时其表面修饰的亲水性配体加快了周围环境中水质子的 T1弛豫过程,因此,在超高场下具有高效的磁共振对比能力,可作为 T1-T2双模态造影剂。

图5 超高频血管成像 T1-T2 双模磁共振造影剂设计示意图[24](红色箭头表示水质子的纵向磁化,蓝色箭头表示水质子的横向磁化)
氧化铁纳米颗粒(IONPs)具有良好的物理化学和生物学特性,已被开发为 T1或 T2加权磁共振成像的造影剂。然而,提高纵向弛豫率的一般策略往往会降低横向弛豫率,因此同时加强 IONPs 的 T1和 T2增强效应仍然是一个挑战。Chen 等[25]研究了基于 Hofmeister 效应的 T1-T2双模磁共振成像与肿瘤增强协同治疗(图6)。他们通过在mPEG-NH2修饰的黑磷纳米片(PNS)表面负载 Fe2O3纳米颗粒,制备了一种纳米复合材料(FePN)。进入肿瘤微环境后,H+和 GSH 首先攻击羧基和 Fe3+离子,导致自组装的 Fe2O3分散降解,提高纵向弛豫效率 r1。然后,Hofmeister 效应引起了横向弛豫效率 r2的增加。另一方面,Sun 及其团队也利用 Fe2O3开发了一种透明质酸(HA)稳定的氧化铁纳米簇(Fe2O3@PFDH NC),不仅具有高的纵向和横向弛豫率,在 T1-T2加权磁共振成像中表现出很强的对比度,而且可作为一种智能可降解的热疗纳米制剂,用于双模 MRI 引导的化疗-光热治疗[26]。

图6 FePN 时间依赖性 T1-T2 双模 MRI 的生物医学应用及机制[25]
据报道,研究人员开发了一种 FePt@Fe3O4核壳纳米粒子用于同步增强 T1和 T2成像效果[27]。随着纳米粒子核心尺寸的增大,核−壳界面交换耦合作用增强,引起饱和磁化强度(MS)的提高,从而使 r1和 r2增加。Li 等[28]使用不同分子量的聚合物包覆超小型超顺磁性氧化铁,其中2% Cys-PMAA@Fe3O4MFs 在体外表现出较高的 T1和T2信号,体内双模成像清晰地显示了肿瘤区域。
Aires 等[29]的研究展示了利用蛋白质工程作为一种新的方法来设计合成超小 IONPs 的支架。通过合理设计含有不同数量金属配位位点的蛋白质,对一组蛋白质稳定的 IONPs(Prot-IONPs)的大小、理化性质和磁性能进行了评价,研究证明其具有良好的 T1和 T2弛豫率、稳定性和生物相容性,显示出潜在的磁共振成像应用能力。此外,还有研究者设计了超小 BSA@Fe3O4纳米颗粒[30]和 F56-DHCA-Fe@Fe3O4[31]、SA-MPDA@SPIO/DOX/Fe3+NPs[32]纳米粒子、特异性靶向 Aβ 的纳米探针UFNPs@PEG/PZD[33]、具有治疗功能的诊疗探针Fe-TA-Fe2O3@PDA[34]等,这些纳米颗粒都展示了作为 T1-T2双模造影剂的潜力。
4 小结
T1-T2双模态成像技术的融合,可在同一台 MRI 设备上获得具有相同穿透深度和空间/时间分辨率的 T1-T2图像,可以实现信息的互相映证,从而提供更为准确的影像学信息。但是,对于 T1-T2双模 MRI 探针目前存在的局限性,有以下几方面的考虑:
⑴对不同疾病适用性的局限性:双模 MRI 探针在提高对肿瘤小病灶的灵敏度和准确性方面表现出显著优势。然而,由于良性疾病和肿瘤微环境的异质性,这些探针在其他疾病诊断中的应用可能面临困难。因此,需要更多的研究来优化探针的设计,使其更适用于不同病理学特征的疾病。
⑵临床应用前的深入评估:在推动临床转化之前,必须充分考虑双模 MRI 探针的生物安全性和生物相容性。尽管已有大量基础研究致力于双模 MRI 探针的设计,但大多数研究仅涉及体外和动物实验。为了更好地了解其在人体内的效力和安全性,需要进行更深入的临床前评估,包括体内药代动力学、毒理学和安全性评价等。
⑶未来临床应用的挑战:虽然在基础研究中取得了显著进展,但将双模 MRI 探针成功应用于临床仍然面临一系列挑战。这包括标准化和规范化的问题,以确保探针在不同临床环境中的可重复性和稳定性。
总体而言,尽管存在这些挑战,对双模 MRI 探针进行深入研究和评估是必要的,以实现其在未来临床中更广泛和有效的应用。

