溴酸钾滴定法测定金属砷中砷含量的改进
赵艳琼,张 洪**,梁德华,洪发珺
(1.红河砷业有限责任公司,云南 个旧 661000;2.云南锡业研究院有限公司,云南 个旧 661000)
前 言
砷在自然界分布非常广泛,是地壳的构成元素,其丰度为1.7~1.8 mg/kg,主要分布在土壤、岩石和水环境中[1]。砷具有亲硫性,常以硫化物或硫代砷酸盐的形式存在于Au、Ag、Cu、Pb、Zn、Sb、Sn、Ni、Hg、Co等矿床中。砷不仅对矿产品的品质有很大影响,而且在冶炼过程中污染环境较严重,因此对砷量的排放标准有严格规定。随着生态环境保护意识的不断增强,砷在生产、生活中作为有毒有害重金属元素之一,含砷物料的排放,已经受到环保部门的关注。
目前,国家标准测定砷的方法主要有亚铁邻菲啰啉光度法、砷锑钼蓝光度法、溴酸钾滴定法[2]、次亚磷酸盐还原-碘滴定法和电感耦合等离子体原子发射光谱法(ICP-AES法)等[3]。其中,亚铁邻菲啰啉光度法、砷锑钼蓝光度法适合测定砷质量分数为0.0005%~0.20%的样品,ICP-AES法适合测定砷质量分数为5%~10%的样品,次亚磷酸盐还原-碘滴定法适合测定砷质量分数大于0.05%的样品。传统溴酸钾滴定法,试样经硫酸、磷酸分解,以硫酸肼(硫酸联胺)将五价砷还原成三价砷,以甲基橙作为指示剂,用溴酸钾标准溶液滴定测砷含量,测定范围受到较大局限。本方法采用浓硫酸加热完全溶解,加水煮沸,加入硝酸、尿素,以甲基橙作为指示剂,用溴酸钾标准溶液滴定至溶液呈无色为终点。缩短了分析时间,降低了成本,适用于快速测定金属砷中砷含量。
1 试剂
1.1 主要试剂
硫酸(98%);硝酸(1+4);尿素溶液(10%);甲基橙溶液(1%);三氧化二砷(99.99%);溴酸钾。
1.2 标准溶液的配制和标定
溴酸钾标准溶液:称取溴酸钾 3.033 g 与溴化钾 3.0 g 于烧杯中,用少量水溶解后移入 1000 mL 容量瓶中,用蒸馏水稀释至刻度,摇匀,放置两天后标定。
标定:称取已烘干至恒重约 0.53 g(精确至 0.0001 g)三氧化二砷(99.99%)3份,分别置于3个 300 mL 烧杯中。加入 20 mL 硫酸,盖上表面皿,加热完全溶解后,冷却至室温,用蒸馏水冲洗表面皿及杯壁,加水 100 mL,摇匀,加热至沸腾。趁热,加入 5 mL 硝酸,5 mL 尿素溶液,在不断搅拌下,自 100 mL 滴定管中滴入94~96 mL 溴酸钾标准溶液,加入2~3滴甲基橙溶液,逐滴滴定至溶液颜色消失为终点。按式(1)计算溴酸钾标准溶液对砷的滴定度,取其平均值:
(1)
式中:T—1 mL溴酸钾标准溶液相当于砷的量,g;
m—称取三氧化二砷的质量,g;
V—标定时消耗溴酸钾标准溶液体积,mL;
0.7574—三氧化二砷换算为砷的换算因数。
若3份滴定度的极差值大于6×10-6g时应重新标定。
2 实验原理与分析步骤
2.1 实验原理
实验利用金属砷与浓硫酸反应生成三价砷,溴酸钾与三价砷发生氧化反应,生成五价砷,过量的溴酸钾会使指示剂褪色(甲基橙被氧化剂氧化破坏了其结构,使红色消失)。溴酸钾与锑会发生反应,计算金属砷含量时,应减去相当于试样中锑量的砷量后得到净砷量,反应方程式如下:

(1)
(2)

(3)
(4)
2.2 分析步骤
1)金属砷样品须经过80目筛网筛分,筛上直径应小于 2 mm。
2)金属砷样品加工后置于干燥器中,当天称取进行分析,并且按照筛上筛下比例为3∶1称取样品。
3)称取 0.4 g 金属砷样品(精确至 0.0001 g)置于 300 mL 烧杯中,加入 20 mL 硫酸,盖上表面皿,加热完全溶解后,冷却至室温,用蒸馏水冲洗表面皿及杯壁,加水 100 mL,摇匀,加热至沸腾。趁热,加入 5 mL 硝酸,5 mL 尿素溶液,在不断搅拌下,自 100 mL 滴定管中滴入94~96 mL 溴酸钾标准溶液,加入2~3滴甲基橙溶液,逐滴滴定至溶液颜色消失为终点。
4)分析结果的计算
按式(2)计算砷的质量分数:
(2)
式中:T—1 mL溴酸钾标准溶液相当于砷的量,g;
V2—滴定金属砷样品时所消耗的溴酸钾标准溶液体积,mL;
m2—样品量,g;
0.6154—锑换算为砷的换算因数。
分析结果精确至小数点后两位。
3 结果与讨论
3.1 硫酸用量的选择
分别称取5份同一样品约 0.4 g(精确至 0.0001 g),选取不同体积的硫酸(98%),按照试样分析步骤,计算结果如表1所示。

表1 硫酸用量的选择
从表1可以看出:在酸度不同的条件下,当硫酸体积为 10 mL 时,金属砷中砷测定结果较低,硫酸体积增加至 20 mL 时,金属砷中砷测定结果增加,继续增加硫酸体积,测定结果趋于稳定,即硫酸体积为20、30、40、50 mL 时,测定结果变化不大。为避免硫酸浪费,并且通过试验,酸度过高,甲基橙指示剂容易被破坏[4],所以在测定金属砷砷含量分析中,硫酸用量优选 20 mL。
3.2 滴定过程中温度的影响
样品溶解完全,冷却后用洗瓶冲洗杯壁,此过程边冲洗,边摇烧杯,防止硫酸飞溅,加水 100 mL,置于电炉上加热至沸,趁热,加入 10 mL 硝酸和 10 mL 尿素,立即用溴酸钾标准溶液滴定,若未及时滴定,试样溶液温度低,反应速度慢,会使滴定体积偏大,容易造成结果偏高[5];在滴定过程中,温度过高,甲基橙指示剂容易被破坏,所以在滴定过程中,试样溶液颜色有部分橙黄色出现时,再加入甲基橙指示剂。在整个滴定过程中应保持试液温度在40~60 ℃ 之间。
3.3 共存元素的影响
在试验条件下,加入一定的砷标准和梯标准后分别加入不同量的共存元素离子,多次试验显示:铬、铅、铋、铁、锡、硫等共存元素都不影响砷的测定。
3.4 锑对砷的影响
称取 0.l g 锑(99.99%)加入己知质量分数砷标准样品溶液,盖上表面皿。加入(1+1)盐酸 10 mL 溶解,加热试液体积至近干,再加入 3 mL 王水,用少量蒸馏水吹洗杯壁,低温加热溶解,冷却,移入 25 mL 容量瓶中,用蒸馏水加至刻度,摇匀。结果见表2。
从表2中数据可以看出,不同砷含量的试样,加入定量的锑,两次测定砷含量结果偏高,说明锑的存在对砷的测定有影响。所以计算金属砷含量时,应减去相当于试样中锑量的砷量后得到净砷量。
3.5 法精密度测定
按照试样分析步骤,分别对样品20230104、样品20230105、样品20230106、样品20230107进行多次测定,测定结果如表3所示。
表3结果表明:本测定方法标准偏差为0.051%~0.072%,变异系数为0.051%~0.073%。
3.6 加标回收试验
按照试验分析方法,分别在已知含量的4个样品中添加一定量的砷标准品,进行样品加标回收试验,并计算回收率,结果见表4。
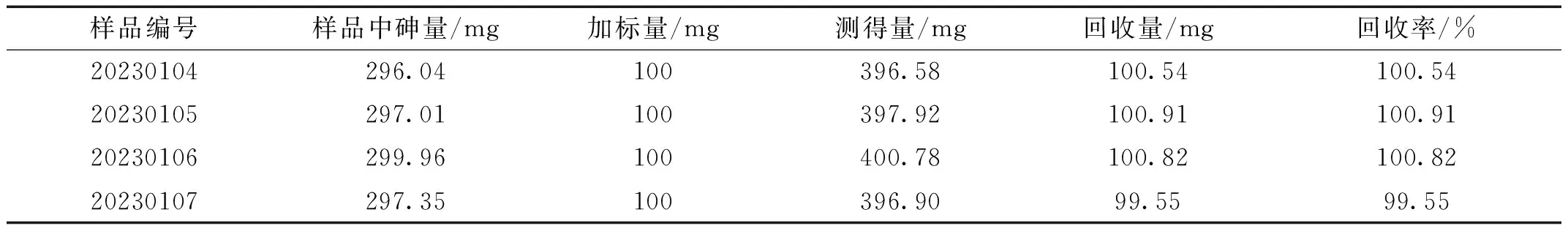
表4 加标试验回收率
从表4加标回收试验中可以看出,溴酸钾标准溶液滴定法测定试验样品的加标回收率在99.55%~100.91%之间。
4 结束语
利用溴酸钾标准溶液滴定法测定金属砷中砷含量,在滴定过程中应保持试液温度在40~60 ℃ 之间。本分析方法标准偏差为0.051%~0.072%,变异系数为0.051%~0.073%,加标回收试验回收率为99.55%~100.91%。本方法常用于金属砷中砷含量的分析,对测定高纯度砷具有简单、快速,结果精准可靠、试剂使用成本低、工作效率高等优点。与传统的溴酸钾滴定法相比较,由于硫酸肼是联氨与硫酸生成的盐类,有毒,有致癌性,本方法回避了硫酸肼试剂的使用,改善了操作环境,为操作者的健康安全提供了保障,同时改进了主要试剂用量和配比,优化了分析步骤。不仅具有操作简单、快速,结果准确可靠等优点,而且进一步扩大了砷含量测定方法的使用范围,提高了分析效率。

