强酸性SnO2/SiO2催化山梨醇脱水制异山梨醇
曹 麒,韩玉福,董运洋,郭佳星,王新承,宋永吉
(北京石油化工学院 新材料与化工学院 恩泽生物质精细化工北京市重点实验室,北京 102617)
由来源丰富的可再生生物质制备高值化学品是当前的研究热点[1]。山梨醇广泛存在于自然界中,可通过氢解、脱水、聚合等反应转化为其他化学品和材料[2-5],它的二次脱水环化产物异山梨醇[6-7]是一种新型材料,广泛用于医药、食品、护肤等领域,也是改性可生物降解塑料聚己二酸-对苯二甲酸丁二醇酯的重要单体[8]。工业上主要通过浓硫酸催化山梨醇脱水的方法制异山梨醇,但转化效率低、能耗高且副产物较多[6,9]。由于化学和区域选择性的影响,山梨醇在二次脱水反应中会生成多种异构副产物,且分子间易发生低聚反应生成腐黑物[9]。介孔硫酸钛[10]、磷酸盐[11]、磷钨酸及其负载型氧化物[12]、硅酸铝分子筛[13]等作为催化剂时,均可得到约70%的异山梨醇收率。苯磺酸基团接枝介孔碳[14]、磺酸树脂[15]、离子交换树脂[16]、二乙烯基苯磺酸钠与对苯磺酸钠混合物[17]等也可高效催化山梨醇脱水,异山梨醇收率甚至超过了90%。然而这些催化剂的制备工艺相对复杂,重复性及经济性差。
酸液浸渍是调控催化剂表面酸性质的有效手段。氧化钽、氧化锆、氧化钛、氧化锡等经磷酸浸渍后,在无溶剂体系中异山梨醇的收率可达70%以上[18],而硫酸化氧化铌体系的异山梨醇收率达到了84.1%[19]。SnO2比表面积大,化学稳定性好,但易膨胀粉化和团聚,直接用于山梨醇脱水反应时催化效果不佳。
本工作通过硅改性的方法制备了SnO2/SiO2复合氧化物,经酸液浸渍后得到强酸性SnO2/SiO2(Sn-Si)催化剂,采用NH3-TPD、FTIR、吡啶吸附FTIR、Raman光谱对催化剂进行了表征,考察了催化剂对山梨醇脱水制异山梨醇反应的催化性能,并优化了催化剂用量和反应温度;同时考察了催化剂的重复使用性,并对催化机理进行了分析。
1 实验部分
1.1 主要试剂
SnCl4·5H2O(≥99.0%(w))、NaOH(≥96.0%(w))、硝酸(65.0%~68.0%(w))、硫酸(95.0%~98.0%(w))、磷酸(≥85.0%(w))、山梨醇(98%(w))、异山梨醇(98%(w)):国药集团化学试剂有限公司。
1.2 催化剂的制备
称取69.8 g SnCl4·5H2O和33.35 g硅溶胶(Sn/Si摩尔比3∶1)共同溶于去离子水中并搅拌均匀,在混合溶液中逐滴加入0.5 mol/L的NaOH溶液至溶液pH=8.5,室温下搅拌2 h后在80 ℃下冷凝回流5 h,将所得乳浊液抽滤、洗涤至中性,将所得产物放入烘箱中在120 ℃下干燥12 h,研磨至20~40目后于450 ℃下焙烧4 h,得到Sn-Si催化剂。
取自制的Sn-Si催化剂置于圆底烧瓶中,分别加入硝酸、硫酸或磷酸,在指定温度下回流搅拌酸化一定时间,清洗、离心、烘干后得到酸化的Sn-Si催化剂,分别记为。
1.3 催化剂的表征
采用Hiden公司QIC-20型质谱仪进行NH3-TPD表征。称取0.1 g催化剂,加热到120 ℃后用30 mL/min的N2吹扫30 min;降温至100 ℃以下,切换为20 mL/min的5%(φ)NH3/N2混合气,在常温下吸附1 h;再切换30 mL/min的N2吹扫10 min后以10 ℃/min速率升温至 800 ℃,同时用硫酸溶液吸收尾气并滴定,确定总酸量。
采用布鲁克公司的Vertex 70型傅里叶变换红外光谱仪进行FTIR和吡啶吸附FTIR表征。采用定制透射池,经500 ℃预处理30 min后降温,称取20 mg催化剂并压片,装入试样池,边抽真空边升温至200 ℃处理30 min,以去除催化剂表面物理吸附的水及其他杂质,在降温过程中采集不同温度下的背景,冷却至室温后向试样池中通入吡啶,并常温吸附30 min以上。最后按设定程序升温脱附,在所需温度(50,100,150,200 ℃)下采集谱图。
采用Renishaw公司inVia Reflex型显微共聚焦Raman光谱仪进行Raman光谱分析,激光器为DPSS型,激光波长532 nm,曝光功率10 mW,曝光时间1 s,累积6次测试信号。
1.4 催化性能评价
称取适量山梨醇,将其与催化剂混合后加入反应器,油浴加热至设定温度,山梨醇呈熔融状态后,启动真空泵至压力达到目标值,开始计时。反应中定时取样,暂停真空泵,从取样口取一滴试样置于2 mL离心管中,准确称重并使用移液枪加入2 mL去离子水稀释试样,试样全部溶解后过滤到色谱进样瓶中,通过Agilent公司Agilent 1200型高效液相色谱仪进行分析。取样后,将装置重新密封,并开启真空泵降压,取样时间保持在30 s内,不计入反应时长。色谱分析条件:折光示差检测器,伯乐Aminex HPX-87H色谱柱,柱箱温度35 ℃,流动相0.005 mol/L硫酸,流量0.5 mL/min。
2 结果与讨论
2.1 催化剂表面酸性质调控对催化性能的影响
不同酸液酸化的Sn-Si催化剂的NH3-TPD曲线见图1。由图1可见,/Sn-Si表面呈弱酸性,表面有中强酸和强酸中心,/Sn-Si表面只有强酸中心。从总酸量看,-Si最高(0.4537 mmol/g),其次是/Sn-Si(0.4296 mmol/g),最低的是/Sn-Si(0.2653 mmol/g)。根据山梨醇脱水反应机理,强酸对反应的催化效果更好[8,15-16,20-21],后续实验结果与此相符。
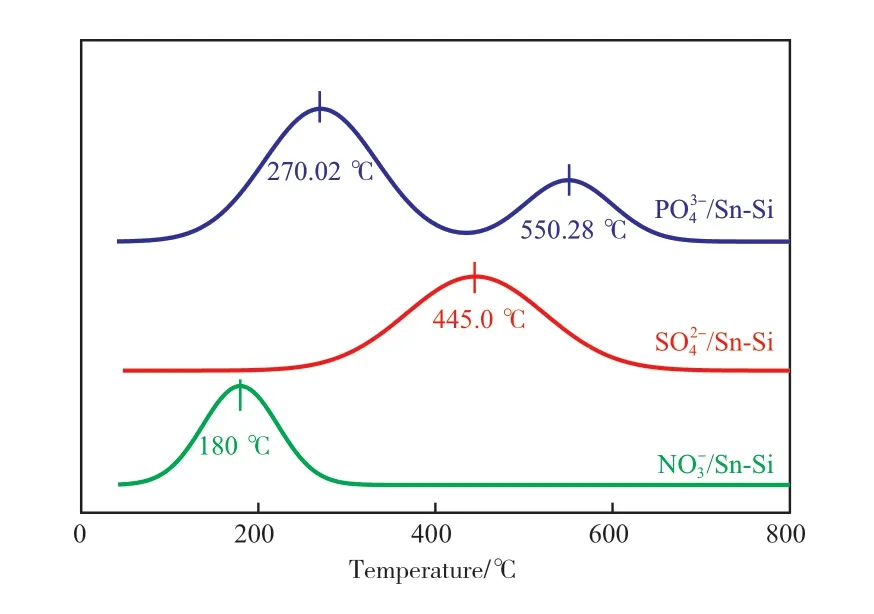
图1 不同酸液酸化的Sn-Si催化剂的NH3-TPD曲线Fig.1 NH3-TPD profiles of different acids acidified SnO2/SiO2(Sn-Si) catalysts.
不同酸液酸化的Sn-Si催化剂的吡啶吸附FTIR谱图见图2。由图2可见,未经酸化的Sn-Si催化剂仅在1450 cm-1处检测到L酸特征峰,表明催化剂表面仅含L酸,不含B酸。经酸化后,催化剂中B酸位均有不同程度的增多,表明催化剂表面有一定量的B酸。对比B酸与L酸的酸量比值(B/L值)可知,-Si催化剂的B/L值最小(1.65),/Sn-Si催化剂的B/L值居中(5.36),/Sn-Si催化剂的B/L值最大(16.30)。因此,硫酸酸化大大提高了催化剂表面的B酸量,使其催化活性大幅提高。

图2 不同酸液酸化的Sn-Si催化剂的吡啶吸附FTIR谱图Fig.2 Pyridine-FTIR spectra of different acids acidified Sn-Si catalysts.
不同酸液酸化的Sn-Si催化剂的FTIR和Raman谱图见图3。
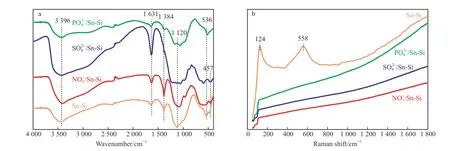
图3 不同酸液酸化的Sn-Si催化剂的FTIR(a)和Raman(b)谱图Fig.3 FTIR(a) and Raman(b) spectra of different acids acidified Sn-Si catalysts.
由图3a可知,四种催化剂在3396,1631 cm-1处的吸收峰归属于水合分子的O—H键的不对称伸缩振动;1384 cm-1处的吸收峰归属于—NO2的伸缩振动,因此/Sn-Si在此处的峰强度最强;1120 cm-1处的宽峰是羟基的特征峰;536 cm-1处的吸收峰归属于Sn—O键的吸收振动[22-24];457 cm-1处的吸收峰为Si—O键的特征峰。由图3b可知,未经酸化的Sn-Si催化剂在124 cm-1处出现了一个峰,归属于金红石SnO2的B1g晶格振动[25-26];558 cm-1处的峰接近于非晶相SnO2的振动[27-28];酸化的Sn-Si催化剂没有Raman振动信号,表明没有Raman活性。
催化剂活性评价结果如图4所示。由图4可见,未酸化的Sn-Si催化剂的山梨醇转化率和1,4-失水山梨醇收率随反应时间的延长逐渐提高,但异山梨醇收率极低(反应8 h后仅为3.38%),表明未酸化的Sn-Si催化剂仅能催化山梨醇的一次脱水反应,对二次脱水反应的催化效果极弱。这可能是因为Sn-Si催化剂仅含L酸,不含B酸,而二次脱水需要B酸与L酸协同作用[3,7,20,29-30]。
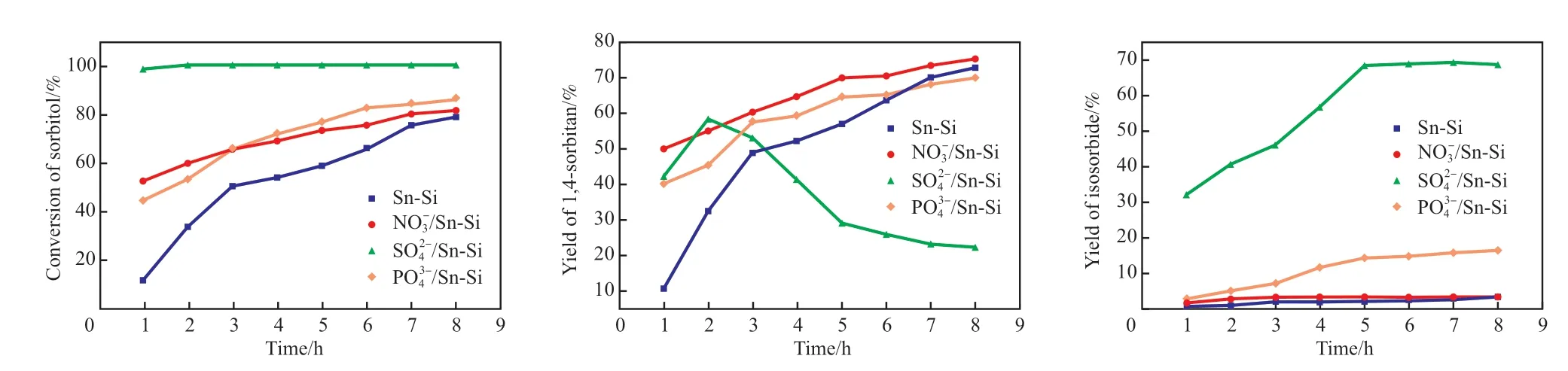
图4 不同酸液酸化的Sn-Si催化剂催化山梨醇转化的反应结果Fig.4 Reaction results of sorbitol conversion catalyzed by different acids acidified Sn-Si catalysts.Reaction conditions:5 g sorbitol,0.5 g catalyst,130 ℃,6 kPa.
2.2 反应条件优化

图5 /Sn-Si催化剂用量对山梨醇转化的影响Fig.5 Effect of /Sn-Si catalyst amount on conversion of sorbitol.Reaction conditions:5 g sorbitol,130 ℃,6 kPa.
反应温度对山梨醇转化的影响见图6。在130~160 ℃的范围内,随反应温度的升高,山梨醇转化速率逐渐加快,当反应温度超过140 ℃时,山梨醇在1 h内便可完全转化;1,4-失水山梨醇的收率先下降后基本保持不变,而异山梨醇收率先增大后保持不变或下降。当反应温度为150 ℃时,反应1 h异山梨醇收率便达到最高值(73.25%),而1,4-失水山梨醇收率为18.45%。因此,最佳反应温度为150 ℃,反应时间为1 h。
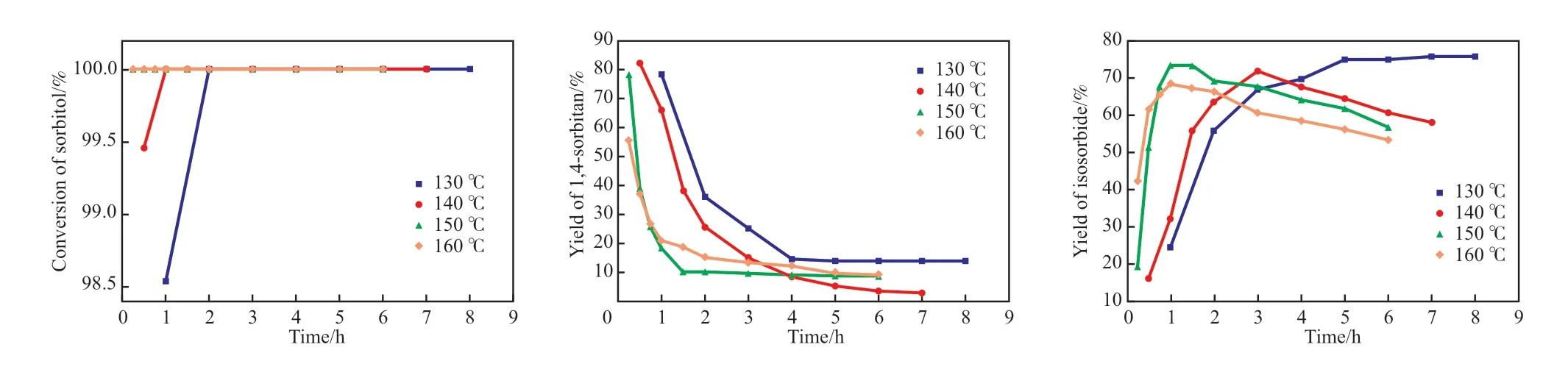
图6 反应温度对山梨醇转化的影响Fig.6 Effect of reaction temperature on conversion of sorbitol.Reaction conditions:5 g sorbitol,0.5 g /Sn-Si catalyst,6 kPa.
2.3 催化剂的重复使用性
为考察催化剂的重复使用性,在反应结束后用去离子水稀释反应液,通过过滤、清洗、烘干、酸化再生催化剂,并对再生催化剂进行评价,评价结果见图7。在5次实验中,山梨醇的转化率均可达到100%,表明山梨醇的一次脱水效果没有下降。催化剂循环使用5次后,中间产物1,4-失水山梨醇的收率略有上升,异山梨醇收率仅下降了1.38百分点,表明再生后催化剂性能稳定,具有较好的重复使用性。
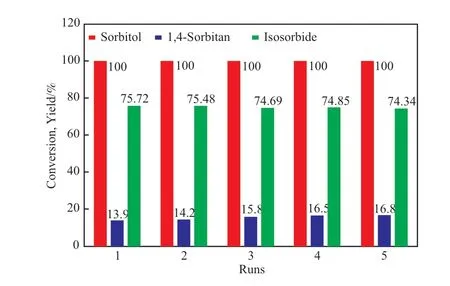
图7 /Sn-Si催化剂的重复使用性Fig.7 Reusability of/Sn-Si catalyst.Reaction conditions:5 g sorbitol,0.5 g catalyst,130 ℃,6 kPa,5 h.
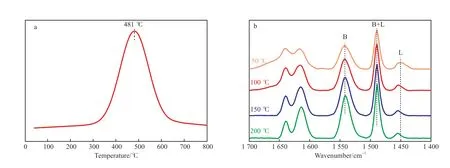
图8 循环使用5次后/Sn-Si催化剂的NH3-TPD曲线(a)和吡啶吸附FTIR谱图(b)Fig.8 NH3-TPD profiles(a) and pyridine-FTIR spectra(b) of /Sn-Si catalyst after five cycles.
2.4 催化机理分析
理论上,山梨醇先脱去一分子水得到中间产物1,4-失水山梨醇,再脱去一分子水得到异山梨醇。酸催化山梨醇脱水反应为准一级反应,两端伯羟基质子化后,与C4羟基或C3羟基发生SN2取代反应,得到反式四氢呋喃环(见图9)[31-32]。一般B酸更易与山梨醇形成配合物,对山梨醇第一步脱水反应的催化作用强于第二步脱水反应,使得1,4-失水山梨醇的脱水反应成为速控步骤[33]。本研究中部分反应结束后中间产物的最终收率高于50%,充分说明了这一点,而使用/Sn-Si催化剂能得到较高的异山梨醇收率,也是高效催化中间产物进一步脱水的结果。
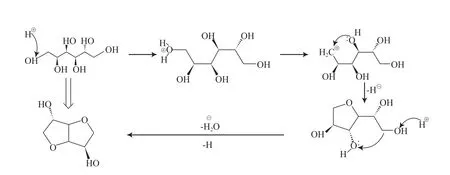
图9 酸催化山梨醇脱水的反应机理Fig.9 Reaction mechanism of acid catalyzed dehydration of sorbitol.
据报道,B酸和L酸都能使山梨醇脱去一个水分子生成1,4-失水山梨醇,且B酸能更有效地催化1,4-失水山梨醇脱去第二个水分子[10,34]。由本研究结果可知,有一定量的L酸存在时异山梨醇收率明显更高,可见L酸对1,4-失水山梨醇的脱水反应有一定的促进作用(见图10)。一方面,L酸可与水协同极化产生O—H键,使催化剂表面产生B酸中心,进而促进1,4-失水山梨醇脱水。另一方面,考虑到反应体系真空度较高,产生的水被及时带出,因此L酸中心可通过与反应物羟基配位来催化脱水反应(图10步骤1)。此外,由于1,4-失水山梨醇的C5和C6羟基间存在氢键,B酸会优先质子化C5位羟基,阻碍脱水反应。因此,本工作提出当L酸中心存在时,可能会与C5羟基配位,从而有利于C6羟基的质子化,促进1,4-失水山梨醇的脱水反应(图10步骤2)。在本研究中,具有一定L酸中心的催化剂(/Sn-Si催化剂,B/L值为24)的活性要优于仅含B酸的催化剂,说明B酸和L酸协同催化有助于抑制副反应,提高异山梨醇收率。因此,通过合理调控催化剂中B酸与L酸中心的比例,可以显著提高催化剂的活性。

图10 1,4-失水山梨醇脱水反应路径Fig.10 Reaction pathway of 1,4-sorbitan dehydration.
3 结论
1)制备了酸改性的Sn-Si催化剂,对酸类型进行了考察,硫酸处理能够有效调控Sn-Si催化剂的表面酸性质、提高催化山梨醇脱水的活性。
3)催化剂的总酸量及B/L值是影响催化剂活性的重要因素。总酸量过低会使反应速率过慢,过高又会加剧副反应导致异山梨醇收率下降,而具有一定L酸中心的催化剂的活性优于只有B酸中心的催化剂。

