慢性肾衰竭尿毒症期患者临床治疗中高通量血液透析的应用价值研究
王 伟,马 达
(新疆医科大学第七附属医院肾病内科,新疆 乌鲁木齐 830028)
慢性肾衰竭(chronic renal failure, CRF)为代谢性疾病,是在多种肾脏疾病共同作用下致使肾脏受到损伤、功能下降,尿毒症期是CRF的特殊阶段,患者多伴有水肿、食欲不振、贫血,部分合并心绞痛、心力衰竭,此类患者机体代谢所产生的各种毒素无法正常排泄,蓄积体内导致脏器功能损害,对患者生命安全造成威胁。血液透析滤过(HDF)是治疗CRF尿毒症期的常见方式,其利用弥散、对流作用能够将小分子物质清除,在改善患者肾功能、提升生存率方面具有一定的效果,但该治疗方式不能有效清除中大分子毒素,长期接受HDF治疗的患者常存在中大分子毒素蓄积,导致治疗效果欠佳[1]。此次研究引入高通量血液透析(HFHD)方式,其选择高通透性的透析器,能够提升对中大分子毒素物质的清除效果[2]。为探究其应用效果,本研究选取200例CRF尿毒症期患者,分别采取HDF和HFHD治疗,旨在探究其疗效,现报道如下。
1 资料与方法
1.1 一般资料 以随机数字表法将新疆医科大学第七附属医院2021年1月至2022年12月期间收治的200例CRF尿毒症期患者分为两组,各100例。对照组患者年龄44~77岁,平均(57.22±6.52)岁;男、女性患者分别为58、42例;尿毒症病程3~10个月,平均(5.82±0.89)个月。观察组患者年龄42~76岁,平均(57.28±6.58)岁;男、女性患者分别为56、44例;尿毒症病程3~10个月,平均(5.76±0.94)个月。两组患者年龄、性别、尿毒症病程等一般资料对比,差异无统计学意义(P>0.05),组间可比。纳入标准:①符合《慢性肾衰竭中西医结合诊疗指南》[3]中CRF的诊断标准,且处于尿毒症期;②血肌酐(SCr)水平> 707 μmol/L,肾小球滤过率(eGRF) ≤ 15 mL/min者;③符合血液透析指征者;④年龄大于18岁者;⑤沟通顺畅、依从性较好者等。排除标准:①危重症患者;②重要脏器损伤严重者;③伴有传染性或免疫性疾病者等。新疆医科大学第七附属医院医学伦理委员会已商讨并批准本研究,患者及家属均签署知情同意书。
1.2 治疗方法 对照组患者采用HDF治疗,采用日本旭化成聚砜膜透析器(上海掌动医疗科技有限公司,型号:APS-15U),膜面积参数为1.7 m2,以稀释法制备置换液,血管通路选择前壁动静脉内瘘,采用中性腹膜透析液(碳酸氢盐-G 1.5%) [贝朗医疗(上海)国际贸易有限公司,规格:2000 mL(725 mL/1275 mL)],每周进行3次血液透析治疗,4 h/次,透析液流量以400 mL/h为宜,完成5次血液透析治疗后,实施1次HDF治疗,时间为4 h,滤过系数设置为55 mL/(mmHg·h)。观察组患者应用HFHD治疗,采用聚砜膜超高通量透析器(北京涵泰科技有限公司,型号REXEED-18AC),透析表面积设置为1.5 m2,透析液流量为800 mL/h,超滤系数46 mL/(mmHg·h),血流速度设置为220~280 mL/min,4 h/次,3次/周。两组患者治疗期间均给予低分子肝素钠抗凝处理,进行为期3个月的治疗。
1.3 观察指标 ①临床疗效。疗效标准:患者治疗后症状、体征消失,SCr较治疗前恢复>60%为显效;治疗后症状、体征得到缓解,SCr较治疗前恢复30%~60%为有效;治疗后症状、体征变化不明显或加重,SCr未改善或改善程度<30%为无效[3]。总有效率=显效率+有效率。②肾功能指标。于治疗前后空腹状态下采血(5 mL),离心处理(3500 r/min,10 min),取血清,应用全自动生化分析仪(山东欧陆商贸有限公司,型号:DS-810)检测SCr、尿素氮(BUN)、血β2-微球蛋白(β2-MG)水平。③血管活性物质水平。血液采集、血清制备及检查方式均同②,检测一氧化氮(NO)、内皮素-1(ET-1)、单核细胞趋化蛋白-1(MCP-1)水平。④不良发应。统计两组患者治疗期间低血压、肌肉痉挛、感染、消化道症状等不良反应发生情况。
1.4 统计学方法 采用SPSS 20.0统计学软件进行数据分析,计数资料以[ 例(%)]表示,采用χ2检验;计量资料符合正态分布且方差齐,以(±s)表示,采用t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较 对照组与观察组患者临床总有效率(75.00% vs 92.00%)比较,观察组更高,差异有统计学意义(P<0.05),见表1。
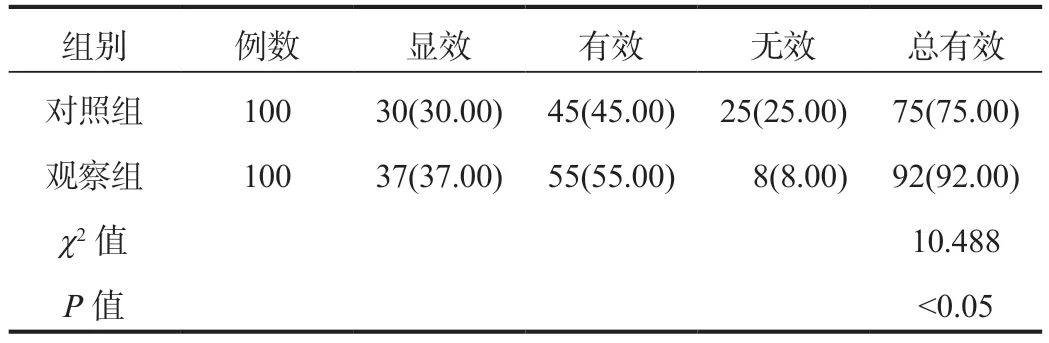
表1 两组患者临床疗效比较[ 例(%)]
2.2 两组患者肾功能指标比较 与治疗前比,治疗后两组患者肾功能指标均下降,且观察组下降幅度更大,差异均有统计学意义(均P<0.05),见表2。
表2 两组患者肾功能指标比较( ±s)

表2 两组患者肾功能指标比较( ±s)
注:与治疗前比,*P<0.05。SCr:血肌酐;BUN:尿素氮;β2-MG:血β2-微球蛋白。
组别例数SCr(μmol/L)BUN(mmol/L)β2-MG(mg/L)治疗前治疗后治疗前治疗后治疗前治疗后对照组100774.24±16.59337.16±27.46*27.37±2.5814.14±1.36*17.03±2.8412.63±1.32*观察组100773.14±13.73306.12±24.94*27.26±2.6411.75±1.15*16.79±2.3610.28±1.52*t值0.5118.3680.29813.4190.65011.673 P值>0.05<0.05>0.05<0.05>0.05<0.05
2.3 两组患者血管活性物质指标比较 与治疗前比,治疗后两组患者血清NO水平均升高,血清MCP-1、ET-1水平均下降,且观察组上述指标变化幅度均更大,差异均有统计学意义(均P<0.05),见表3。
表3 两组患者血管活性物质指标比较( ±s)
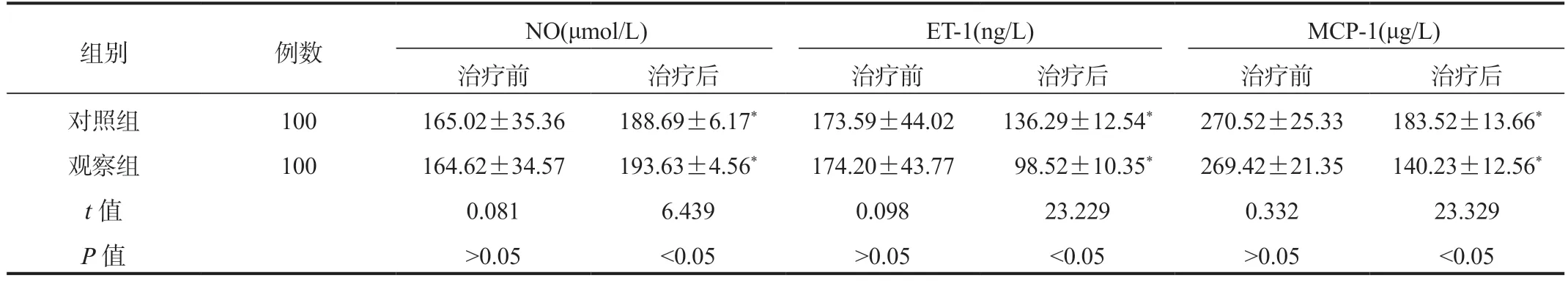
表3 两组患者血管活性物质指标比较( ±s)
注:与治疗前比,*P<0.05。NO:一氧化氮;ET-1:内皮素-1;MCP-1:单核细胞趋化蛋白-1。
组别例数NO(μmol/L)ET-1(ng/L)MCP-1(μg/L)治疗前治疗后治疗前治疗后治疗前治疗后对照组100165.02±35.36188.69±6.17*173.59±44.02136.29±12.54*270.52±25.33183.52±13.66*观察组100164.62±34.57193.63±4.56*174.20±43.7798.52±10.35*269.42±21.35140.23±12.56*t值0.0816.4390.09823.2290.33223.329 P值>0.05<0.05>0.05<0.05>0.05<0.05
2.4 两组患者不良反应发生情况比较 对照组与观察组患者不良反应总发生率(12.00% vs 4.00%)比较,观察组更低,差异有统计学意义(P<0.05),见表4。

表4 两组患者不良反应发生情况比较[ 例(%)]
3 讨论
CRF可以分为1~5期,CRF 5期为尿毒症期,CRF 1~3期患者SCr正常,多数无明显症状表现,少数表现为轻度乏力、恶心、呕吐等胃肠道症状。当肾功能衰竭到4、5期时,会出现SCr升高,伴随电解质代谢紊乱、消化道症状、神经系统症状等。发展至尿毒症期,患者的肾脏功能已经严重受损,无法正常排泄体内废物和水分,导致体内毒素积聚,严重影响身体健康。此时,患者需要进行透析或肾移植等治疗,以维持生命和提高生活质量。HDF是临床治疗CRF尿毒症期的常见手段,其结合了血液透析(HD)和血液滤过(HF)的治疗方法,可以同时通过弥散和对流两种方式清除体内的废物和多余水分,清除效率更高,但HDF清除中大分子毒素能力较差,且在清除毒素分子的同时也会导致体内部分营养物质的流失,效果达不到预期[4]。
HFHD是一种新型血液透析治疗方法,相比于传统HD,其使用的滤器孔径更大,一般在0.2~0.6 μm之间,可以更好地清除大分子物质,如β2-MG、肌酸激酶等;用生物相容膜进行的高通量透析,可更好地保护患者肾功能,从而达到更好的治疗效果。此外,HFHD主要基于人工合成膜透析器的发展,选择容量控制透析机,以高通量血液滤器进行透析治疗,可获得较好的合成膜通透性与理想的溶质扩散性能,能够将血液中大分子溶质向透析液转移,不仅有利于清除大中分子物质,而且能够减少透析相关并发症的发生[5]。本研究通过对比分析两组患者临床疗效及肾功能指标发现,观察组患者临床总有效率高于对照组(75.00% vs 92.00%);治疗后SCr、BUN、β2-MG水平均低于对照组,提示HFHD治疗CRF尿毒症期效果显著,能够有效改善患者肾功能。
血管活性物质是指能够影响血管收缩和扩张的物质,包括部分激素、神经递质及代谢产物等。NO可以调节血管收缩张力及机体血压,而内皮型一氧化氮合酶(eNOS)是NO合成的限速酶,其活性的下降会导致NO含量降低,从而影响内皮功能;ET-1属于血管活性因子,能够调控血管内皮功能,当血管内皮功能下降或受损时,其水平处于高表达状态,CRF尿毒症期患者毒素在体内长时间蓄积,血管平滑肌细胞受到刺激会发生增殖,引起NO下降,ET-1升高;MCP-1可介导炎症细胞聚集,刺激黏附因子的分泌,促进白细胞向肾脏迁移,增加血管内皮通透性,恶化肾脏血管内皮细胞的功能紊乱[6]。本研究中,治疗后观察组患者NO高于对照组,MCP-1、ET-1均低于对照组,表明HFHD治疗可对CRF尿毒症期患者血管活性物质指标起到改善作用。分析原因可能是,HFHD不断地提供新鲜血液及营养物质,促进血液循环,并将毒性物质清除,纠正了机体代谢紊乱,减少了炎症介质的释放,进而降低了MCP-1水平;同时减轻了对心血管的损伤,改善内皮功能,而HDF仅以清除小分子溶质为主,因此在降低血管活性物质方面作用较轻微[7-8]。
与HDF相比,HFHD可以更有效地清除体内的代谢产物和毒素,减轻CRF尿毒症期患者的负担,改善身体的代谢状态,减少对肺部的损伤。在治疗安全性方面,观察组患者不良反应总发生率低于对照组,说明HFHD治疗CRF尿毒症期安全性较高。这是因为HFHD治疗期间,会高效清除中、大分子中的毒素物质,而当中、大分子减少时就会减少不良反应的发生,降低了低血压、感染等的发生率,故保障了患者治疗的安全性[9-10]。
综上,与HDF相比,HFHD治疗CRF尿毒症期效果更好,能够有效改善患者肾功能及血管活性物质水平,安全性较高,值得推广应用。

