氘代抗心血管病药物的合成研究进展
陈贤勇, 周 顺, 金 鑫, 葛真真,, 周鸣强,, 赵建强, 陈永正*, 袁伟成*
(1. 遵义医科大学 药学院 贵州省生物催化与手性药物合成重点实验室,贵州 遵义 563000; 2. 中国科学院 成都有机化学有限公司,四川 成都 610041; 3. 成都丽凯手性技术有限公司,手性药物国家工程研究中心,四川 成都 610041; 4. 浙江金华康恩贝生物制药有限公司,浙江 金华 321016)
氢(Hydrogen, H)是一种化学元素,在元素周期表中排第一位。氢通常的单质形态为氢气,是一种无色无味且易燃的分子气体。氘(Deuterium,D)是氢的稳定性非放射性同位素,在自然界中,氘的丰度约占总量的0.015%,且大多以重水(D2O)的形式存在于海水与普通水中。氘代化是指通过化学反应来使有机化合物中的氢被氘取代,从而改变原有分子的各种特性来达到既定目的。由于氘代前后化合物的物理性质并未发生明显的变化,且C—D键要比C—H键的键长短,这就使C—D键更加稳定[1-2]。同时,氘化化合物由于其在质谱(MS)、核磁共振(1H NMR)和电子自旋共振谱(ESR)中显示出独特的信号,常作为标记化合物广泛应用于生命科学、环境科学、农药残余检测、污染物跟踪以及物质科学等领域[3]。此外,氘代化合物还经常用于药物代谢研究和新药研发[4]。
对人体而言,氘元素也是一种较为安全的元素。人体可以持续4个月耐受含量0.5%血药浓度的氘元素而没有任何毒性反应,而在人体液中含有高达23.0%的重水时,短期内也未见毒副作用[5]。氘代药物是指对某种药物分子上特定位点进行一个或多个氘-氢原子替换所获得的药物,其中应用最广泛的是碳氢键替换成为碳氘键。然而对于早期开发的上市药物通常存在一些缺点,如代谢快、吸收差、药动学参数不理想和药物间存在相互作用等,时常需要一天服用多次或较大剂量来保持有效血药浓度,导致药物毒副作用大[6]。与非氘代药物相比,氘代药物具有明显的优势:(1)能够引起血液内的药物消除速度降低,从而延长药物在体内的半衰期,有利于减少用药剂量,降低药物代谢负担;(2)改变药物代谢和改善药代动力学性质,有效地降低药物代谢速度,提高生物活性、临床疗效;(3)降低药物在进入血液前的代谢速率(例如在肠道中),有助于让更多未代谢的药物进入血液循环,降低其副作用、延缓耐药性到来[7-11]。2017年,美国食品药品监督管理局(FDA)批准了全球首个氘代药物,梯瓦公司的氘代丁苯那嗪片(Deutetrabenazine,安泰坦)上市,用于治疗罕见的常染色体显性遗传病亨廷顿舞蹈病[12],该药物可以有效延缓其在体内的药动曲线,且对于亨廷顿舞蹈病和迟发性运动障碍上有显著的治疗效果与可接受的安全性和耐受性。2020年5月,国家药品监督管理局(NMPA)也在优先审评审批后,免于临床试验批准了该药进口和在中国上市。
经过近几年的快速发展,氘代化在药物中的研究已经取得了一些进展[6,13-14]。考虑到心脑血管疾病具有高患病率、高致残率和高死亡率等特点,开发抗心血管疾病氘代药物无疑会给人类带来福音,同时对于开发新药具有重大意义。本文将按不同药理作用药物分类来简述近年来抗血管疾病氘代药物的合成进展。
1 抗高血压药
盐酸埃他卡林(IptakalimHydrochloride)作为一种新型的抗高血压药物,可以有效的扩张动脉,近年来还有研究表明该药对脑神经,肾脏及肺部亦有一定的保护作用[15-16]。但由于盐酸埃他卡林化学结构中并无共轭体系或生色基团,因此常规的检测方法难以测定药物浓度。张城等[17]以2,3-二甲基-2-丁烯(1)为底物,在混酸的催化下与尿素搅拌反应生成2,3-二甲基-2-丁脲(2),然后在碱性环境下水解生成丁胺(3),最后与溴代异丙烷-d7化合物(4)缩合生成氘代盐酸埃他卡林(5)(图1)。此外,张振清课题组[18]以氘代盐酸埃他卡林为内标物,通过GC-MS研究了该药物的药代动力学性质,表明大鼠和比格犬服药后均表现为一级吸收二房室模型,药代动力学参数均无显著性差别。
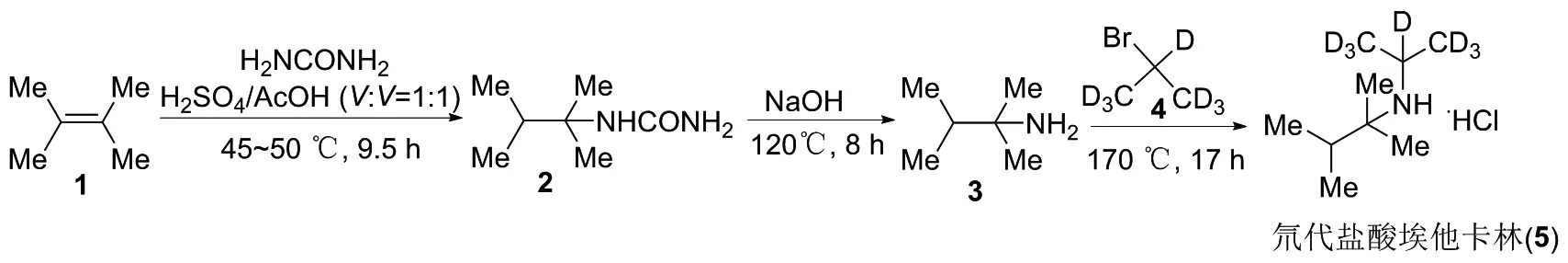
图1 盐酸埃他卡林的合成路线
2 血脂调节药物
2.1 依替米贝
依替米贝(Ezetimibe)又称伊折麦布,是一类新型的选择性胆固醇吸收抑制剂,目前已被批准上市,在临床中主要用于治疗高血脂症所引起的冠心病。陈礼勤课题组[19]为了辅助观察并检测药物在体内的代谢情况,同时进一步开拓更多的药物结构,在原有药物的1个苯环上引入了4个氘原子,从而合成了含有4个氘原子的依替米贝-d4,该项研究以4-苄氧基苯甲醛、4-氟苯胺和氟苯-d5为起始原料,经过大小12步反应,最终成功合成出含有4个氘原子的依替米贝-d4。具体合成路线如下(图2):首先4-苄氧基苯甲醛(6)和4-氟苯胺(7)缩合形成N-(4-氟苯基)-4-苄氧基苯亚甲胺(8);化合物8在LDA的作用下与(S)-3-羟基-γ-丁内酯(9)反应,得到(3R,4S)-N-(4-氟苯基)-3-[(1S)1,2-二羟基乙基]-4-(4-苄氧基苯基)-2-氮杂环丁酮(10);化合物10在高碘酸钠的作用下,氧化生成相应的醛(11);此外,五氘代氟苯(12)在三氯化铝的作用下发生傅克酰基化反应,得到对氟-四氘代苯乙酮(13),然后形成相应的烯醇硅醚(14)。化合物11和化合物14在三氟化硼乙醚的作用下,发生Aldol反应,得到(3R,4S)-N-(4-氟苯基)-3-[3-(4-氟-四氘代苯基)-1-羟基-3-羰基丙基]-4-(4-苄氧基苯基)-2-氮杂环丁酮(15);化合物15在对甲基苯磺酸的催化下发生分子内脱水反应,得到相应的(3R,4S)-N-(4-氟苯基)-3-[3-(4-氟-四氘代苯基)-3-羰基丙烯基]-4-(4-苄氧基苯基)-2-氮杂环丁酮(16);化合物16在三苯基膦氯化铑的催化下,发生选择性氢化还原不饱和双键,得到(3R,4S)-N-(4-氟苯基)-3-[3-(4-氟-四氘代苯基)-3-羰基丙基]-4-(4-苄氧基苯基)-2-氮杂环丁酮(17);化合物17在手性催化剂Cat.1的催化下,发生不对称还原,得到(3R,4S)-N-(4-氟苯基)-3-[3-(4-氟-四氘代苯基)-3(S)-羟丙基]-4-(4-苄氧基苯基)-2-氮杂环丁酮(18),最后化合物18用Pd/C脱苄,得到目标药物依替米贝-d4(19)。
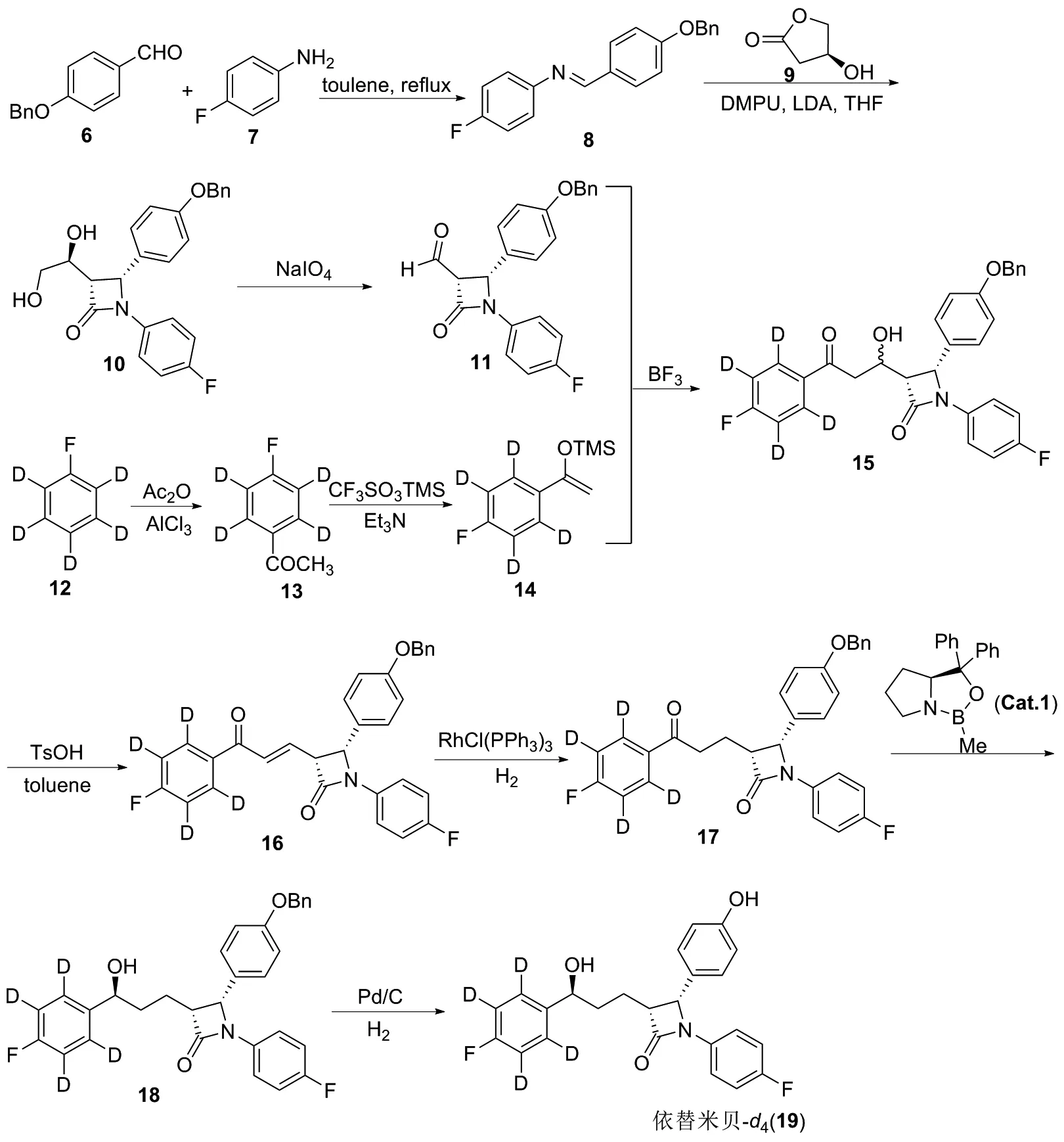
图2 氘代依替米贝的合成路线
2.2 阿托伐他汀
阿托伐他汀(Atorvastatin)又称立普妥,是一种知名的血脂调节药物,其有效成分为阿托伐他汀钙盐,主要用于治疗高胆固醇血症以及混合型高脂血症,也可用于预防高血压、冠心病等心血管疾病。2016年,李文保课题组[20]在经典药物的基础上,研究合成了氘代阿托伐他汀钙的路线,希望通过氘代的方式来改善阿托伐他汀在人体内的代谢。具体合成路线如下(图3):首先异丁酰乙酸甲酯(20)和苯胺(21)发生酰胺化反应,得到酰胺化产物(22);化合物22和苯甲醛发生缩合反应,得到化合物(23);23在卡宾的催化下与对氟苯甲醛反应,得到化合物(24);24和伯胺(25)发生环化反应得到阿托伐他汀酯(26);最后,26发生水解,并与醋酸钙成盐,得到阿托伐他汀钙(27)。
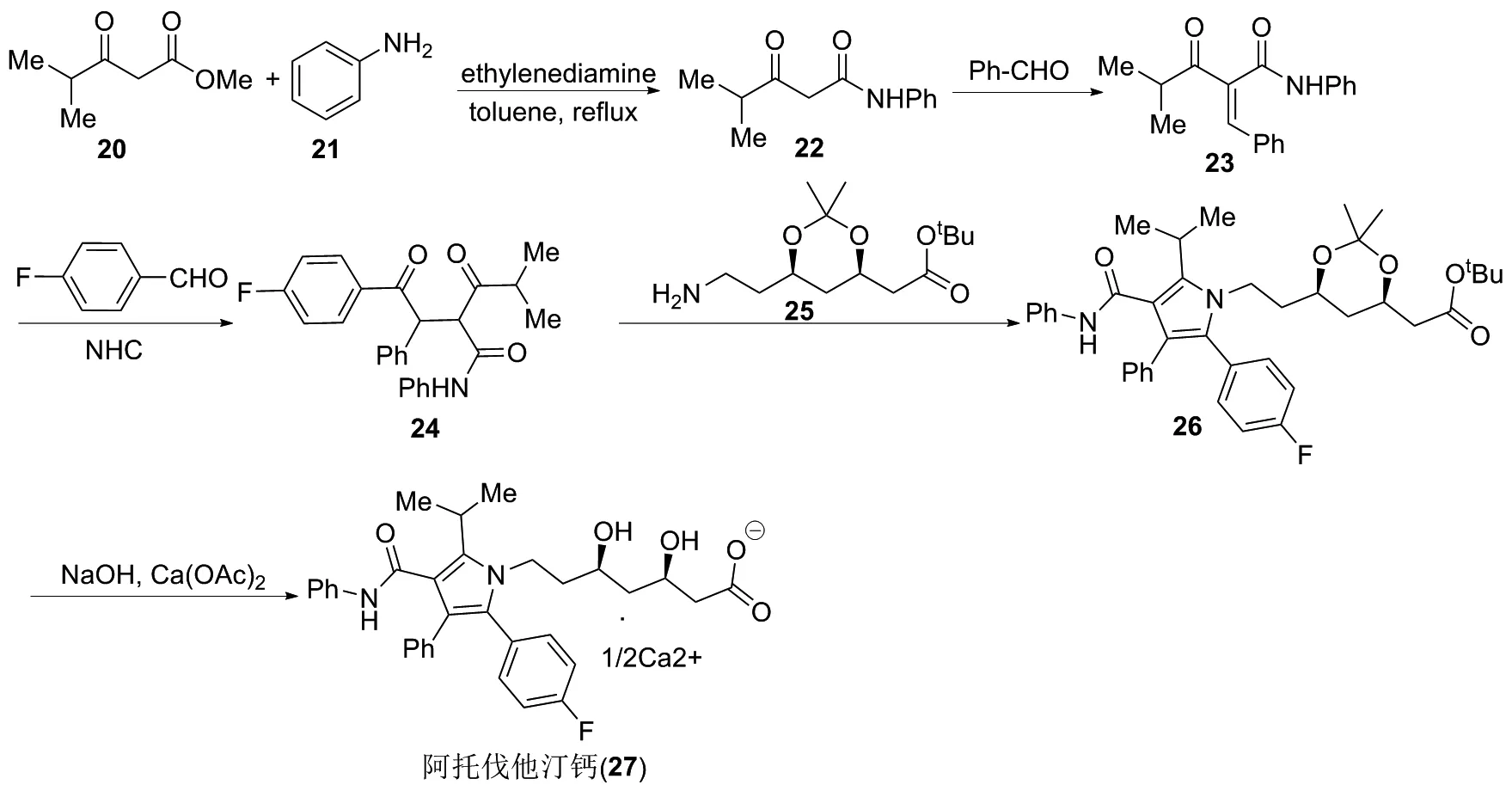
图3 阿托伐他汀钙的合成路线
根据图3所示的合成路线,将原料苯胺换成苯胺-d5,就可以合成氘代阿托伐他汀钙(28);同样的合成步骤,将苯甲醛用苯甲醛-d5代替,也可以氘代阿托伐他汀钙(29);用氘代对氟苯甲醛代替对氟苯甲醛,就可以得到氘代阿托伐他汀钙(30),如图4所示。如果同时使用2/3种氘代原料,就可以得到多种氘代阿托伐他汀钙。
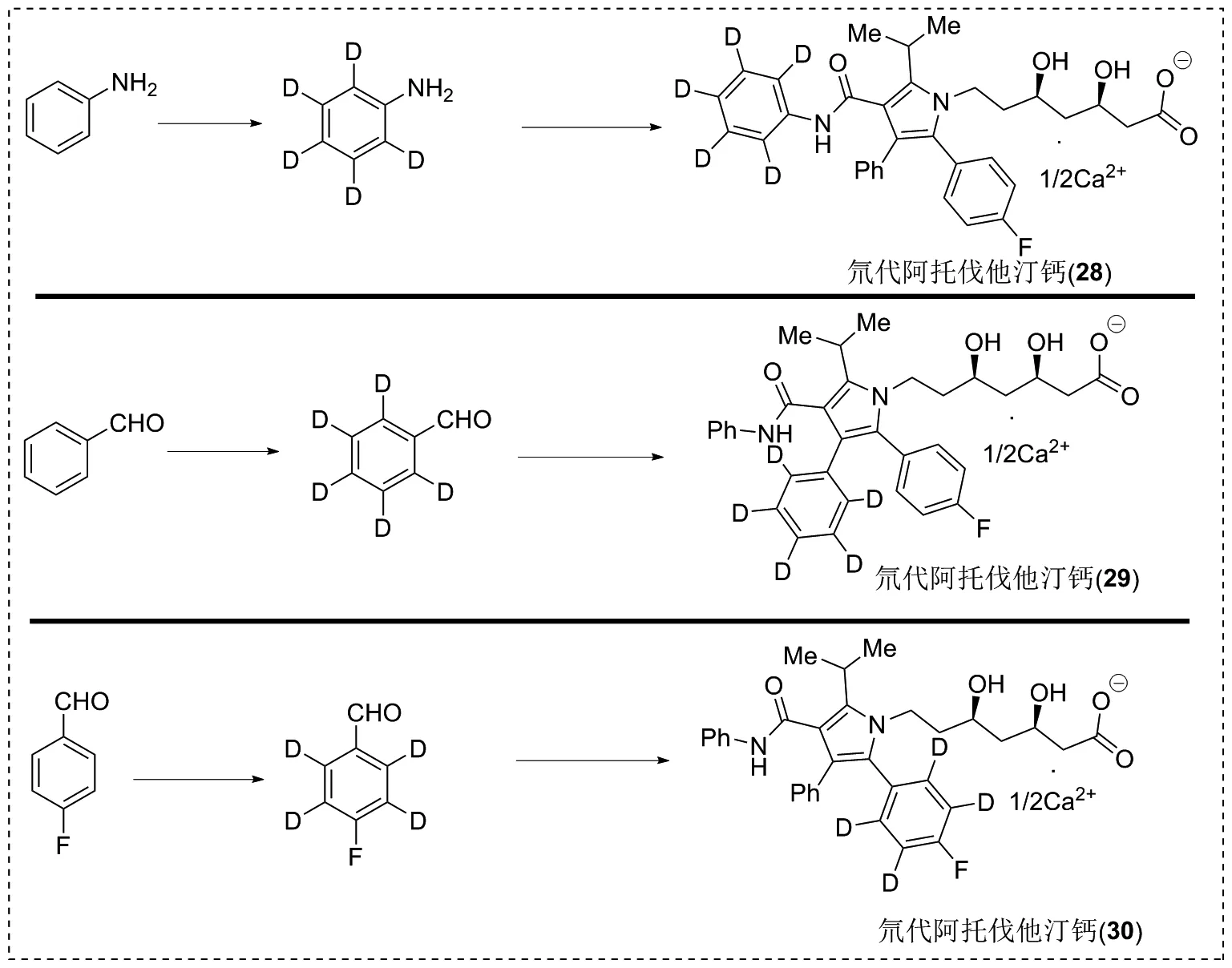
图4 氘代阿托伐他汀钙的合成路线
3 抗凝血药物
3.1 氯吡格雷
氯吡格雷(Clopidogrel)是一种血小板抑制剂,可以选择性的抑制ADP与血小板受体的结合,从而抑制血小板的凝集,最终达到减少血栓形成的可能,目前在临床中主要用于预防以及治疗冠心病。但近日的临床研究表明,该药药效性质受生物活化及代谢效率影响明显,在受试者之间表现出较大的差异性[21]。为了解决药物的代谢稳定性和忍耐性,焦波课题组[22]通过在原药的基础上设计合成了氘代氯吡格雷。具体合成路线如下(图5):首先噻吩乙酸甲酯(31)在甲醇钠和氘代甲醇的作用下,发生氢氘交换反应,得到噻吩乙酸甲酯-d2化合物(32);化合物32用氘代硼氢化钠还原,得到氘代化合物(33);33在三乙胺的作用下与对甲基苯环酰氯反应得到化合物(34);34和(S)-2-氨基-2-(2-氯苯基)乙酸甲酯(35)反应,得到胺化产物(36);最后化合物36和多聚甲醛发生环化反应,得到氯吡格雷-d4(37)。
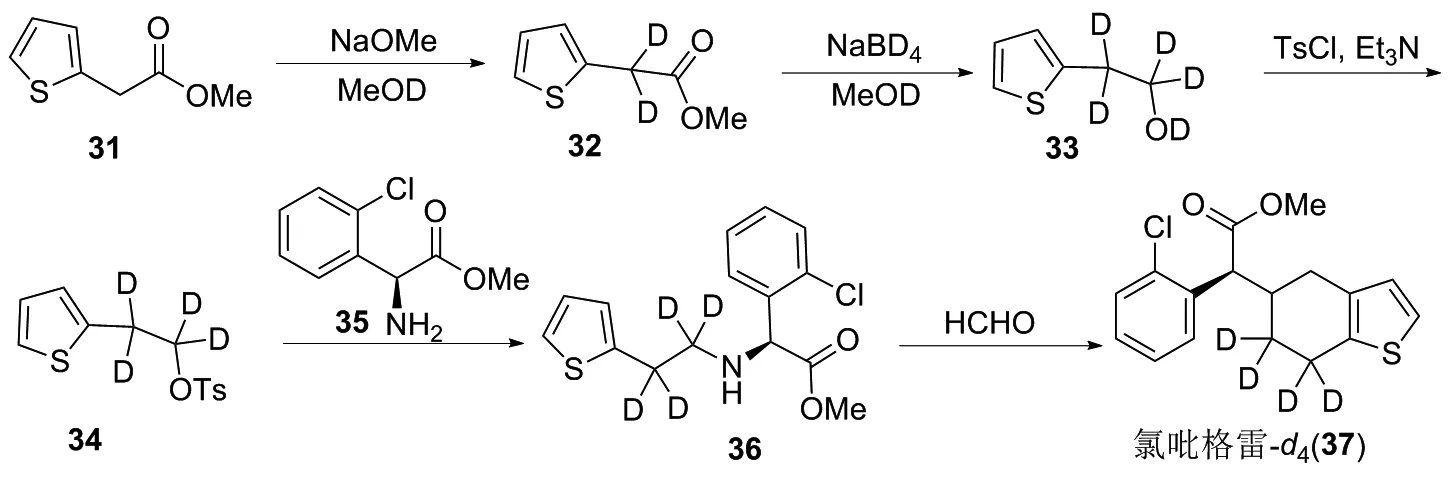
图5 氘代氯吡格雷的合成路线
3.2 替格瑞洛
替格瑞洛(Ticagrelor)同样是一种常用的抗心血管血栓药物,主要用于急性冠脉综合征(不稳定性心绞痛、非ST段抬高心肌梗死或ST段抬高心肌梗死)患者。替格瑞洛一般作为对氯吡格雷抵抗患者的替代疗法,但替格瑞洛相对氯吡格雷来说,其半衰期明显较短,通常替格瑞洛1天需要服用2次,而氯吡格雷只需1天1次,所以延缓替格瑞洛的体内代谢正是目前主要攻克目标之一。2020年,车金鑫等[23]为解决替格瑞洛半衰期短的问题,设计并合成了氘代替格瑞洛,且通过试验表明氘代化减缓了药物的代谢速率且改善了药物的药代动力学特性。具体合成路线如下(图6):首先氘代乙二醇(38)和苄溴反应,生成化合物(39);39在四溴化碳和三苯基膦的作用下,得到溴化产物(40);40和氨基醇衍生物(41)发生亲核取代反应,得到化合物(42);42在钯碳催化下发生氢化脱苄反应,得到氘代氨基醇衍生物(43);化合物43和4,6-二氯-5-氨基嘧啶化合物(44)发生亲核取代反应,得到化合物(45);45在Na2NO2和醋酸的作用下发生重氮化反应,得到氘代三氮唑嘧啶(46);最后46和(1R,2S)-2-(3,4-二氟苯基)环丙胺(47)发生亲核取代反应,得到氘代替格瑞洛。根据氘代取代基的不同,分别可以得到替格瑞洛-d4化合物(48),替格瑞洛-d5化合物(49)和替格瑞洛-d11化合物(50)。
3.3 沃拉帕沙
沃拉帕沙(vorapaxar)是在一种从木兰科植物Galbulimimabaccata树皮中提取分离的生物碱喜巴辛的基础上修饰研发而成的药物,具有抑制凝血酶受体的药理作用,通常用于心脏病发作或动脉堵塞的患者,以降低心脏病进一步发作、中风等死亡危险。2018年,张寅生等[24]为满足临床样品检验分析的需要,直接以沃拉帕沙(51)为原料,通过在高温加热与氘代浓硫酸进行氢氘交换反应,合成了氘代沃拉帕沙(52),如图7所示。
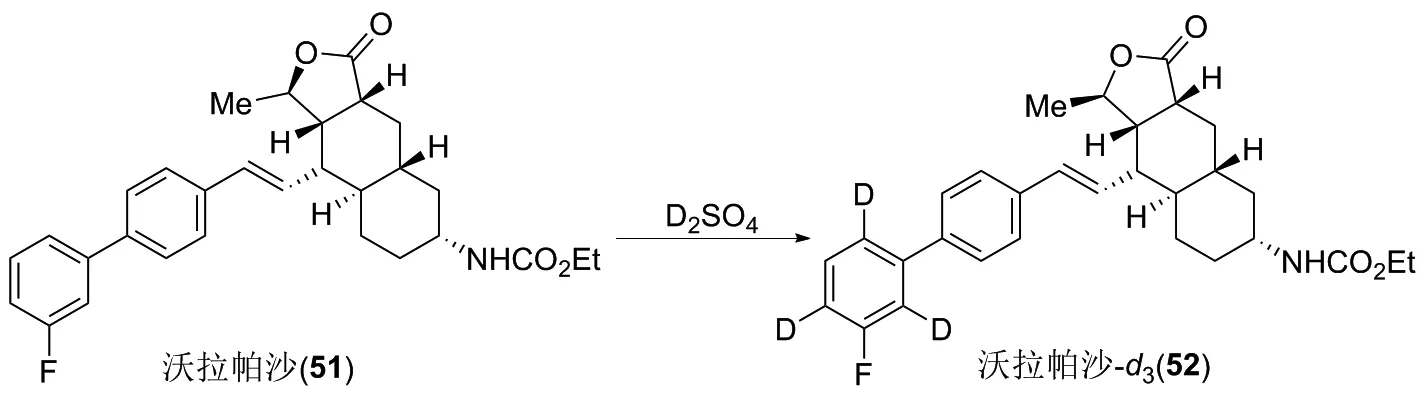
图7 氘代沃拉帕沙的合成路线
3.4 洛沙坦
洛沙坦(LosartanPotassium)是第1个上市的非肽类血管紧张素Ⅱ受体拮抗剂。洛沙坦不仅能够有效的拮抗血管紧张素Ⅱ的受体,从而有效控制血压,还能够延缓慢性肾脏病的恶化,而且其不良反应发生率也比较低。洛沙坦于1994年首次上市,目前已在90多个国家被批准使用,用于治疗高血压。为了研究洛沙坦及其类似物的药理及药代动力学,陈礼勤课题组[25]在2012年成功合成了氘代洛沙坦,具体合成路线如下(图8):首先四氘代-4-溴甲苯(53)和1-(2-甲氧基苯基)噁唑啉(54)发生格氏反应得到氘代化合物(55);55于三氯氧磷中回流得到噁唑啉水解产物(56);56和NBS反应得到溴代化合物(57);57和咪唑衍生物(58)发生亲核取代反应得到化合物(59);59与叠氮化钠在三乙胺作用下发生反应环化,得到四氮唑产物(60);最后60用高锰酸四丁基铵氧化得到氘代洛沙坦(61)。
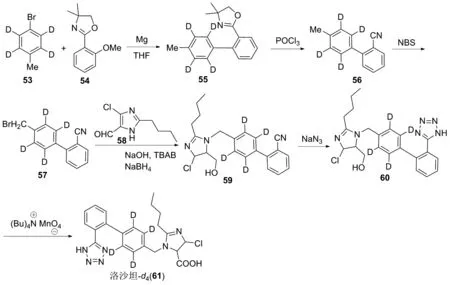
图8 氘代洛沙坦的合成路线
3.5 利伐沙班
利伐沙班(Rivaroxaban)作为一种Xa因子活性位点的选择性阻断剂,是一种新型的抗凝药物,主要用于下肢深静脉血栓、肺栓塞以及非瓣膜病的房颤的抗凝治疗,且目前副作用较小。但目前测量利伐沙班血药浓度的内标物与利伐沙班之间仍存在差异,因此在分析鉴定时仍需要更合适的内标来辅助鉴定。吴小艾课题组[26]选择以苯胺-d5为原料,经过缩合、环化、硝化、还原、取代和酰化等反应合成了氘代利伐沙班。具体合成路线如下(图9):首先五氘代苯胺(62)和2-溴乙醇发生亲核取代反应得到化合物(63);63和氯乙酰氯发生酰化反应得到化合物(64);64在碱的作用下发生分子内亲核取代环化反应得到化合物(65);65在强酸的作用下发生硝化反应得到苯环上硝化产物(66);66上的硝基用铁粉还原得到化合物(67);67和(R)-环氧乙烷衍生物发生亲核开环反应得到化合物(68);68用羰基二咪唑(CDI)关环得到噁唑酮衍生物(69);69用三氟醋酸脱去叔丁氧羰基(Boc)得到化合物(70);最后70和5-氯-2-噻吩酰氯发生酰胺化反应得到目前产物氘代利伐沙班(71)。
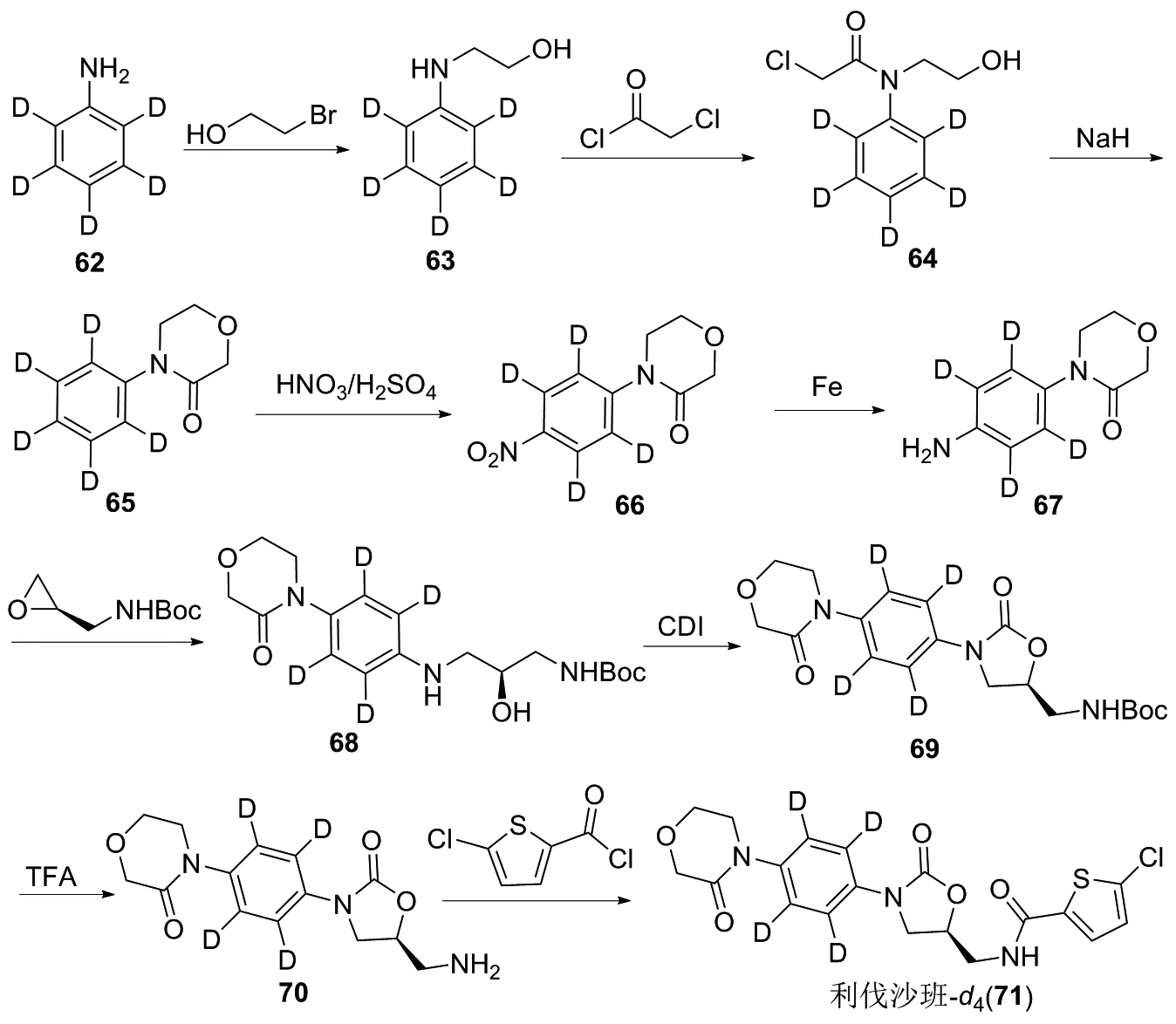
图9 氘代利伐沙班的合成路线
盐酸美西律(MexiletineHydrochloride)又叫做慢心律,实际上是一类钠通道抗心律失常的阻断剂,主要用于治疗室性早搏,对于室性早搏能起到一定的抑制作用。如果室性早搏是劳累或者其它应激因素造成,盐酸美西律可以对症进行治疗,但不宜长期使用,长期使用反而会有促心律失常,甚至有降低心功能和影响心功能的副作用。2021年,Cashman课题组[27]在盐酸美西律的基础上,设计合成了多种氘代盐酸美西律衍生物,并通过细胞实验表明氘代盐酸美西律衍生物不会改变分子的心血管特性,同时可以延长心脏动作电位。具体合成路线如下(图10):化合物(72)中的羰基用氘代硼氢化钠还原得到相应的氘代醇化合物(73);73通过光延反应得到化合物(74);74用水合肼脱去邻苯酰亚胺保护基得到相应的胺(75),最后成盐得到氘代盐酸美西律衍生物(76~79)。
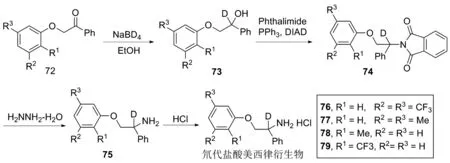
图10 氘代盐酸美西律衍生物的合成路线
氘代化合物目前已经广泛应用于生命科学、环境科学、农药残余检测和污染物跟踪等领域,在医药领域的应用也引起广泛的关注。将氘代技术应用于心脑血管疾病,得到抗心脑血管疾病氘代药物,对于研发新型的抗心脑血管疾病药物具有重要的学术意义和应用前景。然而目前合成氘标记的抗心脑血管病药物非常有限,且合成步骤冗长、成本高,极大阻碍了其商品化的进程。因此,一方面发展可商业化的氘代试剂,减少化学合成步骤,优化合成工艺,从而高效合成抗心脑血管疾病氘代药物;另外一方面,发展新型催化体系,能够在原来药物的基础上精准氘代化,无疑是发展合成抗心脑血管疾病氘代药物的最优方法,这也必将推到氘代药物的快速发展。

