海绵窦区硬脑膜动静脉瘘的介入治疗分析
于正涛 蒋俊文 李 由 李佳梦 陈焕雄 夏 鹰
硬脑膜动静脉瘘(dural arteriovenous fistula,DAVF),又称硬脑膜动静脉瘘样血管畸形,以硬脑膜内的动脉和静脉系统之间的异常分流为主要特征,占颅内血管畸形的10%~15%[1];其中海绵窦区硬脑膜动静脉瘘(cavernous sinus dural arteriovenous fistula,CS-DAVF)是最常见的类型。海绵窦具有独特的解剖结构、静脉交通丰富、引流复杂等特点,决定了CS-DAVF 供血动脉及静脉引流的多样性及治疗的复杂性。2013年1月至2023年1月介入治疗21例CS-DAVF,现报道如下。
1 资料与方法
1.1 一般资料21例中,男6 例,女15 例;年龄18~74岁。眼球突出和(或)结膜充血18例,复视3例,视力下降3例,头痛6例。
1.2 影像学资料术前完善头颅CT及MRI平扫,MRI大部分情况下可见海绵窦区异常血管流空影及眼静脉扩张表现。所有病例均行DSA 明确瘘口位置、供血动脉及引流静脉特征等,瘘口位于右侧海绵窦区4例、左侧海绵窦区16 例、双侧海绵窦区1 例;供血动脉主要包括颈外动脉系统的脑膜中动脉、颌内动脉,颈内动脉系统的脑膜垂体干及下外侧干;引流静脉主要为眼静脉。
1.3 治疗方法全麻成功后,根据脑血管造影明确的瘘的构筑特点,选择合适的入路。首先,尝试股静脉-岩下窦途径。采用Seldinger 法经皮穿刺右侧股动脉、股静脉,分别置6F 血管鞘。造影明确血管构筑后,分别更换6F 中间导引导管,在路图指引下送至病变侧颈内动脉C1 段及颈内静脉岩下窦处。如岩下窦不显影,尝试开通。全身肝素化后,分别将微导管(Echelon-14 或-10)及微导丝送入静脉的6F中间导管内。根据血管构筑,采用双微导管在路图指引下分别将微导管尖端经岩下窦送入扩张的眼静脉处及海绵窦内近瘘口处。造影确认后,先经微导管送入若干合适的弹簧圈,填塞达到要求后,再经微导管内注射Onyx-18 胶,反复造影评估栓塞情况及静脉引流情况,直到栓塞满意。
若经股静脉-岩下窦入路失败,根据瘘的供血动脉情况,可以考虑经动脉入路。更换6F中间导引导管,在路图指引下送至病变侧颈外动脉系统(首选脑膜中动脉)或颈内动脉C1 段。全身肝素化后,分别将微导管(Marathon 或Echelon-14/10)及微导丝送入6F 中间导管内。在路图指引下分别将微导管尖端送入接近瘘口的动脉近端或海绵窦内,单用Onyx-18 胶或联合弹簧圈栓塞,栓塞过程中避免胶逃逸所致的颈内动脉系统栓塞。必要时采用动静脉联合入路进行栓塞瘘口,可采用多微导管技术。
1.4 疗效及预后评价术后即刻和随访造影评价栓塞效果:完全栓塞,瘘口及引流静脉全部消失;次全栓塞,只有小的残存分流而流量和流速明显减小;部分栓塞,大的残存分流而流量和流速仅轻微减少或无变化。预后评价根据临床症状评估,包括治愈、好转、无效和加重。
2 结果
2.1 治疗结果21例中,经股静脉-岩下窦途径治疗16例,其中岩下窦未显影6例;经颈外动脉入路4例,其中脑膜中动脉2 例,颌内动脉2 例;动静脉联合入路1 例。采用弹簧圈联合Onyx-18 胶栓塞17 例,单纯应用弹簧圈1例,单用Onyx-18胶3例。术后即刻造影显示瘘口完全闭塞18例(图1),次全闭塞3例。出院时,21例临床症状得到不同程度的缓解,未见原发症状加重。术后早期出现轻度头痛及复视2 例,对症处理后好转。
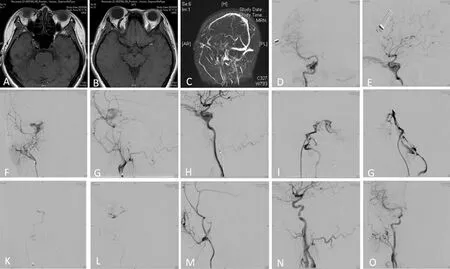
图1 右侧海绵窦区硬脑膜动静脉瘘经颈外动脉-颌内动脉入路栓塞治疗前后影像
2.2 随访结果21例术后随访3~12 个月,突眼及结膜充血症状均缓解,1例术前视力受损严重病人未见恢复;临床治愈17例,好转4例。15例复查造影未见瘘口复发。
3 讨论
海绵窦骑跨中线两侧,颈内动脉走形于海绵窦内,发出脑膜垂体干及下外侧干,参与硬脑膜的供血;颈外动脉系统的脑膜中动脉海绵窦支、脑膜副动脉卵圆孔支、咽升动脉上咽支及颌内动脉等也参与硬脑膜的供血;海绵窦的血供可以来自双侧,且颈内动脉与颈外动脉经常发生“危险吻合”。海绵窦向前与眼眶内的眼上静脉、眼下静脉沟通,向外侧与蝶顶窦、大脑中前静脉沟通,向后与岩上窦、岩下窦和基底静脉沟通,向内与垂体静脉沟通,向下经导静脉与翼丛沟通。此外,海绵窦内分隔明显。这些独特的解剖结构及引流的多样性,决定了CS-DAVF血管构筑的复杂性。CS-DAVF常见的血管结构包括:单侧病变,同侧或对侧单一引流;单侧病变,双侧引流;间窦病变,单侧或双侧引流;双侧病变,单侧引流或双侧相互引流或各自单独引流。目前,血管内治疗治愈率高、并发症发生率低,仍是治疗CS-DAVF 的首选,成功的关键是选择合适的血管内治疗入路,常用的入路包括经动脉入路、经静脉入路或动静脉联合入路。
经静脉入路能使栓塞导管直接进入海绵窦内并最大可能贴近瘘口,是治疗CS-DAVF最安全及最常用的方法,其中经岩下窦路径短、疗效确切是静脉入路的首选[2]。然而,近半数病人的岩下窦常常不显影或重度狭窄,增加了手术难度和风险,故岩下窦再通是手术成功的关键。Rhim等[3]回顾性分析49例岩下窦闭塞的CS-DAVF,岩下窦开通率为54.3%。Cho等[4]采用导引导管放置预判岩下窦开口处,利用微导管及导丝头端成袢技术开通病变同侧岩下窦,再通率达80%。陈圣攀等[5]总结44 例岩下窦未显影的CS-DAVF,依据岩下窦的解剖结构特点,应用泥鳅导丝反复探查的方法,使40 例成功经股静脉-岩下窦入路栓塞,未显影岩下窦探查打通成功率为90.9%。朱廷准等[6]采用逆行静脉窦造影,选用稍硬微导丝携带小球囊对闭塞岩下窦尝试开通,也获得了良好的效果。本文岩下窦不显影6 例,我们采用经动脉造影获得静脉期及窦期路径图,预判岩下窦开口,将6F导引导管放置在预判岩下窦向颈内静脉汇入的开口处,通过多功能导管及泥鳅导丝尝试进入岩下窦,如导丝进入顺利,5F 多功能造影导管进入顺利后,导引导管跟入提供支撑,再进行交换微导管到位;或者直接采用PT2导丝及微导管开通,其中5例(83%)成功开通,1例虽岩下窦开通,但微导管无法通过海绵窦分隔到达近瘘口处,而改为经颌内动脉栓塞。如同侧岩下窦开通困难,在对侧岩下窦开放良好且海绵间窦发育良好的情况下,可以尝试跨海绵间窦栓塞瘘口。文献报道经眶穿刺海绵窦入路[7]、眼静脉入路等也可行,但是穿刺风险及相关并发症发生率较高,临床应用仍相对较少。
在岩下窦开通困难而其他静脉入路技术不成熟的情况下,经动脉入路也值得尝试。结合文献报道及我们经验,经脑膜中动脉或颌内动脉最常见,血管路径相对较好,更容易接近瘘口,但在栓塞过程中警惕累及脑膜中动脉岩支,避免引起面听神经功能障碍。脑膜垂体干及咽升动脉[8]路径也有文献报道,但路径较短,存在危险吻合,有颈内动脉系统及视网膜动脉栓塞的风险,为非常规入路。在病例选择上,建议选择具有脑膜中动脉分支供血,更容易到达瘘口的病例。在条件允许的情况下,建议采用球囊保护,增加栓塞的安全性。
由于海绵窦区解剖及血流动力学特点,双微导管技术可以显著提高CS-DAVF的治愈率[6]。如经岩下窦路径,我们根据血管构筑特征使用双微导管技术,一条微导管尖端送入眼静脉处,另一条送入海绵窦内近瘘口处进行有序精准栓塞治疗。De Castro-Afonso 等[9]回顾性分析62 例CS-DAVF 的临床资料,比较使用弹簧圈或胶栓塞的临床预后,结果发现与单纯使用弹簧圈相比,经静脉栓塞使用弹簧圈联合胶栓塞有更高的闭塞率,且不增加并发症发生率。黄磊等[10]报道经静脉途径应用Eval胶联合弹簧圈栓塞治疗CS-DAVF,完全闭塞率为100%,并发症较少。朱廷准等[6]建议尽量采用弹簧圈联合Onyx胶的方式栓塞瘘口,既可以提供良好的铸型又可限制胶的弥散。本文病例中,单纯应用弹簧圈1例,单纯应用Onyx胶4例,弹簧圈联合Onyx胶16例。通常情况下,首先在扩张的引流静脉汇入海绵窦开口处使用3D 弹簧圈成篮,根据需要再决定放入3D 或2D 弹簧圈,达到一个满意的填塞效果后,再通过微导管缓慢注胶,术中双C臂实时关注栓塞情况,瘘口消失后停止注胶,避免栓塞过度所致的胶逃逸及尽量保留海绵窦生理结构,避免海绵窦完全闭塞。
总之,对CS-DAVF,根据海绵窦区的解剖结构及血流动力学特点,选择个体化的血管内治疗方法,可取得良好的疗效,其中经岩下窦途径适合于大部分CS-DAVF,为首选;如经岩下窦入路失败,可考虑经动脉或其他静脉入路。双微导管的使用、必要情况下球囊辅助以及弹簧圈和Onyx-18 的联合使用,可增加治愈率和栓塞的安全性。同时,尽可能保留海绵窦的生理结构,避免过度栓塞,对减少术后并发症也非常重要。

