湖北省儿科头孢菌素用药安全性主动监测研究*
赵丽,蔡沅璇,赵宇航,上官小芳,彭月,李康玲,杨林慧,黄锐
[1.湖北省药品(医疗器械)不良反应监测中心,武汉 430070;2.华中科技大学同济医学院药学院,武汉 430030;3.武汉科技大学医学院药学系,武汉 430065;4.南昌市医疗保障局,南昌 330038]
据相关报道显示,全球每年有上千万0~5岁的儿童死亡,而其中2/3儿童死于用药不当[1],儿科用药安全问题不容忽视。儿科用药指专门针对儿童(0~14岁)患者群体设计生产的药品[2]。由于儿科用药临床试验过程复杂、试验数据准确性不理想、涉及伦理道德和法律责任等问题直接导致儿科用药研发动力不足以及临床试验开展困难[3]。而药品本身在发挥药效治疗疾病的同时,也存在伤害机体的风险,即发生药品不良反应(adverse drug reaction,ADR)[4]。为破除儿科用药面临的困境,必须持续地密切监测上市后儿科用药情况,在真实世界中对儿科用药进行上市后安全性再评价,以期降低用药风险,保障儿童用药安全。本文前期以湖北省药品(医疗器械)不良反应监测中心2014年1月—2019年12月药品不良反应数据为源数据库,对0~14岁儿童ADR报告进行全面分析与评价。结果显示多种头孢菌素类药品位于高风险药物行列,引起严重ADR的数量较多,故初步将头孢菌素类药物纳入目标药物候选集。再采用比例失衡法对头孢菌素类报告进行风险信号挖掘,选取头孢他啶、头孢孟多酯钠及头孢哌酮/舒巴坦钠作为本次儿科用药监测目标药物[5]。综合考察湖北省各医院目标药物的实际使用频次以及儿童就诊数量,选取湖北省内7家医疗机构进行目标药物重点监测。
1 资料与方法
1.1研究设计 本研究采用前瞻性、药源性、多中心主动监测模式,采取登记的研究方法将在监测时间内使用特定药品的患者列成清单,使用标准化的调查表搜集信息。根据国际通用“三例原则”,在基线ADR发病率为1/1000 的水平时,监测到1 个ADR所需要的样本量为3000例,通过对说明书研究,预期不良反应发生率在0.1%~10%,故单个药物纳入监测病例>3000 份。对其中涉及的ADR累及系统-器官及临床表现对照《世界卫生组织不良反应报告术语集(2015)》进行标准化阐述和分类。本研究经华中科技大学同济医学院医学伦理委员会审核通过,批件号[2020]伦审字(S304)号。
1.2资料纳入与排除条件
1.2.1资料纳入条件 利用预先嵌入目标药物监测卡的中国药物警戒系统,获取2020年1月1日—2021年8月31日在华中科技大学同济医学院附属协和医院、武汉儿童医院、湖北民族大学附属民大医院、武汉市第三医院、十堰市太和医院、荆门市第二人民医院、黄石市中心医院7家医院使用过头孢哌酮/舒巴坦钠、头孢他啶、头孢孟多酯钠,且入院时年龄≤14岁的住院患者信息。住院患者在监测时限内从开始入院至出院作为一份病例。
1.2.2资料排除条件 ①指标异常:包括指标缺失、基值异常、基线信息缺失过多;②肿瘤癌症;③未使用头孢哌酮/舒巴坦钠、头孢他啶、头孢孟多酯钠任意一种;④年龄>14岁。
按照以上条件,共收集患儿资料8249份,其中涉及到头孢他啶3888例,头孢孟多酯钠3053例,头孢哌酮/舒巴坦钠1308例。
1.3统计方法
1.3.1描述性分析 从系统中导出符合条件的病例数据,剔除重复病例以及双人核查缺失重要信息过多数据,形成可用于分析的数据集。计量资料通过均数(Mean)、标准差(Std)进行描述;计数资料分析则使用例数(n)以及百分数(%)。
1.3.2单因素和多因素分析 采用SPSS 25.0版软件及Microsoft Excel(2019)完成数据处理工作和相关统计学分析。计量资料采取t检验,计数资料采取卡方检验或Fisher 精确检验进行单因素分析。多因素分析采用二元Logistic回归分析,计算比值比(odds ratio,OR)值与95%置信区间(confidence interval,CI),获取ADR发生的风险因素。并采用Omnibus Tests和Hosmer and Lemeshow Test 评价模型整体情况和拟合优度,以P<0.05为差异有统计学意义。
2 结果
2.1基本情况 8249份监测病例中,男4974例(60.30%),女3275例(39.70%),男女比为1.52:1。患儿集中在婴儿期与学龄期,患者数量共4605例(55.82%),青春期患儿数量最低,仅361例(4.38%)。见表1。8249份病例中有既往疾病944例(11.44%),明确既往ADR者 557例(6.75%)。

表1 患者的基本人口统计学信息
2.2用药情况
2.2.1给药途径与溶媒 给药途径多为静脉给药,共有7719例,占93.57%。静脉途径包括静脉注射、静脉滴注、静脉泵入等多种方式。头孢他啶药物静脉途径给药比例最高,为3840例 (98.77%)。
2.2.2给药频率与时长 除了2506例用药情况为临时给药及36例给药频率不详之外,多数患儿给药频率为一日2次(4184例,50.72%)或一日1次(937例,11.36%)。从用药时长来看,3种药物时长多在3~7 d,其中头孢孟多酯钠共1813例(59.38%),头孢哌酮/舒巴坦钠共1113例(85.09%),头孢他啶3383例(87.01%)。
2.2.3单次给药量与溶媒 头孢孟多酯钠单次给药量主要为1 g(1096例),依次是2 g(408例),0.5 g(373例);头孢哌酮/舒巴坦钠单次给药量主要为1 g(97例),依次是1.5 g(77例),0.5 g(74例);头孢他啶单次给药量主要为1 g(505例),依次是0.5 g(415例),2 g(183例)。单位体质量给药量为(51.20±28.37) mg·kg-1。头孢菌素类药物单次给药量比较分散,这可能与说明书推荐用量是根据体质量来进行计算有关。溶媒类型最多为0.9%氯化钠注射液和5%葡萄糖注射液(6952例,84.28%),同时也是头孢哌酮/舒巴坦钠与头孢他啶说明书中的推荐溶媒类型。
2.2.4推荐用量 根据说明书内容,头孢孟多酯钠儿童患者推荐用量为50~100 mg·kg-1·d-1;头孢哌酮/舒巴坦钠为40~80 mg·kg-1·d-1,5%葡萄糖注射液或0.9%氯化钠注射液50~100 mL;头孢他啶为30~100 mg·kg-1·d-1,5%葡萄糖注射液或0.9%氯化钠注射液100 mL。以此为基准,对比可知头孢孟多酯钠符合推荐用量的比例最高,达86.72%。见图1。
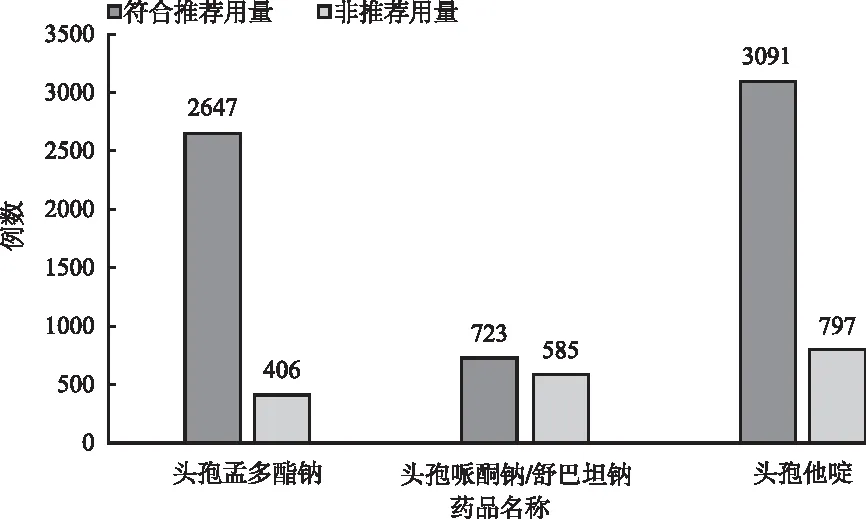
图1 药物是否超量使用例数分布图
2.2.5联合用药 8249份病例资料中共有7835份(94.98%)至少联合使用1种药物。其中联用3种药物情况最常见,共3497例(42.39%),≥5种有519例(6.29%)。绝大多数使用目标药物的病例都发生联合用药行为,见表2。
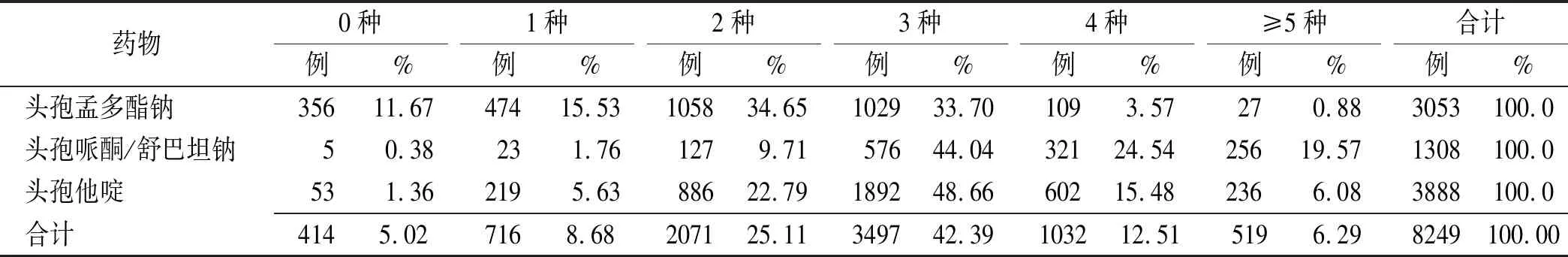
表2 3种药物的联合用药情况
2.3药品不良反应情况
2.3.1ADR发生率 8249份病例经专家咨询判定发生ADR共159例,ADR发生率为1.93%。其中头孢孟多酯钠35例,ADR发生率为1.15%;头孢哌酮/舒巴坦钠83例,ADR发生率为6.35%;头孢他啶41例,ADR发生率为1.05%。
2.3.2ADR病例基本情况 在159份ADR报告中,男95例(59.75%),女64例(40.25%),性别比例为1.48:1。发生ADR最多的年龄段为婴儿期61例(38.36%),其次为学龄前期40例(25.18%)。其中学龄期严重ADR报告比例最高,达到20%,婴儿时期比例最低为8.20%,见图2。
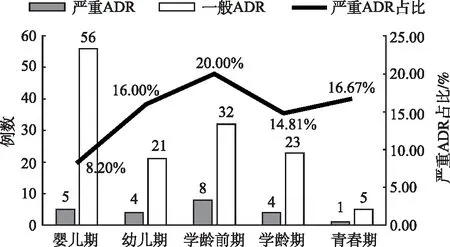
图2 不同年龄段严重ADR报告分布情况
2.3.3ADR累及器官和临床表现 159份儿童头孢菌素类ADR报告共累及11个系统-器官损害和188例次临床表现,主要为皮肤及其附件损害、全身性损害、胃肠系统损害,临床主要表现为皮疹、发热、咳嗽、血小板异常、肝酶升高等。严重ADR临床表现为高热、凝血障碍、白细胞异常、抽搐、急性荨麻疹等。见表3。

表3 159份ADR报告主要累及系统/器官损害及临床表现
其中,儿童头孢哌酮/舒巴坦钠ADR报告共83份,主要临床表现为血红蛋白浓度异常(40例)、血小板异常(12例)、皮疹(6例)和肝酶升高(5例)。儿童头孢他啶ADR报告41份,主要表现为发热(10例)、咳嗽(6例)、皮疹(5例)和感染(4例)。儿童头孢孟多酯钠ADR报告共35份,主要表现为咳嗽(13例)、发热(7例)、皮疹(6例)、肝酶升高(4例)。
2.3.4ADR病例联合用药情况 159份ADR报告中,共有155份(97.48%)至少联合使用1种药物。25例(15.72%)联合用药数量≥5种。联合用药数量为3种时ADR发生率最高,为42.77%。联合用药数量≥2种时出现严重ADR报告。见表4。
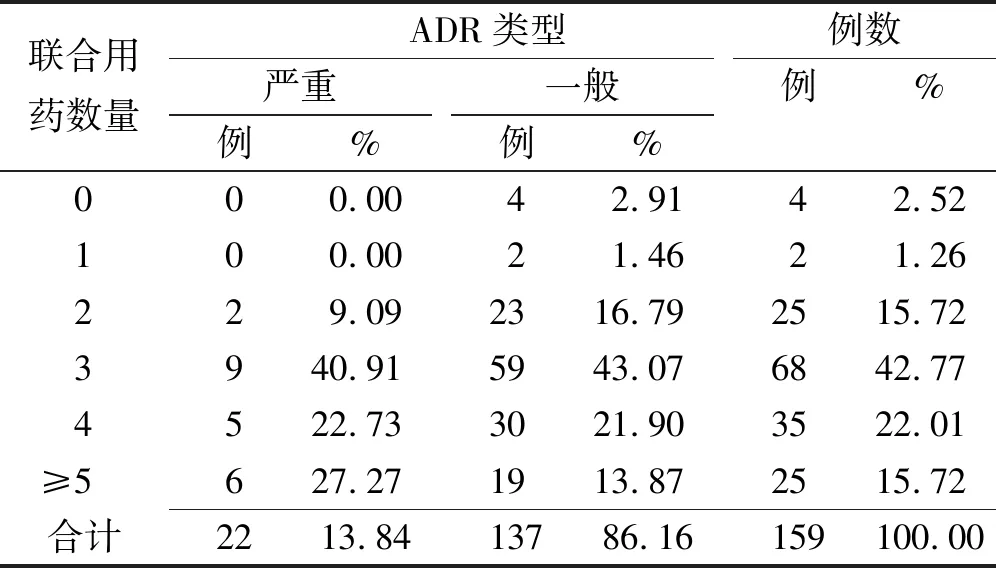
表4 159份ADR报告的联合用药信息
2.4ADR影响因素单因素分析
2.4.1患者基本情况单因素分析 将患者性别、年龄、既往疾病史等因素纳入单因素分析,发现是否发生ADR在不同年龄的分布差异有统计学意义,见表5。
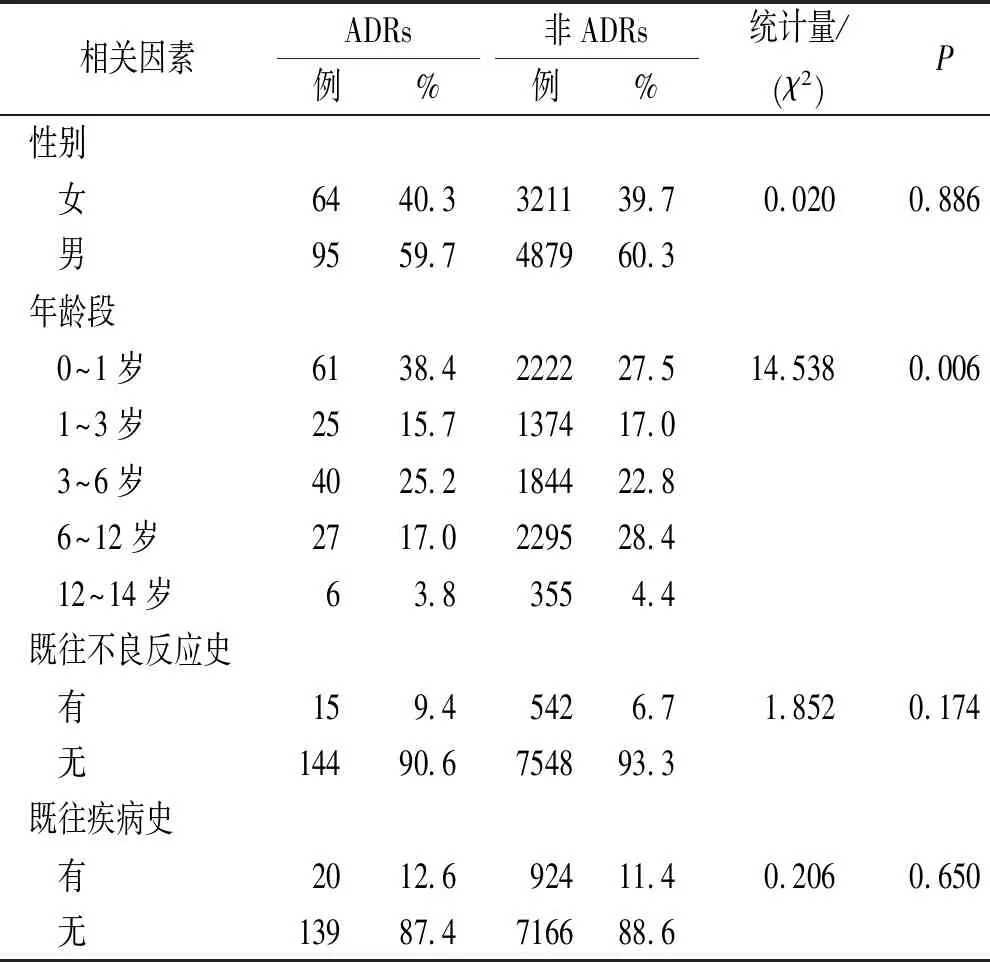
表5 ADR影响因素单因素分析(基本情况)
2.4.2患者用药情况单因素分析 将患者用药名称、给药途径、用药时长、溶媒类型、给药频率、用药浓度、合并用药数量等因素纳入单因素分析,结果发现发生ADR组与未发生ADR组在用药品种、给药途径、用药时长、是否符合推荐用量、给药频率、联合用药数量方面差异有统计学意义,见表6。
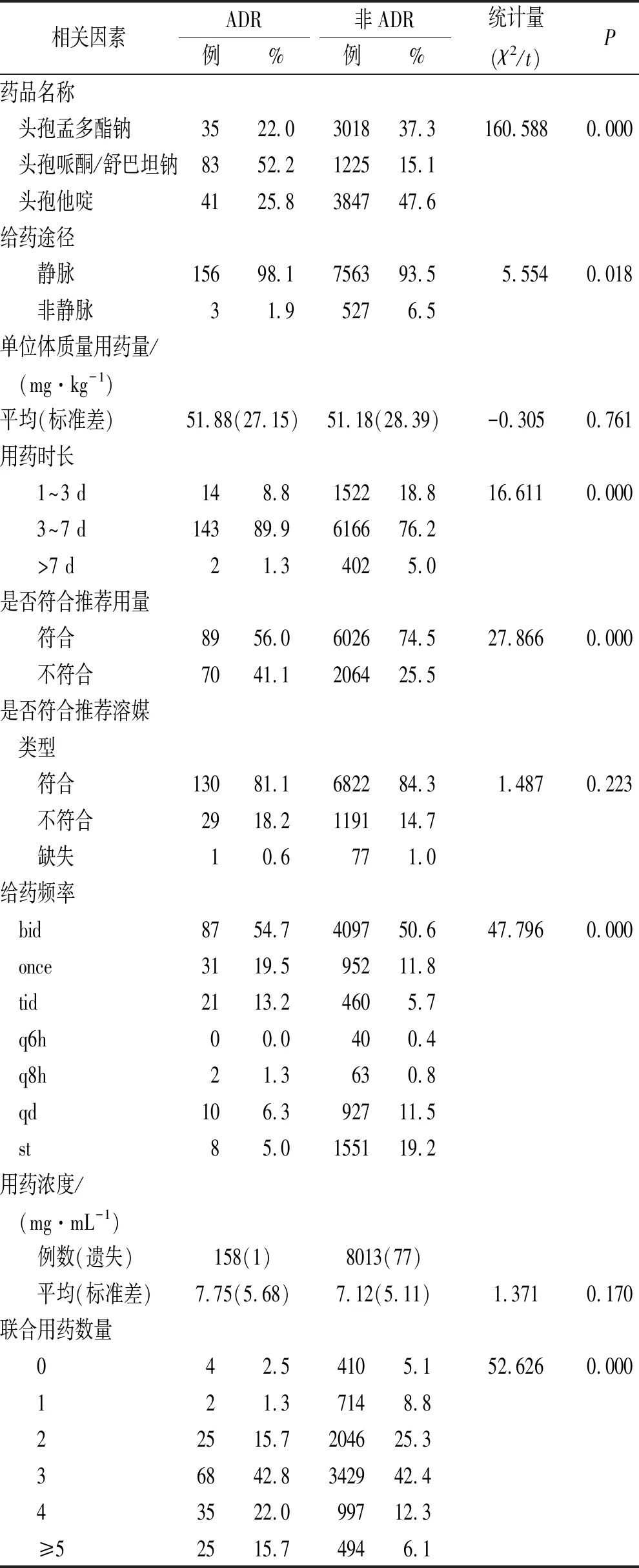
表6 ADR影响因素单因素分析(用药情况)
2.5ADR影响因素多因素分析 本研究以是否发生ADR作为因变量,以患者性别、年龄、既往疾病史、既往不良反应史、用药名称、给药途径、用药时长、给药频率、联合用药数量、单位体质量给药量、是否符合推荐用量等因素作为自变量纳入二元Logistic回归分析,结果见表7。
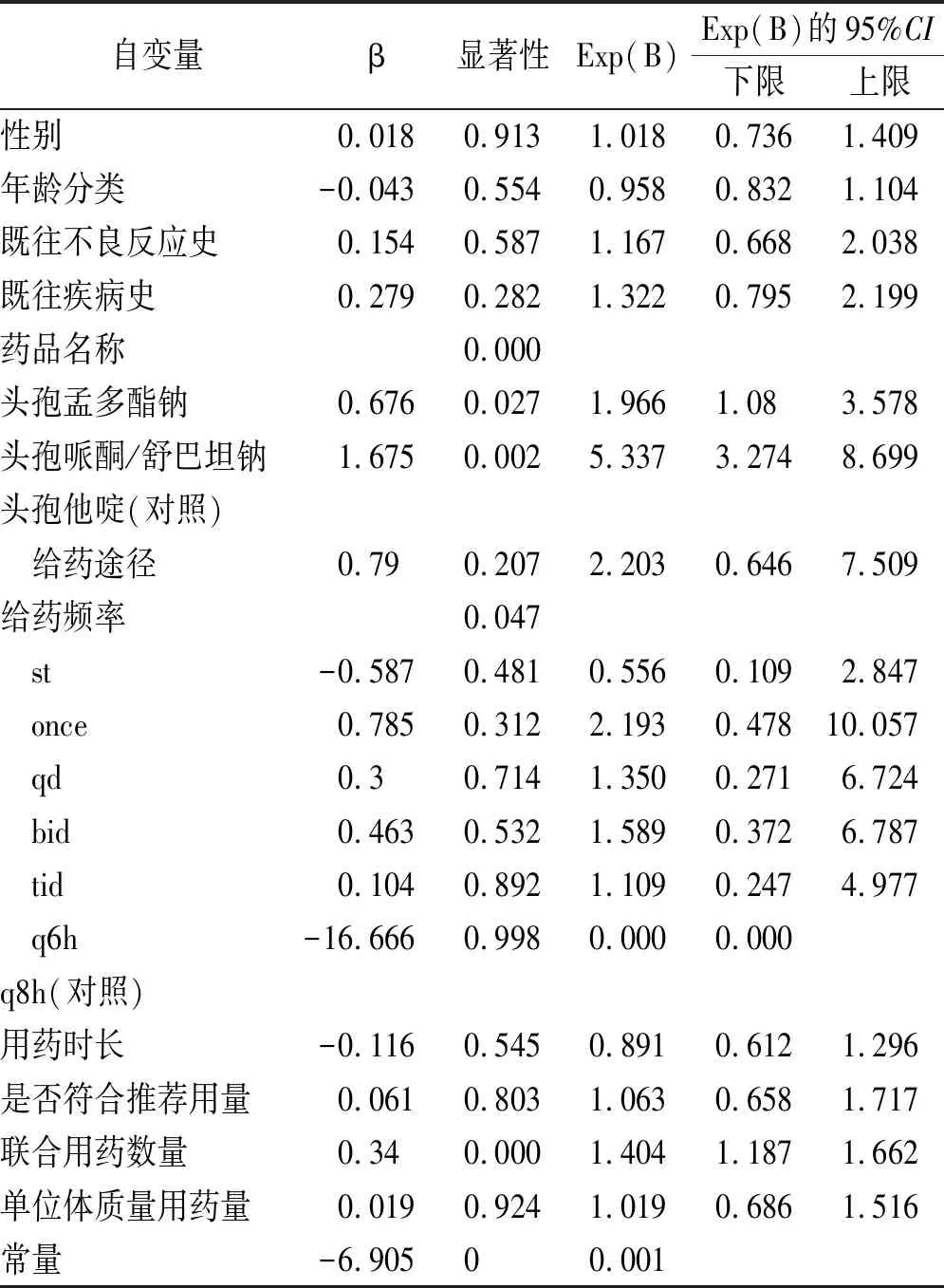
表7 ADR影响因素多因素分析
模型Omnibus 结果显示P=0.000<0.05,说明模型总体有意义。通过Hosmer and Lemeshow Test检验模型拟合优度,P=0.295>0.05,说明数据中信息提取较为充分。表7结果可知,不同药品、给药频率、联合用药数量对是否发生ADR的影响有统计学意义。从药品种类上看,头孢孟多酯钠发生ADR的风险是头孢他啶的1.966倍,头孢哌酮/舒巴坦钠发生ADR的风险是头孢他啶的5.337倍。给药频率方面,一次给药患者发生ADR的风险最高;联合用药数量对于ADR发生有促进作用。随着联合用药数量不断增加,患者发生ADR风险的概率也在不断增加。模型结果显示联合用药数量增加一种,风险发生概率增加0.4倍。
3 讨论
3.1用药品种 3种目标药物中,头孢哌酮/舒巴坦钠ADR发生率高于头孢他啶与头孢孟多酯钠。头孢哌酮/舒巴坦钠的83份ADR报告中,累及系统-器官损害最多为血液系统损害。2019年国家药品监督管理局发布《关于修订含头孢哌酮药品说明书的公告(2019年第13号)》,要求含头孢哌酮药品说明书不良反应项下需增加“血小板减少、低凝血酶原血症、凝血障碍、出血”内容,以及在注意事项和药物相互作用项目中强化凝血障碍和出血的风险。头孢哌酮/舒巴坦钠为复方制剂,其中头孢哌酮化学结构中含有干扰维生素K代谢的基团,导致凝血酶原的合成受阻,体内凝血机制错乱从而表现出较为明显的出血倾向[6]。头孢哌酮/舒巴坦钠具有肠道杀菌作用,导致利于维生素K循环的菌群减少,一定程度上加剧凝血障碍[7]。其机制也很可能与合成维生素的肠道菌群受到抑制有关,包括营养不良、吸收不良(如肺囊性纤维化患者)、乙醇中毒患者和长期静脉输注高营养制剂在内的患者存在出血风险[8]。至于血小板减少极有可能是药物与血浆蛋白质结合后的抗原抗体反应[9],故建议给予患儿头孢哌酮/舒巴坦钠抗感染时预防使用维生素K。此外,头孢哌酮/舒巴坦钠导致肝胆系统损害,主要表现为肝酶升高。头孢哌酮大部分经胆汁排泄[10],本次研究结果中出现肝胆损害患者多数为与其他肝脏代谢药物联用,由此可见当患者本身存在肝脏疾病时,使用头孢哌酮/舒巴坦钠时应酌情减量,以及密切监测患者体内血药浓度,按需调整药量。
儿童头孢孟多酯钠ADR报告共35份,主要表现为胃肠道系统损害和全身性损害。头孢孟多酯钠所致ADR主要涉及儿童和老年人,部分病例出现恶心、呕吐、咳嗽等胃肠道系统损害以及寒战、潮红等全身性损害[11-13]。国家药品不良反应监测中心2011—2015年数据显示,注射用头孢孟多酯钠ADR总例数为9407,数量前3位损害系统主要为皮肤及其附件损害(皮疹、瘙痒等),全身性损害(变态反应、寒战、高热等),胃肠系统损害(恶心、呕吐等)[14]。本研究结果与以上研究基本一致。头孢他啶ADR 41例报告中,累及系统-器官损害最多的同样为全身性损害和胃肠道系统反应。一项涉及162例头孢他啶ADR的研究显示,除了皮肤及其附件损害外,ADR累及最多是全身性损害,包括发热、寒战、胸闷等[15]。也有报道头孢他啶导致患儿腹泻、恶心、咳嗽等胃肠道反应[16-18]。但头孢孟多酯钠和头孢他啶导致胃肠道系统和全身性的损害的机制并未有详细的报道。有研究认为可能是与该头孢菌素类药物普遍存在抑制或破坏患者肠道菌群平衡或导致变态反应、二重感染有关[19-20]。
3.2给药频率 本研究中一次给药相比于其他给药频率发生不良风险概率更高。一般而言,抗菌药物ADR发生及严重程度可能受到药物因素的影响,如给药途径、给药频率、用药时长及单次给药剂量[21]。而儿童临床中广泛使用头孢菌素类药物进行儿童感染性疾病的治疗。一次给药通常为经验给药,并没有具体的给药频率,为达到抗感染效果,医务工作者可能倾向于经验给药。临床应用中,应根据患儿实际病情需求,按照说明书中规定、避免超频次给药,降低ADR风险发生概率。
3.3联合用药数量 本研究结果显示联合用药数量是ADR发生的促进因素。临床通常会通过联合使用其他抗生素扩大抗菌谱,提高抗感染治疗效率。然而,联合用药的安全性风险不容忽视,在临床实践中可能会产生有害的药物-药物相互作用(drug-drug interaction,DDI),导致药物疗效减弱或加重药物的毒副作用,产生严重ADR。据文献报道,因药物停用和ADR导致的住院患者中超过1/5是由DDI引起的[22]。而儿童本身器官发育不完善,肝脏代谢速率不明,过多的联合使用其他药物会加重患儿身体负担,以及免疫功能与神经内分泌功能不完善导致药物耐受性下降等众多原因皆有可能导致联合用药时ADR风险发生概率增加。建议医护人员在临床使用中借助数据库等医疗资源考察DDI情况,尽可能避免ADR的发生。
3.4其他因素 除用药品种、给药频率、用药时长、联合用药数量之外,单因素分析显示年龄、给药途径、是否符合推荐用量为使用目标药物发生ADR的潜在危险因素。
经卡方检验,不同年龄段ADR发生率差异有统计学意义。婴儿期(0~1岁)及学龄前期(3~6岁)两个年龄段发生ADR发生率较高。0~1岁患儿ADR发生率与其他年龄段相比是否具有显著性差异并无一致报道。新生儿免疫系统薄弱一方面导致防御能力差,患儿发生ADR风险增加;另一方面新生儿会得到医务人员更为细致的照顾,用药上也更为谨慎,一定程度上降低风险发生概率。 3~6岁儿童组织器官功能相对不健全,对于药品有更高的敏感性,相比于学龄期与青年期更容易发生ADR。
静脉给药ADR发生比例高于非静脉。一方面是因为静脉给药药物起效快,临床多是静脉给药;另一方面,静脉给药后血药浓度迅速攀升,无首关效应,而注射剂的配药浓度以及注射速度均可引起ADR发生。
本研究结果显示,头孢菌素类药物ADR发生在用药疗程前期的概率较高。在159例发生ADR的患儿中,用药时间最长11 d。多数在3~7 d,疗程相对较短。一方面可能多数头孢菌素通过静脉途径给药,短时间内血药浓度迅速攀升导致ADR,一旦发生可疑事件,临床将采取减量、停用或换药等方式进行处理。另一方面,头孢菌素类药物使用6 d以上神经系统损害比例更高[23],可能与儿童的代谢能力弱于成人,药物长时间蓄积有关。此外,在《抗菌药物临床应用指导原则》(2015版)中明确提出抗菌药物使用与患者感染严重程度、感染部位以及感染的细菌种类有关[24]。在临床使用头孢菌素类抗菌药物进行治疗时,需密切观察用药后的患儿表现,在完成疗程后及时停药。
本研究存在一些限制性。内容方面,本研究主要从医务方、患儿本身出发研究儿科用药安全性,缺乏家长以及护理人员方面的考虑。数据来源方面,数据仅来源于单个省份部分医疗机构,结论的外推性可能较差。样本量方面,由于新冠疫情原因,儿科住院患儿数量同比大幅下降,监测期间内头孢哌酮/舒巴坦钠病例未达到3000例。另外监测时长有限,存在遗漏潜在长期ADR以及罕见ADR的可能。

