液相色谱串联质谱法检测食品中金刚烷胺的方法研究
张慧芳 刘俊峰 李松涛
摘 要:目的:采用液相色谱串联质谱法检测包装食品中金刚烷胺。方法:用1%的乙酸乙腈配制液提取鸡肉和鸡蛋样品,后经脱水、去脂、旋干和复溶、过滤器净化、氮吹,50%乙腈水定容,上机采集和定量。结果:在浓度为2~100 ng·mL-1时,金刚烷胺的标曲线性好,相关系数r为0.999 9,加标回收率在74.4%~117.9%,RSD<10%。结论:该方法便于操作、原理简单、回收率稳定以及重复率高,能用于金刚烷胺的测定。
关键词:金刚烷胺;鸡肉和鸡蛋;液相色谱串联质谱法
Abstract: Objective: To detect amantadine in packaged food by liquid chromatography-tandem mass spectrometry. Method: Chicken and egg samples were extracted with 1% acetic acid acetonitrile solution, and then dehydrated, degreased, spin-dried and redissolved, purified by filter, nitrogen blown, 50% acetonitrile water to constant volume, collected and quantified by computer. Result: In the concentration range of 2~100 ng·mL-1, the standard curve of amantadine is good, the correlation coefficient r is 0.999 9, and the recoveries are 74.4%~117.9%, the RSD<10%. Conclusion: This study is easy to operate, simple in principle, stable in recovery rate and high in repetition rate, and can be used for the determination of amantadine.
Keywords: amantadine; chicken and eggs; liquid chromatography tandem mass spectrometry
目前,金刚烷胺被很多国家列为禁用药物[1]。因其售价较低,养殖户为应对流感爆发,将金刚烷胺类药物较多地使用在饲料中[2],致使金刚烷胺在动物体内形成残留,食用后会对人体产生特别大的影响[3-4]。
因此,我国有必要研究金刚烷胺的检测方法。高效液相色谱串联质谱法能够准确地定性和定量检测农产品中的兽药残留。现行的金刚烷胺检验标准《食品安全国家标准 动物性食品中金刚烷胺残留量的测定 液相色谱-串联质谱法》(GB 31660.5—2019)[5]就采用了高效液相色谱质谱技术。本文主要通过对液相及质谱条件的优化,提高分析的准确性和精密度,进而为鸡肉和鸡蛋中金刚烷胺的检测提供一些参考。
1 材料與方法
1.1 材料与试剂
鸡肉和鸡蛋样品购置于超市,均属包装食品;金刚烷胺标准溶液(Bepure,证书编号为B0019913);D15-金刚烷胺(Bepure,证书编号为D0015046);乙腈(默克)、正己烷(美国Tedia公司);甲醇(色谱纯)、无水硫酸钠(分析纯);甲酸(色谱纯,Fisher公司)、过滤器(北京科德诺思技术有限公司,200 mg/3 mL);本实验室纯水机制一级超纯水。
1.2 仪器与设备
LCMS-4500三重四极杆色谱质谱联用仪(使用ESI离子源,美国AB SCIEX公司);BSA124S-CW电子天平(精密度0.000 1 g,常熟双杰测试仪器厂);IKA VORTEX 3涡旋仪;离心机(德国SIMGA公司);SB-5200DTDN超声波清洗器(昆山市超声仪器有限公司);UGC-45CE电动升降圆形水浴氮吹仪(优晧联合)等。
1.3 试验方法
1.3.1 标准溶液配制
(1)标准贮备液。分别准确称取金刚烷胺、D15-金刚烷胺各10 mg,分别转移至2个10 mL容量瓶中,用甲醇溶解,并定容至刻度,即为1 mg·mL-1的标准配制液。-20 ℃以下保存,有效期为3个月。
(2)标准工作液。用移液枪分别吸取0.1 mL金刚烷胺和D15-金刚烷胺的标准贮备液,各自移入100 mL容量瓶中,用甲醇定容,配制成金刚烷胺、D15-金刚烷胺浓度为1 μg·mL-1的标准工作液。2~8 ℃保存,有效期为2周。
1.3.2 样品前处理
参照《食品安全国家标准 动物性食品中金刚烷胺残留量的测定 液相色谱-串联质谱法》(GB 31660.5—2019)的前处理办法分别对包装食品中鸡肉和鸡蛋样品进行大量重复处理。
1.3.3 仪器条件
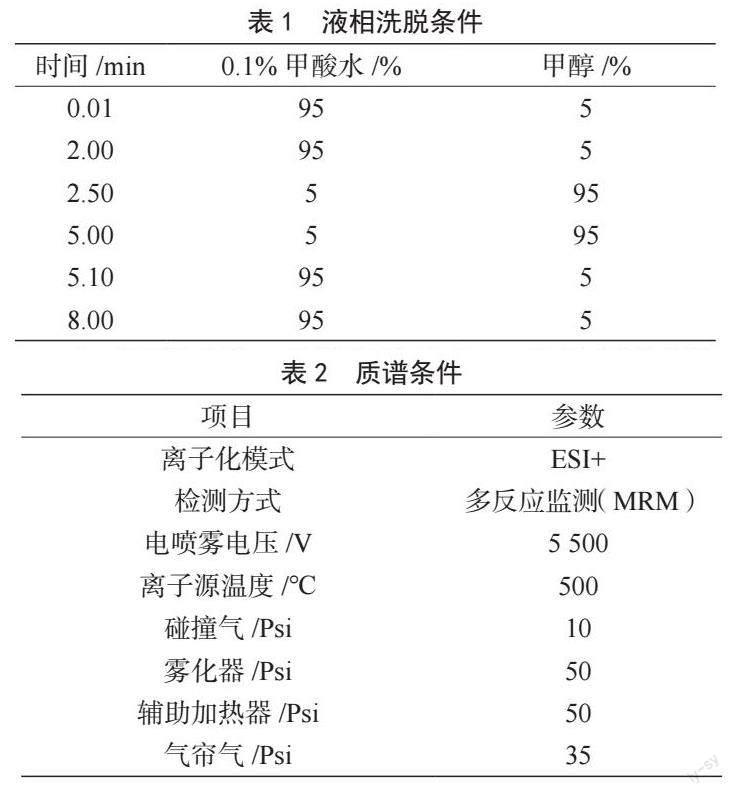
(1)液相条件。两路流动相:0.1%的甲酸水溶液和甲醇;色谱柱:ZORBAX Eclipse Plus C18(2.1×100 mm,3.5 ?m);洗脱条件:见表1;进样量:10 ?L;流速:0.4 mL·min-1;柱温箱温度:40 ℃。
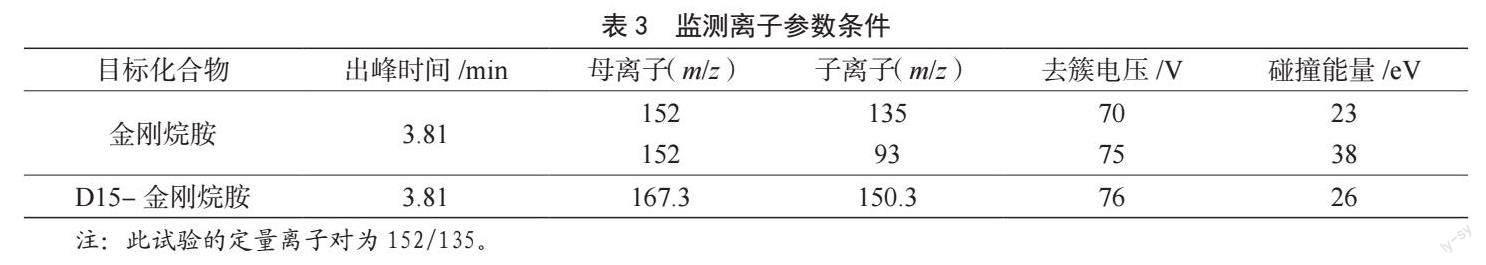
(2)质谱条件。质谱条件见表2,监测离子参数条件见表3。
2 结果与分析
2.1 色谱图
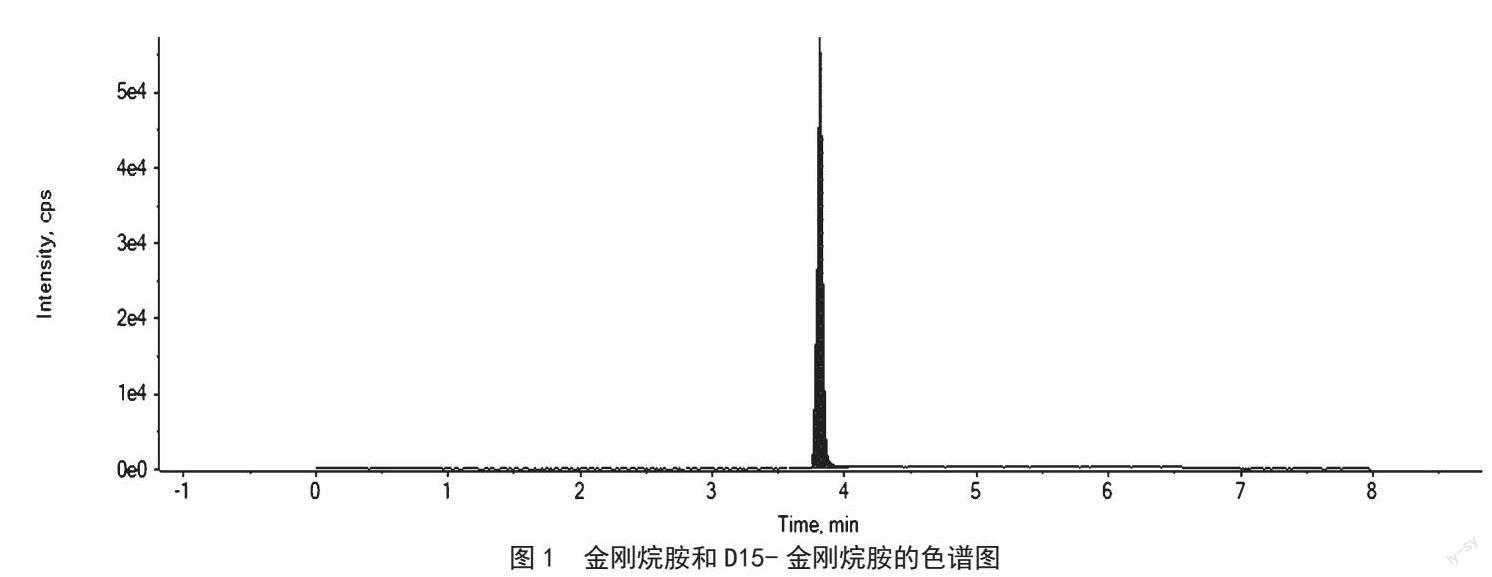
由图1可知,目标化合物的响应可达5×104,内外标出峰时间重合且稳定,峰形细而尖,信噪比(S/N)远超过10,结合前期扫描所得定性离子对(152/93)与定量离子对(152/135)以及内标(167.3/150.3)在对应时间稳定出现,充分说明目标物金刚烷胺和D15-金刚烷胺稳定存在,进而可以准确地定性定量研究。
2.2 线性范围、检出限及定量限信噪比
2.2.1 标准曲线绘制
采用逐级稀释法配制金刚烷胺的质量浓度为2 ng·mL-1、4 ng·mL-1、10 ng·mL-1、20 ng·mL-1、50 ng·mL-1和100 ng·mL-1,D15-金刚烷胺质量浓度均为20 ng·mL-1的系列标准溶液,按照1.3.3仪器条件上机测试,以金刚烷胺与D15-金刚烷胺浓度比为横坐标,两者的面积比为纵坐标,绘制标准曲线,得标准曲线线性方程为y=0.049 9x+0.002 06,相关系数r为0.999 9,表明在2~100 ng·mL-1时,金刚烷胺的线性关系良好。
2.2.2 检出限信噪比
方法检出限为1 μg·kg-1,经公式计算后得上机浓度为2 ng·mL-1,此时定量离子m/z=135的信噪比为573.5,当信噪比为3时,仪器检出限为0.005 23 μg·kg-1,能满足标准GB 31660.5—2019的要求。
2.2.3 定量限信噪比
方法定量限为2 μg·kg-1,经公式计算后得上机浓度为4 ng·mL-1,此时定量离子m/z=135的信噪比为1 037,当信噪比为10时,仪器检出限为0.019 3 μg·kg-1,能满足标准GB 31660.5—2019的要求。
2.3 回收率与精密度
参照标准GB/T 27404—2008[6]的要求,本试验分别在鸡肉和鸡蛋基质的空白样品中添加1、2、5倍定量限浓度的标准溶液,进行双平行加标回收试验,计算回收率,结果见表5。同时,在1倍定量限浓度(4 ng·mL-1)添加水平下做6平行试验,计算精密度RSD值,结果见表6。经测试,该方法的加标回收率为74.4%~117.9%,RSD为0.65%,均能满足标准要求。
3 结论
综上可知,在濃度为2~100 ng·mL-1时,金刚烷胺的线性关系好,相关系数r为0.999 9,加标回收率在74.4%~117.9%,RSD<10%。此方法能够准确测定鸡蛋和鸡肉基质中的金刚烷胺,有较好的稳定性,且鸡蛋基质低于鸡肉基质的加标回收率,说明鸡蛋基质更复杂,对提取金刚烷胺的影响更大,该试验可对研究食品中金刚烷胺的检测提供一些参考依据。
参考文献
[1]付倩,文奇,周银古,等.新余市甲型流感病毒M基因进化及金刚烷胺类耐药性分析[J].实验与检验医学,2017,35(6):870-873.
[2]张颖颖,李慧晨,吴彦超,等.超高效液相色谱-串联质谱法测定动物性食品中8种抗病毒类药物残留量[J].食品科学,2018,39(2):303-309.
[3]何忠伟,李子菲,刘芳.禽流感疫情下我国家禽养殖户防控行为影响因素与对策研究[J].中国畜牧杂志,2020,56(6):185-190.
[4]端礼钦,王静,曹润冬,等.液相色谱串联质谱法测定鸡蛋中喹诺酮类药物残留[J].分析试验室,2018,37(7):843-847.
[5]中华人民共和国农业农村部,国家卫生健康委员会,国家市场监督管理总局.食品安全国家标准 动物性食品中金刚烷胺残留量的测定 液相色谱-串联质谱法:GB 31660.5—2019[S].北京:中国标准出版社,2019.
[6]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.实验室质量控制规范 食品理化检测:GB/T 27404—2008[S].北京:中国标准出版社,2008.

