容积调强在全脊柱骨多发转移瘤放疗中应用研究
陈小君 翁成荫 甘庆权 陈红文 刘枝祥
广州市第一人民医院肿瘤科(广州 510180)
放射治疗对骨转移瘤局部止痛疗效确切,约60%~80%的恶性肿瘤骨转移患者在局部止痛放疗中获得良好的止痛效果,对放疗有反应者50%以上在大剂量放疗2~3次后,疼痛就明显减轻,70%以上患者接受放疗后缓解期达3个月[1]。由于放疗设备的局限,目前直线加速器单中心最大照射范围在40 cm之内,单个治疗中心放射靶区长度不应超过40 cm。由于肿瘤全脊柱骨转移通常为多发,放射靶区常超40 cm(称之超长靶区),需设计2~3个照射中心,平移进行照射,这样相邻照射野间存在衔接问题,衔接区可能会出现剂量热区或冷区,当热区出现在危及器官如脊髓,可能出现放射性脊髓炎,严重者可能截瘫,冷区出现在靶区内意味着放疗剂量不足,影响疗效。随着医疗技术的飞速发展,放疗设备的更新换代,放射治疗也进入精确时代。容积调强(volumetric modulated arc therapy,VMAT)是近年推广的调强放疗技术,具有靶区覆盖度和剂量均匀性相对较好,正常组织保护好,治疗操作相对简单等特点。因此,本项目研究了适形放疗(conformal radiotherapy,CRT)和容积调强放疗在全脊柱骨多发转移瘤应用中剂量学差异及计划执行效率,评估两种放疗技术在全脊柱骨多发转移瘤应用中剂量学特点及安全性,可为有超长靶区的恶性肿瘤治疗提供技术参考。
1 资料与方法
1.1 一般资料
选取2018年1月—2021年1月我科放疗中心收治的全脊柱骨多发转移的肿瘤患者作为研究对象,其中前列腺癌骨转移15例,乳腺癌骨转移14例,肺癌骨转移13例,鼻咽癌骨转移8例。原发肿瘤病灶有病理确诊,并行PET-CT或ECT等相关检查诊断有多发骨转移瘤,放疗靶区>40 cm。排除标准为:①同一部位已接受过放疗的患者;②有放疗禁忌证者。研究方案经我院医学伦理委员会审核通过(伦理批件号:K-2018-103-01)。
1.2 放疗技术
1.2.1 设备和材料 采用美国GE公司大孔径定位CT机进行定位,瑞典医科达公司Synergy直线加速器进行治疗,射野验证系统拍摄位置验证片,固定材料采用人体固定真空袋和固定膜。
1.2.2 体位固定及影像资料获取 患者仰卧于真空袋上,躯体保持水平,双手置额头,通过推砌袋体,抽真空,真空袋固定成型,胸腹部再予固定膜固定。使用2组金点贴在固定膜上作为参考坐标。CT扫描范围为颅底至尾骨,层厚和层距均为2.5 mm,扫描完成后图像传输到计划系统。
1.2.3 靶区及危及器官勾画 采用医科达公司Monaco计划系统进行靶区勾画,首先勾画全脊柱的临床靶区(clinical target volume,CTV)然后外扩0.5 cm为计划靶区(planning target volume,PTV),同时勾画出双肺、心脏、肝脏、肾、胰腺、胃、小肠等危及器官,限制其体积不超过该器官的最大耐受剂量。
1.2.4 计划设计 采用Monaco计划系统对同一患者分别设计两种计划(CRT 和VMAT),CRT称为对照组,VMAT称为研究组。CRT计划:根据靶区长度设计两个照射中心ISO-A和ISO-B,每个中心采用前后两野对穿适形照射,治疗床旋转 90°并适当调整对穿野角度使两个中心的照射野衔接处实现无缝衔接,先给予一半的照射次数,然后平移照射野使衔接处间隙移动到靶区其它处,再给予另一半的照射野次数(如图1)。VMAT计划:设计两个照射中心ISO-C和ISO-D,将靶区分成2段,上段脊柱采用350 rad(185-175)1个双弧度进行治疗,中下段脊柱采用另一个同样角度的双弧进行治疗。2个弧之间交叉2~3 cm,同时优化以解决照射野的衔接问题(如图2)。

图1 CRT 计划设计
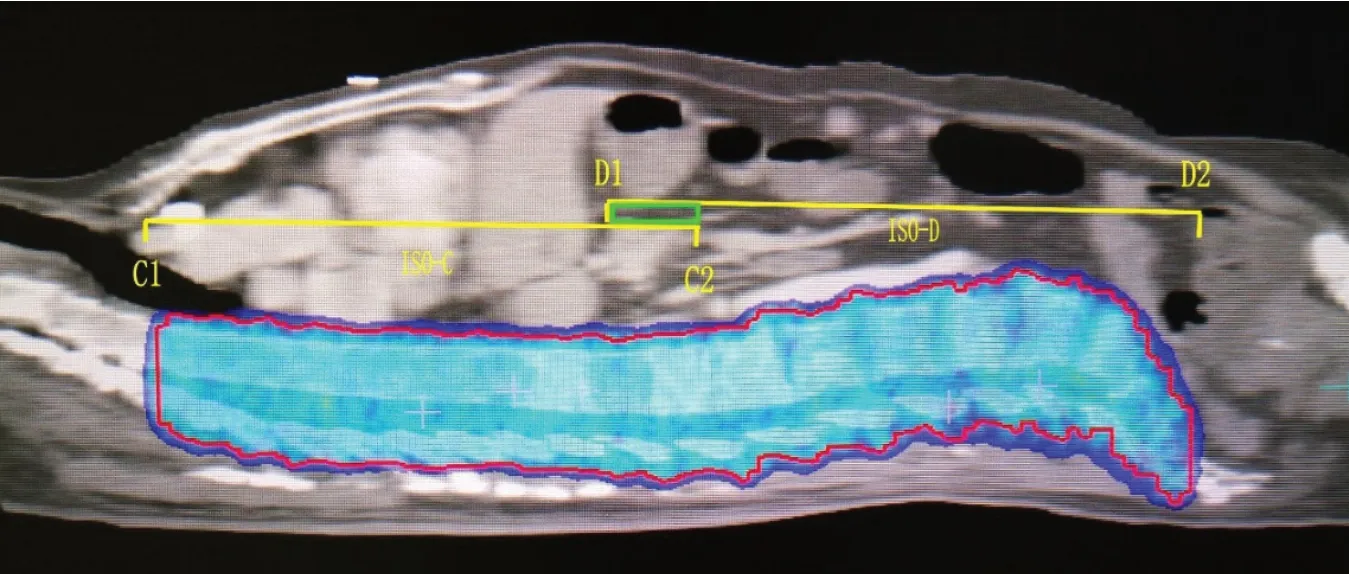
图2 VMAT 计划射野设计
1.2.5 处方剂量 每段照射总剂量为3 000 cGy,采用6MV-X线照射,每天300 cGy,1天1次,1周5次,周末休息,放疗2周。
1.2.6 数据分析及统计 运用剂量体积直方图及对应的统计表去评估靶区及危及器官剂量覆盖情况,了解靶区热点和冷点、靶区外整体剂量以及危及器官受照剂量、出束时间等参数,通过剂量分布图和点测量方式了解射野衔接区剂量分布情况。为了统一比较,靶区剂量归一为处方剂量覆盖95%的体积,靶区覆盖度以V30 Gy(%)、适形指数(conformality index,CI)、均匀指数(homogeneity index,HI)等作为评估目标,热点为大于处方剂量110%的剂量点,冷点为小于处方剂量93%的剂量点。靶区外整体剂量为身体外轮廓减去PTV的受照平均剂量,出束时间为多个照射野射线开始照射至停止的累积时间。靶区适形指数:CI =(PTVref/PTV)×(Tissueref/ PTV);其中,PTVref是接受至少95%处方剂量所包绕的PTV体积,Tissueref是接受至少95%处方剂量的总体积,均匀指数:HI=D5%/D95%;其中,D5%是5%的PTV体积受照剂量,D95%是95%的PTV体的受照剂量。危及器官受照量以V5 Gy%(受照剂量为5 Gy的体积百分比)和V10 Gy代表低剂量受照量,V20 Gy和V30 Gy代表高剂量受照量。应用 SPSS 16.0 软件进行统计学分析,计量数据采用(±s)表示。配对t检验比较传统放疗技术CRT和VMAT技术的剂量学差异,P<0.05为差异有统计学意义。
1.2.7 疗效评价 采用视觉模拟评分法(VAS法)对患者的疼痛程度进行判定,在患者进行放疗之后以患者在活动或者静息状态下均没有疼痛感,VAS评分为 0分;活动时有轻微痛感,静息时没有疼痛感为轻度,VAS评分为1~3分;活动时疼痛加重,静息时有轻微疼痛感为中度,VAS评分为 4~7分;活动时与静息时均有剧烈痛感为重度,VAS评分为 8~10分。疗效判定标准:①完全缓解:疼痛感完全消失;②部分缓解:疼痛感明显减轻,睡眠基本安稳,可以正常生活;③轻度缓解:疼痛有轻微减轻,但是活动时疼痛感依然明显,睡眠以及生活仍受限制;④无效:疼痛无缓解,其中有效标准以完全缓解以及部分缓解认为止痛有效[2]。
1.2.8 随访观察 放疗结束后每3个月对患者进行全脊髓MRI复查一次,随访一年以上,观察患者放疗后的不良反应、野内及重叠区危及器官损伤情况。
2 结 果
2.1 靶区剂量
见图3~4,表1,VMAT的靶区处方剂量覆盖度(V30 Gy/%)高于CRT(P<0.01),CI和HI也优于CRT技术(P<0.05和P<0.01),同时VMAT靶区外整体剂量也高于CRT技术(P<0.01)。
表1 2种放疗技术靶区剂量线覆盖,靶区外整体剂量 (±s ,n=50)
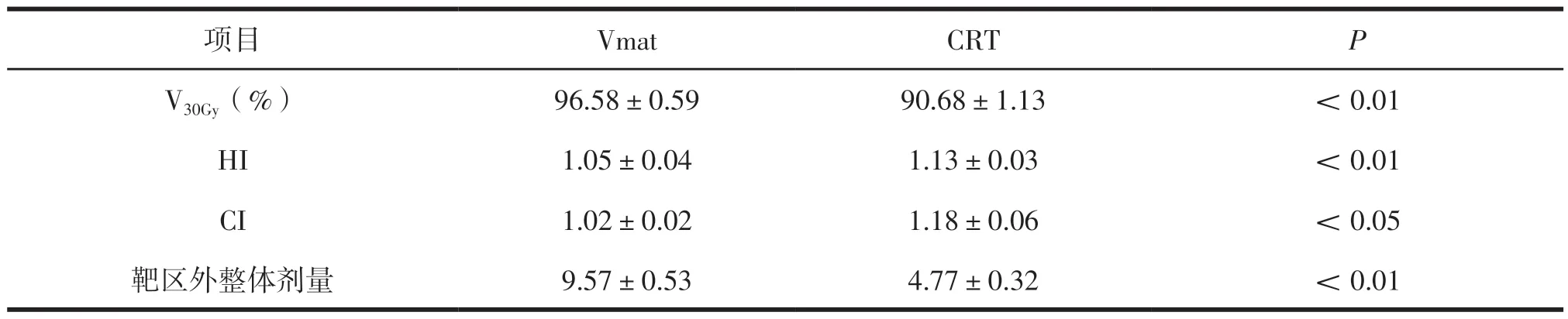
表1 2种放疗技术靶区剂量线覆盖,靶区外整体剂量 (±s ,n=50)
注:V30 Gy(%)为靶区受照量30 Gy时的体积百分比
项目 Vmat CRT P V30Gy(%) 96.58±0.59 90.68±1.13 <0.01 HI 1.05±0.04 1.13±0.03 <0.01 CI 1.02±0.02 1.18±0.06 <0.05靶区外整体剂量 9.57±0.53 4.77±0.32 <0.01

图3 CRT 靶区剂量分布及剂量体积直方图,靶区内不同彩色对应不同剂量
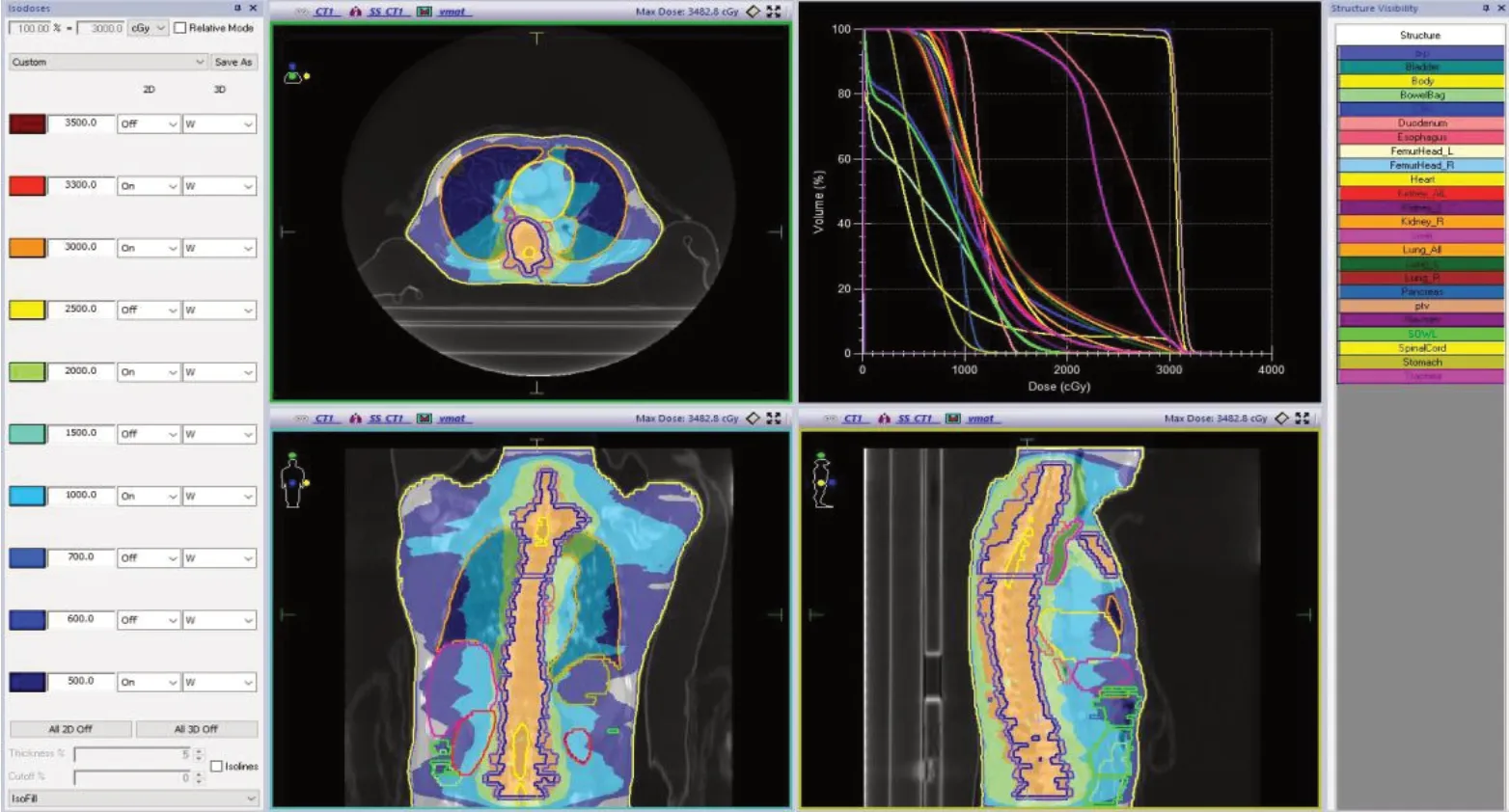
图4 VMAT 靶区剂量分布及剂量体积直方图,靶区内不同彩色对应不同剂量
2.2 危及器官受照量
VMAT技术时危及器官V5 Gy受照体积高于CRT(P<0.01),除了胃、胰腺和小肠,危及器官V10 Gy受照体积高于CRT(P<0.01或P<0.05),危及器官V20 Gy受照体积则低于CRT(P<0.01),除了肾,危及器官V30 Gy受照体积也低于CRT(P<0.01) 。采用VMAT技术时危及器官的最大受照量低于CRT(P<0.01或P<0.05),但除了心脏、胰腺和小肠,VMAT技术危及器官平均受照量高于CRT(P<0.01或P<0.05)。见表2。
表2 2种放疗计划危及器官剂量参数对比 (±s ,n=50)
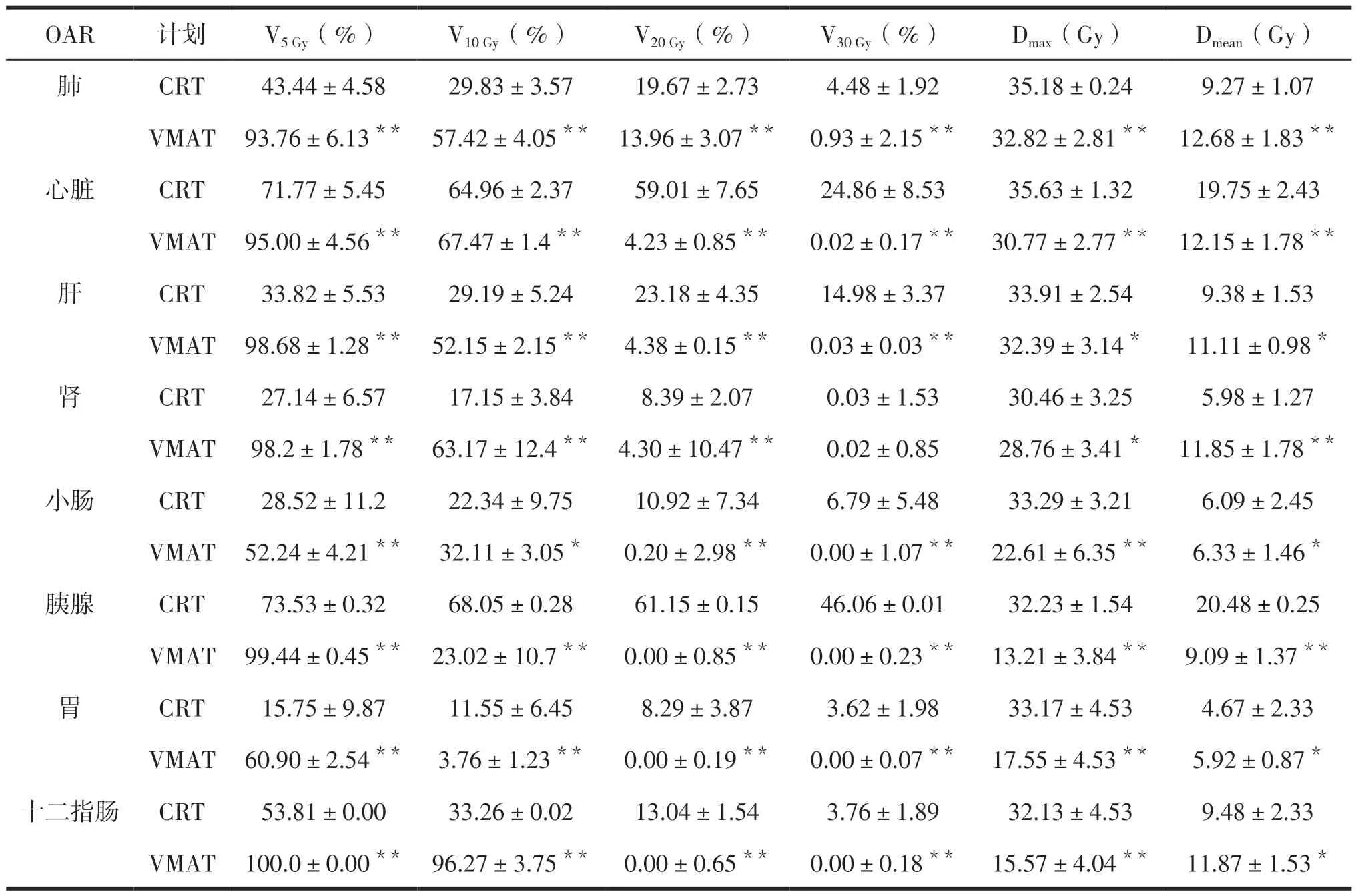
表2 2种放疗计划危及器官剂量参数对比 (±s ,n=50)
注:V5 Gy(%)为危及器官受照射剂量为5 Gy的体积百分比,V10 Gy(%)、V20 Gy(%)、V30 Gy(%)类推。与CRT比较,*P<0.05,**P<0.01。
OAR 计划 V5 Gy(%) V10 Gy(%) V20 Gy(%) V30 Gy(%) Dmax(Gy) Dmean(Gy)肺 CRT 43.44±4.58 29.83±3.57 19.67±2.73 4.48±1.92 35.18±0.24 9.27±1.07 VMAT 93.76±6.13** 57.42±4.05** 13.96±3.07** 0.93±2.15** 32.82±2.81** 12.68±1.83**心脏 CRT 71.77±5.45 64.96±2.37 59.01±7.65 24.86±8.53 35.63±1.32 19.75±2.43 VMAT 95.00±4.56** 67.47±1.4** 4.23±0.85** 0.02±0.17** 30.77±2.77** 12.15±1.78**肝 CRT 33.82±5.53 29.19±5.24 23.18±4.35 14.98±3.37 33.91±2.54 9.38±1.53 VMAT 98.68±1.28** 52.15±2.15** 4.38±0.15** 0.03±0.03** 32.39±3.14* 11.11±0.98*肾 CRT 27.14±6.57 17.15±3.84 8.39±2.07 0.03±1.53 30.46±3.25 5.98±1.27 VMAT 98.2±1.78** 63.17±12.4** 4.30±10.47** 0.02±0.85 28.76±3.41* 11.85±1.78**小肠 CRT 28.52±11.2 22.34±9.75 10.92±7.34 6.79±5.48 33.29±3.21 6.09±2.45 VMAT 52.24±4.21** 32.11±3.05* 0.20±2.98** 0.00±1.07** 22.61±6.35** 6.33±1.46*胰腺 CRT 73.53±0.32 68.05±0.28 61.15±0.15 46.06±0.01 32.23±1.54 20.48±0.25 VMAT 99.44±0.45** 23.02±10.7** 0.00±0.85** 0.00±0.23** 13.21±3.84** 9.09±1.37**胃 CRT 15.75±9.87 11.55±6.45 8.29±3.87 3.62±1.98 33.17±4.53 4.67±2.33 VMAT 60.90±2.54** 3.76±1.23** 0.00±0.19** 0.00±0.07** 17.55±4.53** 5.92±0.87*十二指肠 CRT 53.81±0.00 33.26±0.02 13.04±1.54 3.76±1.89 32.13±4.53 9.48±2.33 VMAT 100.0±0.00** 96.27±3.75** 0.00±0.65** 0.00±0.18** 15.57±4.04** 11.87±1.53*
2.3 出束时间和总治疗时间
见表3采用VMAT技术时较CRT出束时间增加(P<0.01),但CRT时技师摆位时间较VMAT增加(P<0.05),总治疗时间VMAT技术时较CRT增加(P<0.01)。
表3 2种放疗计划执行时间 (±s ,n=50)

表3 2种放疗计划执行时间 (±s ,n=50)
注:与CRT比较,*P<0.05,**P<0.01.
计划 出束时间/min 摆位时间/min 总治疗时间/min CRT 0.75±0.22 4.68±0.68 5.45±1.33 VMAT 7.82±0.58** 4.16±0.45* 12.76±1.06**
2.4 VAS评分及随访结果
8周后,VAS评估疼痛完全缓解16例,部分缓解22例,轻度缓解8例,无效4例,总有效率为76.7%。靶区外整体剂量以及危及器官无不良反应。随访日期截止为2021 年 12月,随诊的患者分别在放疗结束后每3个月复查全脊柱MRI,结果显示VMAT技术放疗照射野重叠处未见脊髓及其他组织急慢性损伤等异常信号(见图3),CRT技术有2例结束放疗3个月后随访发现照射野衔接区内有新破坏灶形成。
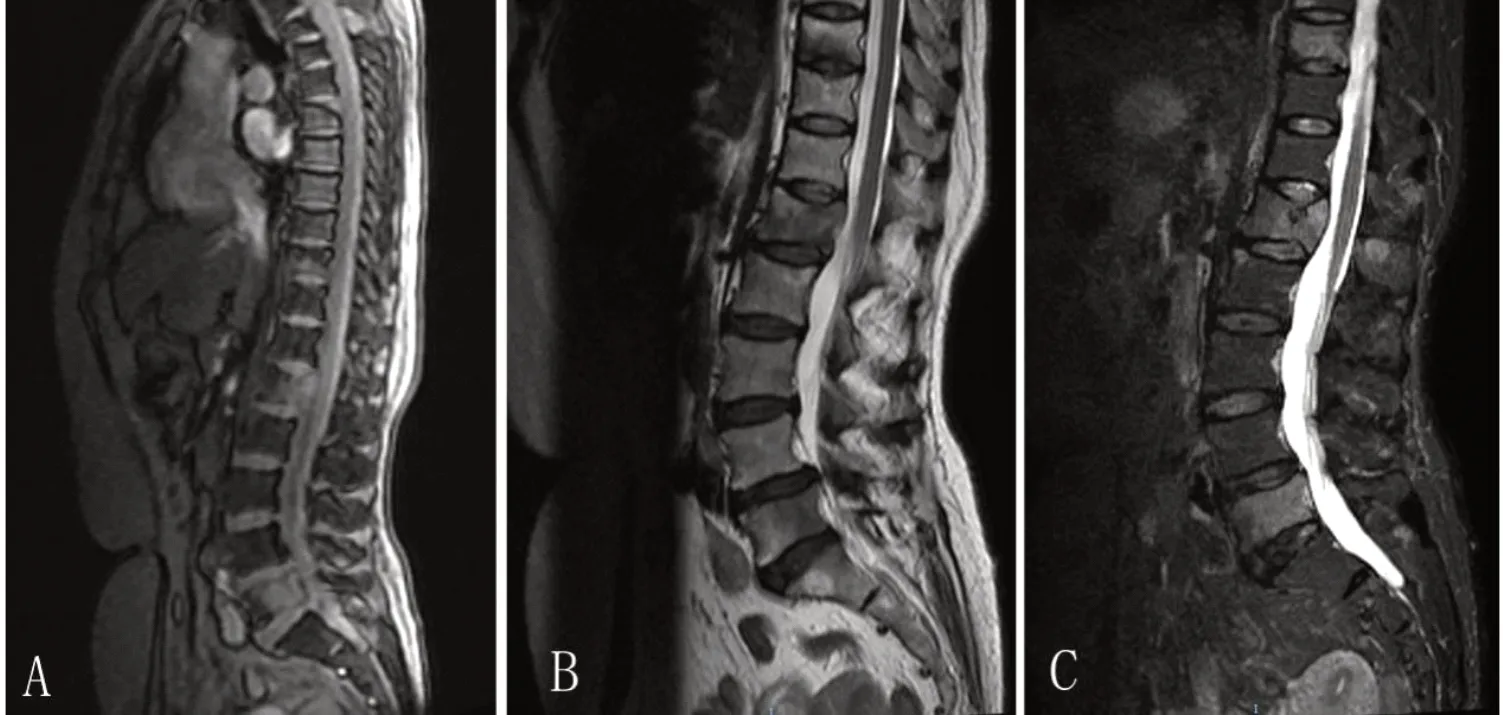
图3 某患者VMAT 放疗后MRI 复查情况
3 讨 论
恶性肿瘤全脊柱骨多发转移局部止痛治疗方式包括药物、放疗与外科手术等,其中放疗是最常见而有效的治疗方式,可以消除或减轻骨转移灶疼痛感,避免患者对麻醉药品形成依赖并减少药品用量,延长其生存期,提高生活质量[3]。射线可抑制或杀死肿瘤细胞,使胶原蛋白合成增加,成骨细胞活性增加而形成新骨,并干扰疼痛信号的传导,抑制缓激肽、前列腺素等疼痛介质的分泌,缓解疼痛[4]。
VMAT作为近年推出的高级调强放疗技术,具有靶区覆盖度和剂量均匀性相对较好的特点,在超长靶区放疗中较普通适形放疗方式优势明显。张怀文等[5]和王秀楠等[6]的研究所示,全脊柱放疗中VMAT 与CRT相比,可提高靶区 CI、改善HI,这与本研究结果相近。本研究表明,VMAT技术靶区处方剂量覆盖度、CI和HI明显优于CRT技术,但靶区外整体剂量则明显高于CRT技术,其原因可能是VMAT技术采用了多角度连续照射野放射剂量多点累积,而CRT技术布野角度相对简单,多数采用2个单角度对穿野,射线穿透靶区外体积减少。
危及器官的受照量是放疗计划评估的重要指标之一。在危及器官评估中,本项目将V5 Gy和V10 Gy代表低剂量受照量,V20 Gy和V30 Gy代表高剂量受照量。我们在研究发现VMAT技术中部分危及器官低剂量受照量的受照体积明显高于CRT,而部分高剂量受照量危及器官的受照体积则明显低于CRT,其原因可能跟危及器官所处的位置有关,靠近靶区的危及器官受照剂量明显增加。
在放射治疗过程中,放疗执行效率也是评价一种放疗技术是否优秀的标准之一。本研究中VMAT较CRT出束时间增加,其原因是VMAT采用了多角度连续照射野,而CRT采用2个单角度对穿野照射。在技师摆位时间方面CRT较VMAT增加,其原因可能由于CRT技术的局限多个照射野之间的剂量衔接和剂量分布不均,为避免照射野衔接处出现“热区”或“冷区”,放疗期间需要定期移动衔接位置去消除衔接区域内的热冷区域,有时为了改善剂量分布不均匀甚至需要旋转治疗床进行非共面照射,增加了操作环节的复杂性也增加了放疗时间[7]。总治疗时间VMAT则较CRT增加,其原因同样是VMAT采用了多角度连续照射野,射线出束时间增加。
项目随访近一年,患者放疗止痛效果明显,但采用CRT技术放疗中有2例患者在复查时发现射野衔接区有新的破坏灶形成,其原因可能是射野衔接区出现了冷点造成剂量不足。VMAT技术照射的所有病例,随访区间照射野重叠处均未见脊髓及其他组织出现急慢性损伤,这说明容积调强放疗在计划设计中有效地优化了多射野衔接处的剂量分布,避免了衔接区剂量过高或过低的问题,同时保证了靶区剂量分布的均匀性,这与马天斌等[8]和常浩等[9]研究结果相似。
综上所述,容积调强放射治疗技术在全脊柱多发骨转移瘤治疗中放疗剂量分布均匀,近期疗效显著,安全性良好。当然也存在一定的不足,如靶区以外低剂量区较大,射线出束时间较长等,这些不足会随着技术的发展会逐步改善。

