环孢素、阿达木单抗、司库奇尤单抗治疗甲银屑病的疗效及安全性比较
汤占汉, 李苏姗, 吕莎, 黄召, 刘哲, 李福秋
吉林大学第二医院,吉林 长春 130041
甲银屑病是皮肤科常见的甲病之一,不仅影响美观,还可引起疼痛、甲周炎症,严重者功能障碍,生活质量受到影响[1]。银屑病作为皮肤科最常见的疾病之一,其发病率高达0.7%~2.9%,银屑病患者甲受累的患病率在10%~80.1%。甲银屑病的终身发病率可达80%以上[2]。因此,甲银屑病的治疗受到广大患者的重视。因甲特殊的生理解剖结构,治疗周期较长,传统治疗不良反应发生率高,疗效不甚理想,具有明显的弊端[3]。目前,甲银屑病的治疗方案主要取决于是否存在皮肤和/或关节受累,甲受累的数量、位置及严重程度等因素。对于病甲累及少于或等于3个者,一般选择局部治疗,可外用或病甲内注射药物,如糖皮质激素类或维生素D3衍生物[4];对于病甲累及超过3个或合并关节症状者,生物制剂较传统治疗方法更具优势。因此可根据临床表现和患者生活质量需求进行局部或全身治疗[5]。目前国内尚无针对甲银屑病的诊疗指南,已有的一些治疗手段不论是传统治疗还是生物制剂的应用均对该病的改善有一定疗效,但缺少统计学数据。因此,本研究使用病例对照研究,评估使用口服环孢素、皮下注射阿达木单抗及皮下注射司库奇尤单抗治疗甲银屑病的疗效及安全性。
1 对象与方法
1.1 研究对象
选取2022年1—11月就诊于我院门诊的甲银屑病患者。纳入标准:①性别不限,年龄大于18周岁;②皮损经临床或组织病理确诊为银屑病伴甲损害,或仅有甲损害且经病理诊断为甲银屑病[6];③近6个月内未接受过银屑病及甲银屑病的相关治疗;④病甲真菌镜检阴性。排除标准:①甲板脱失或甲周严重破损;②合并严重感染;③合并结核、乙肝、丙肝、HIV等感染;④对环孢素、阿达木单抗、司库奇尤单抗严重不耐受者;⑤处于妊娠期、哺乳期的妇女,或者短期内有生育计划患者;⑥合并恶性肿瘤者;⑦初次筛查指标不合格者;⑧未及时复诊或用药不规律者。本研究经吉林大学第二医院伦理委员会批准(版本号:1.0,版本日期:2022.11.17)。研究符合赫尔辛宣言,所有患者均签署知情同意书。

1.2 治疗方法
环孢素组:每日分早晚两次口服环孢素3 mg/(kg·d)。阿达木单抗组:第0周皮下注射阿达木单抗80 mg,第2周注射40 mg,以后每2周注射40 mg。司库奇尤单抗组:第0、1、2、3、4周皮下注射司库奇尤单抗300 mg,以后每4周注射1次。三组均治疗24周。
1.3 疗效判定
治疗前(基线)收集患者甲银屑病程度指数(nail psoriasis severity index,NAPSI)评分、皮肤病生活质量调查问卷(dermatology life quality index, DLQI)评分;治疗12周收集患者NAPSI评分、NAPSI评分改善率;治疗24周后收集患者NAPSI评分、NAPSI评分改善率、DLQI评分,并进行临床疗效判定。
NAPSI评分[7]:将每个甲划分为 4 个象限,对每个象限有无甲母质或甲床受累进行评分。甲母质损害包括点状凹陷、白甲、甲半月红斑、甲板碎裂或增厚,若受累记1分,反之记0分;甲床损害包括油滴征、甲剥离、甲下角化过度、裂片状出血,若受累记1分,反之记0分。单甲评分为0~8分,全部甲评分为0~160分。
DLQI评分[8]:调查前对相关人员进行统一培训,包括调查流程、调查内容及注意事项等。正式调查前抽取10例符合标准的患者进行预调查,填写全部问卷用时均在15~20 min,属可接受范围,具有可行性。为保证问卷质量,调查时由研究员本人现场统一发放问卷、现场指导与解答,由患者本人填写或研究员根据其描述代写,填写时长为15~20 min;研究员本人回收问卷,并进行统一录入。若选项超过15%未填写,则视为无效问卷。原始数据录入时由另一名研究员再次核查,以确保准确性。
临床疗效判定[8]:以NAPSI评分改善率计算临床有效率。NAPSI评分改善率=(基线评分-治疗后评分)/基线评分 ×100%。治愈:NAPSI评分改善率=100%;显效:NAPSI评分改善率≥60%;有效:30%≤NAPSI评分改善率<60%;无效:NAPSI评分改善率<30%。临床有效率=(治愈例数+显效例数)/总例数×100%。
1.4 安全性评估
观察三组不良反应类型及其发生率。不良反应包括高血压、肾功异常、毛囊炎、上呼吸道感染、注射部位反应等。不良反应发生率=不良反应例数/总例数×100%。
1.5 统计学方法
利用SPSS 26.0软件进行统计分析。年龄、DLQI评分、NAPSI评分改善率均采用均数加减标准差描述,组间比较采用方差分析,两两比较采用SNK-q检验;三组内治疗前后DLQI评分的比较采用配对t检验;三组间临床疗效的比较采用卡方检验,不良反应发生率的比较采用Fisher精确检验,组间临床疗效的两两比较采用Bonferroni法调整P值;治疗前后NAPSI评分采用混合线性模型进行分析,进一步组内各个时间点的两两比较采用Bonferroni 法调整P值。双侧P<0.05认为差异有显著统计学意义。
2 结果
2.1 三组NAPSI评分比较
治疗前,环孢素组、阿达木单抗组、司库奇尤单抗组的NAPSI评分分别为52.97±20.21、50.74±18.72、51.53±18.33,三组NAPSI评分无统计学差异(F=1.02,P=0.900);治疗12周后,三组NAPSI评分分别为42.20±16.66、32.16±13.82、32.37±10.97;治疗24周后,三组评分分别为31.17±15.14、17.81±14.72、19.27±9.90。三组NAPSI评分组间、时间、交互比较均存在显著差异(F交互=209.97,P<0.001;F时间=3.20,P=0.045;F组间=4.96,P<0.001),治疗12周后(F=5.06,P=0.008)、24周后(F=8.93,P<0.001),阿达木单抗组及司库奇尤单抗组NAPSI 评分均显著低于环孢素组,阿达木单抗组与司库奇尤单抗组之间无统计学差异(P>0.05,图1)。
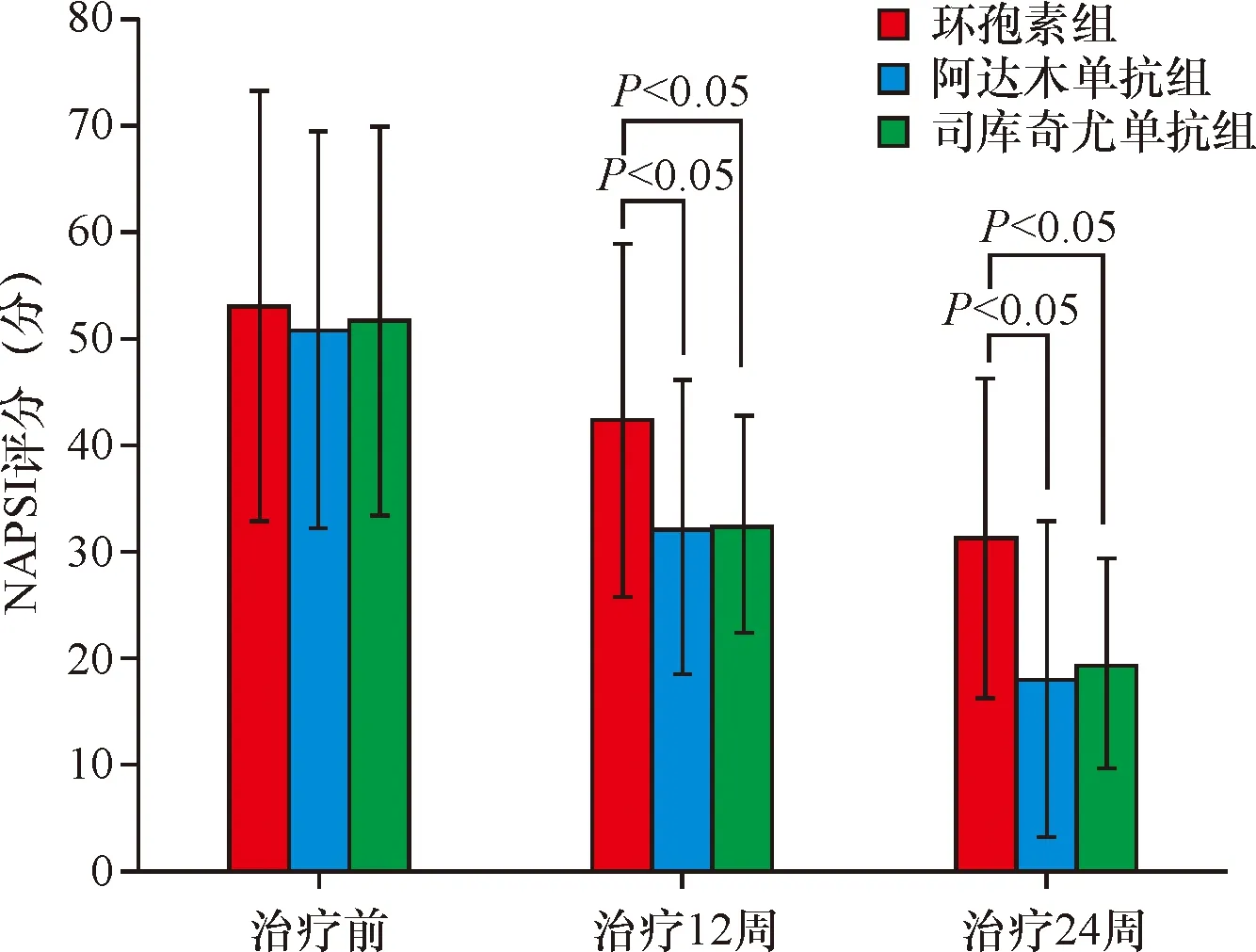
图1 三组治疗前后NAPSI评分比较Figure 1 Comparison of NAPSI after the treatment among the three groups.
2.2 三组NAPSI评分改善率比较
治疗12周后,环孢素组、阿达木单抗组、司库奇尤单抗组的平均改善率分别为(20.38±8.15)%、(37.34±13.00)%、(35.42±9.61)%;治疗24周后,三组的平均改善率分别为(42.84±15.29)%、(66.86±22.97)%、(61.86±15.68)%。在治疗12周后(F=23.74,P<0.001)和治疗24周后(F=14.41,P<0.001),阿达木单抗组和司库奇尤单抗组的NAPSI评分改善率均高于环孢素组,阿达木单抗组与司库奇尤单抗组之间无统计学差异(P>0.05,图2)。
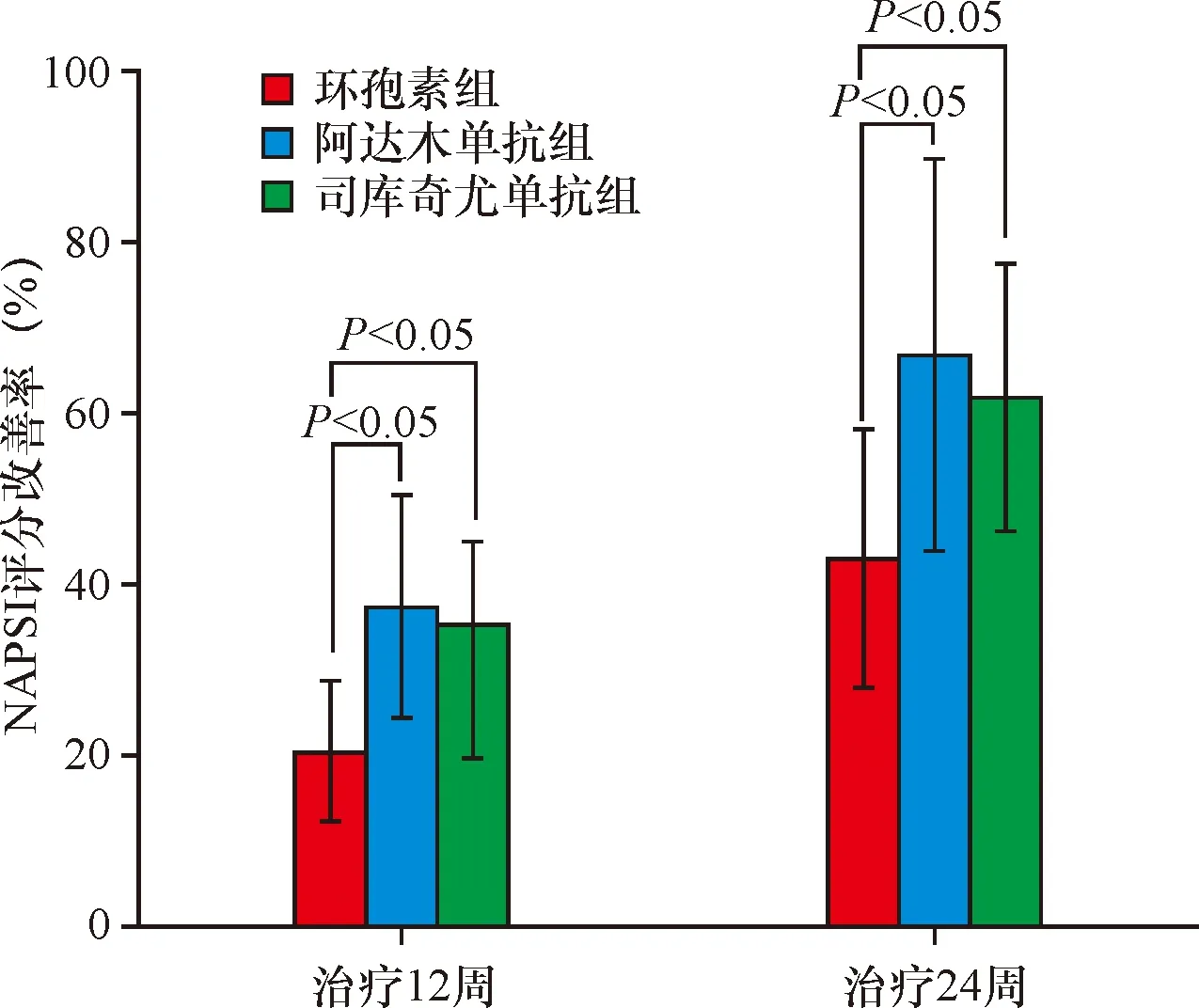
图2 三组治疗前后NAPSI评分改善率比较Figure 2 Comparison of average improvement rate of NAPSI after the treatment among the three groups.
2.3 三组DLQI评分比较
治疗前,环孢素组、阿达木单抗组、司库奇尤单抗组的DLQI评分分别为13.63±8.02、10.94±7.84、12.2±6.85,三组间DLQI评分无统计学差异(F=0.97,P=0.385)。治疗24周后,环孢素组、阿达木单抗组、司库奇尤单抗组的DLQI评分分别为10.43±8.50、4.71±4.52、6.30±5.04,三组DLQI评分均较治疗前下降(t环孢素=-3.57,P=0.001;t阿达木单抗=-6.09,P<0.001;t司库奇尤单抗=-8.44,P<0.001),阿达木单抗组和司库奇尤单抗组的DLQI评分均低于环孢素组(F=6.77,P=0.002)。治疗后,环孢素组、阿达木单抗组、司库奇尤单抗组的DLQI评分降低的差值分别为-6.23±5.70、-5.90±3.83、-3.20±4.92,阿达木单抗组、司库奇尤单抗组的DLQI评分降低差值均大于环孢素组(F=3.49,P=0.035),而阿达木单抗组与司库奇尤单抗组之间差异无统计学意义(P>0.05,图3)。
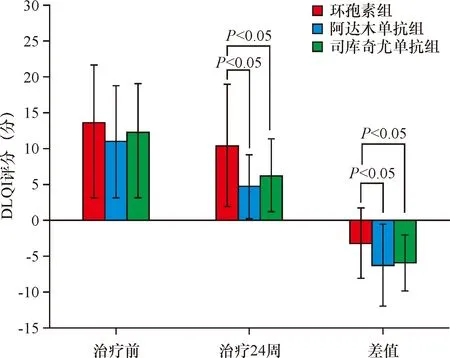
图3 三组治疗前后DLQI评分比较Figure 3 Comparison of DLQI after the treatment among the three groups.
2.4 三组临床疗效的比较

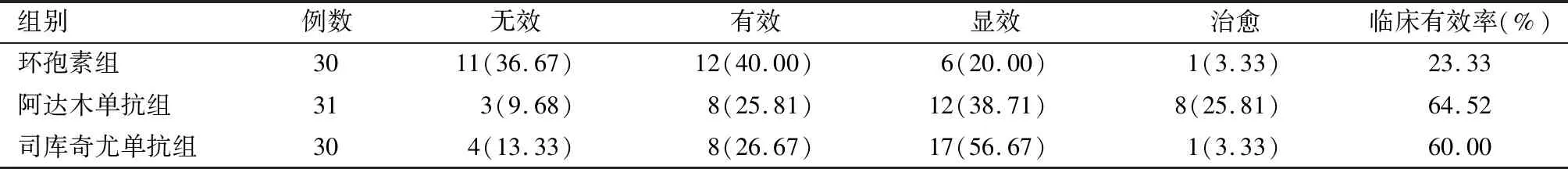
表1 三组治疗24周后临床疗效比较情况 [例(%)]Table 1 Comparison of clinical efficacy among the three groups after 24 weeks of the treatments [Case(%)]
2.5 药物安全性
治疗过程中,环孢素组患者出现高血压1例,肾功能异常2例,毛囊炎1例,上呼吸道感染3例;阿达木单抗组患者出现上呼吸道感染4例,注射部位反应3例;司库奇尤单抗组患者出现上呼吸道感染3例,注射部位反应2例,三组间不良反应发生率的差异无统计学意义(P>0.05,表2)。通过药物减量或对症用药处理后不良反应症状均缓解或消失,均未停止治疗。

表2 三组不良反应比较 [例(%)]Table 2 Comparison of adverse reactions among the three groups [Case (%)]
3 讨论
银屑病甲受累的严重程度与皮肤受累程度及病程长短具有一定相关性,但有些患者可仅有甲银屑病损害表现而无皮肤表现,一般甲银屑病患者男性多于女性[9]。甲银屑病的发病机制与炎症细胞因子信号转导通路密切相关,角质形成细胞释放的LL-37和 DNA/RNA 复合物刺激树突状细胞活化产生的IL-12和IL-23,继而刺激辅助T细胞产生白介素相关因子(Th1细胞释放TNF-α、Th17细胞释放 IL-17、Th22细胞释放IL-22),IL-17和TNF-α是维持银屑病的标志性炎症因子[3]。此外其机制还可能与白色念珠菌感染、HLA-Cw*0602等多个基因以及指尖关节受累的 Koebner 反应有关[10]。
环孢素通过抑制活化T细胞核因子(NFAT)的去磷酸化过程,阻止其转运至核内影响促炎症因子相关基因的转录,进而减少IL-2、IL-4、IL-8、TNF-α及转化生长因子(TGF-β)等相关炎症因子,进一步抑制调节性T淋巴细胞、辅助性T淋巴细胞等细胞功能,除此之外,环孢素还可以抑制角质形成细胞增殖,从而发挥治疗作用[11]。环孢素对伴有甲损害的银屑病疗效优于其他传统治疗银屑病的药物(如阿维A、甲氨蝶呤),其主要不良反应包括肾功能受损、高血压、疲劳、多毛、胃肠道疾病等[12]。一项关于环孢素与甲氨蝶呤治疗甲银屑病的单盲随机研究显示,应用环孢素24周后[前12周5 mg/(kg·d),后12周2.5~3 mg/(kg·d)],NAPSI平均改善率为37.9%[13]。该结果低于本研究(42.84%),但其完全治愈率(5.89%)高于本研究(3.33%),考虑可能与本研究使用的环孢素剂量不同有关。
IL-17A可与角质形成细胞表面受体结合,刺激多种抗菌肽及趋化因子产生,募集中性粒细胞及淋巴细胞等炎症细胞,促进角质形成细胞增殖并抑制其分化[14]。司库奇尤单抗是一种针对靶点IL-17A的全人源单克隆抗体,目前已被FDA批准应用于治疗成人斑块型银屑病、关节型银屑病、强直性脊柱炎,其主要不良反应包括上呼吸道感染、口腔疱疹、腹泻等[15]。2021年一项关于司库奇尤单抗治疗甲银屑病的32周双盲随机对照研究结果显示,应用16周后NAPSI评分改善率为45.3%,应用32周后NAPSI评分改善率为63.2%[16]。本研究应用司库奇尤单抗治疗12、24周后NAPSI评分改善率分别为35.42%、61.86%。可能因随访时间与既往报道不同,且本研究患者平均年龄(42.23岁)低于该报道平均年龄(45.10岁),本研究NAPSI评分改善率基本等于或略高于该报道。
TNF-α能够诱导角质形成细胞间黏附分子(ICAM-1、CD40)和主要组织相容性抗原(HLA),引起细胞内角质蛋白表达的改变,引起角质形成细胞病理性改变,在甲银屑病的发生发展中起着重要作用[17]。阿达木单抗是人源化抗TNF-α单抗,已被FDA批准应用于包括成人斑块型银屑病、关节型银屑病、成人类风湿关节炎等约10个适应症,其主要不良反应包括呼吸道感染、除黑素瘤外的皮肤肿瘤风险增加、白细胞减少症、血脂异常、头痛等[18]。2018年的一项为期26周的3期临床试验评估了阿达木单抗在中重度甲银屑病中的疗效及安全性,结果显示,在26周平均目标NAPSI的改善率为54.6%,总体mNAPSI 75应答率达到46.6%[19]。本研究应用阿达木单抗治疗12周NAPSI评分改善率为37.34%,治疗24周后其改善率为66.86%。本研究NAPSI评分改善率略高于既往研究,考虑原因为既往研究纳入银屑病患者为中重度(BSA>5%),评分方式选择mNAPSI评分,而本研究不限制皮肤受损程度。
本研究共纳入91例甲银屑病患者,治疗12、24周后,阿达木单抗及司库奇尤单抗组的NAPSI评分改善率均明显优于环孢素,但阿达木单抗组与司库奇尤单抗组之间无统计学差异。治疗24周后,阿达木单抗组(64.53%)、司库奇尤单抗组(60.00%)的临床有效率显著优于环孢素(23.33%),而阿达木单抗组与司库奇尤单抗组之间无统计学差异。表明阿达木单抗与司库奇尤单抗治疗甲银屑病的皮损改善情况及临床疗效无明显差异,但均优于环孢素。
甲银屑病有碍美观,严重者可有功能障碍,与关节型银屑病高度相关,严重影响患者的生活质量[20]。本研究采用DLQI问卷评估甲银屑病患者的生活质量,发现三种药物均可改善甲银屑病患者生活质量,且应用司库奇尤单抗及阿达木单抗的患者DLQI评分改善明显优于应用环孢素的患者。
针对长期使用药物治疗甲银屑病的安全性问题,除注射部位局部反应外,阿达木单抗组和司库奇尤单抗组均出现了上呼吸道感染的不良反应,其机制可能与TNF-α通过促炎基因激活MAPK 和 NF-κB 信号传导途径建立炎症反应以此起到对病原体的免疫防御作用有关[20]。IL-17作为TNF-α的上游因子也有类似机制,同时IL-17A和IL-17F可以调节趋化因子CXC和G-CSF的产生,并诱导产生抗菌肽(如b防御素S100A家族蛋白)起到抵御病原体的作用,而阿达木单抗和司库奇尤单抗作为TNF-α、IL-17的抑制剂,削弱了其对机体的抗感染作用[21]。阿达木单抗组及司库奇尤单抗组的其余不良反应发生率均低于环孢素组,三组总不良反应发生率无统计学差异。
综上,环孢素、阿达木单抗、司库奇尤单抗均对甲银屑病的治疗有一定疗效,阿达木单抗、司库奇尤单抗疗效明显优于环孢素,提示生物制剂可作为治疗甲银屑病的有效方法。但本研究收集病例数较少,将来应扩大样本量进一步研究,观察不同治疗方式导致不良反应的差异。同时,因甲本身生长周期长,患者至少需要6~9个月的持续用药,因此应在患者能耐受情况下继续延长治疗时长,以观察治疗甲银屑病的长期疗效以及长期用药安全性。

