化学实验基础题的解题思路和策略
邓彦平
化学是一门以实验为基础的学科,从近几年全国卷高考试题看,化学实验在选择题中共出现7次,出现概率为100%。试题考向有以下四个方面:一是化学实验常识及基本操作;二是物质的检验、分离和提纯;三是实验方案的评价;四是物质制备和性质验证实验。我将从这四个方面的题型对化学实验基础题的解题方法和解题策略进行简单的总结。
一、化学实验基础题的解题方法
(一)化学实验常识及基本操作题
例题一:(2020山东卷,1)实验室中下列做法错误的是( )
A.用冷水贮存白磷
B.用浓硫酸干燥二氧化硫
C.用酒精灯直接加热蒸发皿
D.用二氧化碳灭火器扑灭金属钾的燃烧
[必备知识]物质的保存、气体的干燥、仪器的使用、事故处理。
[能力素养]试题以实验基本操作的正误判断为载体,从药品保存、气体净化、仪器使用和事故处理等角度,考查学生的推理判断等能力。
1.推理判断能力
①基于物质性质的药品保存判断。
白磷的着火点低,白磷在空气中易自燃,白磷的密度大于水的密度,基于以上几条白磷的性质,所以白磷应冷水贮存。
②基于物质性质的除杂判断。
二氧化硫与浓硫酸不反应,浓硫酸有吸水性,故可用浓硫酸干燥二氧化硫。
③基于仪器特征的使用判断。
蒸发皿形状是弧面 ,蒸发皿的厚度较大且较为均匀,不易破裂,故可直接用酒精灯加热。
④基于物质性质的事故处理判断。
钾燃烧生成过氧化钾、超氧化钾,过氧化钾、超氧化钾与二氧化碳反应生成氧气且反应放热,所以金属钾燃烧时不能用二氧化碳灭火。
2.批判性思维能力
烧杯和蒸发皿的主要成分都是硅酸盐,为什么蒸发皿能用酒精灯直接加热而烧杯不能?
[答案]D
[失分原因剖析]由于不能根据钠与氧气反应的产物推测钾与氧气反应的产物,不能根据过氧化钠与二氧化碳的反应推测过氧化钾或超氧化钾与二氧化碳的反应,而错判D项。
(二)物质的检验、分离和提纯
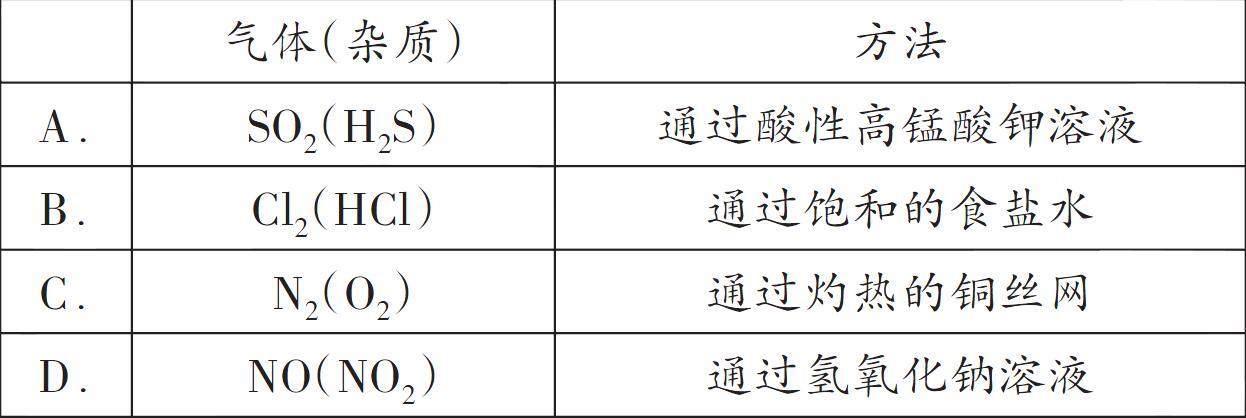
例题二:(2020全国一卷,9)下列气体去除杂质的方法中,不能实现目的的是( )
[必备知识]物质的性质、气体的除杂。
[能力素养]试题以物质除杂方法的正误判断为载体,从物质的性质、除杂方法的选择等角度,考查学生的推理判断等能力。
1.推理判断能力——基于物质性质的除杂方法判断
①含硫化合物SO2具有较强的还原性,H2S具有较强的还原性,二者都能被酸性高锰酸钾溶液氧化
②氯及其化合物氯化氢易溶于饱和食盐水,氯气难溶于饱和食盐水,氯气中的氯化氢用饱和食盐水可除去
③氧气能与灼热的铜反应,氮气不能与灼热的铜反应,除去氮气中的氧气用灼热的铜丝网
④氮及其化合物的性质 ,NO2可以与NaOH反应,NO与NaOH 溶液不反应,故可通过NaOH溶液除去NO2
2.批判性思维:NO?和NO混合气体可以与NaOH溶液发生反应生成NaNO2,为什么还可以用NaOH溶液除去NO中的NO2呢?[答案]A
[失分剖析]忽视SO2也能被酸性高锰酸钾溶液氧化而错判A项。
例题三:(2022全国乙卷,9)某白色粉末样品,可能含有[Na2SO4]、[Na2SO3]、[Na2S2O3]和[Na2CO3]。取少量样品进行如下实验:
①溶于水,得到无色透明溶液。
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加[BaCl2]溶液有沉淀生成。
该样品中确定存在的是( )
A.[Na2SO4、Na2S2O3] B. [Na2SO3、Na2S2O3]
C. [Na2SO4、Na2CO3] D. [Na2SO3、Na2CO3]
[试题情境]本题是以判断混合物组成作为情境,属于实验探究情境。
[必备知识]元素化合物性质、物质的鉴别。
[能力素养]试题给出了物质鉴别的操作过程和实验现象,要求判断该混合物的组成,要考查学生信息获取与加工、逻辑论证能力。
1.信息获取与加工能力
关键信息:①取少量样品溶于水得到无色透明溶液;②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出;③取②的上层清液,向其中滴加BaCl2溶液,有沉淀生成。
2.逻辑论证①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在Na2S2O3发生反应S2O2-
3 +2H+=S↓+H2O+SO2↑,离心分离,③取②的上层清液,向其中滴加BaCl2溶液,有沉淀生成,则沉淀为BaSO4,说明固体中存在Na2SO4,不能确定是否有Na2SO3和Na2CO3,Na2SO3与过量盐酸反应生成二氧化硫,Na2CO3与过量盐酸反应生成二氧化碳,而这些现象可以被Na2S2O3与过量盐酸反应的现象覆盖掉,综上分析,该样品中确定存在的是:Na2SO4、Na2S2O3。[答案]A
[失分原因剖析]对硫代硫酸钠与酸反应认识不清。
(三)实验方案的评价
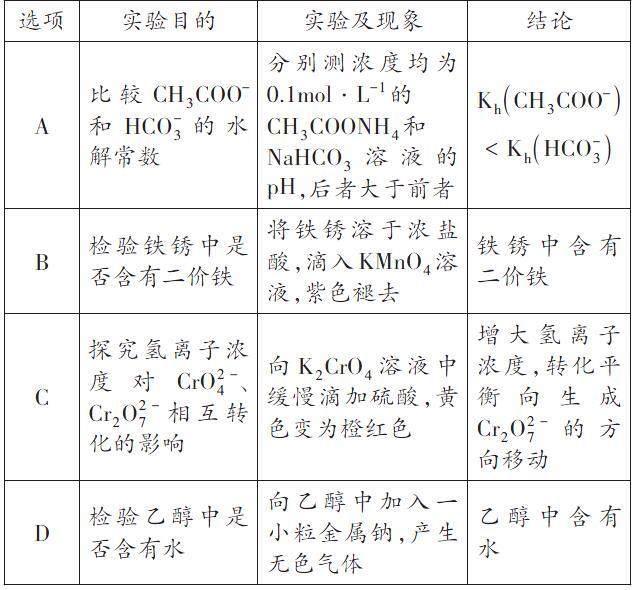
例题四:(2022年全国甲卷,13)根据实验目的,下列实验及现象、结论都正确的是( )
A. A B. B C. C D. D
[必备知识]物质的检验和物质的性质、氧化还原反应、水解反应、根据实验现象的判断。
[能力素养]试题给出了四组实验操作和实验现象,分别涉及盐类的水解、氧化性、物质的检验、物质的性质以及,需要评价实验操作和实验现象能否得到相应的结论,主要考查学生信息获取与加工、逻辑论证能力。
A.CH3COONH4中[NH+4]水解,[NH+4+H2O][]
[NH3?H2O+H+],会消耗CH3COO-水解生成的OH-,测定相同浓度的CH3COONH4和NaHCO3溶液的pH,后者大于前者,不能说明Kh(CH3COO-)<Kh([HCO-3]),A错误;
B.浓盐酸也能与KMnO4发生反应,使溶液紫色褪去,B错误;
C.K2CrO4中存在平衡2[CrO2-4](黄色)+2H+[]
[Cr2O2-7](橙红色)+H2O,缓慢滴加硫酸,H+浓度增大,平衡正向移动,故溶液黄色变成橙红色,C正确;
D.乙醇和水均会与金属钠发生反应生成氢气,故不能说明乙醇中含有水,D错误;[答案]C
[失分原因剖析]忽略铵根离子的水解和Cl-与酸性高锰酸钾溶液反应。
(四)物质制备和性质验证实验
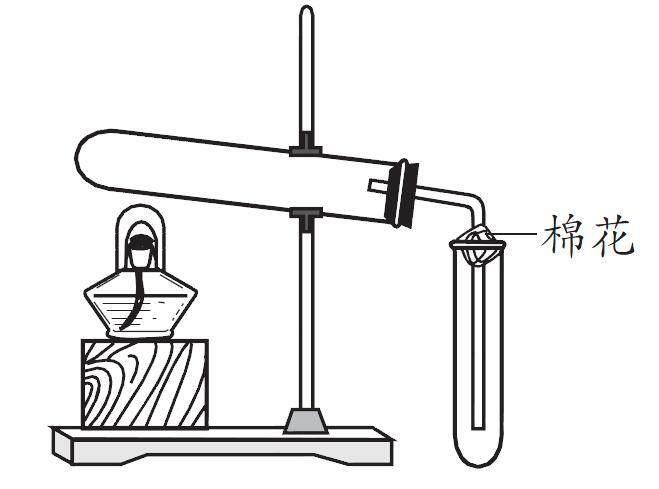
例题五:(2021全国乙卷,8)在实验室采用如图装置制备气体,合理的是( )
[棉花]
[必备知识]常见气体制备的反应原理和实验装置。
[能力素养]试题给出了实验装置和四组化学试剂,判新所给实验装置和试剂能否制备品需气体,主要考查学生的信息获取与加工、逻辑论证和推理判断能力。
1.信息获取与加工能力
Ca(OH)2+NH4Cl和MnO2+KClO3均为固态药品;MnO2+HCl和 NaCl+H2SO4(浓)均为固态和液态药品的反应。
2.逻辑论证——基于实验装置证据的综合分析
由大试管口向下倾斜可知反应物应为固态药品
需加热一有酒精灯一小试管口向上一向上排空气法一气体密度应大于空气的气体
3.推理判断能力
(1)基于气体发生装置的状态分析。气体发生装置,试剂应均为固态,Ca(OH)2+ NH4Cl和MnO2+KClO3,均为固态药品,符合要求,MnO2+HCl(浓)和NaCl+H2SO4(浓)中均有液态药品,不符合要求;(2)基于气体收集装置的密度分析。气体收集装置,气体密度应大于空气,NH3的密度小于空气,不符合要求,O2的密度大于空气,符合要求;(3)基于反应条件的原理分析。反应条件:酒精灯加热,MnO2+KClO3的反应需要加热→符合要求。
4.批判性感维能力
(1)收集气体的小试管口处有一团棉花,棉花的作用是什么?(2)哪种物质也可以用该装置制备氧气?(3)利用该装置收集的氧气可能带有一定的颜色,其原因是什么?(4)制备氧气时是否需要除杂装置和吸收装置?
5.模型构建:气体制备装置的分析思维
第一步,看反应装置:根据反应装置判断反应物的状态和反应条件;第二步,看除杂装置。根据所含杂质判断除杂装置和除杂试剂的正误:第三步,看收集装置:根据气体的性质判断收集装置和收集方法的正误;第四步,看吸收装置:根据气体的性质判新吸收装置和吸收试剂的正误。[答案]C
[失分剖析]易混清向上排空气法和向下排空气法而错选A项。
例题六:(2021年全国甲卷,9)实验室制备下列气体的方法可行的是( )
[必备知识]常见气体的制备。
[能力素养]试题给出了四种气体以及制备方法,需要根据所给试剂判断能否制备所需气体,主要考查学生推理判断能力。
(1)推理判断能力:①基于反应物性质的原理分析。浓硝酸有强氧化性,铝通冷浓硝酸,铝表面会被纯化反应停止,无法制备二氧化氪;浓硫酸有强氧化性,硫离子有强还原性,两者发生氧化还原反应生成S单质,无法制备硫化氢;②基于生成物性质的原理分析。加热氯化铵固体生成NH3和HCl,NH3和HCl遇冷又生成氯化铵固体无法制备氨气;③基于气体制备原理的综合分析。加热氯酸钾和二氧化锰的湿合物,反应物生成物和反应条件均符合要求。
(2)批判性思维能力
①实验室可能有哪些制备氨气的方法?各自的反应原理是什么?②铝片和冷浓硝酸是否能发生反应?铝片和热浓硝酸能否反应生成二氧化氮?
(3)模型构建:气体制备的分析思维
第一步,看反应物;第二步,看反应条件;第三步,看生成物。[答案]D
[失分原因剖析]误认为加热氯化铵可生成氨气,从而错判A项。
二、化学实验基础题的解题策略
化学实验选择题的命题范围(或考查范围)很广,例如:从知识方面来说,如无机元素化合物的实验、有机化合物的实验、电化学实验;从“定性”与“定量”方面来说,既有定性实验,也有定量实验;从实验本身来说,往往涉及实验目的、实验过程与不足、实验仪器的选择与使用方法、实验现象的描述与应用、实验结论的归纳与表达,等等。所以给大家的解题策略具体如下。
(一)熟悉常考的题型结构和考查点。通过题型分析归纳,全面渗透地掌握考情考法归纳及其稳定与变化的规律,以此为纲进行针对性复习和做题,提高得分率。
(二)掌握化学实验基本操作要求及常见仪器的使用方法,掌握评价行实验题的常见类型及分析方法。
(三)要强化整理和记忆热点题型,由于本部分知识相对杂乱,易出现细节上的错误,要整理常见易错点并强化记忆,做题时根据平时的记忆进行做题,从而提高做题速度和得分率。
(四)做实验题时不能孤立地看待实验,要学会理解与变通,将实验题与元素化合物的性质进行紧密联系,因为仪器的选择、分离提纯、物质的检验、物质的制备等均与元素化合物的性质密切相关。

