脑深部电极植入术对帕金森病患者冻结步态及日常活动能力的影响
齐再利
(济南市第三人民医院神经外科,山东济南 250132)
帕金森病(PD)是一种神经系统退行性病变,高发于老年人群,患者常伴有肌强直、运动迟缓、步态异常、日常活动能力受限等症状,对患者日常生活造成较大影响[1]。 PD 应及时予以有效的治疗方案,以控制患者病情,防止进一步损害神经系统,改善预后[2]。 临床治疗PD 首选药物疗法,操作简单,具有一定效果,但单用药物治疗时疗程较长,部分患者易出现不良反应,或停药后易复发,整体效果并不理想[3]。 脑深部电极植入术(DBS)是利用立体定向技术向患者颅内植入电极,神经调控装置安装于胸部皮下,二者相连接可通过体外遥控器调节刺激参数从而改善患者症状,临床应用具有微创、可调控、安全等优势,但关于DBS对PD 患者冻结步态的改善效果尚未可知[4]。 鉴于此,本研究选取该院收治的50 例PD 患者作为对象,进一步探讨DBS 对PD 患者冻结步态及日常活动能力的影响。 现报道如下。
1 资料与方法
1.1 一般资料
选取2021 年6 月—2023 年3 月该院收治的50 例PD 患者作为研究对象。 纳入标准:(1)符合PD诊断标准[5];(2)视听功能正常,意识清楚;(3)自愿接受治疗;(4)患者依从性良好,可配合研究进行;(5)对本研究均知情,并签署同意书。 排除标准:(1)脑部出现器质性病变或合并其他恶性病变;(2)出现痴呆或精神障碍,无法进行日常交流;(3)不耐受本研究治疗方案;(4)合并精神分裂症、焦虑、抑郁等精神疾病;(5)近期使用抗血小板药物。 根据随机数字表法将研究对象分为对照组和观察组,各25 例。 对照组:男性14 例,女性11 例;年龄42~79 岁,平均年龄(60.29±6.17)岁;体重41~87 kg,平均体重(75.38±7.15)kg;病程3~16 年,平均病程(8.76±1.22)年;术前药物使用时间为2~14 年,平均时间(7.39±1.07)年。 观察组:男性15 例, 女性10 例; 年龄41~78 岁, 平均年龄(60.39±6.42)岁;体重41~86 kg,平均体重(75.43±7.37)kg;病程3~15 年,平均病程(8.49±1.58)年;术前药物使用时间为2~12年,平均时间(7.11±1.02)年。 两组一般资料比较,差异无统计学意义(P>0.05)。 本研究经院医学伦理委员会批准。
1.2 方法
对照组采用常规治疗,使用抗PD 药物,口服左旋多巴(精华制药集团股份有限公司,国药准字H32 022244)治疗,0.25 g/次,3 次/d。
观察在对照组基础上加用DBS 治疗, 具体内容如下:术前12 h 停用所有抗PD 药物,使其处于关期状态。 实施局麻,随后安装立体定向头架[医科达(瑞典)医疗器械有限公司,国械注进20142056130,型号:Leksell C],行MRI 扫描检查,明确脑深部电刺激丘脑底核(STN)的坐标。 局麻下在颅骨上钻孔,选择脑神经刺激系统(北京品驰医疗设备有限公司,国械注准20163210990), 刺激电极经最佳针道植入手术靶点,随后连接临时刺激器,打开开关,进行刺激,观察不同靶点的刺激情况, 可根据患者实际情况调整各项参数,防止出现不良反应。明确电极最佳位置后,可在颅骨上固定电极,并对切口进行缝合。将头架拆除,实施全麻,通过皮下隧道将植入电极使用延长导线将其与电刺激器连接,并于胸部皮下埋藏电刺激器。术后1 周,再次进行头颅MRI 检查,观察电极植入位置。14 d 后开启刺激器,刺激器开启当日切勿服用抗PD 药物,设置初始刺激参数:频率130~180 Hz,脉宽60~90 μs,电压1.0~3.5 V,随后可酌情调整刺激参数,由低到高进行调整。
1.3 观察指标
(1)冻结步态:分别于治疗前、治疗后,比较两组冻结步态评分,参考Ziegler 等[6]的研究设计,要求两组患者完成4 种行走任务, 包括原地逆时针旋转360°、转弯、原地顺时针旋转360°、起步,总分36 分,评分越高表明患者步态障碍越严重。
(2)日常活动能力:分别于治疗前、治疗后,比较两组日常活动能力, 使用日常生活活动能力量表(ADL)[7]评估,从穿衣、洗漱、站立等多个方面评估,总分100 分,评分越高表明患者日常活动能力越好。
(3)步长、步速:分别于治疗前、治疗后,比较两组步长、步速,使用足印分析法测量并记录两组患者步行过程的平均步长、步速,反复测试3 次,取均值作为最后结果。
1.4 统计方法
采用SPSS 22.0 统计学软件进行数据分析。 计量资料以()表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验; 计数资料以n表示,组间比较采用χ2检验。P<0.05 为差异有统计学意义。
2 结 果
2.1 两组患者治疗前后冻结步态、ADL 评分对比
治疗前,两组冻结步态、ADL 评分对比,组间差异无统计学意义(P>0.05);治疗后,两组冻结步态评分均低于治疗前,ADL 评分均高于治疗前,且观察组冻结步态评分低于对照组,ADL 评分高于对照组,差异有统计学意义(P<0.05)。 见表1。
表1 两组PD 患者治疗前后冻结步态、ADL 评分对比[)),分]
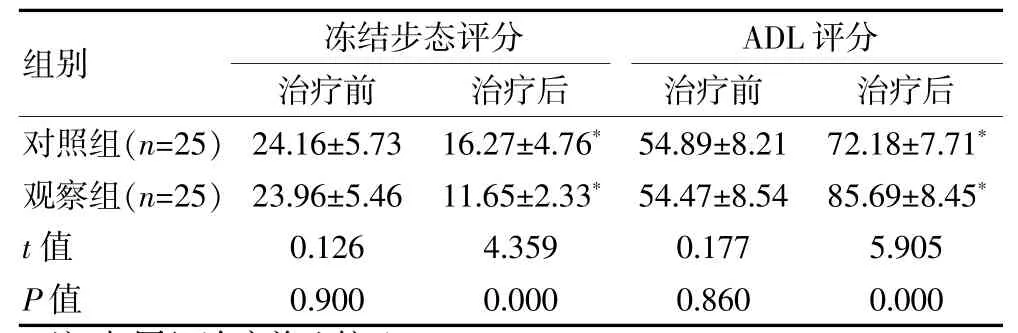
表1 两组PD 患者治疗前后冻结步态、ADL 评分对比[)),分]
注:与同组治疗前比较,*P<0.05。
?
2.2 两组患者治疗前后步长、步速对比
治疗前,两组步长、步速对比,组间差异无统计学意义(P>0.05);治疗后,两组步长均较治疗前延长,步速均较治疗前加快,且观察组步长长于对照组,步速快于对照组,差异有统计学意义(P<0.05)。 见表2。
表2 两组PD 患者治疗前后步长、步速对比()
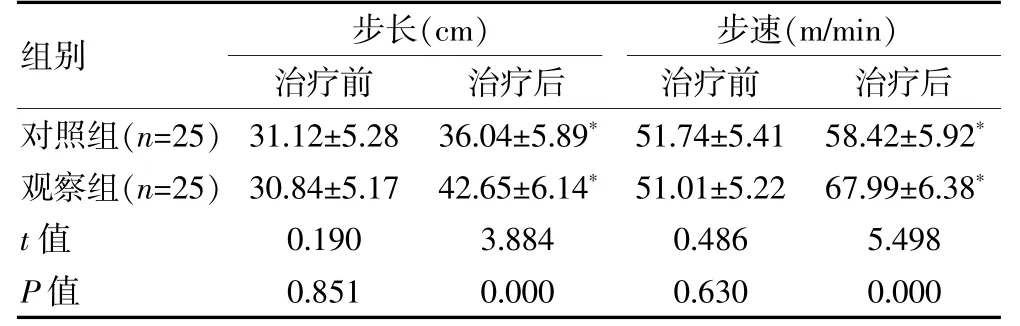
表2 两组PD 患者治疗前后步长、步速对比()
注:与同组治疗前比较,*P<0.05。
?
3 讨 论
PD 的发病机制较为复杂, 具体原因至今尚未完全明确,与年龄、遗传、氧化应激等多方面因素有关,当疾病发展至中晚期时患者易出现冻结步态,主要表现为步长减小、步速减慢[8-9]。 冻结步态通常发生于步态起始、转弯以及遇到障碍物或步行时同时执行其他任务时,易导致患者意外摔倒,出现受伤,严重者甚至骨折,对患者造成的损害较大,临床应予以及时有效的治疗,以缓解冻结步态,改善患者预后[10]。
目前临床治疗PD 以药物最为常用,通过使用抗PD 药物能够有效改善患者病情,恢复运动功能,但因存在个体差异性,部分患者对药物不敏感或不良反应多,导致药物治疗效果有限[11]。 但冻结步态仅予以常规药物治疗效果较差, 应寻找更加高效的治疗方法。DBS 又被称为“脑起搏器”,将电极刺激器植入脑组织深部,发放电脉冲刺激相关神经核团,对异常的神经电活动进行调节, 从而能够控制或减轻患者症状。DBS 治疗难治性PD 具有一定效果,通过刺激靶点可改善运动障碍,减少抗PD 药物使用量,临床应用备受认可。本研究结果显示,治疗后,两组冻结步态评分均低于治疗前,ADL 评分均高于治疗前,且观察组冻结步态评分低于对照组,ADL 评分高于对照组,差异有统计学意义(P<0.05);两组步长均较治疗前延长,步速均较治疗前加快, 且观察组步长长于对照组,步速快于对照组,差异有统计学意义(P<0.05)。 这表明PD 患者采用DBS 治疗效果确切,利于改善患者冻结步态,提升日常生活活动能力,增加患者步幅,加快步速,值得临床广泛应用。分析其原因为,DBS 作为一种神经调控手术,具有创伤小、效果确切、安全可靠等优势,且术后能够灵活调控,是当前最先进的PD 治疗手段[12]。 DBS 通过向大脑内植入微电极,对脑深部的特定核团进行刺激,从而控制患者病情,且能够减少其他药物剂量,降低不良反应发生风险,并可根据患者情况合理调整刺激参数,且具有可逆性,能够有效改善患者冻结步态症状,提升日常生活能力及生活质量。
综上所述,PD 患者采用DBS 治疗效果确切,利于改善患者冻结步态,提升日常生活活动能力,增加患者步幅,加快步速,值得临床广泛应用。

