基于快速CYP2C19基因检测发现携带功能缺失等位基因的急性轻型缺血性卒中双抗治疗1例报道
冯博,赵彩君,常立国
1 病例介绍
患者男性,73岁,农民。主诉“言语不清伴右侧肢体麻木无力4.5小时”,于2021年11月2日入院。患者于入院前4.5 h吃饭时突然出现言语不清,但语句尚连贯,伴右侧肢体无力,右面部及右上、下肢麻木不适,右上肢抬举及持物尚可,右下肢行走无明显拖拽。无头晕、头痛、恶心、呕吐,无声音嘶哑,无视物模糊、变形、闪光,无耳鸣、耳聋、听力下降,无肢体抽搐,无意识障碍。为求系统诊治来我院就诊,门诊以“缺血性卒中”收入院。
既往史:高血压病史10余年,收缩压最高达170 mmHg(1 mmHg=0.133 kPa),目前未口服降压药物。糖尿病病史10余年,目前口服二甲双胍、格列本脲治疗,血糖水平控制不详。2个月前曾因“言语不清6小时”在外院以缺血性卒中进行治疗,给予标准双联抗血小板药物(首次服用阿司匹林100 mg,氯吡格雷300 mg,第2日开始服用阿司匹林100 mg,每日1次,氯吡格雷75 mg,每日1次,持续21 d后改用氯吡格雷75 mg,每日1次,服用至本次发病前)及降脂(阿托伐他汀钙20 mg/d)治疗,住院10 d症状完全缓解后出院。
入院查体:体温36.5 ℃,心率84次/分,呼吸21次/分,血压155/76 mmHg。精神差,双肺呼吸音清,未闻及干、湿性啰音,心律齐,各瓣膜听诊区未闻及杂音。腹软,无压痛及反跳痛,肝脾肋下未及,双下肢无浮肿。神经系统查体:神志清,不完全运动性失语,无眼震,面纹对称,伸舌居中,右侧上、下肢肌力4级,左侧肢体肌力5级,肌张力正常,右侧Babinski征阳性。无脑膜刺激征。全身深浅感觉查体正常。NIHSS 3分。
辅助检查:
外院头颅CT(2021-11-02):未见明显梗死灶。
实验室检查:血糖11.78 mmol/L;血常规、感染性标志物、凝血功能、肝肾功能、血脂、脑钠肽、肌钙蛋白I、电解质、尿常规加沉渣分析、大便常规及潜血未见明显异常。
心脏彩色超声(2021-11-03):左心室充盈异常,主动脉瓣反流(轻-中度)。颈部血管彩色超声(2021-11-03):右侧颈动脉内膜增厚,左侧颈动脉斑块形成,右侧锁骨下动脉斑块形成,双侧椎动脉阻力增高。
表妹夫吭吭哧哧地有点不好意思:“我心目中最理想的妻子就是嫂子这样的!能和表哥一起承担养家压力,有自己喜欢的工作,有个人生活和朋友圈子,信任、理解表哥,给表哥充分的自由空间,表哥是我认识的已婚男人当中最有福气的一个!”
头颅MRI(2021-11-03):左侧丘脑急性或亚急性期梗死(图1),SWI序列未见明显异常;MRA显示双侧颈内动脉虹吸部管腔粗细不均,血流信号不均匀,双侧大脑中动脉主干管壁僵直,主干及远端管腔粗细不均,血流信号欠均匀,远端及分支尚可,基底动脉未见明确异常,双侧大脑前动脉及大脑后动脉管壁毛糙,管腔局限性血流信号减弱,双侧后交通动脉开放。
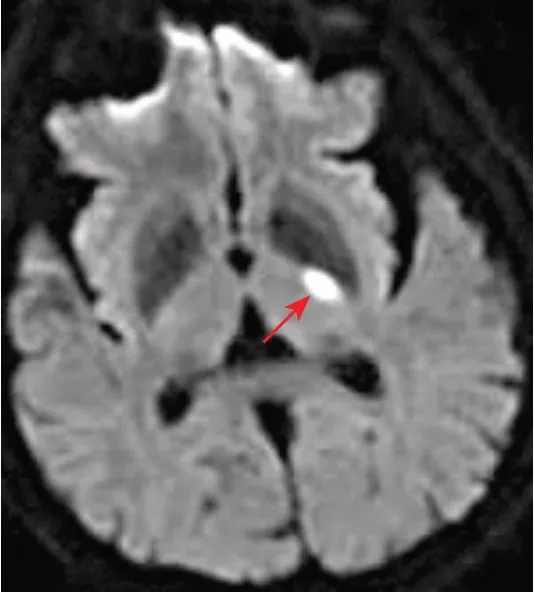
图1 患者发病1 d头颅MRI检查结果
TCD(2021-11-03):高阻型脑血流改变,双侧大脑中动脉狭窄(左侧中度;右侧轻度),右侧颈内动脉终末段狭窄(中度),左侧大脑前动脉狭窄(轻度),基底动脉狭窄(中度)。
头颈部CTA(2021-11-04):动脉粥样硬化表现,双侧颈总动脉中远段非钙化斑块影,管腔轻度狭窄;左侧颈内动脉C1段钙化及非钙化斑块影,管腔轻度狭窄;双侧椎动脉钙化及非钙化斑块影,双侧V4段管腔中-重度狭窄;颅内段管腔多发局限性狭窄(图2)。
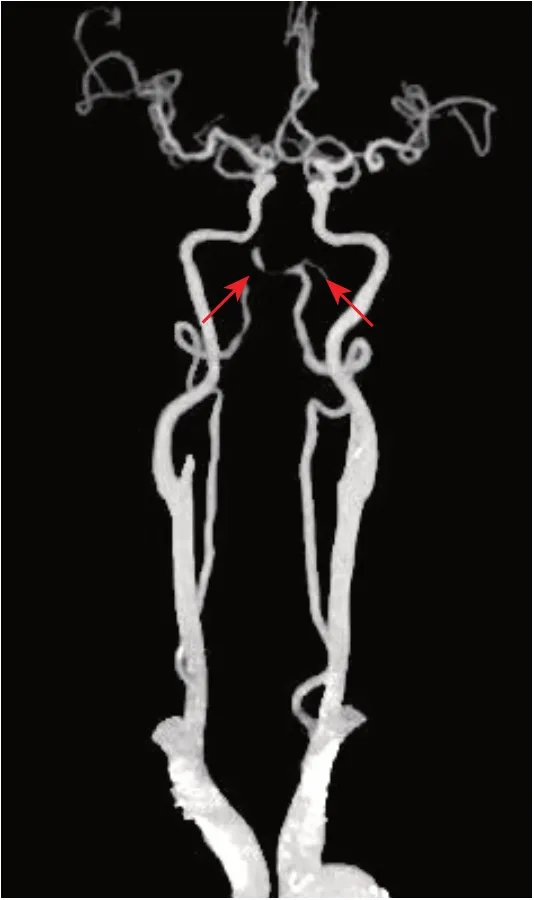
图2 患者发病2 d时头颈部CTA检查结果
DSA(2021-11-06):右侧椎动脉颅内段闭塞,左侧椎动脉V4段重度狭窄(狭窄率80%);左侧椎动脉与基底动脉交汇处重度狭窄(狭窄率80%)。
初步诊断:
缺血性卒中
高血压2级(极高危)
2型糖尿病
诊疗经过:本患者确诊为急性缺血性卒中,发病时间在24 h内,NIHSS 3分,为急性高危非致残性缺血性脑血管事件(high-risk non-disabling ischemic cerebrovascular events,HR-NICE)患者。采集患者咽部脱落细胞,采用全自动医用PCR分析系统(重庆京因生物科技有限责任公司)进行CYP2C19*2、*3及*17等位基因检测,结果为CYP2C19*1/*2(*2:GA;*3:GG),中间代谢型,考虑患者存在氯吡格雷抵抗可能,故给予阿司匹林首剂量100 mg,替格瑞洛首剂量180 mg口服双联抗血小板治疗,第2日开始给予阿司匹林100 mg,每日1次,替格瑞洛90 mg,每日2次。另外给予阿托伐他汀钙20 mg/d降脂治疗。
综合检查结果考虑患者的TOAST分型为大动脉粥样硬化型。继续给予阿司匹林、替格瑞洛抗血小板聚集,阿托伐他汀钙降脂治疗,患者病情好转,住院10 d出院。出院时查体:神志清楚,言语流利,无眼震,面纹对称,伸舌居中,四肢肌力5级,肌张力正常,双侧Babinski征阴性。无脑膜刺激征。全身深浅感觉正常。NIHSS 0分。出院后继续服用阿司匹林100 mg,每日1次、替格瑞洛90 mg,每日2次至21 d,后改用替格瑞洛90 mg,每日2次治疗,持续应用阿托伐他汀钙20 mg/d。
最终诊断:
缺血性卒中
左侧颈内动脉系统
大动脉粥样硬化型
脑动脉狭窄
高血压2级(极高危)
2型糖尿病3个月随访患者病情无复发,NIHSS 0分。
复查TCD(2022-02-10):脑动脉硬化血流频谱改变,双侧大脑中动脉狭窄(左侧中度;右侧轻度),右侧颈内动脉终末段狭窄(中度),左侧大脑前动脉狭窄(轻度),左侧椎动脉狭窄(重度),基底动脉狭窄(轻度)。6个月随访时患者病情稳定,无复发,NIHSS 0分。复查头颅CT(2022-05-21):左侧丘脑点状低密度影,双侧脑室形态可,脑沟裂池增宽、加深。TCD(2022-05-21):脑动脉硬化血流频谱改变,脑血管狭窄程度同前无显著变化(图3)。
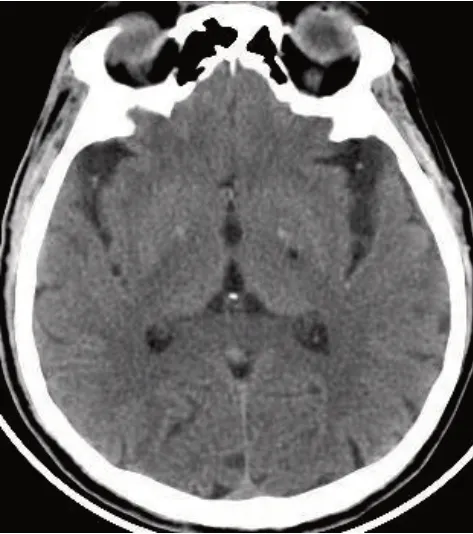
图3 患者发病6个月随访头颅CT结果
2 讨论
HR-NICE包括发病24 h内的高危TIA(ABCD2≥4分)和轻型缺血性卒中,通常急性期内神经功能缺失较轻,易被临床忽视,但可在短期内症状进展或复发,临床上约65%的缺血性脑血管病是此种类型[1-2]。HR-NICE患者在3个月时卒中复发率高,复发后临床预后不良[3]。因此,早期进行临床评估和针对性的二级预防对改善患者的临床预后、降低早期卒中复发以及减少治疗花费都具有积极意义。
HR-NICE最重要的急性期治疗及二级预防手段之一就是长期服用抗血小板聚集药物。2013年氯吡格雷用于急性非致残性脑血管事件高危人群(clopidogrel in high-risk patients with acute non-disabling cerebrovascular events,CHANCE)研究发现,阿司匹林联合氯吡格雷相比单独应用阿司匹林可显著降低HR-NICE患者新发血管事件的风险,且不增加出血风险[4]。《中国缺血性脑卒中和短暂性脑缺血发作二级预防指南2014》建议对发病24 h内的HR-NICE患者采用阿司匹林联合氯吡格雷的短程、双联抗血小板治疗方案进行治疗和二级预防[5]。
氯吡格雷是第2代噻吩并吡啶类,在十二指肠被机体吸收后,通过肝脏的细胞色素P450(cytochrome P-450,CYP)2C19系统转化为活性代谢产物,最终与血小板P2Y12受体结合,从而阻止血小板聚集活化[6]。研究发现,氯吡格雷对部分患者抗血小板聚集疗效欠佳,这种反应性差异的原因包括非遗传因素和遗传因素[7-8]。目前研究认为CYP450酶系中的CYP2C19、CYP1A2和CYP2B6参与氯吡格雷的氧化过程,CYP2C19、CYP2C9、CYP2B6和CYP3A4参与其水解过程。其中CYP2C19基因调控的酶参与了氯吡格雷生物转化中的2个代谢步骤,是促进氯吡格雷活化的主要代谢酶[6]。CYP2C19基因突变后,氯吡格雷代谢状态发生改变,可能导致体内血小板反应性增高,即发生氯吡格雷抵抗,还可能导致氯吡格雷活性增强而出现药物性出血[9]。
替格瑞洛作为新型P2Y12受体拮抗剂,主要是通过CYP3A4酶进行代谢,与氯吡格雷相比,可能具有更快、更强、更稳定的血小板抑制作用,且不受CYP2C19基因突变的影响。氯吡格雷联合阿司匹林用于急性非致残性脑血管事件高危人群(clopidogrel with aspirin in high-risk patients with acute non-disabling cerebrovascular events 2,CHANCE 2)研究发现,对于携带CYP2C19功能缺失(loss-offunction,LOF)等位基因的HR-NICE患者,经替格瑞洛联合阿司匹林治疗可相对氯吡格雷联合阿司匹林降低23%的90 d卒中复发风险[10]。
本例患者第1次卒中后使用氯吡格雷联合阿司匹林的双抗方案,但效果欠佳,2个月后卒中复发再次入院。但幸运的是,患者第2次卒中发作仍无严重的神经功能缺失症状。入院后快速基因检测显示患者携带CYP2C19LOF等位基因,这也可以解释患者在首次卒中发作后使用氯吡格雷联合阿司匹林的双抗方案未能有效预防卒中复发。根据基因检测的结果,为患者选择了替格瑞洛联合阿司匹林的“绕行基因”方案,治疗后半年随访,患者未再有卒中复发,提示对于此例患者,替格瑞洛联合阿司匹林21 d的双抗方案可能更加有效。

