丹红注射液对感染性休克大鼠肺损伤的保护作用机制
王丽娜
感染性休克(SS)是指病原菌及其毒素引起的以低血压、代谢性酸中毒以及全身炎症反应为特征的病理过程,给病人健康造成严重威胁[1]。在SS 发病过程中,肺是最早受累器官之一,数据显示,约有50%病人伴有肺损伤,严重时可发展为急性呼吸窘迫综合征[2]。病原菌感染后释放的毒性介质如脂多糖等可使免疫系统过度活化,产生大量的炎性因子如肿瘤坏死因子-α(TNF-α)、白细胞介素(IL)-6 等。这种破坏性的全身性炎症反应是SS 肺损伤的主要病理过程,并有可能引起多器官功能障碍综合征[3]。近年来研究显示,丹红注射液(DHI)除具有活血化瘀的功效之外,尚有良好的抗炎、肺保护作用[4]。2018 年4 月至2019 年8 月,本研究通过腹腔注射脂多糖建立大鼠SS 肺损伤模型,观察DHI 对SS 大鼠肺损伤的保护作用,并初步探讨其作用机制,现报告如下。
1 材料与方法
1.1 实验动物健康雄性SD 大鼠48 只,周龄范围为6~8 周,体质量范围为200~240 g,由北京维通利华实验动物技术有限公司提供,实验动物生产许可证号SCXK(京)2018-0024,实验动物使用许可证号SCXK(冀)2017-0004,于25 ℃、55%相对湿度、12 h/12 h 光暗周期条件下饲养,自由进食水。本研究符合一般动物实验伦理学原则。
1.2 主要试剂与仪器脂多糖(美国Sigma 公司),生理盐水(山东华鲁制药有限公司),DHI(山东丹红制药有限公司),地塞米松(浙江仙居仙乐药业有限公司),水合氯醛(上海信裕生物科技有限公司),核因子-κB(p65)[NF-κB(p65)]和κB 抑制因子α(IκBα)免疫组织化学染色试剂盒(武汉博士德生物工程有限公司),TNF-α、IL-6 酶联免疫吸附测定(ELISA)试剂盒(南京建成生物工程研究所)。BL-420 生物机能实验系统(成都泰盟科技有限公司),恒温烤箱,倒置显微镜(Olympus 公司),全自动酶标免疫分析仪(Biotex公司)。
1.3 大鼠模型制备及分组将所有48 只大鼠于实验室环境下给予适应性喂养后,采用随机数字表法分为对照组、模型组、DHI 干预组和阳性对照组,12只/组。大鼠SS 模型建立方式[5]:腹腔注射2%戊巴比妥钠40 mg/kg麻醉后,暴露右颈总动脉,插管连接生物机能系统(BL-420)以监测血压。待血压稳定后,模型组、DHI干预组和阳性对照组经腹腔注射脂多糖15 mg/kg,观察大鼠动脉压直至大鼠达到休克状态(动脉压降低至基础血压2/3 以下时,脉压小于20 mmHg 为判断大鼠休克的指标),对照组给予等量的生理盐水。大鼠SS 模型造模成功后,DHI 干预组立即经腹腔注射DHI 2 mL/kg,阳性对照组经腹腔注射1 mL/kg 地塞米松,模型组和对照组大鼠均予以等体积生理盐水。
1.4 样本采集及处理给药24 h后,以10%水合氯醛5 mL/kg 腹腔注射将大鼠麻醉后固定,放血处死后严格无菌开胸取肺组织,留取右上肺组织,用生理盐水冲洗表面血液并吸取表面水分,放入10%甲醛固定液中,常规包埋、切片,进行苏木精-伊红(HE)染色后镜检及读片,取左肺组织置于-80 ℃超低温冰箱冻存待检。
1.5 大鼠肺湿/干质量测定取各时间点处死的大鼠肺组织,称量其湿质量(W)后,置烤箱中于70 ℃条件下烘烤24 h 至恒重,称量并记录干质量(D),计算肺组织湿干质量比(W/D)。
1.6 大鼠肺组织TNF-α、IL-6检测制备肺组织匀浆,离心后取上清液,使用酶联免疫吸附测定(ELISA)检测肺组织中TNF-α、IL-6 含量水平,操作严格按照试剂盒说明进行。
1.7 免疫组织化学法检测肺组织NF-κB 及IκB-α蛋白表达病变组织以石蜡包埋,4 μm 连续切片至过胶玻片上,56 ℃条件下烤片2 h,使用二甲苯连续脱蜡3次,梯度乙醇脱二甲苯,水洗。采用免疫组织化学SABC 法染色。采用3%过氧化氢孵育5 min后,加入5%山羊血清孵育20 min,甩去多余液体,加入适当稀释的兔抗鼠NF-κB(p65)多克隆抗体4 ℃下孵育过夜,磷酸缓冲盐溶液(PBS)冲洗后滴加羊抗兔免疫球蛋白G(IgG)二抗,37 ℃下孵育20 min,PBS冲洗后滴加SABC,37 ℃下孵育30 min。采用DAB 显色,控制显色时间,苏木素轻度复染、脱水、透明、封片,显微镜观察染色结果。IκB-α 染色步骤同NF-κB,所用一抗为兔抗鼠IκB-α 多克隆抗体。400 倍镜下每张切片随机选取5 个视野,利用Motic Images Advanced 3.2 图像采集系统分析每个视野阳性细胞百分比,阳性细胞的百分比表示阳性染色面积占被测量面积的比值,最后取5 个视野均值作为测量值。
1.8 统计学方法使用SPSS 20.0 统计软件,以±s 表示计量资料,多组间比较使用单因素方差分析,多组间的两两比较使用SNK 法;计数资料采用率表示,行χ2检验。检验水准α=0.05。
2 结果
2.1 各组大鼠行为表现对照组神态正常,皮毛顺滑有光泽,进食正常;模型组腹腔注射脂多糖后,大鼠逐步出现活动减少,神态倦怠,皮毛杂乱无光,进食开始减少,反应力下降,且上述症状有加重趋势,表现为躁动、寒颤、腹泻等;DHI 干预组和阳性对照组在注射脂多糖初若干小时内与模型组具有类似的表现,在给予DHI 和地塞米松干预后实验大鼠活动增多,躁动、寒颤等症有所减轻。观察期内对照组大鼠无一死亡,DHI 干预组和阳性对照组大鼠死亡率分别为8.33%(1/12),8.33%(1/12),显著低于模型组的58.33%(7/12)(χ2=10.67,P=0.005)。
2.2 大鼠肺组织病理形态观察HE 染色下可见对照组大鼠肺组织结构清晰,肺泡及间质无明显充血、渗出及炎症细胞浸润,具有完整的肺泡壁。而模型组镜下可见肺泡壁破坏严重,肺泡隔增厚,肺间质及肺泡腔严重水肿、渗出及出血,大量粒细胞浸润及透明膜形成。DHI 干预组肺泡壁多数完整,肺泡隔较模型组明显缩窄,腔内仅见少许出血、渗出及炎症细胞浸润。阳性对照组可见肺泡壁多数完整,肺泡隔较模型组明显缩窄,腔内几乎无出血、渗出及炎症细胞浸润。见图1A。
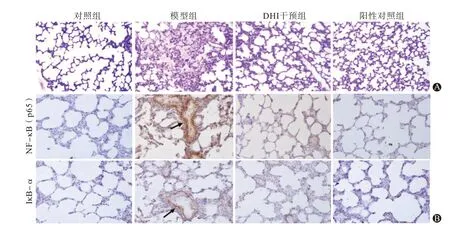
图1 各组大鼠肺组织染色图:A为病理变化(苏木精-伊红染色×200);B为NF-κB(p65)、IκB-α蛋白表达(免疫组织化学染色×200)
2.3 大鼠肺组织W/D 变化对照组、模型组、DHI干预组、阳性对照组大鼠肺组织W/D 分别为4.02±0.37、5.56±0.51、4.72±0.44、4.45±0.46(F=15.72,P<0.001);与对照组相比,模型组大鼠肺组织W/D显著增加(P<0.05),DHI 干预组较模型组降低(P<0.05),阳性对照组与DHI 干预组比较差异无统计学意义(P>0.05)。
2.4 各组大鼠肺组织TNF-α、IL-6检测与对照组比较,模型组大鼠肺组织TNF-α、IL-6 含量升高(P<0.05),DHI干预组TNF-α、IL-6含量较模型组均下调(P<0.05),阳性对照组TNF-α、IL-6 水平与DHI 干预组比较差异无统计学意义(P>0.05),见表1。
2.5 各组大鼠肺组织细胞中NF-κB 及IκB-α 蛋白表达对照组肺组织NF-κB(p65)、IκB-α 表达呈弱阳性免疫反应,阳性产物均多分布于气管黏膜上皮细胞细胞质,NF-κB(p65)在细胞核中极少见或没有,IκB-α 细胞核中未见。各组NF-κB(p65)、IκB-α阳性细胞百分比差异有统计学意义(P<0.05)。与对照组比较,模型组NF-κB(p65)、IκB-α呈强阳性免疫反应,均主要分布于气管黏膜上皮细胞、浸润炎症细胞和血管内皮细胞,NF-κB(p65)在细胞质和细胞核均可见,可见明显的细胞核易位,IκB-α 见于细胞质内,阳性细胞百分比均升高(P<0.05)。给予DHI干预后,与模型组比较,肺组织NF-κB(p65)、IκB-α阳性反应均明显减弱,阳性细胞百分比均下降(P<0.05)。阳性对照组与模型组比较,NF-κB(p65)、IκB-α 均呈弱阳性免疫反应,阳性细胞百分比均降低(P<0.05);与DHI 干预组比较,NF-κB(p65)、IκBα 阳性细胞百分比均差异无统计学意义(P>0.05)。见图1B,表2。
表1 各组大鼠肺组织TNF-α、IL-6水平比较/± s
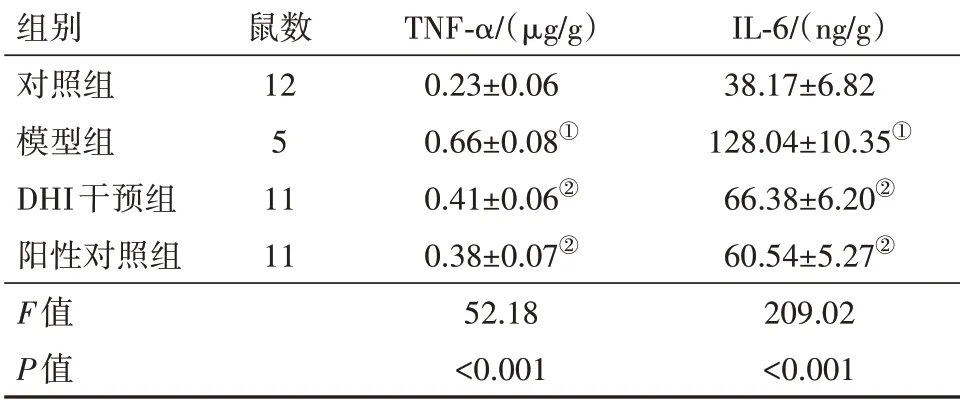
表1 各组大鼠肺组织TNF-α、IL-6水平比较/± s
注:TNF-α 为肿瘤坏死因子-α,IL-6 为白细胞介素-6,DHI 为丹红注射液。①与对照组比较,P<0.05。②与模型组比较,P<0.05。
组别对照组模型组DHI干预组阳性对照组F值P值鼠数12 5 11 11 TNF-α/(μg/g)0.23±0.06 0.66±0.08①0.41±0.06②0.38±0.07②52.18<0.001 IL-6/(ng/g)38.17±6.82 128.04±10.35①66.38±6.20②60.54±5.27②209.02<0.001
表2 各组大鼠肺组织NF-κB(p65)、IκB-α阳性细胞百分比比较/(%,± s)
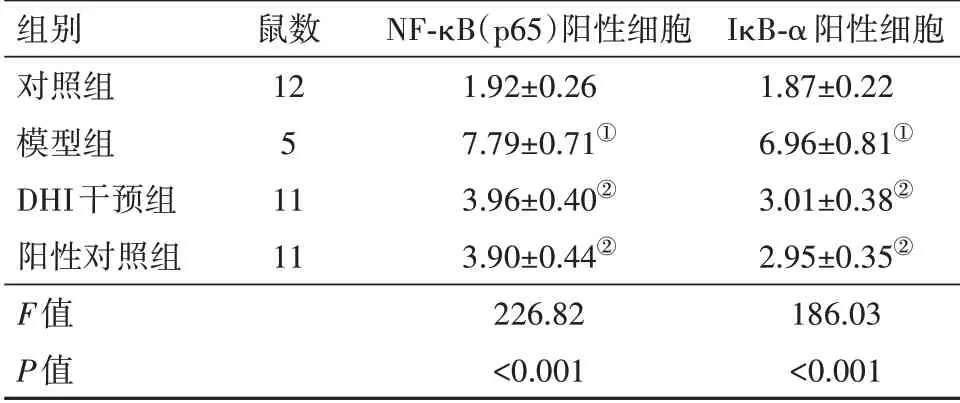
表2 各组大鼠肺组织NF-κB(p65)、IκB-α阳性细胞百分比比较/(%,± s)
注:NF-κB(p65)为核因子-κB(P65),IκB-α 为κB 抑制因子α,DHI为丹红注射液。①与对照组比较,P<0.05。②与模型组比较,P<0.05。
组别对照组模型组DHI干预组阳性对照组F值P值鼠数12 5 11 11 NF-κB(p65)阳性细胞1.92±0.26 7.79±0.71①3.96±0.40②3.90±0.44②226.82<0.001 IκB-α阳性细胞1.87±0.22 6.96±0.81①3.01±0.38②2.95±0.35②186.03<0.001
3 讨论
SS 亦被称为脓毒症休克,是临床导致肺损伤最常见的病因之一,约占肺损伤发病原因的40%左右。因此本研究采用常用的腹腔注射脂多糖的方法建立脂多糖导致SS 的大鼠模型,模拟临床SS 肺损伤的发生,观察DHI对SS肺损伤大鼠的治疗作用并探讨其作用机制。地塞米松作为临床上常用的治疗SS肺损伤的药物之一,因此本研究选用地塞米松作为阳性对照药物。本研究中,采用腹腔注射15 mg/kg脂多糖建立大鼠SS肺损伤模型。实验中观察到大鼠注射脂多糖后出现一系列SS 症状,如躁动、寒颤、腹泻等表现,同时平均动脉压降至基础压2/3以下,与文献[6-7]报道相一致。肺组织HE 染色结果显示,对照组肺组织结构清晰,模型组HE 染色中,肺泡壁破坏,炎症细胞浸润等符合SS 肺损伤病理表现。另外,模型组肺组织W/D 较对照组明显增加,表明注射脂多糖后大鼠有明显肺水肿表现,结合上述几点可见本研究大鼠SS 肺损伤模型构建是成功的。
众多研究显示,SS 病程中免疫系统激活引起大量的炎性因子释放,炎性介质进一步引起肺毛细血管通透性增加并造成肺损伤[8-9]。本研究中,DHI 可以明显下调TNF-α、IL-6 水平,减轻肺组织水肿,改善肺组织炎症细胞浸润状态,且作用与地塞米松相当。TNF-α 主要由巨噬细胞和T 淋巴细胞产生,参与肺组织损伤的炎症反应过程[10]。IL-6是一种主要由单核一巨噬细胞分泌的炎性因子,可促进多种炎性因子的生成。李燕等[11]的研究显示,TNF-α、IL-6等炎症细胞因子水平在脂多糖所致的小鼠急性肺损伤模型中明显升高,其变化与疾病进展明显相关,这提示DHI 可能通过抑制炎症细胞因子表达发挥保护肺损伤作用。
NF-κB 是一种重要的细胞转录因子,在免疫炎症相关信号通路中居于核心地位[12]。正常生理状态下,NF-κB 与IκB 结合,以非活性形式存在于细胞质中,在外源性配体刺激下,IκB-α 先后被磷酸化和泛素化,导致其构象发生改变并被降解,NF-κB 与IκB 解离后进入细胞核与靶序列结合,促进TNF-α、IL-6 等炎性因子的表达,参与肺损伤病理过程[13-14]。本研究中,免疫组织化学染色结果显示,DHI可以明显下调SS 大鼠NF-κB(p65)、IκB-α 的表达。宋丽娟等[15]的研究显示,羟基红花黄色素A 不同剂量组可以不同程度抑制脂多糖致急性肺损伤小鼠NF-κB的激活和NF-κB(p65)核转位,并抑制早期炎性相关因子TNF-α、IL-6 和IL-1β 的大量释放,其中羟基红花黄色素A是DHI中红花药理功效的最有效水溶性成分。提示DHI 可能通过抑制SS 大鼠肺组织NFκB 活化,减少TNF-α、IL-6 等促炎细胞因子表达而发挥保护肺损伤作用。
综上所述,在大鼠脂多糖致SS 肺损伤模型中,DHI 可能通过抑制大鼠肺组织NF-κB 活化,减少TNF-α、IL-6 等促炎细胞因子表达而发挥保护肺损伤作用。
(本文图1见插图9-1)

