失效模式与影响分析中两种方法在临床试验药物管理中的应用
丁琮洋,邱博,宋浩静,孙雪,李亚静,李宵,董占军
(河北省人民医院药学部,石家庄 050051)
试验药物是药物临床试验的基础和核心,贯穿于整个临床试验过程中,加强试验药物管理对临床试验的规范性和受试者的安全性至关重要[1]。国家药品监督管理局发布的2015年5月—2017年7月药物临床试验数据核查阶段性报告显示,试验药品管理过程与记录方面的缺陷在所有缺陷条款中排名第3,临床试验药物管理正面临整顿和规范的局面[2]。依据《药物临床试验质量管理规范》(good clinical practice,GCP)[3],我院设有临床试验中心药房,2名兼职药师对临床试验药物实行统一管理。随着我院临床试验数量的增加和试验药物种类的增多,药物管理的流程需要不断更新和修正,迫切要求用合适可操作的方法完善试验药物管理过程。
评价临床试验药物的安全性和有效性是临床试验的目的,而临床试验药物是试验成功进行的基础,其管理过程包括药房人员管理、药物管理和环境管理,管理中可能造成药物失效的因素众多,需要使用合适的工具对药物管理进行失效分析与影响评估,失效模式与影响分析(failure mode and effects analysis,FMEA)作为一种常用的风险控制工具,用于发现并评价产品或过程中潜在的失效及其后果,找到能够避免或减少潜在失效发生的措施。FMEA由美国格鲁曼公司开发并应用于飞机制造业和发动机故障评估,取得很好的实效,如今FMEA已成为一个国际化的标准,应用在电子、医药、计算机等领域[4]。2003年美国医疗机构联合评审委员会推荐FMEA作为医院安全评估的一种方法,旨在医疗风险事件发生之前对其进行预测评估,并采取相应措施,从而有效降低医疗风险事件发生[5]。我国引入FMEA时间较晚,目前已有研究应用于降低围手术期医疗风险、住院患者行为症状风险防范、血液样本管理等方面[6-8]。FMEA主要包含设计FMEA(design failure mode and effects analysis,DFMEA)和过程FMEA(process failure mode and effects analysis,PFMEA),PFMEA是一种动态文件,在可行性研究阶段之前或期间启动,包含可能造成失效的潜在失效模式与起因,可以减少失效发生并制定纠正和预防措施[9]。
1 评价方法
旧版FMEA手册用风险系数(risk priority number,RPN)对失效模式评分,RPN是严重度(severity,S)、发生度(occurrence,O)和可探测度(detection,D)的乘积,严重性代表失效模式对临床试验的影响严重程度,发生度代表失效模式发生频率,可探测度代表失效模式被发现的难易度[10]。RPN数值越大表明失效风险越高。新版FMEA手册用行动优先级(action priority,AP)代替RPN对失效模式评级,结果不以SOD乘积表示,而是以各项S、O、D评分进行AP评级。其中,H代表高行动优先级,团队必须采取措施进行预防或改进;M代表中行动优先级,团队应当采取措施进行预防或改进;L代表低行动优先级,团队可以采取措施进行预防或改进。传统的RPN 3个指标赋值比重相同,结果仅是3个指标的简单乘积,无法体现哪种指标较为重要而进行针对性改进,缺乏一定的逻辑性和科学性,而新版的AP表则赋予3个指标不同的分值和比重,按S、O、D的顺序列出评分表,提高严重度S的重要性,明确指出在实际应用中应优先处理对结果产生较大影响的因素[11]。新版FMEA手册中已用AP替代RPN进行风险评估,而AP表是否适用于临床试验药物管理尚未可知,故笔者分别应用RPN和AP对临床试验药物管理过程中失效模式进行评分或评级,比较两种方法评分或评级结果,并对新旧两版数据评价的方法进行比较。
2 研究方法
2.1层次约定 以GCP和FMEA手册为指导,对GCP药物管理中研究对象进行3个层次约定。初始约定层次为“临床试验药物管理”,中间约定层次为“人员”“药物”“环境”,最低约定层次为中间约定层次下的11个子环节,其中,人员包括:接收(Z1)、保存(Z2)、发放(Z3)、回收(Z4)、返还(Z5);药物包括(Z6)、效期(Z7)、纸质文件(Z8);环境包括温度(Z9)、湿度(Z10)、光照(Z11)。
2.2问卷设计 根据各最低层次下的失效模式设计问卷,通过问卷星发放调查问卷,问卷发放对象包括临床试验机构人员、临床试验申办方、临床试验研究者和合作研究组织人员。为确保问卷结果具有统计学意义,需确定问卷的样本量。样本量计算公式为:N=[Z2P(1-P)]/E2,N为样本量,Z为统计量,P为概率值,E为误差值[12]。
2.3数据处理 应用SPSS 21.0版软件对问卷结果进行处理,采用Cronbach's α系数计算问卷所得数据信度。α系数取值为0~1,α系数0.7~0.8表示数据信度可信,0.8~0.9表示数据信度好,>0.9表示数据信度非常可信。采用Grubbs检验法剔除离群数值,剩余数值求各项S、O、D平均值和中位数。取各项平均值计算RPN=S×O×D,取各项中位数进行AP评级,Excel软件将RPN值降序排列并标注AP评级。
3 研究结果
本研究令P=0.5,问卷样本量置信区间为90%,通过查表:Z=1.65,E=0.15,代入样本量计算公式N=[Z2P(1-P)]/E2得N=30.25,即样本置信度90%,样本误差在15%内,需问卷样本量31份。本研究调查问卷实际发放51份,回收51份,α系数为0.965,表明问卷结果信度非常可信。通过Grubbs检验剔除35个离群数值,保留3637个数值。失效模式RPN值范围是24.661~54.302,AP评级均为L,按RPN降序排列,结果见表1。
4 讨论
4.1RPN平均值和AP中位数的选择 本研究计算RPN评分和AP评级时,分别选择平均数和中位数,选择数据的不同主要考虑到两种方法的适用范围和使用便利性。在已有的众多研究中[5-10],计算RPN均采用平均值进行计算,如采用中位数,其SOD评分均为整数,计算RPN时会出现部分一样的数值,不利于排序比较,而平均值绝大多数为非整数,RPN数值一样概率极小,因此,使用平均值得到的结果更适合进行RPN排序。如SOD使用平均值,使用AP表时某些数值可能落在某两个分级之间的数值,从而无法定级,而中位数均为整数,配合AP表使用更加便利。
4.2RPN和AP结果对比 旧版RPN仅是3个因素SOD的乘积,3个因素在RPN计算中比重一致,而新版AP高中优先级主要分布在严重度得分较高的失效模式中,提高严重度在结果判定中的比重,如严重度得分最高的第10,第12位的失效模式,其发生度较低、可探测度高,表明工作人员对风险较高的失效模式有一定的预防和控制,而排序第1位的失效模式,其严重度得分为6,但发生度为4、可探测度为1,属于表1中严重度中、发生度中、可探测度高的失效模式,表明工作人员对试验药物管理中一些常见且影响较小的环节专注度不够,未能给予足够重视。因此,RPN相较于AP能更有效区分各种失效模式造成的影响,依据RPN进行排序更为合理有效。
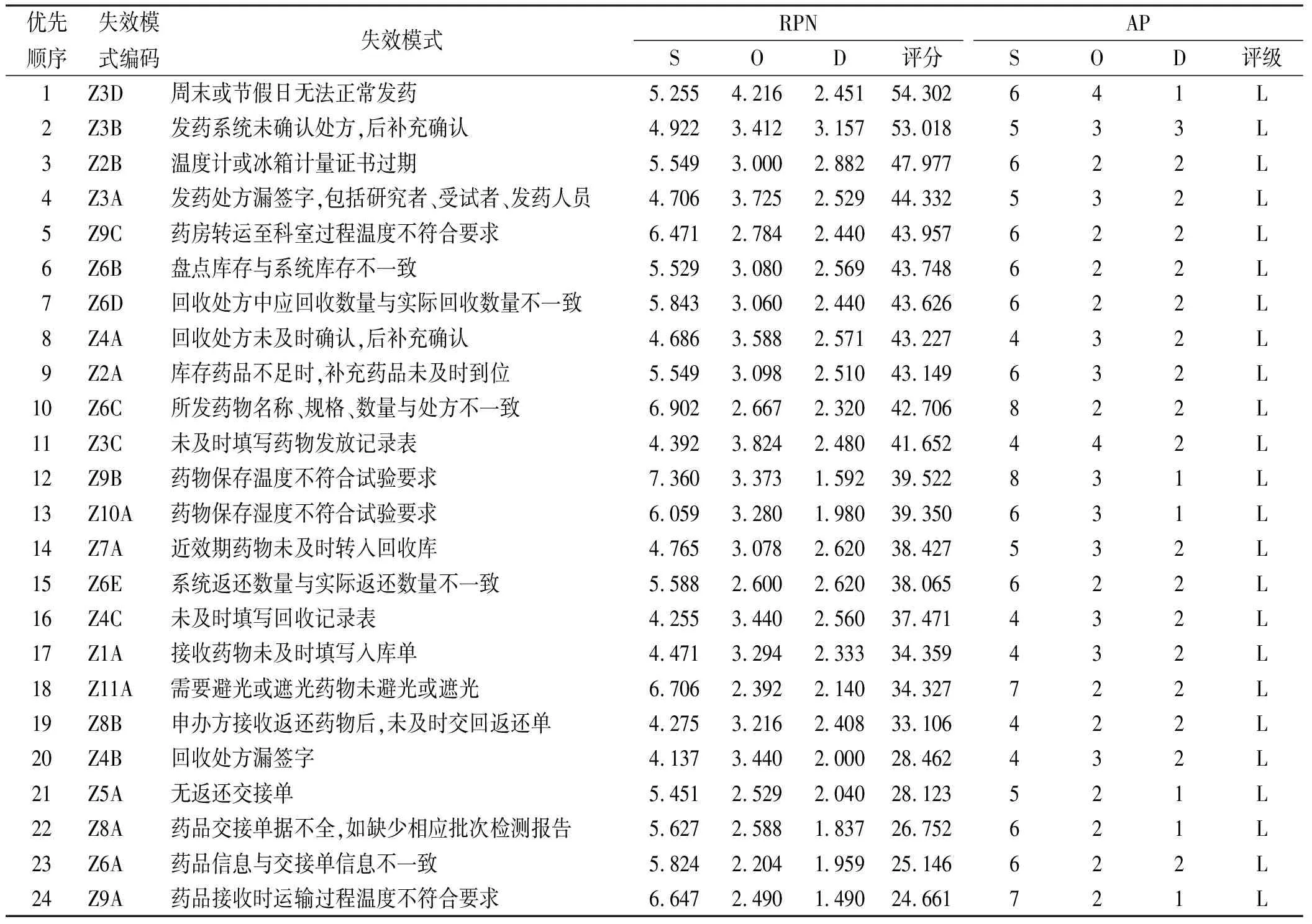
表1 失效模式RPN评分和AP评级
4.3风险分析 依据RPN分值分布,将失效风险分为高、中、低3个分段,高风险分段RPN>40,需立即采取措施控制风险;中风险分段30 4.3.1高风险失效模式 排名第1,第3,第4位的失效模式均属于最低约定层次“发放”下内容,因此应当把试验药物发放流程整改置于首位,药房人员和科室领药人员应掌握受试者和药物基本信息,熟悉药物发放和领取过程。“周末或节假日无法正常发药”是排名第1的失效模式,可能与本机构药房仅设置了两名兼职药师,人员安排已不能满足现有临床试验工作量,此情况也见于其他临床试验机构[13]。2018年美国医院药剂师协会颁布的《临床试验药物指导原则》指出,临床试验药房可利用正式的药房人员和临床研究药师的临时支持来补充人员的需要,以保证持续分发临床试验药物,同时可以设置专职药师以利于统一管理和信息沟通,此外,我国对试验药物的领取时间并没有详细的规定,期待我国药品监督管理部门能够尽快制订相关的指南[14]。 4.3.2中风险失效模式 温度、湿度和光照是影响药物稳定性的重要因素,尤其温度是影响药物质量的关键因素[15],如冷藏保存的药物,其温度升高10 ℃,有效期将缩短1/4~1/2,因此应严格监控药物保存环境,特别是对温度的严密监控[16]。在临床科室中开展的临床试验,由于试验项目时间较长、受试者筛选和入组流程较复杂、涉及的药物种类和数量较多,申办方常多次运送试验药物到中心药房,导致药物批次较多、有效期各不相同,不同效期的同一种药物常放置在同一环境,容易混淆。为避免将近效期试验药物发放给受试者,应进行色标管理,并在GCP药房管理系统中设置颜色提醒[17]。 本研究应用PFMEA对 GCP药物管理作了失效模式和影响分析,依据旧版RPN评分和新版AP评级进行对比研究,AP采用中位数进行评价,而RPN采用平均数进行评价,相较于AP,RPN更适合于本院临床试验药物管理。本研究仅分析了药物管理过程中部分失效模式,未分析或未察觉的潜在失效模式,需设计新问卷或采用新方法进一步评价。PFMEA是一组动态活动,应不断进行分析和更新改进措施,以完善药物管理过程,保证临床试验的规范性。

