SBA-3对非诺贝特溶出速率和口服生物利用度的影响*
李江,谢瑞
(浙江中医药大学附属第一医院药剂科,杭州 310000)
非诺贝特(fenofibrate,FNB)是一种安全高效的降脂药物,最适用于治疗高三酰甘油血症及以三酰甘油增高为主的混合型高脂血症[1]。FNB属于难溶性药物,几乎不溶于水,使其在临床上的应用受到很大限制[2]。据统计,约40%新药属于难溶性药物[3],如何改善难溶性药物的溶出速率一直是药物制剂研究者需要解决的难题。传统上常常将药物微粉化,减小药物粒子大小来提高溶出速率[4]。而目前多通过制备成固体分散体、纳米晶体等途径来改善药物低水溶性问题[5-6],取得很大进展。更多研究者利用纳米介孔材料运载难溶性药物制备固体分散体,包括介孔碳,介孔硅和介孔钛等材料[7-10]。于超峰等[11]以介孔硅为载体制备他达那非的固体分散体,显著提高药物的溶出度。李鹤然等[12]利用介孔硅材料MCM-41对盐酸左氧氟沙星较高吸附能力,改善释药行为。这是由于纳米介孔材料具有稳定有序的孔道,很大的比表面积和可控制的空间,很大程度限制难溶性药物的粒子大小,使其以无定形状态存在于介孔孔道中,从而提高药物的溶出速率。笔者制备一种介孔硅材料载体SBA-3来提高难溶性药物FNB的溶出速率,利用吸附法将FNB载入SBA-3孔道中制备载药体系,并对载药体系进行相关表征、体外毒性、溶出实验和体内药动学实验,报道如下。
1 仪器与试药
1.1仪器 JEM-1010透射电镜(日本电子株式会社);UV757CRT紫外分光光度计(杭州俊升科学器材有限公司);DSC-60差示扫描量热仪(日本岛津公司);DF-101S集热式恒温加热磁力搅拌器(建湖县大龙玻璃仪器有限公司);ZRS-8G 智能溶出度测试仪(深圳市博大精科技实业有限公司);TDP-1.5德科单冲压片机(新昌县德科机械有限公司)。
1.2试药 非诺贝特(上海源叶生物科技有限公司,含量>99%,批号:20180322);非诺贝特酸(上海嵘崴达实业有限公司,含量>98%,批号:20170502);非诺贝特市售片(上海衡山药业有限公司,批号:20170223);吲哚美辛(郑州市安达医药有限公司,含量>99%,批号:20171011);十六烷基三甲基溴化铵(hexadecyl trimethyl ammonium bromide,CTAB,上海雪捷化工有限公司,色谱级);盐酸,正硅酸乙酯(天津市光复精细化工有限公司)。噻唑蓝(MTT,江苏奥赛康制药有限公司,批号:070901)。
2 方法与结果
2.1SBA-3的制备 SBA-3的典型合成参照文献[13-15]。CTAB 0.63 g溶解于盐酸溶液,室温下充分搅拌。在酸性溶液中缓慢滴加正硅酸乙酯,使CTAB:正硅酸乙酯:盐酸:水的摩尔比为1:1:9:130,继续搅拌45 min。得到白色沉淀物,在100 ℃进行油浴3 h。滤过,清洗,室温干燥过夜,并在空气中823 K下煅烧6 h,获得载体SBA-3。通过透射电镜法对载体SBA-3的微观结构进行考察,结果见图1所示,SBA-3呈现均一有序的介孔孔道,孔径2~3 nm。
2.2载药及载药量的测定 通过药物吸附法[16]将FNB载入SBA-3的纳米介孔孔道中。先将FNB 100 mg充分溶解于三氯甲烷溶液1 mL里,加入适量载体SBA-3避光孵育4~5 h,离心,弃去上清液,对沉淀物进行干燥,即得载药体系FNB-SBA-3。取FNB-SBA-3粉末5 mg溶解于甲醇中,采用紫外-可见分光光度法测定载药量,FNB的最大吸收波长为286 nm[17]。载药量(%)=药物FNB测得质量/载药体系FNB-SBA-3总质量×100%。结果FNB在SBA-3中载药量为43.03%。

图1 SBA-3的透射电镜图
2.3载体及载药体系的表征 通过差示扫描量热法检测药物结晶度[18],对FNB、SBA-3、载体和药物混合物、载药体系FNB-SBA-3进行分析。考察FNB在SBA-3中的存在状态。检测条件:扫描范围为50~100 ℃,扫描速度为10 ℃·min-1。扫描结果见图2。FNB 的扫描曲线在82 ℃处具有一个明显的特征吸热峰,而SBA-3 没有出现特征峰,且为一条平滑曲线。载体和药物混合物的扫描曲线与FNB相似,特征峰位置一致,这表明药物和载体之间没有发生化学反应。载药体系FNB-SBA-3在82 ℃特征吸热峰消失,这个现象表明有晶型的FNB在SBA-3介孔孔道中以无定形的状态存在。
2.4细胞毒性实验 通过细胞毒性实验考察SBA-3的生物安全性。将处在对数生长期Caco-2细胞用胰酶消化,混匀后接种在96板中,埋板密度为每孔105个细胞。37 ℃培养24 h后进行加药处理。用培养基将载体SBA-3分别稀释成浓度为10,25,50,100,200,300,400和500 μg·mL-1。每个浓度设复孔4个,同时设4个未加药孔作为对照。加药处理24 h后,每孔加MTT 50 μL,孵育4 h。甩去上清液,每孔加入二甲亚砜(DMSO) 200 μL,避光震荡15 min,酶标仪在波长490 nm处检测吸光度(A值)。SBA-3处理后Caco-2细胞的存活率分别为98.90%,100.03%,97.31%,95.69%,95.41%,94.17%,92.52%和90.66%,结果显示SBA-3在不同浓度下,Caco-2细胞存活率都高于90%。即使在最大浓度500 μg·mL-1,细胞存活也较高,这表明SBA-3具有良好的生物安全性,可作为一个载体进行给药。

图2 FNB、SBA-3、混合物和FNB-SBA-3的DSC图
2.5体外溶出实验 采用2015年版《中华人民共和国药典》的溶出度测定法桨法进行检测。检测条件:溶出介质为1%SDS溶液1000 mL,温度为37 ℃,转速为100 r·min-1。同时投入FNB原料药100 mg,载药体系FNB-SBA-3为232 mg(相当于FNB100 mg)。分别在投药后5,10,20,30,45和60 min,取样5 mL,取样后迅速补充溶出介质5 mL。样品用孔径0.45 μm微孔滤膜滤过,采用紫外-可见分光光度法,在最大吸收波长286 nm处测定FNB的吸光度。各个时间点累积溶出度结果见图3。FNB在5 min溶出度为5.82%,而FNB-SBA-3在5 min溶出度却达到20.36%。当FNB-SBA-3接近100%时,FNB的溶出度也只有30.96%。证明FNB为难溶性药物,而SBA-3作为载体显著地提高FNB的溶出速率。
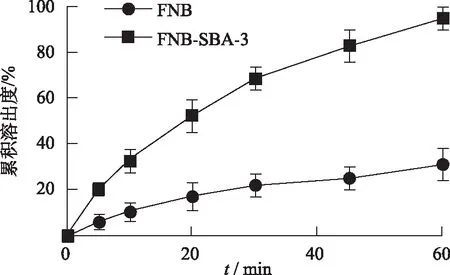
图3 FNB和FNB-SBA-3的累积溶出图
2.6片剂的制备
2.6.1片剂制备 采用粉末直接压片法[19-20]制备FNB-SBA-3片剂,精密称取FNB-SBA-3量为232 mg(相当于FNB 100 mg)和适量的辅料,过筛,混合均匀后,干燥,8 mm冲模进行压片。压片后片剂表面光滑,色泽均匀,无断裂粉碎现象出现。硬度均>50 N,符合片剂质量要求。
2.6.2填充剂的种类选择 每片质量347 mg,崩解剂羧甲基淀粉钠(CMS-Na)30 mg,黏合剂羟丙基甲基纤维素(HPMC)3 mg和润滑剂硬酯酸镁2 mg,使用填充剂80 mg,选用常用乳糖、微晶纤维素和淀粉作为片剂的填充剂进行筛选,考察不同填充剂对FNB-SBA-3自制片中FNB累积溶出度的影响。结果见图4。3种填充剂乳糖,微晶纤维素和淀粉对FNB的累积溶出度没有明显的差别,表明填充剂的种类对溶出度的影响较小。淀粉可压性差,而乳糖由于价格便宜,流动性和可压性良好,常作为粉末直接压片的填充剂,所以本实验选用乳糖作为FNB-SBA-3自制片的填充剂。
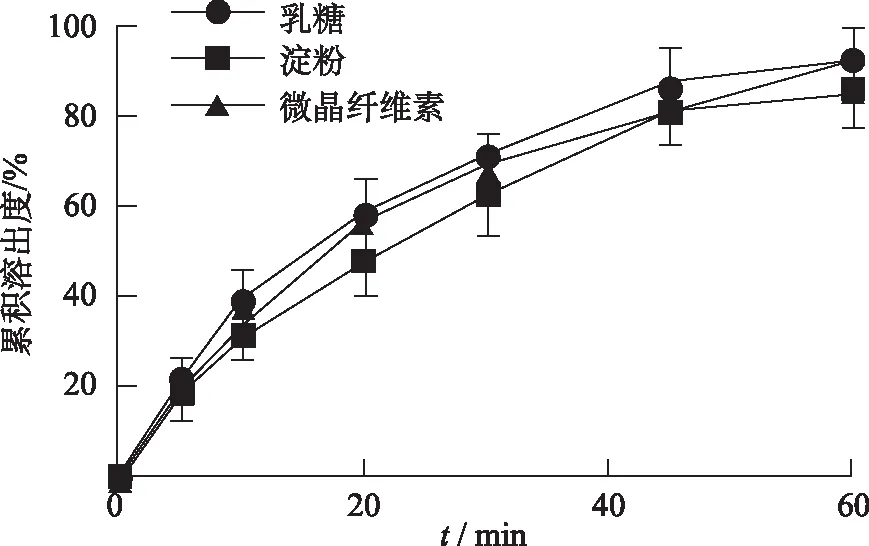
图4 填充剂种类对FNB-SBA-3自制片累积溶出度的影响
2.6.3黏合剂的种类选择 每片质量347 mg,填充剂乳糖 80 mg,崩解剂CMS-Na 30 mg和硬酯酸镁2 mg,使用黏合剂3 mg,选用常用HPMC,CMC-Na和聚维酮(PVP)作为片剂的黏合剂进行筛选,考察不同黏合剂对FNB-SBA-3自制片中FNB累积溶出度的影响。结果见图5,结果显示HPMC作为黏合剂时FNB的累积溶出度在各个时间点保持最高,60 min累积溶出度达93.30%,药物释放完全。而CMC-Na和PVP作为黏合剂时,60 min累积溶出度仅为83.95%,85.40%。因此本实验选用HPMC作为FNB-SBA-3自制片的黏合剂。
2.6.4崩解剂的种类选择 每片质量347 mg,填充剂乳糖 80 mg,黏合剂HPMC 3 mg和硬酯酸镁2 mg,使用崩解剂30 mg,选用常用CMS-Na,低取代羟丙基纤维素(L-HPC)和干淀粉作为片剂的崩解剂进行筛选,考察不同崩解剂对FNB-SBA-3自制片中FNB累积溶出度的影响。结果见图6,结果显示CMS-Na作为崩解剂时FNB的累积溶出度在各个时间点保持最高,药物溶出能力最好。而L-HPC和干淀粉作为崩解剂时,药物溶出速率都较低。因此本实验选用CMS-Na作为FNB-SBA-3自制片的黏合剂。
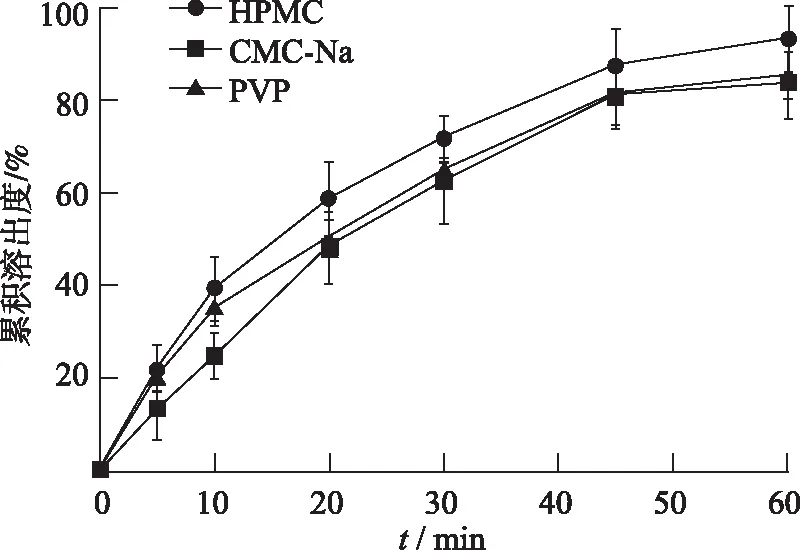
图5 黏合剂种类对FNB-SBA-3自制片累积溶出度的影响
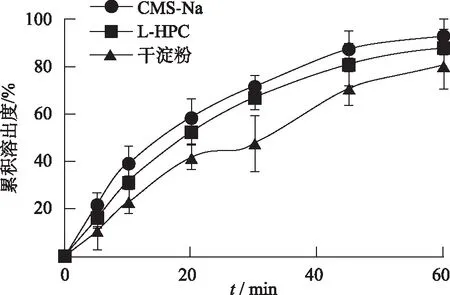
图6 崩解剂种类对FNB-SBA-3自制片累积溶出度的影响
2.6.5FNB-SBA-3自制片的最优处方 通过单因素考察法对填充剂,黏合剂和崩解剂种类进行筛选,确定FNB-SBA-3自制片的最佳辅料,并添加适量的硬脂酸镁作为润滑剂,最佳处方:FNB-SBA-3为232 mg(FNB含100 mg),乳糖80 mg,HPMC 3 mg,CMS-Na 30 mg,硬脂酸镁2 mg。
2.6.6自制片和市售片体外溶出度的比较 通过体外溶出实验对FNB-SBA-3自制片和FNB市售片进行比较。同时向溶出介质中投入含有100 mg FNB市售片和自制片。分别在5,10,20,30,45和60 min进行取样,286 nm波长下采用紫外分光光度法测定FNB的A值。结果见图7所示,市售片在10 min时FNB的累积溶出度为22.65%,而自制片在10 min时累积溶出度却已经达到39.27%。当FNB-SBA-3自制片FNB的累积溶出度达93.30%时,市售片FNB的溶出度只有65.25%,表明自制片明显改善了药物溶出速率。
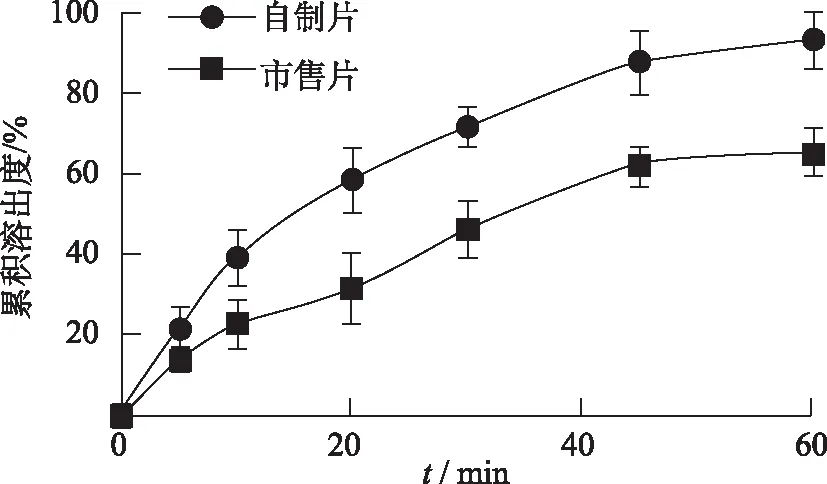
图7 自制片和市售片的累积溶出度
2.7体内药动学实验
2.7.1色谱条件 用C18色谱柱(4.6 mm×250 mm,5 μm),以甲醇-0.1%醋酸溶液(75:25)为流动相,流速1 mL·min-1,在波长286 nm下检测血浆中FNB的含量。
2.7.2血样采集 将12只健康家兔[体质量(2.5±0.5) kg,动物合格证号:211002300068496]随机分成2组,每组6只,雌雄各半,给药前禁食12 h。一组口服给药FNB市售片,一组口服给药FNB-SBA-3自制片。规格:含FNB100 mg。分别在给药后0.08,0.25,0.5,0.75,1,1.5,2,4,6,8,10,12和24 h,耳缘静脉取血2~3 mL,离心,取上层血浆,在-20 ℃储存。
2.7.3血样处理 向400 μL血浆中加入1 mol·L-1盐酸溶液400 μL,甲醇20 μL和内标吲哚美辛溶液(200 μg·mL-1)20 μL,混合5 min。加入无水乙醚3 mL,混匀5 min,离心,取上层快速挥干。流动相50 μL重悬,离心,取20 μL进行高相液相色谱法(HPLC)分析[16]。
2.7.4标准曲线的绘制 向400 μL血浆中分别加入0.25,0.5,1,2,4和8 μg·mL-1非诺贝特酸溶液20 μL,再加入200 μg·mL-1吲哚美辛20 μL,混合均匀,进行血样处理。非诺贝特酸作为标准品,吲哚美辛作为内标物,进行HPLC分析。非诺贝特酸浓度(C)为横坐标,非诺贝特酸与吲哚美辛峰面积比(A)为纵坐标,作标准曲线。结果回归方程为A=1.534 6C+0.688 5,R2=0.982 6,结果表明血浆药物在检测范围0.25~8 μg·mL-1内线性关系良好。
2.7.5精密度实验 取低浓度(2 μg·mL-1)、中浓度(4 μg·mL-1)和高浓度(6 μg·mL-1)非诺贝特酸处理后的血浆样本,一天内每个浓度样本测定5次,为日内精密度。连续5 d测定每个浓度样本,为日间精密度。结果3个浓度下日内精密度的RSD分别为5.38%,4.97%和4.26%,日间精密度的RSD分别为7.56%,9.34%和4.55%,RSD均<15%,符合要求。
2.7.6回收率实验 取低浓度(2 μg·mL-1)、中浓度(4 μg·mL-1)和高浓度(6 μg·mL-1)非诺贝特酸处理后的血浆样本,每个浓度5个样品,HPLC测非诺贝特酸峰面积。另取相同浓度的非诺贝特酸标准溶液,HPLC测峰面积。回收率为血浆中非诺贝特酸与标准溶液非诺贝特酸的峰面积之比。结果3个浓度下回收率分别为81.1%,82.5%和80.1%,回收率均>80%,符合要求。
2.7.7稳定性实验 取低浓度(2 μg·mL-1)、中浓度(4 μg·mL-1)和高浓度(6 μg·mL-1)非诺贝特酸处理后的血浆样本,放置1,2和3 d。结果3 d内非诺贝特酸与吲哚美辛峰面积比的RSD<5%,药物在血浆中稳定性良好,符合要求。
2.7.8体内药动学实验 FNB市售片和FNB-SBA-3自制片在家兔体内给药后,体内血药浓度变化情况见图8所示,结果显示自制片的血药浓度一直高于市售片的血药浓度。药动学参数见表1。给药后2 h,自制片达最高血药浓度6.02 μg·mL-1,而市售片仅为3.27 μg·mL-1。市售片半衰期(t1/2) 为2.35 h,自制片为4.14 h。结果表明FNB-SBA-3自制片不仅提高FNB在体内的血药浓度,而且延长药物在体内的存留时间。根据AUC自制片与市售片的比值,计算出相对生物利用度为181.83%,证明FNB-SBA-3自制片显著地提高FNB在体内的口服生物利用度。
3 讨论
药物按照水溶性和肠道渗透性进行生物药剂学分类。FNB属于BCS 2类,是低溶解性和高渗透性药物,DSC表征也证实FNB为晶型药物,溶出速率低,这也是FNB导致其生物利用度低的主要原因。因此,本实验制备纳米介孔材料来提高FNB溶出速率,提高体内生物利用度。但由于FNB进入体内代谢为非诺贝特酸,检测不到FNB原药,所以用非诺贝特酸作为体内检测非诺贝特的标准品。
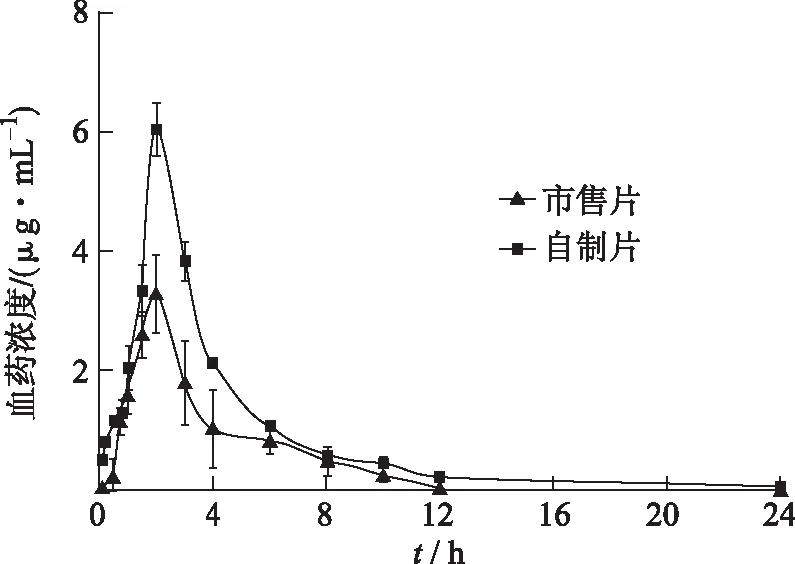
图8 自制片和市售片在家兔体内的血药浓度-时间曲线图

表1 2种制剂药动学相关参数
介孔硅材料SBA-3的介孔孔道有序均一,限制FNB结晶程度,产生空间抑制作用,使药物在SBA-3介孔孔道呈现无定形状态,DSC表征也得到进一步证实。根据Noyes-Whitney公式,粒子大小和比表面积都是决定药物溶出速率的主要因素。SBA-3由于介孔孔道空间抑制效应,使FNB粒子明显减小,相对比表面积增大,从而使FNB的溶出速率增加,体外溶出实验结果显示FNB-SBA-3相对于FNB的溶出速率明显提高。但在家兔体内FNB-SBA-3自制片与FNB市售片相比达峰时间相同,半衰期相对延长,其原因可能与体内测定药物为非诺贝特酸而不是非诺贝特原型药物有关。FNB-SBA-3自制片生物利用度显著提高,证实SBA-3作为载体对难溶性药物FNB改善溶出速率具有很好的潜力。

