海藻酸钠/羊毛角蛋白纤维的氢键作用及其结构与性能
宋 学 翠, 管 福 成, 郭 静, 杨 云 明, 李 峰, 杨 强
( 大连工业大学 纺织与材料工程学院, 辽宁 大连 116034 )
0 引 言
日益严重的环境问题使科学家把研究目光聚焦到天然生物材料[1]。海藻酸钠(SA)是一种从褐藻中提取的可降解的生物高分子材料,其来源广泛、价格低廉、黏度高、离子吸收率高、生物相容性好具有生物可降解性,广泛应用于生物医学[2]、纺织、食品卫生[3]和废水处理[4]领域。然而,纯海藻酸钠纤维的机械强度低、耐水性差,限制了其应用。近年来,对利用海藻酸盐-蛋白质混合物构建具有优异性能和潜在价值的复合材料进行了大量研究,已经成功开发了海藻酸钠/磷虾蛋白[5-6]、海藻酸钠/丝素蛋白[7]和海藻酸钠/角蛋白[8-10]等复合材料。
羊毛织物是最受欢迎的纺织品之一,但废弃羊毛织物造成的污染问题和资源浪费问题备受关注。羊毛中富含角蛋白[11],因此可以作为角蛋白源加以利用。已有研究通过氧化法、还原法、酸碱法和离子液体法[12]等提取角蛋白,并将其用于纺织品功能整理、组织工程支架、药物传递和功能膜等方面[13]。Silva等[14]成功制备了一种用于软组织再生的含有SA和羊毛角蛋白(WK)的新型复合水凝胶,发现水凝胶的组成对其物理性能有显著影响。Heliopoulos等[15]使用藻酸盐和铜离子制备具有抗菌性能的改性羊毛织物。此外,SA的化学结构类似于壳聚糖、纤维素,含有多个氢键结合位点[16],WK富含氢键供体和受体,当两者混合时会发生氢键作用,且这种氢键作用必将伴随纤维的凝胶化过程、拉伸过程,并对纤维的结构和性能产生影响。有关SA/WK复合体系氢键作用的定量分析鲜有报道。
本实验以废羊毛织物为原料,采用酸碱法提取WK,用湿法纺丝技术制备不同质量比的SA/WK纤维,定量分析了SA/WK共混体系的氢键类型和相对强度,明确了氢键作用对SA/WK复合体系结构与性能的关系,以期为SA和WK的应用提供一种新途径。
1 实 验
1.1 材 料
海藻酸钠,相对分子质量500万,青岛明月海藻集团有限公司;无水氯化钙,分析纯,天津市科密欧化学试剂有限公司;氢氧化钠,分析纯,天津市瑞金特化学品有限公司;盐酸,分析纯,天津市瑞金特化学品有限公司;皂片,上海制皂公司有限公司;废弃羊毛织物,收集。
1.2 方 法
1.2.1 角蛋白的提取
在含有5 g/L皂液的浴槽中清洗切碎的羊毛织物,液织比为30∶1,在40 ℃下清洗30 min。然后离心脱水、蒸馏水冲洗,在50 ℃的真空烘箱中干燥,直到达到恒定质量。
将处理后的清洁羊毛放入质量分数为1%的NaOH溶液中,液织比为30∶1,在60 ℃的水浴中进行机械搅拌提取。通过真空过滤去除不溶性杂质,得到可溶性角蛋白。用盐酸滴定角蛋白直至沉淀出现。抽吸过滤,用蒸馏水冲洗样品并在室温下干燥,得到羊毛角蛋白。
1.2.2 SA/WK纤维的制备
将所需用量的1.5、3.0、4.5、9.0 g羊毛角蛋白溶于500 mL质量分数0.5%的氢氧化钠溶液中,在65 ℃下搅拌溶解,得到一系列质量分数梯度羊毛角蛋白溶液。将一定量的SA加到角蛋白溶液中,在65 ℃下搅拌均匀,得到SA/WK溶液。在室温下真空静置脱泡。在纺丝溶液中,WK相对于SA的添加量分别为10%、20%、30%和40%,命名为10%WK、20%WK、30%WK和40%WK。
SA/WK复合纤维的工艺流程示意图如图1所示。纺丝条件:喷丝头12孔,直径0.40 mm;凝固浴为质量分数为5%的氯化钙水溶液,温度条件为30 ℃;洗涤温度为45 ℃,整个生产过程中拉伸比为1.30,拉伸温度为80 ℃。

图1 SA/WK复合纤维的工艺流程示意图Fig.1 Schematic diagram of preparing the SA/WKcomposite fibers
1.3 性能与表征
红外光谱测试:采用KBr压片法,用傅立叶变换红外光谱仪(FT-IR,Spectrum-One B,PE公司;美国)测试SA/WK纤维,扫描范围为4 000~500 cm-1。
流变特性测试:用旋转黏度计(DV-C,Brookfield公司;美国)测试SA/WK溶液黏度。选用4号转子,温度20~80 ℃,转速5~100 r/min。
X射线衍射测试:用X射线衍射仪(S-4800,日本理学公司)对SA/WK纤维粉末进行测试。
拉伸测试:用电子单纤维强度计(LLY-06ED,莱州市电子仪器有限公司)测试SA/WK纤维力学性能。实验条件:间距10 cm,拉伸速度20 mm/min,温度(20±1) ℃,空气湿度(65±5)%。
SEM测试:用液氮淬断纤维,镀金后用扫描电子显微镜(S-4800,HITACH公司,日本)观察复合纤维的表面形貌,加速电压10 kV,放大倍数2 000倍。
2 结果与讨论
2.1 SA/WK纤维的FT-IR分析
由图2(a)可以看出,SA的峰值出现在3 426、2 921、1 614和1 417 cm-1,分别对应六元环上的 —OH伸长振动吸收峰、—CH伸长振动吸收峰、—COO-不对称拉伸振动吸收峰和—COO-对称拉伸振动吸收峰[6]。WK的特征吸收带主要位于多肽链的肽键(—CONH—)上。WK在3 700~3 100 cm-1的宽带是由 —O—H和 —N—H(酰胺A)的伸缩振动引起的,在1 539、1 239和1 653 cm-1处出现的峰分别属于酰胺Ⅱ、酰胺Ⅲ以及酰胺Ⅰ带[14]。从图2(b)可以看出,SA/WK的特征峰存在于SA和WK的特征峰,且无新峰出现,表明SA与WK复合成功。对比不同质量比的SA/WK纤维特征峰可以发现,随着WK含量的增加,3 000~3 800 cm-1吸收峰位置向低频移动,吸收强度增加。这表明SA与WK之间存在氢键相互作用。
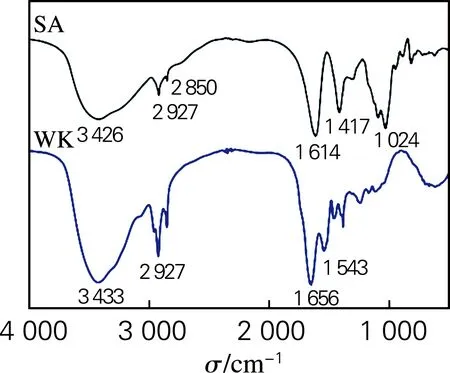
(a) SA与WK

(b) SA/WK
将不同质量比的SA/WK纤维在3 000~3 800 cm-1的光谱截出,用Origin 9.0通过Savitzky-Golay法对曲线进行平滑并求其二阶导数光谱,结果如图3所示。结合Origin中Gaussian分峰拟合的方法得到各种氢键类型子峰的分布强度,结果如图4所示。计算各子峰的峰面积并统计各种氢键的相对百分比,相应的结果总结在表1中。

图3 SA/WK纤维二阶导数光谱Fig.3 The second-derivative spectroscopy spectraof SA/WK fibers
由图4和表1可以看出,WK质量分数由10%增加到30%时,分子内氢键比例由原来的50.06%降低到45.28%,而分子间氢键比例由47.78%升高到52.05%,游离 —OH相对稳定。当WK质量分数继续增加至40%时,分子内氢键的比例由45.28%增加至48.67%,分子间氢键的比例由52.05%减少至46.58%。其中OH…OH对分子内氢键贡献最大,OH…醚氧和OH…π对分子间氢键贡献最大。
2.2 SA/WK溶液的流变性能
图5为不同WK质量分数的SA/WK溶液的流变曲线。WK质量分数在10%~30%,SA/WK 溶液的表观黏度随WK质量分数增加而增大。这是由于WK与SA分子间氢键增多,分子间相互作用增强,分子运动需要克服更大的阻力,客观表现为黏度增大。同时也证实了FT-IR的结果。当WK质量分数增加到40%时,SA/WK 复合体系的溶液黏度降低。可以解释为,当WK的质量分数超过一定值时,WK与SA分子间氢键减少,分子间相互作用减弱,导致溶液黏度降低;另一方面,过多的WK具有较高的电荷,导致溶液体系斥力,分子之间相互作用较弱,黏度减小。

(a) 10%WK(b) 20%WK(c) 30%WK(d) 40%WK图4 不同WK质量分数的SA/WK纤维曲线拟合图Fig.4 Fitting curves of SA/WK fibers with various WK contents

表1 不同质量比SA/WK纤维不同氢键的拟合结果Tab.1 Fitting results of hydrogen bonds in SA/WK fibers with different mass ratios
2.3 SA/WK复合纤维的XRD分析
SA、WK和SA/WK纤维的X射线衍射谱图如图6所示。SA在2θ为13.85°和21.56°出现弱的衍射峰,说明SA纤维存在较弱的结晶性,主要还是以无定型形式存在。WK分别在21.28°(峰较强)、32.20°、45.51°(峰较弱)出现衍射峰。结晶峰是由WK中肽链的α-螺旋结构和β-折叠结构所致[17]。从SA/WK纤维的XRD光谱可以看出,SA/WK纤维的结晶度很小,大部分以非晶态存在,WK在2θ为32.20°和45.51°处的衍射峰消失,SA在2θ为13.85°和21.56°处的结晶峰强度减弱,说明SA与WK之间存在相互作用,破坏了SA与WK二者原有分子链的规整性,使结晶度很大程度降低。

图5 不同WK质量分数的SA/WK溶液的流变曲线Fig.5 Rheological curves of SA/WK solutions withvarious WK contents
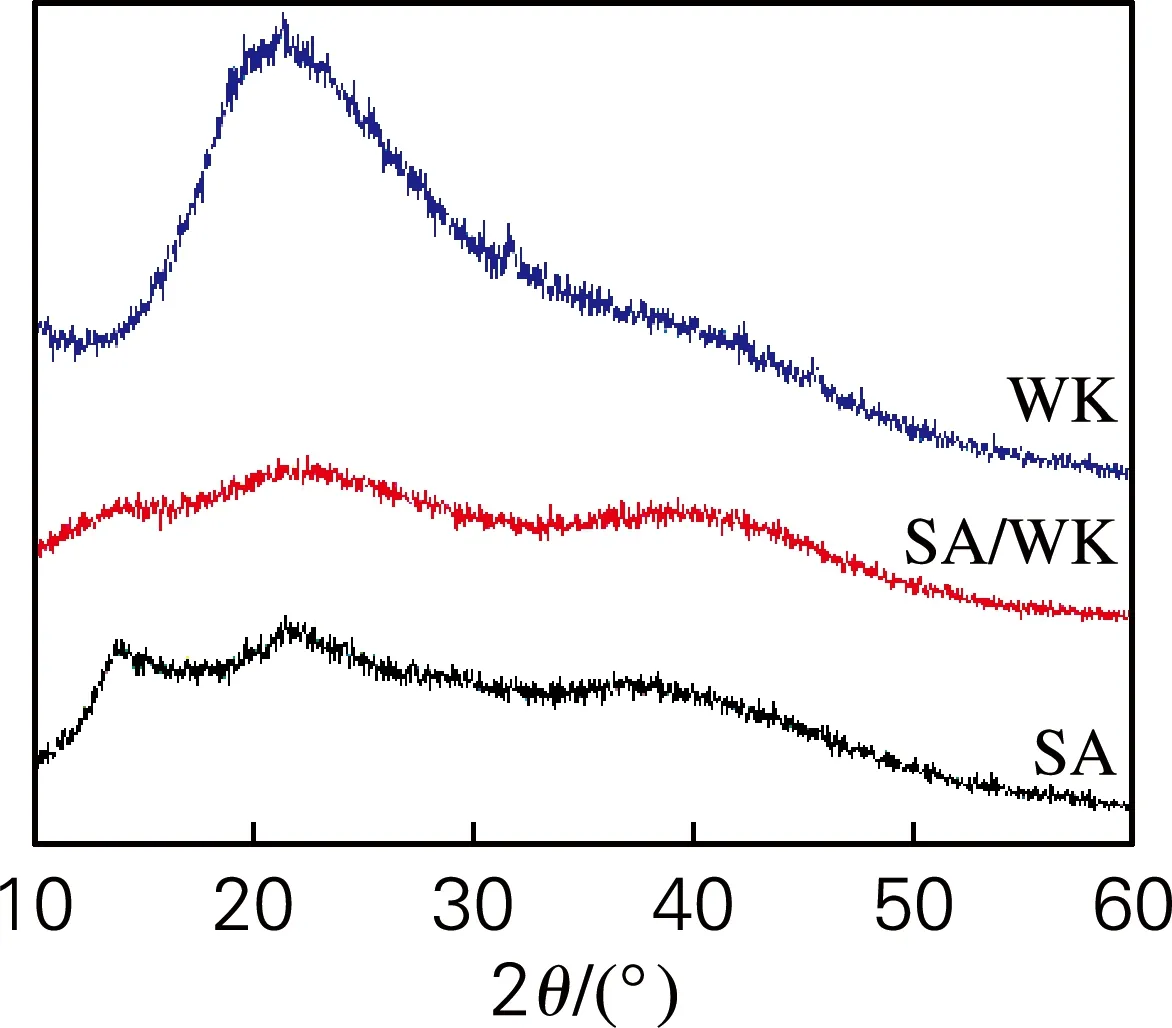
图6 SA,WK和SA/WK纤维的XRD曲线Fig.6 XRD patterns of SA, WK and SA/WK fibers
2.4 SA/WK纤维的力学性能
图7为WK质量分数对SA/WK纤维的断裂强度的影响。由图7可以看出,SA/WK纤维的断裂强度优于纯SA纤维,提高了36.15%。当WK质量分数为30%时,SA/WK纤维断裂强度达到最大值为1.87 cN/dtex,这与SA和WK之间的静电力和氢键有关。随着WK含量的增加,分子间氢键的数量增加,分子间相互作用增强,断裂强度增大;氢键作用的增加也制约了分子链的旋转和滑移,使得抗拉伸能力提高。但是,当WK质量分数达到40%时,SA/WK纤维的断裂强度降低。一个原因是当WK质量分数从30%增加到40%时,SA/WK分子间氢键的减少,分子间的相互作用力减小;另一个重要原因是,当WK含量过高时,角蛋白会部分聚集,造成应力集中。
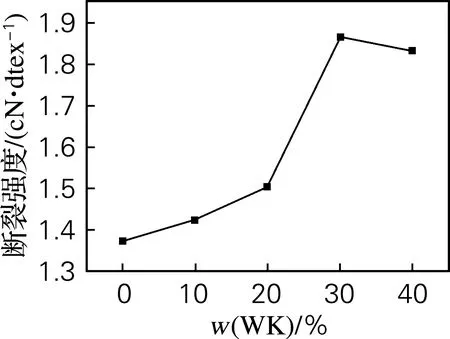
图7 WK质量分数对断裂强度的影响Fig.7 Effect of WK content on the breakingstrength of fibers
2.5 SA/WK纤维的表面形貌
图8为不同WK质量分数对SA/WK纤维的表面形貌的影响。由图8可观察到SA/WK纤维表面存在明显的不同深度的沟槽结构。这是由湿法纺丝过程中的双扩散反应机理造成的。凝固浴中的Ca2+首先扩散到纤维表面,与纤维表面的SA进行离子交换,并在纤维表面形成凝胶层(皮层);SA中Na2+向凝固浴中扩散。后续双扩散反应过程必须通过皮层完成,进而导致纤维内外的传质速率不同。这种由于双重扩散和传质速率不同导致纤维各方向收缩不均匀,在纤维表面形成条纹沟槽结构[18]。此外,对比不同WK含量的SEM图发现,随着WK含量的增加,纤维表面的沟槽结构深度加深,数量增多。这是因为WK含量增加,双扩散和传质速率加快,纤维收缩大,异形度增加,宏观表现为沟槽深度加深。

(a) 10%WK(b) 20%WK

(c) 30%WK(d) 40%WK
3 结 论
SA/WK纤维的红外光谱图显示,SA和WK为物理共混,但SA和WK存在氢键作用,其分子间氢键在WK质量分数为30%时达到52.05%,且主要来自OH…π。SA/WK溶液的表观黏度随WK含量呈先增大后减小趋势,在WK质量分数为30%时黏度最大。30%WK纤维具有最大断裂强度1.87 cN/dtex,较纯海藻纤维强度提高36.15%。SA/WK纤维的结晶度小于WK,主要以非晶态存在。SA/WK纤维表面具有沟槽结构,且随WK含量增加,沟槽深度和数量增加。

