内科胸腔镜确诊表现为大量胸腔积液的胸膜肺结节病1例并文献复习
谈洁 于晶 陈文静 闫冰迪
结节病是一种累及全身多系统的肉芽肿性疾病,原因未明,最易侵犯肺组织,其中累及胸膜者称为胸膜肺结节病(pleuropulmonary sarcoidosis,PPS)。PPS患者胸膜结节可与肺结节同时出现,也可继发于肺结节之后,临床上多表现为胸闷、气促等胸腔积液的表现,易误诊为结核性胸腔积液、恶性胸腔积液。本文通过报道一例经内科胸腔镜确诊的PPS,提高广大医生对PPS的认识。
临床资料
患者,女,52岁,以“胸闷、气短6个月”为主诉入院。患者6个月前无明显诱因出现胸闷、气短,活动后加重,自行口服药物治疗,症状略缓解,未正规诊治。6个月来上述症状反复加重,1天前于我院门诊行胸部CT检查示右肺门软组织密度影,两肺多发结节,纵隔多发淋巴结,右侧大量胸腔积液(见图1)(A、B),为求进一步诊治收入我科。入院查体:体温:36.7 ℃,心率:76次/分,呼吸:18次/分,血压:125/75 mmHg。右下肺语颤减弱,语音传导减弱,右肺呼吸音弱,左肺呼吸音正常,未闻及干湿性啰音及胸膜摩擦音,未触及浅表淋巴结肿大。余查体无明显异常。入院后肝功示总蛋白 64.3 g/L,白蛋白39.1g/L,血沉17.0 mm,ANA谱示抗线粒体M2抗体:++;TO-1抗体:++;余化验检查均未见明显异常。行胸腔穿刺术引流出黄色胸腔积液,胸水常规:白细胞总数3600×106/L、李凡他实验 +,多核>单核;胸水生化:总蛋白10.5 g/L,葡萄糖 9.28 mmol/L,腺苷脱氨酶 15.85 U/L,乳酸脱氢酶 119.0 U/L,氯 109.0 mmol/L。胸水脱落细胞:见大量淋巴细胞、红细胞,少量间皮细胞及噬细胞,未见恶性细胞。因未能明确诊断,遂行内科胸腔镜探查:见右侧脏层胸膜与壁层胸膜黏膜多发隆起,表面覆盖有坏死,于黏膜隆起处多次钳夹组织送检(见图2)(A、B)。病理回报(右侧壁层胸膜活检)见多量慢性肉芽肿性炎,周边有少量纤维素样渗出,并见有较多慢性炎细胞浸润,不除外结节病(见图3)(A、B)。明确诊断为胸膜肺结节病,给予口服醋酸泼尼松片25mg/d治疗,1周后患者呼吸困难症状较前略有改善,1个月后患者症状基本消失,复查胸部CT:右肺门软组织影未见明显变化,右肺下叶结节减小,右侧胸腔积液完全吸收(见图4)(A、B),激素逐渐减量,2个月后复查胸部CT,结节较前减小,右侧胸膜增厚(见图5)(A、B),半年后复查胸部CT:双肺结节影较前减少,右肺下叶结节影较前减小。右侧胸膜增厚(见图6)(A、B),停药观察。
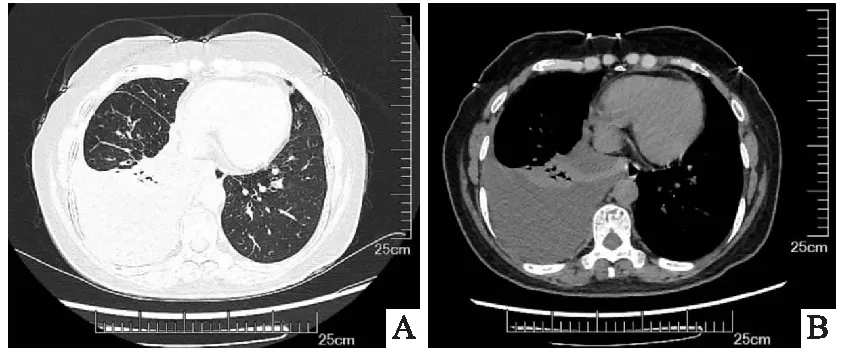
图1 A、B 胸部CT双肺见多发结节状高密度影,较大者位于右肺下叶(IM42),边缘毛糙,牵拉胸膜,右侧胸腔内见液体密度影
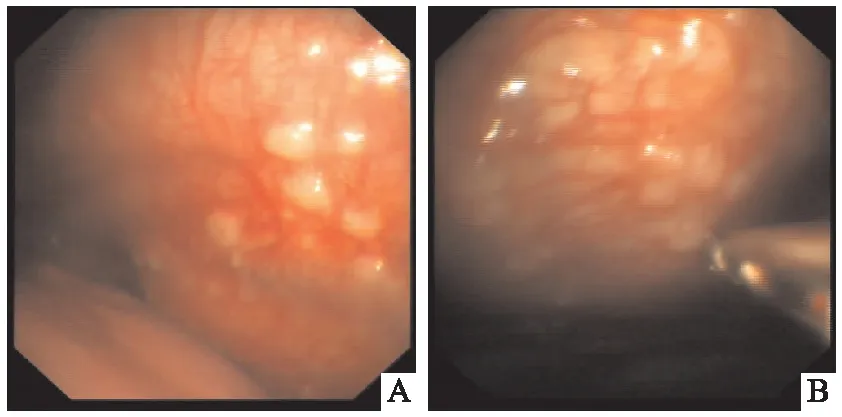
图2 A、B 内科胸腔镜下见右侧脏层胸膜与壁层胸膜黏膜多发隆起,表面覆盖有坏死
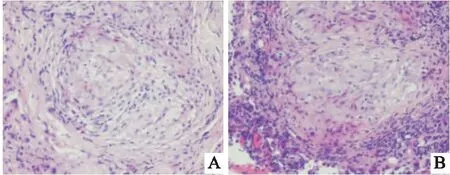
图3 A、B病理 HE染色(×200)多量慢性肉芽肿性炎,周边少量纤维素样渗出,并见较多慢性炎细胞浸润
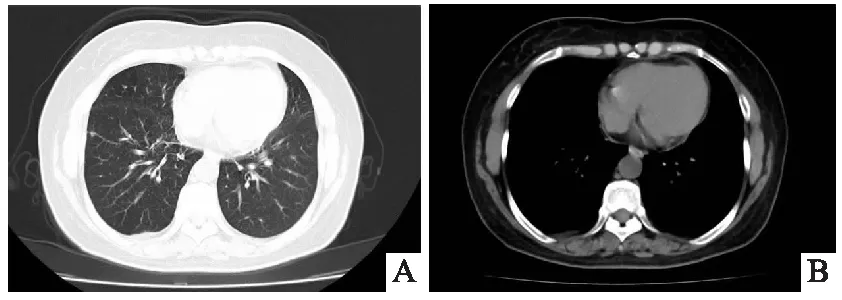
图4 A、B 胸部CT 双肺可见结节状高密度影,较大者位于右肺下叶(IM32),直径约5 mm,纵隔可见多发淋巴结显示,两侧胸腔未见液体密度影

图5 A、B 胸部CT 双肺可见散在结节影,最大者于右肺下叶(IM35)直径约3mm。右侧胸膜增厚
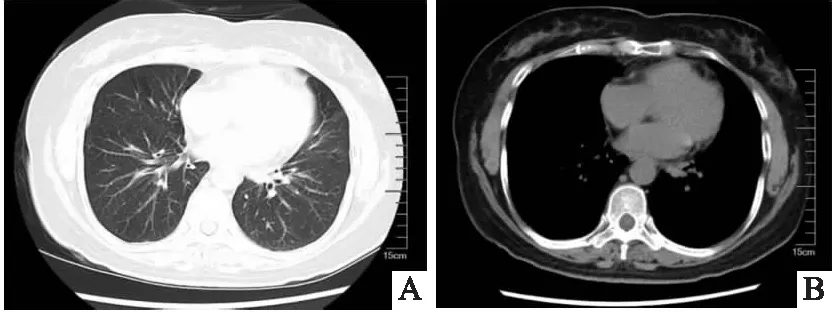
图6 A、B 胸部CT 双肺结节影较前减少,右肺下叶结节影较前较小。右侧胸膜增厚
讨 论
结节病(PPS)是一种原因不明的非坏死性肉芽肿性疾病,可累及全身多系统,肺和淋巴系统最常受累,其病理特征主要表现为非干酪样坏死性肉芽肿性改变。有文献称约90%的结节病可累及于肺部,胸膜组织受累少见[1]。外国学者在上世纪90年代初已经提出PPS的概念[2],但在国内尚未有明确的诊断标准。肺结节病需要依靠病理组织活检结果确诊,然当其累及胸膜时,其病理表现极易与结核性胸膜炎的慢性干酪样肉芽肿性炎相混淆。但近年来通过对内科胸腔镜技术的广泛开展,人们对PPS的认识不断提高,诊断率不断上升。Huggins[3]等对国外181例结节病患者进行研究,发现伴有胸腔积液表现的患者占2.8%,并且只有1.1%是由胸膜结节所致,提出结节病患者的胸腔积液可能与结节病无关的观点。孙永昌等[4]对国内发表的结节病病例进行总结,发现结节病胸膜病变的发生率为3.4%~16.7%。结节病的病因与发病机制目前仍无确切的说法,其病因考虑可能与慢性炎症、免疫、遗传及环境等多种因素相关[5]。此外有研究表明Th17细胞不仅参与结节病中肺泡/肉芽肿生成的过程,也参与了肺纤维化的过程,在激素治疗过程中可能也发挥着重要作用[6]。
PPS主要表现为胸膜增厚、胸膜结节、胸腔积液和气胸,其中胸膜增厚和胸膜结节常同时出现,胸腔积液相对少见,气胸则多出现于疾病晚期,可能与肉芽肿侵犯胸膜,导致胸膜破裂有关[5]。其临床表现以胸膜病变的常见症状为主,比如低热、咳嗽、气促、胸闷、胸痛、呼吸困难等,部分患者在查体时可发现肿大的浅表淋巴结。部分患者实验室检查可出现白细胞减少,血沉增快,C反应蛋白升高等。亦有研究表示肿标中CA125会轻度升高,腺苷脱氨酶可能降低。以胸腔积液为主要临床表现的PPS患者,胸水常为渗出性,部分可迁延为纤维素性胸膜炎。
PPS的胸部影像学表现多为肺门及纵隔淋巴结肿大,单双侧均可出现。国外学者将其胸部X线表现分为4期[7],国内病例Ⅱ期多见,其胸部CT多表现为肺门、纵隔淋巴结增大伴有胸腔积液[8]。PPS患者内科胸腔镜下多表现为大小不等的结节,弥漫性分布于壁层、脏层胸膜上,呈白色、灰白色或粉红色,甚至可累及膈肌,同时可伴有结节周围胸膜充血水肿。若患者存在有内科胸腔镜探查的禁忌时,纤维支气管镜活检及浅表淋巴结穿刺活检,也可以帮助诊断该病。PPS的活检病理组织多表现为非干酪性坏死性肉芽肿性炎,免疫组化及抗酸染色均为阴性。PPS的确诊以病理组织活检结果为金标准,同时应结合患者临床表现、实验室化验及影像学等辅助检查,排除其他肉芽肿性疾病。其治疗方案与结节病基本一致,糖皮质激素一般可以获得较好的疗效,部分患者需同时联用免疫抑制剂、细胞毒性药物等。但注意使用中必须要严格随访,根据患者状态调整激素用量,避免激素相关性肺结核的发生[9]。
本例患者初期表现为胸闷、气短等典型胸腔积液压迫肺组织的症状,但因患者未前往医院进行正规诊治,无法判断患者当时病情严重程度。入院时胸部CT表现为双肺多发结节,右肺门软组织影及纵隔淋巴结肿大,右侧大量胸腔积液,易误诊为肺癌。胸水为黄色渗出液,内科胸腔镜下表现为壁层及脏层胸膜弥漫性分布的白色结节,大小不等,易与结核性胸膜炎或肺癌等恶性肿瘤的胸膜转移相混淆。
由此可见,PPS的临床表现无特殊性,仅靠临床症状、影像学表现及实验室指标极易误诊为结核或恶性肿瘤,进行组织活检的病理结果是确诊该病的可靠手段。本例患者入院后经胸腔穿刺术未能明确诊断,行内科胸腔镜下组织病理活检后明确诊断为PPS,给予激素治疗有效,定期复查胸部CT见右肺门软组织影、两肺结节及纵隔淋巴结较前明显缩小或消失。证明内科胸腔镜对于胸膜疾病的诊断而言是一种行之有效的技术手段,当胸腔积液患者经胸腔穿刺术不能明确诊断其病因时,可考虑行内科胸腔镜进行检查,以免延误疾病的诊断及治疗。

