左乙拉西坦联合奥卡西平治疗儿童癫痫的疗效及对患者免疫功能、脑电图及认知功能的影响
陈书远,刘金宝,刘世祺
惠州市第一人民医院儿科,广东 惠州 516001
癫痫在儿童中经常可见,其发病率在一岁左右时最高,儿童时期是大脑机能发育的重要时期,癫痫会损伤患儿的正常脑细胞,影响正常的免疫、神经系统功能,从而影响患儿正常的认知功能与免疫力[1]。药物治疗是目前常用的临床癫痫治疗方法,其中奥卡西平药物使用最广泛[2]。研究表明,奥卡西平的安全性很高,但不能有效地改善患儿认知功能[3]。本研究主要观察左乙拉西坦联合奥卡西平治疗儿童癫痫的疗效,并探讨其对患者免疫功能、脑电图及认知功能的影响,现报道如下:
1 资料与方法
1.1 一般资料 选择2018 年10 月至2020 年10月在惠州市第一人民医院治疗的49 例癫痫患儿为研究对象,所有患儿均符合《2005 年国际抗癫痫联盟癫痫诊疗指南》中的小儿癫痫诊断标准[4]。纳入标准:①无使用抗癫痫药物史;②就医前4 周内未使用抗癫痫药物;③每个月≥1次癫痫发作。排除标准:①现阶段身体有感染性疾病,内脏、血液系统、脑部有疾病;②免疫系统有缺陷;③精神、意识存在异常。采用随机数表法将患儿分为对照组24例和观察组25例。两组患儿的基线资料比较差异均无统计学意义(P>0.05),具有可比性,见表1。本研究经医院医学伦理委员会批准,患儿家属均知情并签署同意书。
表1 两组患儿的基线资料比较(±s)

表1 两组患儿的基线资料比较(±s)
组别观察组对照组t/χ2值P值例数2524年龄(岁)5.32±1.285.25±1.360.1850.427病程(月)9.41±2.479.29±2.580.1660.434发作频率(次/月)2.55±0.292.51±0.330.4500.327男1413女11110.0170.897性别(例)
1.2 治疗方法 对照组患儿为单独服用奥卡西平片药,北京诺华制药有限公司制造,批准文号:国药准字J20140103,开始服药时按10 mg/(kg·d)标准,以后根据患儿情况每周增加用药量,但患儿的最大用药量控制在48 mg/(kg·d)以内,治疗16 周。观察组患儿在对照组用药的基础上,同时服用左乙拉西坦口服液[UCB Pharma S.A,国药准字J20160060 (H20160152)]治疗,初期按5~10 mg/(kg·d)确定用药量,以后根据患儿情况每周增加用药量,但最大用药量≥60 mg/(kg·d),治疗16周。
1.3 观察指标与评价方法 (1)免疫功能:分别在入院当天、治疗16 周后,抽取患儿清晨的空腹静脉血5 mL,用1~14 型高速离心机(德国Sigma 公司,转速:3000 r/min,离心半径:80 mm)离心10 min,分离得到血清样本,采用ELISA 法检测免疫功能指标(IgA、IgM、IgG)水平,CD3+、CD4+水平的检测选择用BD全自动多色分析仪进行。(2)脑电图(EEG):在治疗的8周、16 周选择脑电图仪对患儿脑部异常放电情况进行记录,放电消失,为“控制”;放电减少量在50%以上,记为“明显好转”;放电减少量在25%~49%间,记为“好转”,放电减少量小于25%,记为“无效”。有效率=(控制+明显好转+好转)/例数×100%。(3)认知功能:治疗前后运用韦氏儿童智力量表[5]评估全量表智商(FIQ)、操作智商(PIQ)、言语智商(VIQ)。(4)治疗有效性:癫痫没有发作,记为“控制”;癫痫频次减少量≥75%,记为“显效”;癫痫频次减少量50%~75%,记为“好转”;治疗后,癫痫频次减少量<50%,记为“无效”;有效率=(控制+显效+好转)/例数×100%。(5)安全性:记录两组患儿治疗期间出现的不良反应情况。
1.4 统计学方法 应用SPSS21.0 统计软件进行数据分析。计量资料以均数±标准差(±s)表示,组间比较采用t检验,计数资料比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患儿治疗前后的免疫功能指标比较 治疗后,两组患儿的IgA、IgM、IgG 明显低于治疗前,且观察组明显低于对照组,两组患儿的CD4+、CD3+明显高于治疗前,且观察组明显高于对照组,差异均有统计学意义(P<0.05),见表2。
表2 两组患儿治疗前后的免疫功能指标比较(±s)
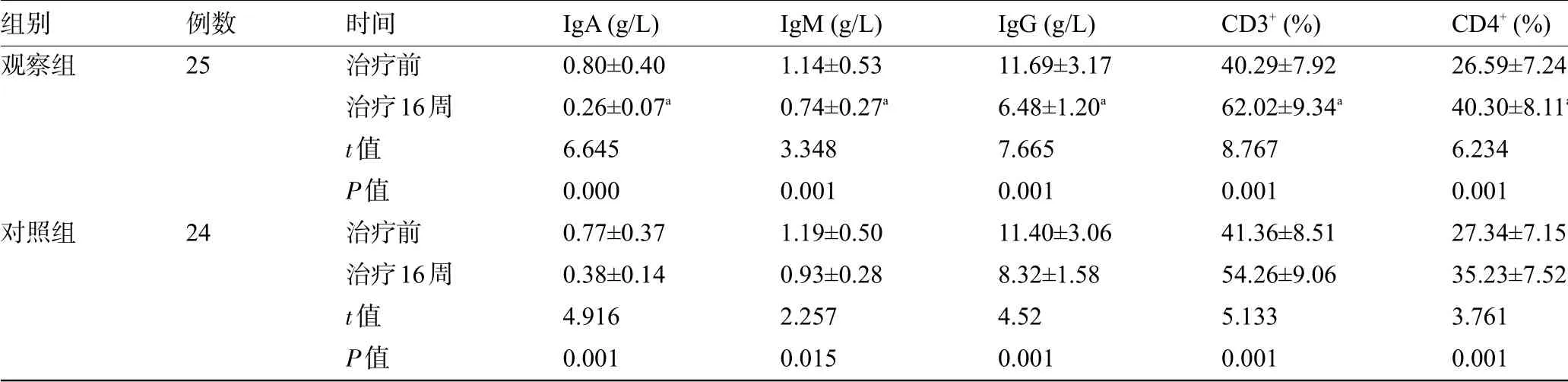
表2 两组患儿治疗前后的免疫功能指标比较(±s)
注:与对照组治疗后比较,aP<0.05。
组别观察组对照组例数2524时间治疗前治疗16周t值P值治疗前治疗16周t值P值IgA(g/L)0.80±0.400.26±0.07a 6.6450.0000.77±0.370.38±0.144.9160.001 IgM(g/L)1.14±0.530.74±0.27a 3.3480.0011.19±0.500.93±0.282.2570.015 IgG(g/L)11.69±3.176.48±1.20a 7.6650.00111.40±3.068.32±1.584.520.001 CD3+(%)40.29±7.9262.02±9.34a 8.7670.00141.36±8.5154.26±9.065.1330.001 CD4+(%)26.59±7.2440.30±8.116.2340.00127.34±7.1535.23±7.523.7610.001
2.2 两组患儿治疗前后的EEG比较 治疗16周后,两组患儿异常放电均得到改善,且观察组明显优于对照组,差异均有统计学意义(P<0.05),见表3。

表3 两组患儿治疗前后的EEG比较(例)
2.3 两组患儿治疗前后的认知功能比较 与治疗前比较,治疗后两组患儿的认知功能指标均明显提高,且观察组明显优于对照组,差异均有统计学意义(P<0.05),见表4。
表4 两组患儿治疗前后的认知功能比较(分,±s)
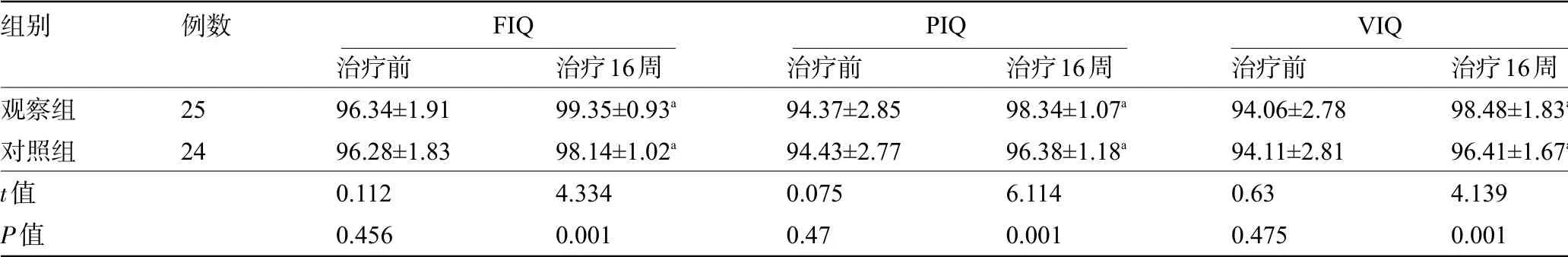
表4 两组患儿治疗前后的认知功能比较(分,±s)
注:与本组治疗前比较,aP<0.05。
组别观察组对照组t值P值例数2524治疗前96.34±1.9196.28±1.830.1120.456治疗16周99.35±0.93a 98.14±1.02a 4.3340.001治疗前94.37±2.8594.43±2.770.0750.47治疗16周98.34±1.07a 96.38±1.18a 6.1140.001治疗前94.06±2.7894.11±2.810.630.475治疗16周98.48±1.8396.41±1.674.1390.001 FIQ PIQ VIQ
2.4 两组患儿的临床疗效比较 治疗后,观察组患儿的治疗有效率为88%,明显高于对照组的58.33%,差异有统计学意义(χ2=5.529,P=0.019<0.05),见表5。

表5 两组患儿的临床疗效比较(例)
2.5 两组患儿的不良反应比较 治疗期间,两组患儿均未发生严重不良反应。两组患者儿的总不良反应发生率比较差异无统计学意义(χ2=5.556,P=0.456>0.05),见表6。
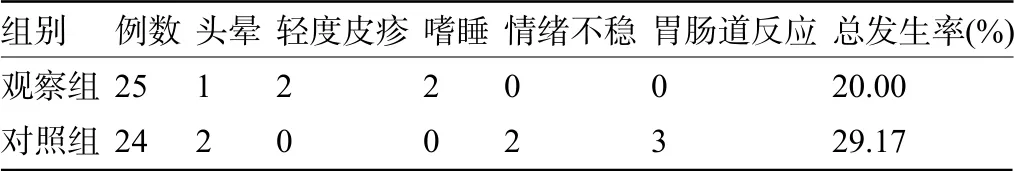
表6 两组患儿的不良反应比较(例)
3 讨论
癫痫在全球范围内大约影响着5000 万人。尽管在过去的三十年中,癫痫的治疗手段已经有了极大的进步,但它仍在世界疾病负担中排名前列。目前,治疗抗癫痫药物多达三十几种,这之中,由于奥卡西平具有良好的抗癫痫效果,运用也最为广泛,有研究发现,奥卡西平不能有效地控制痫样放电,由于神经元的痫样放电可致患儿的自身反应时间产生延迟,造成认知功能减退[6-7],长时间连续地服用奥卡西平有可能会使患者神经元造成受损,影响患者的自身学习能力,主要表现在不能集中注意力、反应力迟缓、警觉性降低等[8-9]。这种危害对于小儿,尤其是处于学龄期的儿童是不可挽回的。至于为什么会出现这种情况,现在还不明确,但可以采用多药物的配合使用,从而控制痫样放电,能一定程度上降低对认知功能的损害[10-11]。
左乙拉西坦系吡咯烷酮衍派生,通过与SV2A 联合[12],神经递质能够有效释放从而阻断异常的神经放电情况,有效改善癫痫的发病情况。左乙拉西坦使用风险低,能很好地与其他抗癫痫药物配合使用[13]。与奥卡西平联合用药时能弥补奥卡西平的不足,药物间相互作用,治疗效果明显增强,且不良反应也较单独使用奥卡西平明显减少、降低[14]。此外,左乙拉西坦几乎不对患儿脑电波产生影响,而且还能够有效控制痫样放电,患儿EEG得以改善[15]。左乙拉西坦能够正向促进那些存在认知功能损害的癫痫患儿的执行功能恢复[16],本研究也进一步证明,在对患者的认知及EEG功能的效果上,联合用药比单一用药效果更好。近年在癫痫病因机制研究中发现,患儿免疫系统、神经系统与癫痫发病紧密关联[17]。二者相伴而生,彼此间影响及调节。癫痫的多种因素(患儿年龄、病程、药物、发作的频次、病因等)均可影响患者免疫。患儿癫痫发作后,患者的免疫指标(IgG、IgM、IgA、CD4+、CD3+)均有明显异常,治疗后,情况得到逐步改善,而这一现象也在本次研究中被观察与证实,且通过左乙拉西坦与奥卡西平联合用药,有效地改善了患者的免疫指标、同时促进患者免疫功能和神经功能双向调节,不良反应明显减少、降低,这也证实双药联用是安全可靠的。
综上所述,左乙拉西坦联合奥卡西平联合治疗,不仅可以提高治疗效果,而且还有效调节其自身免疫功能,达到了患者免疫功能和神经功能双向调节。这为今后的进一步临床研究与临床诊疗提供有效依据。

