例说基于课程核心素养的初中化学教学设计与实践
吴丛铎

摘要:以人教版初中化学(九年级上册)第五单元课题1“质量守恒定律”教学设计与实践为例,通过创设真实情境、激发探究热情,重视分类比较、培养科学态度,开展实验探究、发展科学思维,解决实际问题、形成化学观念等路径来发展学生的核心素养,落实学科育人的根本任务。
关键词:质量守恒定律;教学设计;核心素养;学科育人
文章编号:1008-0546(2022)04-0037-05
中图分类号:G632.41
文献标识码:B
doi:10.3969/j.issn.1008-0546.2022.04.008
初中化学是引导学生从化学视角认识物质世界的一门基础自然科学课程,具有启蒙性、实践性与发展性的特点,对落实立德树人根本任务,促进学生全面发展具有重要价值。课程核心素养是学科育人价值的集中体现,是学生通过课程学习而逐步形成的适应个人终身发展和社会发展需要的正确价值观、必备品格和关键能力[1]。初中化学课程核心素养包括化学观念、科学思維、探究实践和科学态度与责任四个方面,它们是相辅相成的整体,体现了化学学科育人的基本要求。
人教版九年级化学教材将《质量守恒定律》安排在上册第五单元课题1,内容包括从宏观和微观两个层面认识质量守恒定律。课标要求认识质量守恒定律,能说明化学反应中的质量关系,认识定量研究对于化学科学发展的重大作用[2]。学生在学习本课题之前,已经了解一些化学反应,知道化学变化过程中物质的种类一定发生变化,也了解化学反应的微观本质,知道化学变化中分子可分而原子不可以再分。
本文以“质量守恒定律”教学实践为例,谈谈如何在课堂教学中发展学生的核心素养,落实学科育人的根本任务。
一、创设真实情境,激发探究热情
活动1:明确本课的学习任务
师:(出示如图1所示的奇石图片)大家看到这幅图,想到了哪一种实验仪器?
生:天平。
师:对!现代化学之父拉瓦锡几乎在他的每一个实验中都运用了天平,他用科学实验和定量研究,使化学走向科学。
师:你能回忆起有关拉瓦锡对化学学科发展的贡献吗?
生1:第一单元里有介绍,拉瓦锡利用天平进行定量研究,弄清楚了物质燃烧的本质。
生2:在学习“水的组成”时,我知道了“拉瓦锡做了一个氢气在氧气中燃烧的实验”,证明了水是由氢元素和氧元素组成的。
师:其他同学有补充吗?大家至少还知道一个拉瓦锡的贡献。
生3:拉瓦锡用定量方法研究了空气的成分,得出了空气由氧气和氮气组成,其中氧气约占空气总体积1/5的结论。
师:在拉瓦锡时代,科学家思考化学反应前后,物质的质量发生了怎样的变化?有的科学家认为,质量变小了,如木炭燃烧;有的科学家认为质量变大了,如金属的煅烧;而拉瓦锡通过精确的实验,证明了化学反应前后物质的质量不变。
师:今天我们将通过实验来探究化学反应前后各物质的质量总和是否相等。
师:(出示托盘天平和电子天平)同学们愿意选择哪种天平来完成今天的实验探究?为什么?
生4:我们组选电子天平。因为使用方便。
生5:我们组也选电子天平。不仅因为使用方便,还在于它精确度更高。
设计意图:创设情境要围绕学习目标,紧扣学习内容,遵循认知规律。通过天平引入,让学生感受到本节课的实验主题是定量研究;通过托盘天平和电子天平的比较,让学生学会分析和选择;通过简单化学史的回顾与介绍,让学生明确本节课的探究目的,有效地引导学生学习,激发学生的探究热情。
二、重视分类比较,培养科学态度
活动2:寻找研究的物质体系
师:请同学们用符号表达式写出你已知的化学反应,并将写出的化学反应进行分类。
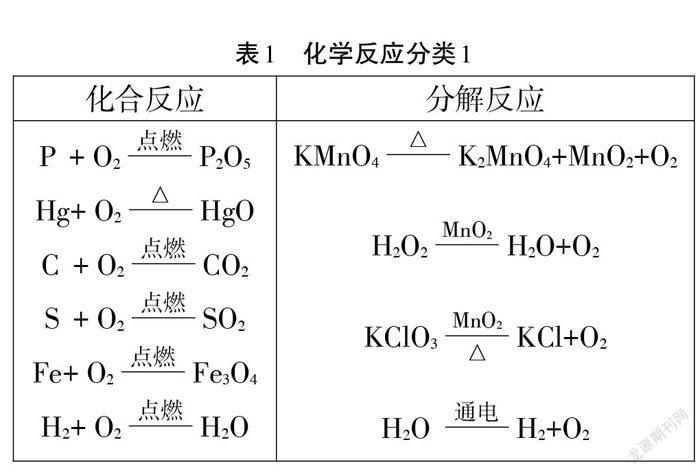
生6:我们组写了10个表达式(表1),分成了两大类,一类是化合反应,一类是分解反应。
生7:我们组写了9个表达式,跟第7组(表1)类似,分成两大类,一类是有氧气参加的反应,一类是有氧气生成的反应。
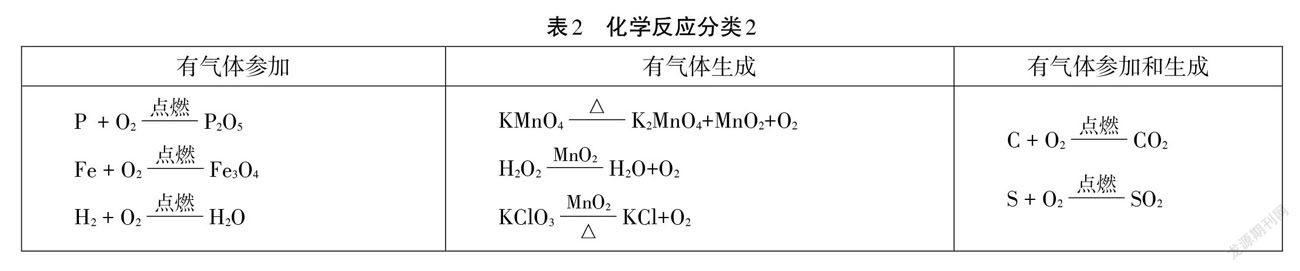
生8:我们组写了8个表达式(表2),分成了三大类,一类是有气体参加的反应,第二类是有气体生成的反应,第三类是既有气体参加又有气体生成的反应。
师生充分交流,约定用第9组(表2)的分类标准对反应体系进行分类。
师:请同学们关注课本(92-95页)提供的三个用于探究的化学反应:红磷在空气中燃烧,铁钉与硫酸铜溶液反应,碳酸钠与盐酸反应。如果让你们分类,后二个反应分别放在哪一类呢?为什么?
教师写出反应的符号表达式:
Fe+CuSO4—Cu+FeSO4,Na2CO3+HCl—NaCl+H2O+CO2
生9:碳酸钠与盐酸的反应放在第二类,因为有二氧化碳气体生成。
生10:铁钉与硫酸铜溶液的反应应为第四类,是既没有气体参加也没有气体生成的反应。
师:可否将上述四类反应分成二类?
生11:可以。以“有无气体参加或生成”为分类标准。
设计意图:通过回顾所学化学反应、书写反应的符号表达式,感知化学变化的普遍,感知化学变化中物质的改变。通过分类和比较,让学生意识到在选择实验体系时,有气体参加和有气体生成的反应需要特别关注,培养学生严谨的实验态度。
活动3:合作设计实验装置
师:这些反应前后的质量是否不变呢?我们可以通过实验来探究。
分小组进行实验设计。一个学习小组选择上述三个反应中的其中之一,进行实验设计。要求:使用已知的常见的器材,画出组装好的实验装置(天平除外),并陈述小组的设计思路。
设计意图:引导学生合作设计实验装置,并形成设计稿,培养学生的空间想象力、表达与交流能力,同时感受实验设计是进行实验探究的重要环节。
三、开展实验探究,发展科学思维
活动4:选择合适的实验装置
师:请各小组将你们的设计图进行展示,并简要说明设计思路。
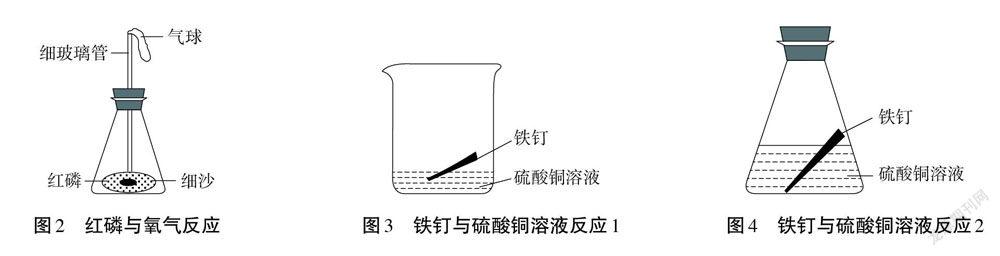
生12:我们组要做红磷与氧气反应的实验,这是我们的实验装置图(图2)。
生13:我们组准备做铁钉与硫酸铜溶液反应的实验,这是我们的设计稿(图3)。
生14:我们组也准备做铁钉与硫酸铜溶液反应的实验,这是我们的设计稿(图4)。
师:表述时请说清楚设计依据。如:在设计红磷与氧气反应时,为何考虑密闭体系?细沙、玻璃管、气球的作用是什么?如何引燃红磷?什么时候称量?称量什么?怎么称量?预期看到什么现象?
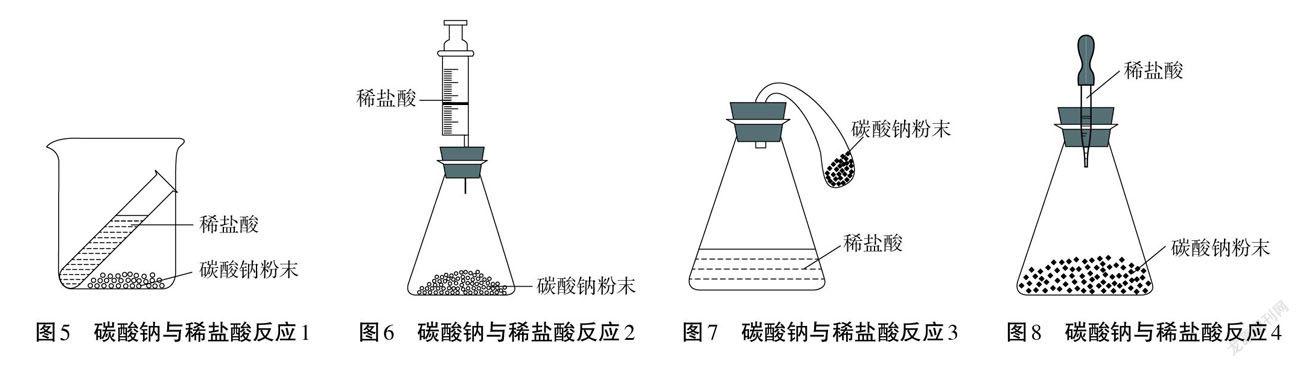
生15:我们组准备探究碳酸钠与盐酸反应前后的质量关系,这是我们组的实验装置图(图5)。
生16:你们组的装置不密闭,而且反应后有气体生成。请看我们组的实验装置图(图6)。
生15:课本上就是这个装置。
生16:我们今天的探究任务是验证质量守恒定律,使用你们组的装置达不成实验目的。
生17:我们组拟选用的装置(图7)与第3组(图6)
类似,是一个密闭体系,这样生成的二氧化碳气体仍在实验体系中。我们准备先称量整套装置和药品的质量,然后将少量碳酸钠粉末倒入稀盐酸中,等反应结束后再称量整套装置的质量。
生18:我们组拟选用的装置(图8)与第3组(图6)更为相似。
生16:我们组(图6)的比你们组(图8)要好一些,你们装置中的橡皮塞在实验过程中说不定会迸出去。
教师对各组设计的装置进行审核与评价,分发准备好的实验器材与药品,学生分组进行实验测量。
设计意图:通过分析比较设计方案,讨论实验体系的密闭与开放问题,实现了将猜想和实验目标与实验设计相结合的过程,使学生体会主动参与设计实验的乐趣,初步感知定量研究的意义。
活动5:实验探究化学反应前后物质的质量关系
师:请各小组按照分工,用选定的方案一、二、三(分别如图2、图4、图7所示)进行自主实验,在实验过程中,注意观察实验现象,并及时记录。
各小组有序进行实验,记录实验现象。
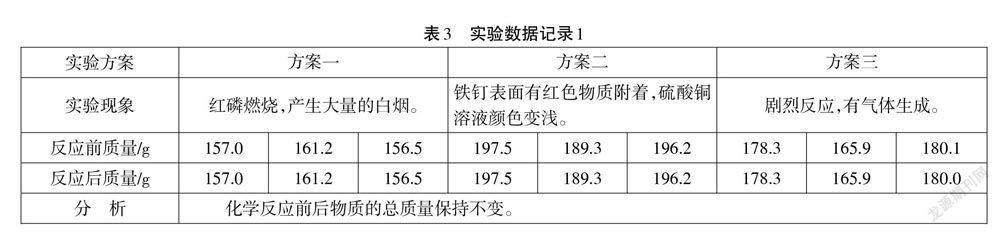
实验结束后汇报、交流。其中九个小组的实验记录如表3。
师:仅通过这三个反应能说明所有化学反应前后物质的总质量均不改变吗?
生19:可以。我们做了多组平行实验,而且有两类不同的反应体系。
生20:不可以。我们的实验组太少,重复实验的次数太少,选用的反应也太少,仪器精确度也太低。
师:随着科技的进步,科学家运用更精密的仪器,经过大量严谨科学的定量实验研究,才归纳总结出质量守恒定律。
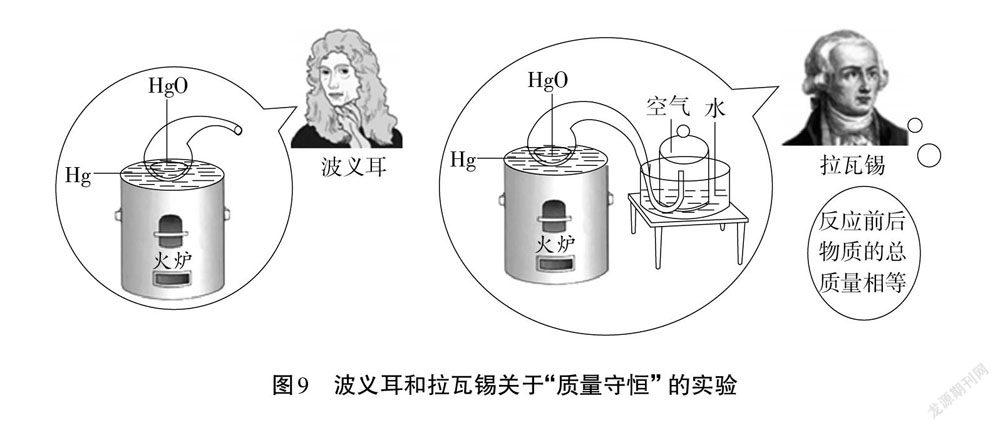
师:在化学史上,波义耳和拉瓦锡两位科学家做了两个类似的实验(图9)。请你说一说,两者的区别是什么?为什么波义耳没能得到“质量守恒”的结论?
生21:我曾看过关于这个化学史的小故事。因为波义耳实验后打开了仪器,他的实验不算是在密闭体系中完成的。
设计意图:质量守恒定律是物质发生化学变化所遵循的基本规律,它的发现是化学史上的里程碑,实现了化学研究从质的变化到量的变化的转化,定量研究开始逐渐成为化学研究的主要方法,是化学成为一门理科的重要标志之一,也促进了化学的发展。通过让学生亲历该实验探究过程、分析讨论实验方案、观察和记录实验现象、反思和评价实验结论,认识了质量守恒定律,认识了定量研究的重要性,形成了一定的归纳判断能力、证据推理能力,发展科学思维。
四、解决实际问题,形成化学观念
活动6:称量镁条在空气中燃烧前后固体的质量
指导学生分组完成课本94页的[实验5-2],学习用质量守恒定律解释实验结果。
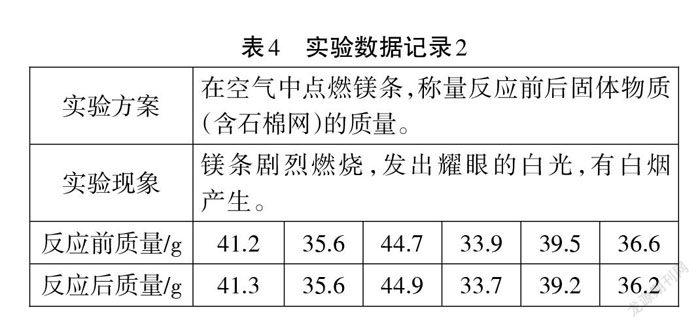
实验结束后汇报、交流。其中六个小组的实验数据见表4。
师:该实验的体系与前面三个实验的体系有什么不同?
生:这是敞开体系。
师:根据质量守恒定律,从理论上讲,反应后固体物质的质量是应该增大还是减少呢?为什么?
生22:增大。增加的质量是参加反应的氧气的质量。
师:那为什么我们实验的结果是有的增大,有的减少,有的不变呢?
各小组热烈讨论。
生23:我们小组认为,我们测得反应后的质量之所以减少,是因为在实验过程中产生了大量的白烟。
生22:我们小组认为,我们测得反应后的质量之所以增加,是因为有氧气参加了反应。
师:是不是所有小组的实验中都有氧气参加反应?都有白烟生成?
生:是的。
师:那我们应该怎样表达更完整更科学呢?各小组继续讨论。
生24:我们小组弄明白了。因为氧气参加反应,生成固体的质量增加;因为白烟散逸到空气中,使得固体质量减少。最终结果是大还是小还是不变都有可能。
师:很好!同学们能够透过不同情况下测量结果的表象,更为深入地认识化学反应前后的质量关系的本质,是学习能力提升的表现。
设计意图:通过实验、比较、判断、分析,不断地揭示矛盾和解决矛盾,学习用科学的眼光看待具体的实验,具体问题具体分析,从而获得科学的结论。通过这一活动,学生进一步明确“密闭体系”在验证质量守恒定律实验中的作用,形成正确的实验观;也进一步意识实验体系对化学实验研究的重要性,體系决定着反应的探究装置。
活动7:对质量守恒定律进行微观解释师:为什么所有化学反应都遵守质量守恒定律呢?
师:以水的分解为例,你能说说这一反应的本质是什么?从微观角度来说,为什么反应前后物质质量不变?
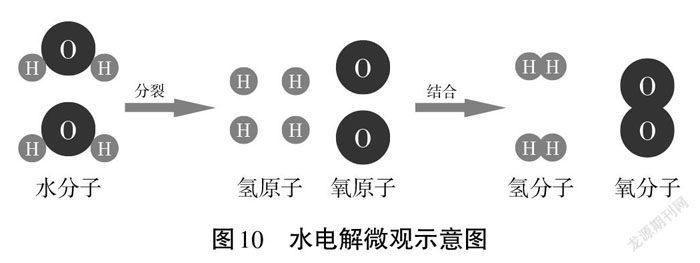
小组讨论。教师出示水分解变化的微观示意图(图10),播放动画视频。
生25:我们小组认为,水分解的过程中,水分子分裂成氢原子和氧原子,每两个氢原子结合成一个氢分子,每两个氧原子结合成一个氧分子。在分解前后,因为氢原子和氧原子的个数没有改变,所以,总质量不变。
师:是的。因为化学反应前后,原子的種类、数目、质量均不变,所以,化学反应前后元素的种类、质量不变,物质的总质量不变。
设计意图:核心素养与化学观念的形成是密不可分的,引导学生从微观层面粒子的种类、数目、质量不变推理到宏观物质反应前后的总质量不变,建立宏观与微观相结合的思想,能从微粒和变化的视角分析和解释质量守恒定律,形成微粒观,发展变化观。
质量守恒定律是初中化学的一个重要规律,其应用贯穿于整个化学学习过程。在此之前,学生已学习分子、原子、元素、化学式等知识,有了一定的微观想象能力。本节课教学中,笔者设计了多样化的学习任务,从学生熟悉的化学反应入手,进行分类和比较,并分层次进行定量实验和科学推理,进而从微观角度分析化学反应的实质,引导学生建构化学反应中“物质变化的定量关系”这一大概念。从定量的角度来认识物质间的化学变化是重要的科学思维方式,借助实验数据来分析问题,凸显了数据作为证据的有效性和充分性,由此可见,定量研究对于科学发展是非常重要的。
紧扣学习目标的话题设置,有条有理的实验设计,围绕问题解决的合作学习,小组间的自评和互评,促进学生自主学习和深度学习,增强了学生认识问题、解决问题的能力,发展科学思维能力;化学史料情境蕴含科学思维和科学研究方法,引导学生理性看待科学发展过程中的失误或局限性,通过实验验证科学家的重要结论,建立结论和证据之间的逻辑关系,有利于学生树立正确的科学价值观,最终达到学科育人的目的[3]。
参考文献
[1]叶立军,王思凯.学科育人指向的课堂教学特征及策略研究[J].教学与管理,2021(11):96-98.
[2]中华人民共和国教育部.义务教育化学课程标准(2011年版)[S].北京:北京师范大学出版社,2012.
[3]王琳.聚焦学科核心素养提升的初中化学教学探索[J].化学教育(中英文),2021,42(21):66-72.

