内镜黏膜下剥离术治疗早期胃癌患者术后出血的危险因素分析
何修玲,刘 燕
(济南市钢城区人民医院消化内科,山东济南 271104)
胃癌是发生于胃上皮的恶性肿瘤,发病率高,临床将仅出现在黏膜及黏膜下层的隆起型、浅表型、凹陷型的早期病变定义为早期胃癌。该疾病早期多无明显症状,部分患者可出现恶心呕吐、上腹部胀痛、反酸及嗳气等消化道症状。目前,临床治疗胃癌的方式有药物、手术、放疗、化疗等,内镜黏膜下剥离术(ESD)是早期胃癌的主流内镜治疗技术,具有方法简便、创伤小等特点,已在临床上较为广泛地应用,但该手术方式有较高的继发出血的风险,术后出血是其最常见的并发症,预防术后出血在医学界已有较高的关注度。临床报道显示,内镜下黏膜切除术(EMR)和ESD后出血发生率分别约为4%、7%[1]。本研究旨在探究ESD治疗早期胃癌患者术后出血的危险因素,并将研究结果作以下报道。
1 资料与方法
1.1 一般资料 选取济南市钢城区人民医院收治的200例早期胃癌患者,选例时间为2019年1月至2020年12月,进行回顾性分析。所有患者均进行ESD治疗,将手术过程中及结束时未出现活动性出血,在术后48 h观察期出现黑便、呕血、便血症状的患者分为术后出血组(10例),手术过程中及结束时未出现活动性出血,且在术后48 h观察期未出现黑便、呕血、便血症状的患者分为术后未出血组(190例),两组一般资料,具体见表1。本研究经济南市钢城区人民医院医学伦理委员会批准。诊断标准:参照《肿瘤临床诊疗指南》[2]中的关于早期胃癌的相关诊断标准。纳入标准:①满足上述诊断标准者;②胃镜检查、CT检查确诊者;③病理活检找到癌细胞者;④生命体征较为平稳者。排除标准:①凝血功能障碍者;②手术不耐受者;③术后使用抗凝或抗血小板药物者。
1.2 治疗方法 在胃镜(日本奥林巴斯公司,型号:GIF-H260)下以一次性黏膜切开刀(Dual Knife)头端于病灶边缘约0.5 cm处行间隔电凝标记,于标记点外侧黏膜下多点注射生理盐水;以Dual Knife沿标记点外侧切开黏膜,剥离病灶下方的黏膜下层,剥离过程中反复注射生理盐水。对于裸露于创面外的小血管,进行预防性止血处理;对于局部剥离较深或肌层有裂隙者使用金属夹封闭部分损伤肌层的创面。间隔10 min后再次观察创面,无活动性出血后退出内镜。所有患者术后给予抗感染治疗,并观察48 h。
1.3 观察指标 ①ESD治疗早期胃癌患者术后出血的单因素分析。对两组患者临床资料进行分析整理,包括年龄、性别、基础病史(高血压、高脂血症、心血管疾病)、肿瘤家族史、服药史(阿司匹林、氯吡格雷)、多发病变情况、主要病变大小、主要病变部位(胃底、贲门、胃体、胃角、胃窦)、是否长期使用抗凝药物。②对于单因素分析后差异有统计学意义的指标使用多因素非条件Logistic回归进行分析,筛选ESD治疗早期胃癌患者术后出血的危险因素。
1.4 统计学分析 应用SPSS 22.0统计软件进行数据分析,计量资料与计数资料分别以(±s)、[例(%)]表示,组间比较分别采用t、χ2检验;危险因素分析采用多因素非条件Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 ESD治疗早期胃癌患者术后出血的单因素分析 单因素分析结果显示,术后出血组中患有心血管疾病、服用氯吡格雷、具有多发病变情况、主要病变大小≥2 cm、主要病变部位在胃底-贲门、长期使用抗凝药物的患者占比均高于术后未出血组,术后出血组的年龄高于未出血组,差异均有统计学意义(均P<0.05),见表1。

表1 ESD治疗早期胃癌患者术后出血的单因素分析
2.2 ESD治疗早期胃癌患者术后出血的多因素非条件Logistic回归分析 以ESD治疗早期胃癌患者术后出血为因变量,将单因素分析中差异有统计学意义的指标作为自变量,纳入多因素非条件Logistic回归模型进行分析,结果显示,高龄、患有心血管疾病、服用氯吡格雷、具有多发病变情况、主要病变大小≥2 cm、主要病变部位在胃底-贲门、长期使用抗凝药物均为ESD治疗早期胃癌患者术后出血的危险因素,差异均有统计学意义(OR=2.217、1.665、3.328、2.426、4.007、2.250、2.277,均P<0.05),见表2。
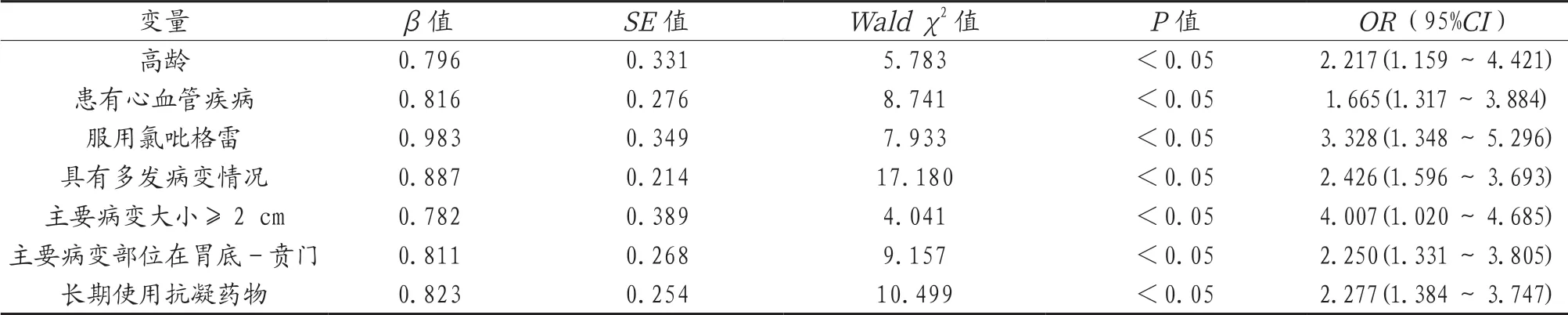
表2 ESD治疗早期胃癌患者术后出血的多因素非条件Logistic回归分析
3 讨论
胃癌的发病与感染、环境、饮食、遗传、免疫等因素有关,患有慢性胃病、饮食习惯不良、有胃癌家族史、幽门螺旋杆菌感染等人群是胃癌的高发人群,同时,随着年龄的升高,胃癌的发生率也逐渐提升[3]。术后出血作为ESD治疗早期胃癌的主要并发症,不仅延缓患者恢复速度,增加感染风险,还严重影响生活质量,导致负面情绪出现。
本研究单因素分析结果显示,术后出血组中患有心血管疾病、服用氯吡格雷、具有多发病变情况、主要病变大小≥2 cm、主要病变部位在胃底-贲门、长期使用抗凝药物的患者占比均高于术后未出血组,术后出血组的年龄高于未出血组。分析原因可能在于:患有心血管疾病的患者,术后血压常高于正常水平,故术后创面渗血或血管出血的概率更高,此外,患有心血管疾病的患者体外循环易出现紊乱,导致血流重新分布,同时体外循环紊乱会释放大量的炎性因子,致使胃肠黏膜微血管痉挛,黏膜屏障受损,引发出血。因此,应密切观察患者病情变化,严密监测其生命体征并给予针对性的治疗,叮嘱患者若自觉不适也应立即告知医护人员,及时对患者病情变化采取相关措施;同时,服用氯吡格雷等药物,会直接影响机体凝血功能,延长凝血时间,进而引发术后出血;有研究显示,氯吡格雷服用2 h后开始发挥抑制磷酸二酯酶受体介导的血小板聚集效果,同时在术前7 d持续服用氯吡格雷能显著增加术后患者出血和异体输血[4-5]。具有多发病变和主要病变大小≥2 cm的患者术中剥离面积会更大或深度更深,同时增加胃壁细胞碳酸酐酶活性,使得胃酸分泌增多,易出现胃黏膜糜烂坏死,增加了伤口愈合的难度,进而导致术后出血的概率更高[6-7]。因胃底-贲门属于胃上部分的2/3处,且胃部上2/3处黏膜下的血管直径较胃部的下1/3处的黏膜血管直径更大,数量也比胃部的下1/3黏膜处的血管数量较多,连接食管-胃的部位黏膜肌层较为薄弱,并且浆膜层对其的保护功能较弱,另在进行手术操作时,胃底部的视野具有局限性,多需在内镜下反转进行操作,手术难度随之增加,故当患者主要病变部位位于胃底-贲门时,术后出血的风险相对较高,术中在患者手术部位黏膜下注射可减少其出血情况的发生,故可通过术中多次进行黏膜下注射,达到黏膜被充分抬举的目的,出血的风险随之降低[8]。长期使用抗凝药物可使患者耐药性增强,同时对其凝血功能造成不良影响,术后出血的风险随之增加[9]。老年患者多耐受性差,合并多种基础疾病且免疫功能较为低下,老年患者血管弹性较差,在多上述种因素的影响下,手术风险及难度均较大,发生出血的几率也相对较高,本研究多因素非条件Logistic回归分析结果显示,高龄、患有心血管疾病、服用氯吡格雷、具有多发病变情况、主要病变大小≥2 cm、主要病变部位在胃底-贲门、长期使用抗凝药物均为ESD治疗早期胃癌患者术后出血的危险因素,表示上述因素均可造成患者在经ESD治疗后发生术后出血,和刘思等[10]研究结果相符。临床上应密切观察老年患者病情变化情况,应为患者做好术前准备,术中应严格遵守手术操作标准,及时处理出血血管,尽量缩短手术时间,降低老年患者术后出血的概率[11]。
综上所述,高龄、患有心血管疾病、服用氯吡格雷、具有多发病变情况、主要病变大小≥2 cm、主要病变部位在胃底-贲门、长期使用抗凝药物均为ESD治疗早期胃癌患者术后出血的危险因素,临床需重点关注术后出血的危险因素和发生情况,并据此制定急救预案,降低ESD治疗早期胃癌患者术后出血的发生率。本研究未对早期胃癌患者病变特征与ESD术后出血的关联进行探究,还需进一步的研究。

