不同HPLC-MS/MS法检测骨髓移植患者雷帕霉素血药浓度的相关性及意义*
王 磊,卢光泽,孙文利,刘红星,2,3△
1.河北燕达陆道培医院检验科,河北廊坊 065201;2.北京陆道培医院,北京100176;3.北京陆道培血液病研究院,北京 100176
雷帕霉素(RAP)作为大环内酯类免疫抑制剂,可减少骨髓移植后急性排斥反应和耐激素排斥反应的发生,亦可通过抑制mTOR激酶活性进而抑制肿瘤细胞生长,还兼具低肾脏毒性和糖代谢保护作用等优点[1-2]。而RAP血药浓度过低易发生急性排斥反应,浓度过高又可导致血小板减少、白细胞减少等不良反应[3]。1995年,YATSCOFF等[4]就指出应监测RAP血药浓度,且推荐采用色谱法作为RAP血药浓度检测的标准方法;2001年,MAHALATI等[5]又指出RAP血药浓度检测可选用高效液相色谱法(紫外检测器)或质谱法;2005年,STENTON等[6]推荐了RAP血药浓度监测频率和范围,进一步推动了RAP血药浓度检测在临床的广泛应用。目前,用于RAP血药浓度检测的高效液相色谱-串联质谱(HPLC-MS/MS)法有采用同系物子囊霉素作内标,亦有采用RAP稳定同位素(RAP-d3)作内标。本研究团队前期亦建立了以子囊霉素为内标的HPLC-MS/MS法用于RAP血药浓度测定[7]。由于RAP-d3色谱性能更接近于RAP,为更好地避免基质效应及仪器等对RAP血药浓度测定的影响,本研究特建立以同位素RAP-d3为内标的HPLC-MS/MS法,同时对两种内标的HPLC-MS/MS法检测结果进行分析,以确定哪种内标的HPLC-MS/MS法更适合用于骨髓移植患者的RAP血药浓度测定。
1 资料与方法
1.1一般资料 收集2020年10月至2021年2月送河北燕达陆道培医院药理室检测RAP血药浓度的骨髓移植患者新鲜剩余全血标本,共173份。要求血标本无黄疸、无乳糜、无溶血及凝血,剩余全血量不小于1 mL。
1.2仪器与试剂 采用4000 Q TRAP质谱仪(美国AB Sciex公司),岛津 20A型高效液相色谱仪(日本岛津公司),AnalystV1.5.2 工作站(美国 AB 公司),涡旋振荡器(其林贝尔),微量台式低温离心机(Thermo Fisher)。 RAP校准品和质控品为ClinCal®-Calibrator(RECIPE CHEMICALS+INSTRUMENTS GmbH)和ClinChek®-Control(RECIPE,CHEMICALS+INSTRUMENTS GmbH);RAP-d3(HPLC Grade,Toronto Research)。其余试剂及仪器详见本研究团队前期研究[7]。
1.3方法 分别采用内标为RAP-d3和子囊霉素的HPLC-MS/MS法同时对173份标本进行RAP血药浓度检测。RAP-d3为内标的HPLC-MS/MS法测定RAP血药浓度的参数:RAP-d3质子数/电荷数(m/z)为934.6>864.6,其余质谱参数、色谱系统参数及性能验证方法同以子囊霉素为内标的HPLC-MS/MS法[7]。残留结果验证需符合FDA方法学验证的指导原则[8-9]。根据STENTON等[6]在2005年推荐的RAP血药浓度监测范围,并结合河北燕达陆道培医院实际监测情况,把两种HPLC-MS/MS法检测RAP血药浓度结果分成<4、4~10、>10 ng/mL。
1.4统计学处理 使用SPSS 22.0 对两种方法检测173份标本RAP血药浓度的结果通过配对t检验进行差异分析,以P<0.05为差异有统计学意义;同时对两种方法检测结果进行相关性分析,并把两种方法检测结果分布情况绘制成山峦图,以观察其数据分布及对比两种HPLC-MS/MS法检测结果的一致性。
2 结 果
2.1以RAP-d3为内标的HPLC-MS/MS法性能验证结果 通过对3条标准曲线进行拟合,计算线性回归的相关系数(r)。方法确证曲线为Y=0.126X+0.064 3,r2=0.998 8,结果表明,RAP血药浓度在0~54.9 ng/mL线性关系良好。RAP出峰保留时间为1.73 min,内标RAP-d3保留时间为1.73 min,二者峰高比恒定,确定RAP-d3作为RAP的内标较为合适。同时亦表明,全血中的基质对RAP及内标RAP-d3的测定不产生干扰,专属性较好,内标归一化的基质因子在0.90~1.00,基质效应对最终结果影响较小。RAP日内CV为2.28%~2.89%,回收率为98.52%~104.61%;日间CV为2.37%~3.39%,回收率为97.04%~103.52%;二者CV均小于4%,回收率位于98%~105%,回收率高。稳定性实验所测得结果回收率为100%~110%,CV均小于5%。残留结果验证:空白标本的峰面积小于最低定量下限峰面积的20%,内标残留结果为0,符合FDA方法学验证的指导原则。
2.2差异分析 以子囊霉素为内标的HPLC-MS/MS法和以RAP-d3为内标的HPLC-MS/MS法检测173例骨髓移植患者RAP血药浓度结果,两种方法检测结果数据均符合正态分布,其均值分别为4.16 ng/mL和4.30 ng/mL,差异无统计学意义(t=2.127,P=0.35>0.05)。
2.3相关性分析 根据两种HPLC-MS/MS法检测结果绘制散点图,以子囊霉素为内标的HPLC-MS/MS法测定结果为自变量X,以RAP-d3为内标的HPLC-MS/MS法测定结果为函数Y,进行线性回归,回归方程为Y=0.932X+0.158,两种HPLC-MS/MS法检测结果相关性较好(r2=0.915)。见图1。
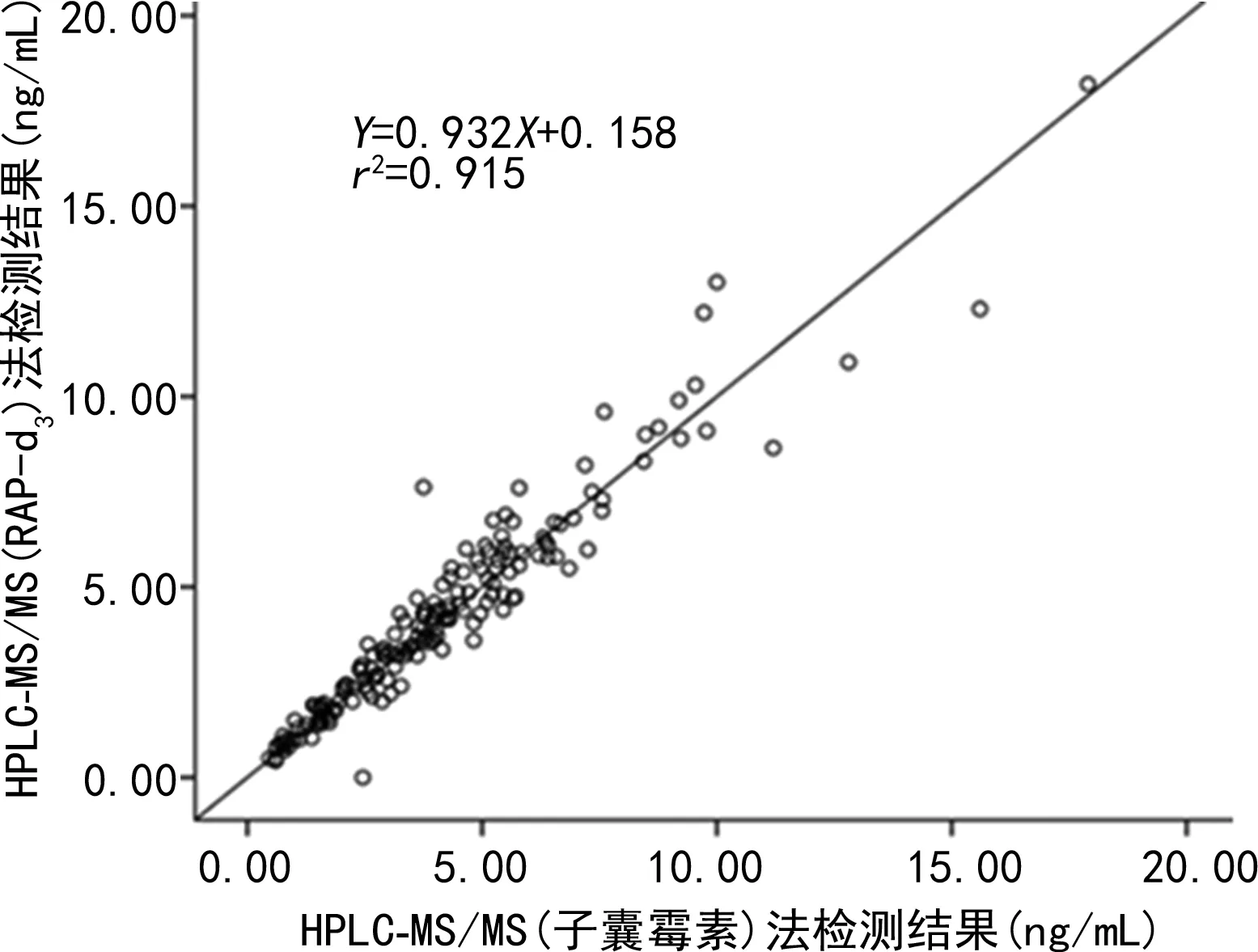
图1 两种HPLC-MS/MS法检测结果相关性分析
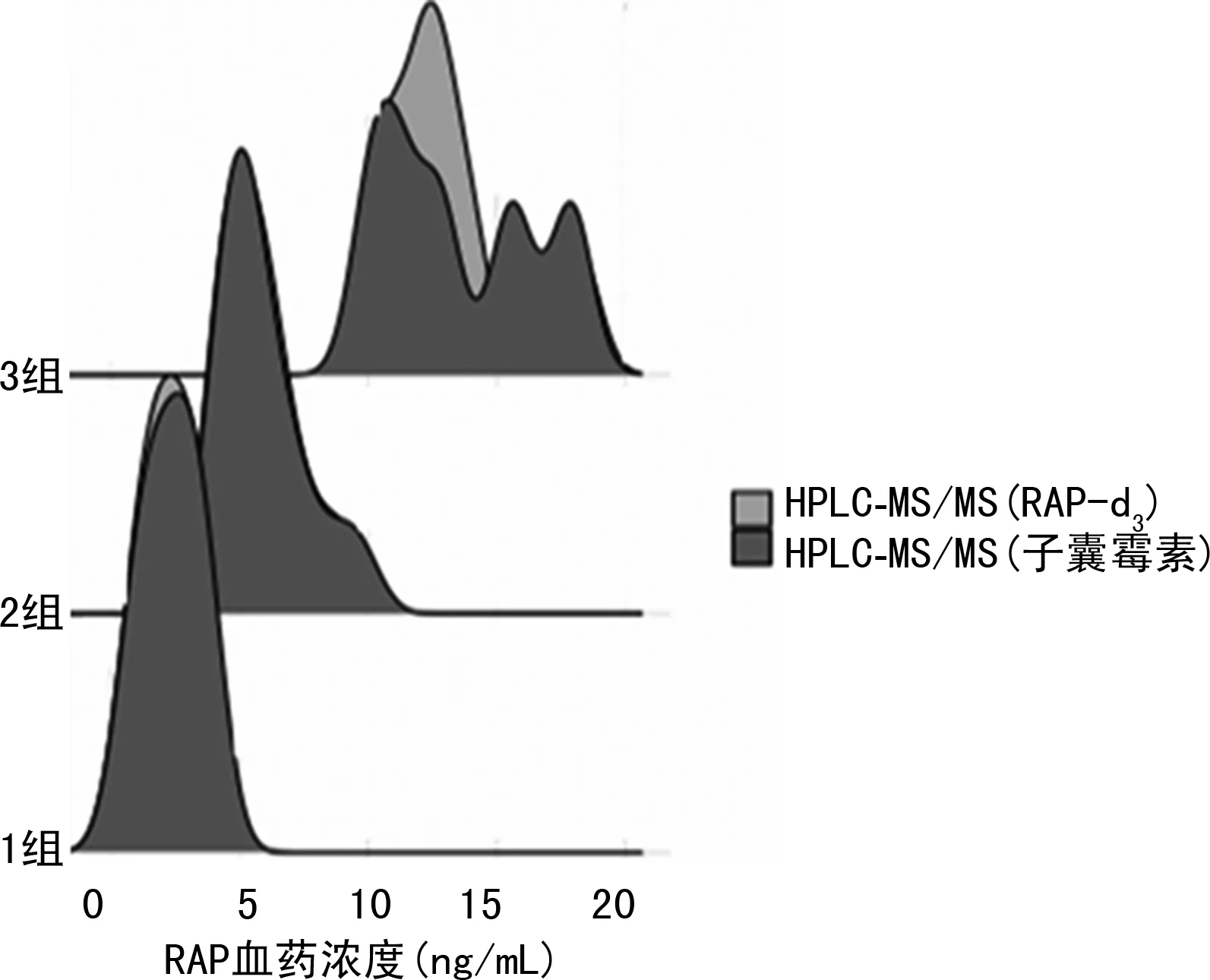
注:1组为<4 ng/mL;2组为4~10 ng/mL;3组为>10 ng/mL。
2.4一致性分析 HPLC-MS/MS(RAP-d3)方法检测RAP血药浓度,173份标本中,RAP血药浓度<4 ng/mL的占50.87%,4~10 ng/mL的占44.55%,>10 ng/mL的占4.58%。HPLC-MS/MS(子囊霉素)方法检测RAP血药浓度,173份标本中,RAP血药浓度<4 ng/mL的占54.91%,4~10 ng/mL的占42.20%,>10 ng/mL的占2.89%。两种HPLC-MS/MS法检测结果主要集中于<4 ng/mL和4~10 ng/mL两部分,两种检测方法这两部分结果基本重叠,一致性较好,而>10 ng/mL数据比较分散,一致性较差,说明两种方法在检测高RAP血药浓度时可能存在差异。见图2。
3 讨 论
骨髓移植作为可能根治恶性血液病的一种有效治疗手段,其移植后的移植物抗宿主病(GVHD)是影响移植物存活和患者生存质量的主要原因[10]。而RAP作为一种强效、低毒的免疫抑制剂,往往与环孢素或其他低效的免疫抑制剂联用于GVHD的预防和治疗[11]。但RAP像其他免疫抑制剂一样,具有治疗窗窄、个体差异大等特点,须在用药的过程中进行血药浓度监测,避免不良反应,提高移植成功率。
目前RAP血药浓度检测方法主要有色谱法和HPLC-MS/MS法,内标的选择多为子囊霉素和同位素RAP-d3,鲜见关于此两种不同内标对HPLC-MS/MS法检测结果影响的报道。本研究建立的以RAP-d3为内标的HPLC-MS/MS法特异性强,重现性好,能准确、灵敏、快速地检测骨髓移植患者全血RAP浓度。子囊霉素是一种RAP的乙基类似物,结构上与RAP相似[12];而RAP-d3拥有与RAP相同的物理化学性质,其离子化效率和分离度几乎一样,可以最大限度消除分析方法的误差。就两者理化结构和化学性质进行比较,稳定性同位素为理想内标首选,而我国2015版《中华人民共和国药典》对生物样品定量分析中使用同位素内标也有相关规定:当在生物分析方法中使用质谱检测时,推荐尽可能使用稳定同位素标记的内标[8]。稳定性同位素作为内标使用后,由于待测组分与内标是同一种物质,两者离子丰度比相同,误判率极小,可以进一步确证化合物,所以,当两种内标法所测结果不一致时,推荐以稳定同位素内标法所测结果为准。
根据国内RAP临床试验结果,建议RAP全血谷浓度术后0~3个月控制在5~10 ng/mL,术后4~6个月控制在3~8 ng/mL,而本次试验随机选取173份骨髓移植患者的全血中RAP浓度(RAP-d3为内标的HPLC-MS/MS法)≤10 ng/mL占95.42%,说明河北燕达陆道培医院对RAP浓度控制较为理想[13]。进一步对173份全血RAP血药浓度结果分析可看出,以RAP-d3为内标的HPLC-MS/MS法检测结果与以子囊霉素为内标的HPLC-MS/MS法检测结果相关性较好,结果差异小,但是对于RAP血药浓度>10 ng/mL的患者标本而言,两种方法一致性较差,可能存在差别。究其原因,可能跟子囊霉素为RAP的结构类似物,其物理化学性质与RAP存在细微差别,导致其色谱行为不一致有关;而RAP-d3作为RAP的同位素,其物理化学性质和色谱学行为与RAP一致性更好,受仪器状态和前处理环节影响更小,结果相对更可靠。在针对RAP血药浓度监测内标的选择上,本研究选择的为氘代内标,可能不如13C内标的检测效果,后期本研究团队会继续对氘代内标和13C内标的选择做进一步研究,以期为临床RAP血药浓度测定内标的选择提供参考,让检测结果更可靠。