大概念统摄下高三二轮专题复习课教学探讨
夏添
摘要:在高三二轮专题复习课教学中,以催化剂相关真实问题情景为载体,引导学生认识催化剂对化学反应(发生、过程、结果)的调控,抽提出学科大概念,进而促进学生对催化剂的结构化认识和思维的发展。
关键词:催化剂;专题复习;大概念;教学设计
文章编号:1008-0546(2022)01-0060-05中图分类号:G632.41文献标识码:B
doi:10.3969/j.issn.1008-0546.2022.01.015
催化剂的研究和开发,是现代化学工业的核心问题之一,高考中相关知识的考查也从简单概念判断转变为实验设计、数据分析、图像分析与绘制等综合考查[1],所涉及到的情景素材多来源于前沿学术期刊、工业生产实际,陌生度高、知识点分散、综合性强,学生解决起来常常感到较为困难。近几年,与催化剂教学相关研究主要体现在三个方面:①对催化剂相关迷思概念、认知困境的研究,如范晓凤,姜雪琴对催化剂认识中常见迷思概念进行了辨析[2];吴晗清,李豆豆对学生存在催化剂相关认知困境进行了实证研究,并提出针对性教学建议[1]。②以案例为主的化学教学尝试,如金雄鹰,毛杨林探讨了催化剂整合式教学复习[3];江合佩,刘炯明,郑玉海以“合成氨的反应历程分析”为例,提供了动力学催化剂反应机理专题复习的操作模式和教学案例[4]。③与催化剂相关实验研究,如豆真,高洪芳利用手持技术对不同催化剂对双氧水的催化作用进行了比较[5]。相关文献缺乏对催化剂所承载的学科大概念及对“化学反应条件调控化学反应”的结构化认识。为此,本文以大概念为统领,以催化剂相关真实问题情景为载体,就如何在高三二轮专题复习课教学中帮助学生完善知识结构,促进学生思维的发展,形成分析和解决相关问题的思路和方法展开探讨。
一、“从催化剂角度看化学反应的调控”相关知识分析
《普通高中化学课程标准(2017年版)》(以下简称新课标)[6]在化学反应的方向、限度和速率主题中对“化学反应的调控”的内容要求为:认识化学反应速率和化学平衡的综合调控在生产、生活和科学研究中的重要作用。知道催化剂可以改变反应历程,对调控化学反应速率具有重要意义。
从学科知识角度看,化学反应条件是影响化学反应的发生、过程(反应快慢、反应历程)及结果(反应产物、能量转化、反应程度等)的因素[7]。催化剂是重要的化学反应(外在)条件,其对化学反应的调控有着重要意义。催化剂通过参与反应改变化学反应历程;通过改变反应活化能来改变反应速率;催化剂不能改变化学反应的平衡常数,不能改变平衡的转化率。但在实际工业生产中,为提高生产效率,经常未平衡就进行后续反应,此时催化剂的使用能加快反应速率,提高单位时间内反应的转化率(产率);同时在给定条件下反应物之间如果同时发生多个反应,选择适当的催化剂能提高反应的选择性,从而提高目标产物的产率。
从教材看,催化剂相关知识跨越三个年级:人教版《化学》(九年级上)通过实验认识了MnO2是H2O2分解反应催化剂,并进而给出催化剂的概念;人教版《化学》必修第二册以探究实验的形式认识可以改变反应条件(浓度,温度,催化剂)来调控反应速率;人教版《化学》选择性必修1介绍了化学反应速率与活化能关系以及催化剂改变反应历程、降低反应活化能示意图。鉴于教材知识零散、浅显,而高考考题综合、深入的特点,基于新课标“重视以学科大概念为核心,使课程内容结构化”“教师在组织教学内容时应高度重视化学知识的结构化设计,充分认识知识结构化对于学生化学学科核心素养发展的重要性”[6]的要求,在高三二轮专题复习课中有必要从学科大概念的视角重新梳理相关内容(见图1),形成关注学生知识结构化、认识思路结构化的教学,进而促进学生核心素养的发展。
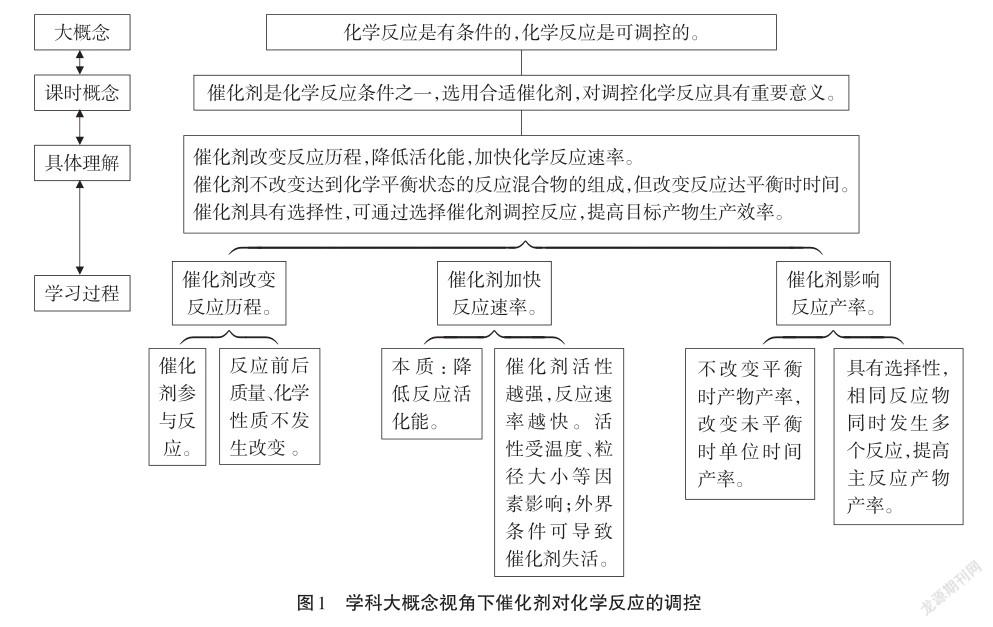
二、学情分析
在高三阶段,学生通过之前的学习,对催化剂知识有一定的了解,如:知道催化劑加快反应速率;催化剂反应前后质量和性质不发生变化;催化剂可降低反应活化能等;并能设计实验探究催化剂对化学反应速率的影响。
学生学习的困难主要在于:部分同学未形成催化剂参与反应的认识,对催化机理理解不清晰;大多数同学认为催化剂不能改变反应的产率,对催化剂能改变未平衡时单位时间产率,提高主反应产物产率不能理解。
三、大概念统摄下“从催化剂角度看化学反应的调控”教学实践
在高三二轮专题复习课中通过H2O2分解反应中系列真实问题的具体解决引导学生认识催化剂对化学反应(发生、过程、结果)的调控,抽提出“催化剂是化学反应条件之一,选用合适催化剂,对调控化学反应具有重要意义”的概念,再通过知识间纵向向上的联系,抽象概括出“化学反应是有条件的,化学反应是可调控的”的学科大概念,从而实现催化剂相关知识结构化改造;同时将抽象概括获得的大概念用于指导解决工业催化剂使用中的实际问题,实现知识纵向向下的联系,进而促进学生学科能力与学科思维的发展。教学过程中的学习任务及主要活动如下:
环节一:认识催化反应历程
【问题1】结合你所学的知识,分析H2O2和K2Cr2O7反应吗?若反应,请你预测可能出现的实验现象。
【学生活动1-1】学生依据已有氧化还原反应知识,推测H2O2和K2Cr2O7发生氧化还原反应,H2O2被氧化成O2,Cr2O72-被还原成Cr3+,溶液中有气泡产生,溶液颜色变为绿色。
【学生活动1-2】完成分组实验:分别向两支装有2 mL 5%的H2O2、2 mL蒸馏水的试管中加入等量0.1 mol/L K2Cr2O7溶液。学生观察到:试管1(H2O2溶液中加入K2Cr2O7溶液)中,溶液立即变为棕褐色,一段时间后,逐渐产生大量使带火星木条复燃的气体,溶液颜色慢慢变浅,6分钟后溶液颜色与试管2(蒸馏水中加入K2Cr2O7溶液)中颜色几乎一样(见图2)。
【问题2】分析K2Cr2O7在反应中的作用,谈谈你的判断理由。
【学生活动2-1】K2Cr2O7参与反应,加快了H2O2分解速率,在反应中做催化剂。
【追問】K2Cr2O7参与反应,是反应的反应物又是生成物,加快了反应速率,是否就能证明K2Cr2O7是催化剂?

【学生活动2-2】还需要检验K2Cr2O7反应前后质量和性质是否发生变化。试管1、2对比,溶液颜色几乎一样,说明两支试管中K2Cr2O7中浓度基本相同,质量基本不变;取少许试管1反应后溶液滴加入试管3(装有2 mL 5%的H2O2溶液),发现再次出现活动1-2中实验现象,推测K2Cr2O7反应前后性质未发生变化。
【展示】利用色度传感器分别测定一段时间试管1、2中溶液色度,结果见图3,进一步证明反应前后K2Cr2O7反应前后质量未发生变化。
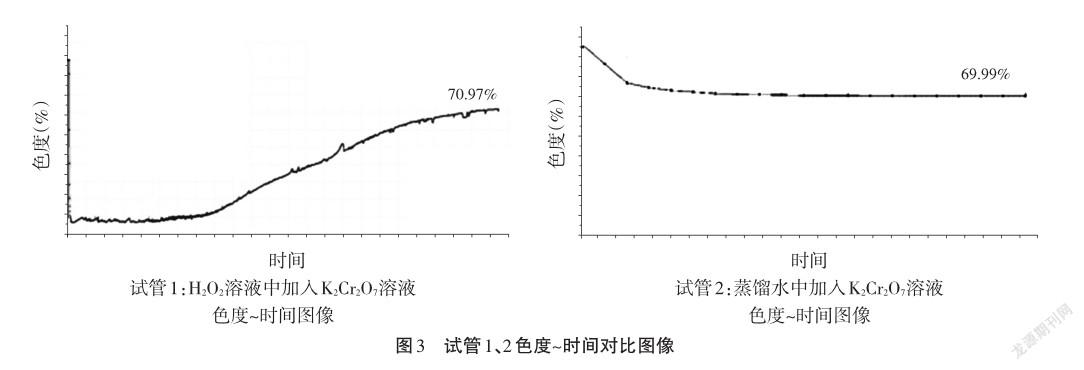
【追问】催化剂参与反应,加快反应速率,反应前后质量、性质均未发生变化,是否说明催化剂可以无限循环使用?
【学生活动2-3】阅读材料“催化剂的活性和失活”(见图4),获取知识:催化剂活性受温度、粒径大小等因素影响;外界条件可导致催化剂失活。


【学生活动4】学生绘制、展示“反应过程—能量”示意图。加入催化剂后,反应速率加快,降低反应活化能。反应i速率快于反应ii,图示中反应i活化能应低于反应ii。
【问题5】在整个催化过程中,哪些量发生变化,哪些没变?
【学生活动5】加入催化剂后,反应活化能减小,反应速率加快;反应物、生成物能量不发生改变,反应ΔH不变;反应达平衡后,K值不变,平衡转化率不变。
【展示】100℃时,在不同金属离子存在下,纯过氧化氢24小时的分解率见表1。
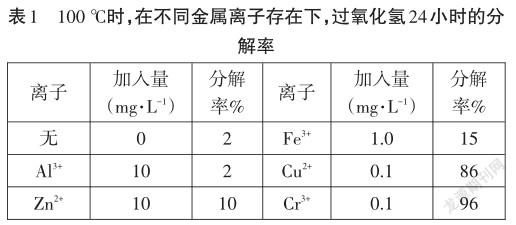
【问题6】分析图表数据,你能获得哪些信息?
【学生活动6-1】不是所有金属离子都可用作过氧化氢分解的催化剂;同一反应可以有多种催化剂;不同催化剂催化效果不同。
【追问】为何24小时过氧化氢分解率不同?
【学生活动6-2】24小时过氧化氢分解反应未达平衡,催化剂加快反应速率,可加大相同时间内反应物的转化率。不同催化剂催化效果不同,单位时间内反应物的转化率不同。
设计意图:认识催化剂通过降低活化能,加快反应速率;学会利用“能量-反应历程”示意图表征催化机理;深化催化剂与转化率之间关系的认识。
环节三:认识催化剂的选择性
【展示】甲苯和氯气可以发生如下反应:
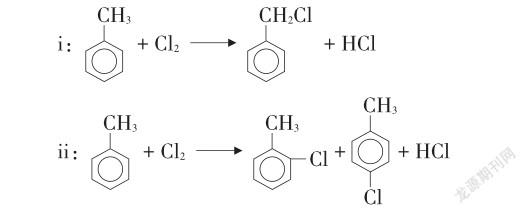
【问题7】加入FeCl3后,主要发生哪个反应?体现了催化剂的什么性质?
【学生活动7】加入FeCl3后,主要发生反应ii,体现了催化剂的选择性。
【过渡】在工业生产中,选用合适的催化剂可以提高反应的选择性,从而提高目标产物的产率。
【总结】构建大概念统摄下“从催化剂角度看化学反应调控”认识模型。(见图5)
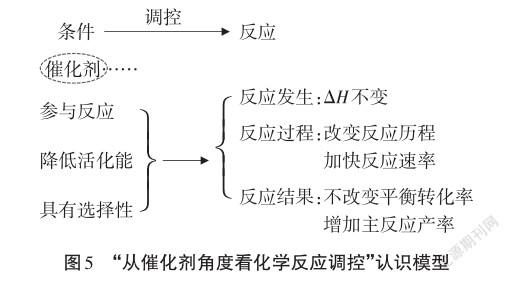
设计意图:认识催化剂的选择性,建构“从催化剂角度看化学反应调控”的认识模型。
环节四:为反应选催化剂

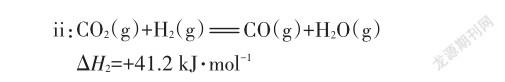
某实验控制压强一定,CO2和H2初始投料比一定,按一定流速通过不同催化剂,经过相同时间测得如下实验数据(见表2)(反应未达到平衡状态):
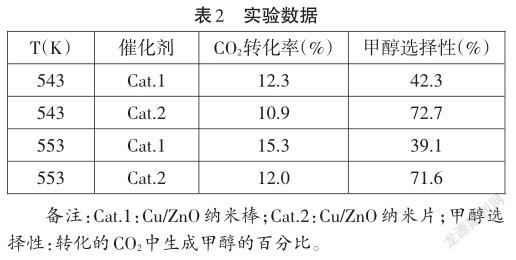
【问题8】请为反应选择合适的催化剂,谈谈你的理由。
【学生活动8】选择催化剂2,原因是相同温度、时间内CO2的转化率变化不大而甲醇的选择性明显增大。
【问题9】分析选用相同催化剂时,升高温度,CO2的实际转化率提高而甲醇的选择性降低的原因。
【学生活动9】升高温度,反应ⅰ、ⅱ速率都增大,但反应ⅱ速率增大得更多。
【演示实验】向装有2 mL 5 %的H2O2溶液的试管中加入0.1mol/L酸性K2Cr2O7溶液。
【学生活动10】观察到溶液中出现大量气泡,溶液颜色变绿,推测发生氧化还原反应,进一步认识到其它反应条件(浓度、温度、酸碱性)等也能够调控化学反应的发生、过程和结果。
设计意图:巩固提升,基于催化剂认识模型解决复杂真实问题,进一步认识反应条件对化学反应的调控。
四、结束语
本节课是大概念统摄下高三二轮专题复习课的一次尝试,在教学过程中并未对催化剂的相关知识进行面面俱到的复习,而是选取与大概念、概念建构相关的教学情景进行深入挖掘。整节课引导学生经历了从具体事实中抽提大概念和运用大概念指导、解决具体问题的过程,对高三学生知识结构的建构、思维的发展起到了一定的促进作用。随着高三学生认识的进一步深入,还可以继续针对“化学反应是有条件的,化学反应是可调控的”这一大概念背后的内容、认识角度进行拓展和丰富。
参考文献
[1]吴晗清,李豆豆.“催化剂”认知困境与教学对策[J].化学教学,2018(3):87-90.
[2]范晓凤,姜雪琴.消除错误前概念.重新认识催化剂[J].化学教与学,2019(7):11-15.
[3]金雄鹰,毛杨林.催化剂知识整合式教学的实践与思考[J].中学化学教学参考,2020,527(10):47-60.
[4]江合佩,刘炯明,郑玉海.“情境结构,模型认知”促进催化剂反应历程有效复习——以“合成氨的反应历程分析”为例[J].化学教学,2020(11):57-64.
[5]豆真,高洪芳.利用手持技术比较不同催化剂对双氧水的催化作用[J].中学化学教学参考,2018,480(10):64-65.
[6]中华人民共和国教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018:4,71,33.
[7]何彩霞.围绕学科知识结构与思维方法组织教学——以初三“化学反应条件”为例[J].化学教学,2017,(11):44-48.
[8]何法信.谈谈重铬酸钾与过氧化氢的反应[J].化学通报,1989(11):54-57.

