走向深度学习的大单元整体教学设计
——以“原电池到化学电源”为例
周 峰
(合肥一六八中学 安徽合肥 230601)
一、什么是“大单元教学”设计
核心素养导向下的大单元教学设计,要求教师建立好学科内容与核心素养之间的关系。目前课堂教学的最大问题是知识逻辑性太紧密,学生总是被动接受大量的符号和概念,体会不到真实、有趣、有用的感觉,导致不愿意学。所以伴随着大单元教学同步到来的新教材就做出了重大改变,在内容的编排上不仅仅以知识为主轴组成一个个单元,更多的要基于大主题、大情境和大概念来组成大单元。
大单元是一个课程单元,能满足不同学生素养发展的要求。大单元教学是以一个主题为研究对象,可以根据不同知识点之间的联系,整合多种教学形式和教学策略,让学生围绕有趣且有挑战性的真实情境,开展以化学实验为主的探究活动。通过若干节课的教学实践,学生经历一个相对完整的知识单元学习,促进深度学习发生。
原电池的单元教学流程框架为,结合实际问题,设计紧密联系的教学情境,构建电化学认知模型,引出问题并在问题驱动下推动教学。下面以高中化学选择性必修1第四章第一节“原电池”单元教学为例进行分析。
二、基于深度学习的单元整体教学设计案例
(一)教学背景分析
1.单元教学内容分析
原电池是高中化学的主干知识之一,可以看作是氧化还原反应的应用,同时又是化学反应中的一种能量转化形式,是一个实用性、综合性较强的知识点。教材通过探究实验抽离出原电池模型,利用模型解决实际问题,并不断增加学生思维的深度,提高学生解决实际问题的能力,最终实现对知识深层次的理解和运用。
2.单元教学学生情况分析
原电池的学习在高中阶段是一个循序渐进、层层推进的过程,在学习了单液原电池的构成及工作原理基本知识的基础上展开实验,围绕车用电源的发展创设情境,探究几种原电池的工作效率,帮助学生理解三种原电池装置在工作原理上的异同。
(二)单元教学目标设计
第一课时教学目标
(1)通过探究三种原电池装置工作效率的实验活动,在观察现象和讨论原因的过程中树立宏微结合的思想和变量控制的思维。
(2)在对原电池不断改进的探究过程中,学会化学反应条件控制和优化的一般思路,发展创新意识,落实核心素养。
(3)利用传感器将发生的过程可视化,实现从宏观到微观、从符号到曲线的四重表征。
第二课时教学目标
(1)运用建立的原电池模型,说明论证干电池、铅蓄电池、锂电池、燃料电池的工作原理。
(2)设计并制作简单的氢氧燃料电池,培养学生的科学探究与创新意识。
(3)在探究化学电源发展历史的过程中培养学生的科学态度,体现化学学科的社会责任。
(三)单元教学设计流程
情境、活动、问题三线贯穿单元教学,任务驱动教学发展。
(四)教学重难点
1.重点
(1)构建原电池理论模型。
(2)分析实际化学电源。
2.难点
(1)盐桥的作用。
(2)不同环境下燃料电池的电极方程式的书写。
(五)教学内容
(第一课时)【引入新课】请大家欣赏《绝命毒师》片段,运用所学知识设计电池使小车跑起来。
【学生活动】观看影片,思考情节中的化学知识,回忆化学必修第二册第六章实验活动6相关知识,复习原电池的定义、构成条件等。

图1 原电池驱动小车
【提出问题】你知道主人公描述的是什么装置吗?你能否设计出影片中的装置?这个装置产生电流需要满足哪些条件?
【点评,引导复习】(此部分重点引导学生回顾重点知识)
评价学生书面设计的简单原电池,引导学生复习原电池的工作原理。
【结合口诀】升者负极降者液,只要惰者为正极
【设计意图】结合学生“最近发展区”复习巩固必修2中所学的原电池知识,进一步明确原电池的装置构成、反应本质和工作原理,培养学生的总结归纳能力。回顾旧知,动手尝试,再现必修二简单原电池的学习情境,在此基础上展开深层次的实验探究。
【过渡】清楚了原理,学生自然产生了想为主人公设计原电池的愿望,遂让学生试着用提供的材料设计电池,来探究这两组原电池的放电情况。将学生分成两大组进行,一组利用万用表记录电流变化情况,另一组观察原电池驱动小车的运行情况。要求学生认真观察、记录现象,并解释现象。
【提问】刚刚大家在做实验的时候,有没有观察到电流大小有没有变化?电流表的指针是不是一直指着最大值?
【现象】一段时间后:锌片逐渐溶解,也有红色物质析出,铜片有红色物质析出,指针偏转角度变小,最后指向零。同时小车也不能持续运动。
【现象再分析】为什么负极的锌片也有红色物质析出?
【过渡】请大家思考上述电池是否具有实用性。
【引导学生提出设想】能否设计实验装置来阻止溶液中的铜离子在负极表面析出?
【讨论交流】负极不能与反应的电解液直接接触,只能用不与锌反应的溶液。
【引导学生提出方案】要是有一份充满了离子的溶液,能和两个烧杯连通,则就能同时向两边补充阴阳离子,维持两边的电中性。有没有这样一个“法宝”呢?
【实验材料】铜丝、电极电势测试仪(虹吸管沟通、琼脂盐桥、湿纸巾)
【分组实验】
四组学生分别用不同介质沟通内电路,观察记录电流情况。
【现象分析】
铜丝——有电流,不稳定。
虹吸管,盐桥,纸巾——能产生稳定的电流,但电流较小。
电流大小:湿纸巾>盐桥>虹吸管
【设计意图】通过学生的自主选择沟通介质,引导学生理解外电路(电子通路)和内电路(离子通路)的区别。并通过比较不同介质下电流的大小,引导学生探究增大电流的方法。
【分析原因】盐桥导致电池内阻变大,使得电流变小。
【解决方案】降低电池内阻,用离子交换膜分隔正负极,隔膜型原电池——化学电源雏形。
【过渡】通过一步步的探索,设计出了能够产生持续稳定大电流的原电池装置,也就是“隔膜型原电池”,使得氧化剂和还原剂近乎完全隔离,在不同的区域之间通过特定的装置实现了电子的定向转移,并使电流内阻减小,实现持续稳定大电流供电的愿景。
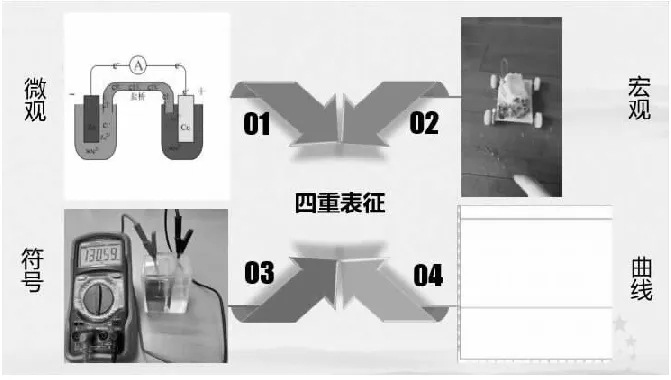
图2 原电池模型的四重表征
【设计意图】利用宏观上小车在隔膜型原电池的驱动下持续运动,万用表的稳定数字和电流传感器的平稳曲线,实现对隔膜原电池微观变化的“四重表征”。再通过“四重表征”融合,启发学生学习构建思维模型,促进学科思维的形成与发展,从中发展解决相关问题的化学学科核心素养。
【课堂小结】
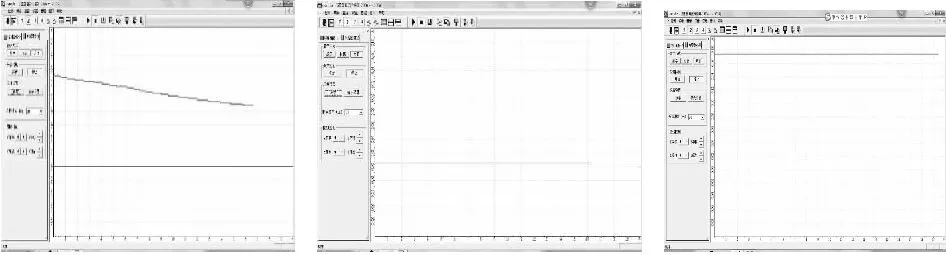
图3 数字传感器表征不同原电池的电流大小
单液原电池:电流不稳定,衰减较快。
双液原电池:电流稳定,但电流较小。
隔膜原电池:电流大且稳定
【作业拓展】化学兴趣小组设计不同的原电池模型,探究模型小车的驱动能力,比比看谁的小车跑得又快又远。
(第二课时)【新课引入】以合肥国轩高科和蔚来汽车的磷酸铁锂电池拆解视频引入新课。
介绍常见的车用电源,玩具车——干电池,电动自行车——铅蓄电池,电动汽车——锂电池、氢氧燃料电池。
【引出衡量电池的几个指标】
1.能量的大小。
2.输出功率的大小,即功率的大小。
3.电池的存储时间的长短。
4.电池的使用安全和环保情况。
【设计意图】通过衡量电池性能的指标,引导学生根据电池的发展过程,不断探究电池性能的优化和提升方向,体现化学的学科价值和社会责任。
【应用模型】
任务一:分析碱性锌锰电池的优点
从电极材料、电解液角度分析区别,总结优点。
普通锌锰电池 碱性锌锰电池
电解液:糊状氯化铵 湿氢氧化钾
(离子导电性增强) (固体接触面增大)
负极:锌筒 锌粉
优点:能量储存时间有所提高,不易泄露。
任务二:分析铅蓄电池和磷酸铁锂电池的正负极和充放电方程式
了解二次电池的工作原理,利用原电池模型,分析实际电源的四要素,判断正负极材料,书写电极方程式。
学生对燃料电池比较陌生,可以利用氢燃料电池演示器进行实验。
【学生实验】组织实验装置,观察实验,记录现象。

图4 氢燃料电池演示器(质子交换膜燃料电池)
【设计意图】通过观察电流表指针偏转情况,实际感受化学能与电能、电能与机械能之间的转化。引导学生进一步探究燃料电池的工作原理。
任务三:分析燃料电池的原电池四要素

图5 氢燃料电池模型
【分析总结】燃料电池的优点:能量转化率高,无污染。
【学生练习】分析燃料电池原理工作,重点强调不同电解质环境下电极方程式的书写
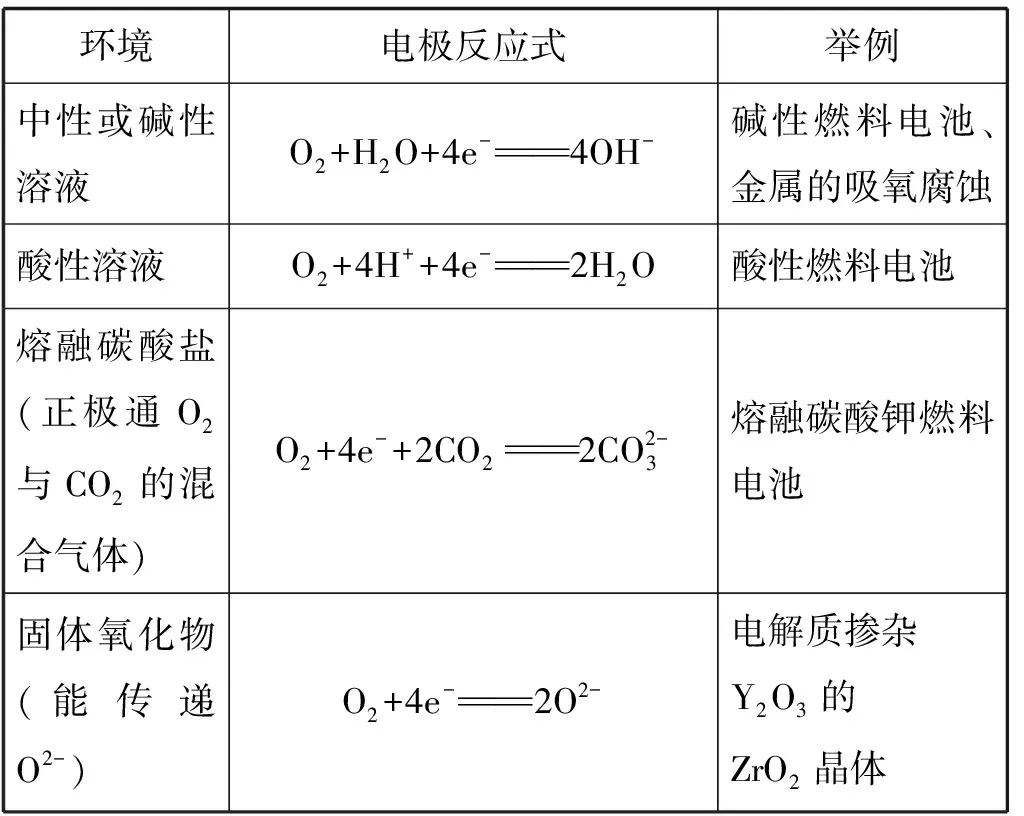
环境电极反应式举例中性或碱性溶液O2+H2O+4e- 4OH-碱性燃料电池、金属的吸氧腐蚀酸性溶液O2+4H++4e- 2H2O酸性燃料电池熔融碳酸盐(正极通O2与CO2的混合气体)O2+4e-+2CO2 2CO2-3熔融碳酸钾燃料电池固体氧化物(能传递O2-)O2+4e- 2O2-电解质掺杂Y2O3的ZrO2晶体
【设计意图】掌握不同环境下电极方程式的书写,是本节课的重点内容。利用燃料电池总反应式减去正极反应式即可得到负极反应式,培养学生证据推理和模型认知的核心素养。
【查阅资料】石墨烯材料在电池中的应用。
强调新材料在新电池中的应用,通过改变膜的结构,增加离子通过性,改变充电方式,提高充电速度,增大电池比能量,提高电池储量。
【拓展提升】展示形形色色的化学电源。
结合新冠肺炎病毒——病毒电池
利用仿生技术——生物电池
南开大学陈军教授为应对我国锂资源储量不足的问题,研发了钾电池、钠电池,确立我国在电池研发上的领先地位。
【社会责任】
合肥作为新能源汽车之都,随着高性能电池的日益发展,一定可以制造出更多更好的新能源汽车,提升大家的驾乘体验。
【设计意图】结合新能源汽车这一热点情境,引发学生的学习兴趣;通过电池的发展促进我国在新能源汽车领域的弯道超越,增强学生的民族自豪感和对家乡的认同感,体现化学学科的社会责任。
【作业拓展】上网查阅资料,了解国内外最新的电池研究进展和新能源汽车的发展方向。
三、单元整体教学反思
本单元课程是提升展示课,在学生已有认知的基础上,设定学习目标,拓展相关内容,达到深度学习的目的。本单元的教学是以小汽车的驱动电池的发展过程为情境,串联起本单元的两课时内容:第一课时层层推进,逐步构建原电池模型,通过宏观现象的描述、微观变化的探析、数字符号的读取、曲线图像的变化,来实现原电池原理的四重表征;第二课时运用原电池的模型,分析各类车用电源的原理,解决车用电源存在的各种问题。整个单元教学在探究几种电池工作效率的科学活动中,很好地发展了学生的模型认知和证据推理核心素养;在探寻车用电源发展历史的过程中,培养了学生的社会责任和科学态度。

