伏立康唑不同途径给药抗肺结核并发肺曲霉菌病的效果分析
闫莎莎
(河南省郑州市第六人民医院胸膜炎科 郑州 450015)
肺结核(Tuberculosis,TB)是器官结核病的常见类型,占结核病的80%~90%,可损伤机体免疫功能,易导致真菌感染,诱发肺曲霉菌病(Pulmonary Aspergillosis,PA)[1~2]。相关研究显示,TB并发PA易造成误诊,增加治疗难度,有较高的病死率[3]。因此,确诊后应及时采取有效的干预措施。伏立康唑为广谱类真菌抗生素,抗真菌活性较强,尤其对曲霉菌效果更好。伏立康唑的常见的给药途径为口服,具有操作简单、起效迅速等优势,但肠道代谢会造成药效流失,影响治疗效果[4]。随着临床研究的不断深入,序贯疗法在临床的应用逐渐广泛,能优化治疗机制,提高疗效。基于此,本研究选取126例TB合并PA患者为研究对象,分组探讨伏立康唑序贯疗法的临床优势。现报道如下:
1 资料与方法
1.1 基线资料 本研究经医院医学伦理委员会审核批准(批号:2019-003-007)。选取2019年7月至2022年2月收治的126例TB并发PA患者为研究对象。结合X线影像检查、结核菌素皮肤试验(TST)、临床症状,符合肺结核基层诊疗指南(实践版·2018)[5]中TB相关诊断。X线:呈现片状、结节或钙化阴影,密度不均匀;TST:注射结核菌纯蛋白衍生物,皮肤硬结直径≥5 mm为阳性;临床症状:结核中毒症状(体质量减轻、盗汗、食欲不振、乏力、低热等),咳痰、咳嗽>2周或咳血;符合2016美国感染病学会(IDSA)临床实践指南更新版(曲霉病的诊断和管理)[6]中PA相关诊断,并经支气管镜、痰液培养确诊。纳入标准:年龄23~50岁;患者均初次感染曲霉菌;对研究相关药物无过敏;患者无认知功能异常或精神疾病,签署知情同意书。排除标准:心、肝、肾功能严重障碍者;恶性肿瘤确诊者;其他病原菌引起的肺部感染者;妊娠或哺乳期女性;近期服用免疫抑制剂者。采用随机法进行分组。两组基线资料、对比、无显著差异(P>0.05)。见表1。
表1 两组基线资料比较()
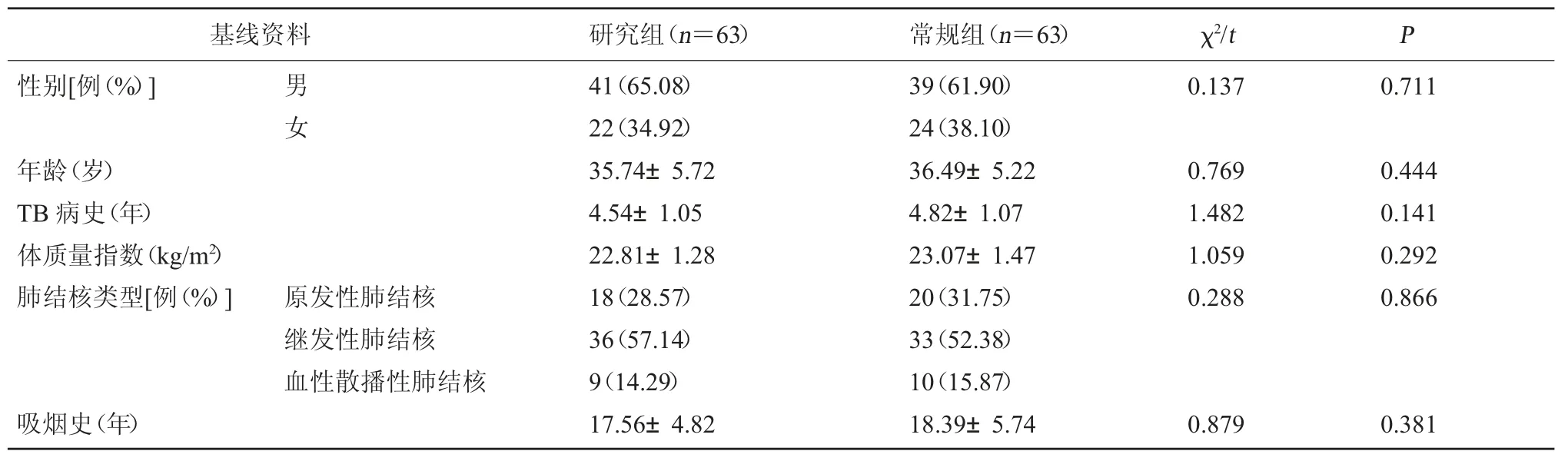
表1 两组基线资料比较()
基线资料 研究组(n=63) 常规组(n=63) χ2/t P性别[例(%)]年龄(岁)TB病史(年)体质量指数(kg/m2)肺结核类型[例(%)]吸烟史(年)男女原发性肺结核继发性肺结核血性散播性肺结核41(65.08)22(34.92)35.74±5.72 4.54±1.05 22.81±1.28 18(28.57)36(57.14)9(14.29)17.56±4.82 39(61.90)24(38.10)36.49±5.22 4.82±1.07 23.07±1.47 20(31.75)33(52.38)10(15.87)18.39±5.74 0.137 0.769 1.482 1.059 0.288 0.879 0.711 0.444 0.141 0.292 0.866 0.381
1.2 治疗方法 两组均给予对症治疗,包括止咳、化痰、营养支持、抗菌等。在此基础上,常规组给予伏立康唑片(注册证号H20150052)口服,200 mg/次,2次/d。研究组给予伏立康唑序贯疗法:静脉滴注注射用伏立康唑(国药准字H20058962),初始剂量6 mg/kg,2次/d,次日开始剂量为4 mg/kg,2次/d,治疗2周后改为口服伏立康唑片,用法用量同常规组。治疗期间,医师需根据患者病情调整用药剂量。随访2个月。
1.3 观察指标 (1)临床疗效。显效,治疗后临床症状及体征消失或基本消失,实验室、影像检查均显示正常,TST显示皮肤硬结直径<5 mm;有效,治疗后临床症状及体征较治疗前减轻,影像检查阴影病灶减小,实验室结果轻微异常;无效,未达上述标准或病情较治疗前加重。治疗总有效率=(显效例数+有效例数)/总例数×100%。(2)炎症介质。抽取患者5 ml静脉血,室温静置30 min,采用全自动血型分析仪IH-1000(生产厂家:伯乐公司,规格:IH-1000,批准文号:20163222578)对3 ml静脉血进行离心操作,取上层血清-70℃冷藏待测。采用酶联免疫法(ELISA)测定血清肿瘤坏死因子-α(TNF-α)、白细胞介素-8(IL-8)、C反应蛋白(CRP)。试剂盒购于北京北方生物技术研究所有限公司。余下2 ml静脉血给予抗凝干预,采用全自动血沉仪(生产厂家:ALIFAX公司,规格:Roller 20,批准文号:20162221113),通过魏氏法测定红细胞沉降低率(ESR)。(3)免疫功能。采用免疫比浊法测定血清免疫球蛋白IgA、IgM、IgG水平。试剂盒购于四川迈克生物科技股份有限公司。(4)肺功能:采用肺功能测试系统(生产厂家:德国Vaire,规格:MasterScreen SeS,批准文号:20152070346)测定治疗前后肺动态顺应性(Cdyn)、响应频率(Fres)、气道阻力(RAW)、气道峰压(PIP)。(5)不良反应发生情况。记录两组呕吐恶心、肝功能异常、视力障碍、精神兴奋等不良反应发生情况。
1.4 统计学分析 采用SPSS22.0统计学软件分析数据,计数资料用%描述、行χ2检验;计量资料用()描述,行t检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较 研究组治疗总有效率(92.06%)高于常规组(76.19%)(P<0.05)。见表2。
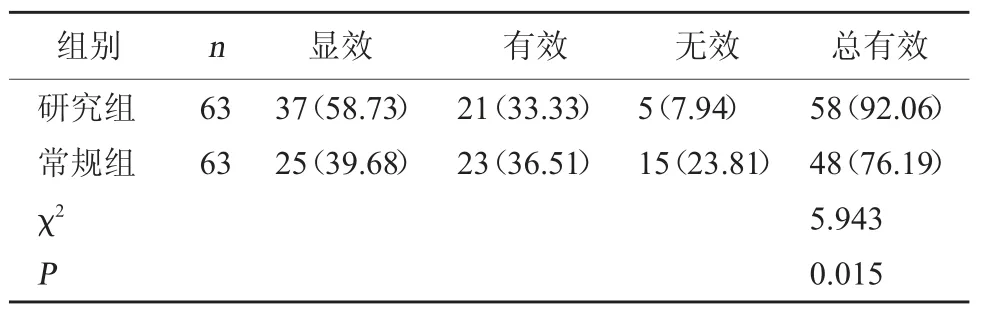
表2 两组临床疗效比较[例(%)]
2.2 两组炎症介质水平比较 治疗前,两组TNF-α、IL-8、CRP、ESR水平比较无显著差异(P>0.05);治疗后,两组TNF-α、IL-8、CRP、ESR水平均较治疗前明显下降,且研究组低于常规组(P<0.05)。见表3。
表3 两组炎症介质水平比较()
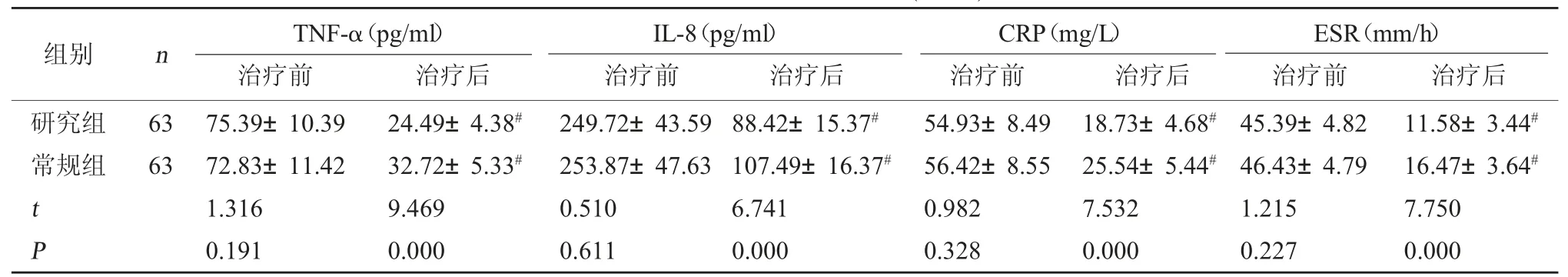
表3 两组炎症介质水平比较()
注:与本组治疗前比较,#P<0.05。
ESR(mm/h)治疗前 治疗后研究组常规组组别 n TNF-α(pg/ml)治疗前 治疗后IL-8(pg/ml)治疗前 治疗后CRP(mg/L)治疗前 治疗后63 63 t P 75.39±10.39 72.83±11.42 1.316 0.191 24.49±4.38#32.72±5.33#9.469 0.000 249.72±43.59 253.87±47.63 0.510 0.611 88.42±15.37#107.49±16.37#6.741 0.000 54.93±8.49 56.42±8.55 0.982 0.328 18.73±4.68#25.54±5.44#7.532 0.000 45.39±4.82 46.43±4.79 1.215 0.227 11.58±3.44#16.47±3.64#7.750 0.000
2.3 两组免疫功能比较 治疗前两组IgA、IgM、IgG水平比较无显著差异(P>0.05);治疗后,两组IgA、IgM、IgG水平均较治疗前升高,且研究组高于常规组(P<0.05)。见表4。
表4 两组免疫功能比较(g/L,)
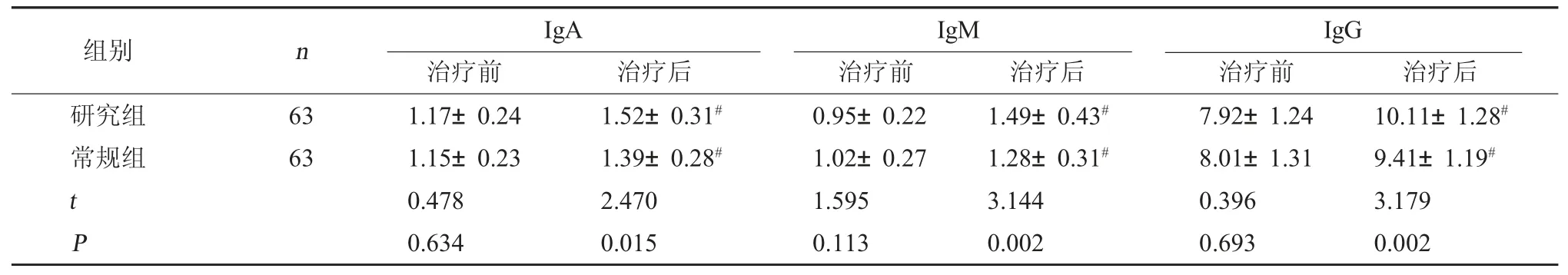
表4 两组免疫功能比较(g/L,)
注:与本组治疗前比较,#P<0.05。
IgG治疗前 治疗后研究组常规组组别 n IgA治疗前 治疗后IgM治疗前 治疗后63 63 t P 1.17±0.24 1.15±0.23 0.478 0.634 1.52±0.31#1.39±0.28#2.470 0.015 0.95±0.22 1.02±0.27 1.595 0.113 1.49±0.43#1.28±0.31#3.144 0.002 7.92±1.24 8.01±1.31 0.396 0.693 10.11±1.28#9.41±1.19#3.179 0.002
2.4 两组肺功能比较 治疗前,两组Cdyn、Fres、RAW、PIP比较,差异无统计学意义(P>0.05);治疗后,两组Cdyn较治疗前升高,Fres、RAW、PIP较治疗前下降,且研究组Cdyn高于常规组,Fres、RAW、PIP低于常规组,差异有统计学意义(P<0.05)。见表5。
表5 两组肺功能指标比较()
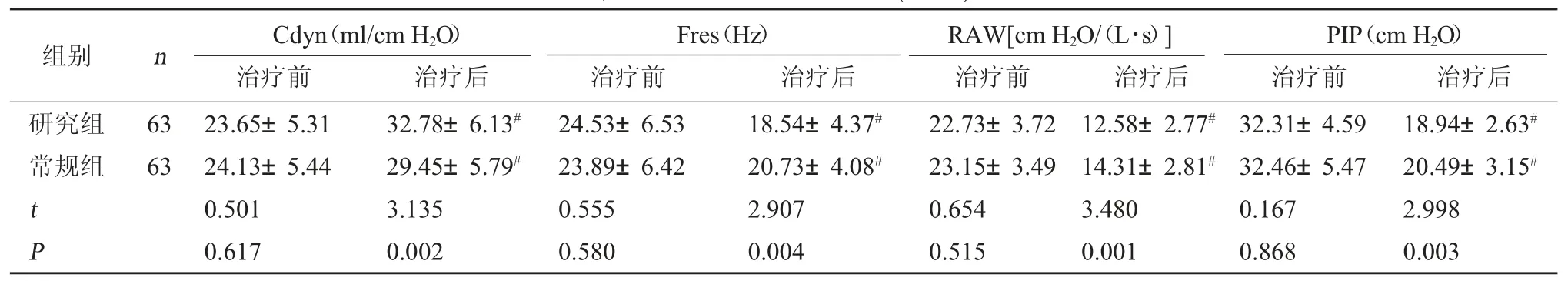
表5 两组肺功能指标比较()
注:与本组治疗前比较,#P<0.05。
PIP(cm H2O)治疗前 治疗后研究组常规组组别 n Cdyn(ml/cm H2O)治疗前 治疗后Fres(Hz)治疗前 治疗后RAW[cm H2O/(L·s)]治疗前 治疗后63 63 t P 23.65±5.31 24.13±5.44 0.501 0.617 32.78±6.13#29.45±5.79#3.135 0.002 24.53±6.53 23.89±6.42 0.555 0.580 18.54±4.37#20.73±4.08#2.907 0.004 22.73±3.72 23.15±3.49 0.654 0.515 12.58±2.77#14.31±2.81#3.480 0.001 32.31±4.59 32.46±5.47 0.167 0.868 18.94±2.63#20.49±3.15#2.998 0.003
2.5 两组不良反应发生情况比较 研究组不良反应发生率与常规组比较无显著性差异(P>0.05)。见表6。
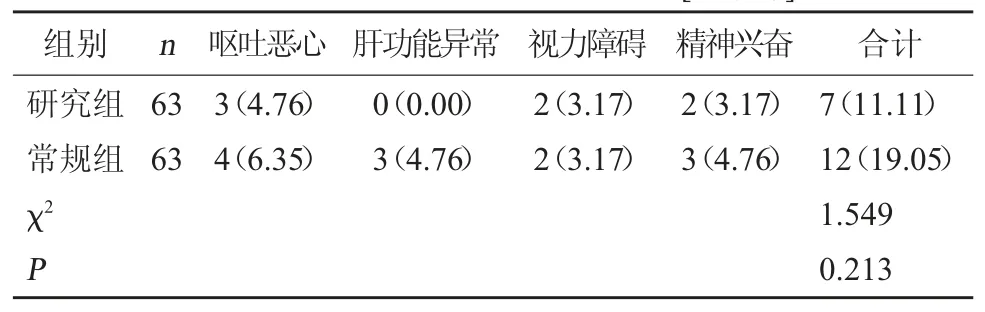
表6 两组不良反应发生情况比较[例(%)]
3 讨论
TB是常见的呼吸道传染性疾病,以咯血、呼吸困难、神疲乏力等为主要表现,其迁延难愈、治疗难度较大,可对患者身体健康及生活质量造成严重影响[7]。TB患者免疫功能下降,易诱发真菌感染,且以曲霉菌感染居多,会导致肺组织损伤和肺功能衰竭,严重可致患者死亡,相关研究显示[8],PA患者病死率超过80%。伏立康唑为现阶段临床治疗PA患者常用的抗真菌药物,通过减少麦角固醇生物合成,抑制多种曲霉菌,同时改善病原菌细胞膜通透性,促进病原菌凋亡[9~10]。然而临床关于伏立康唑的使用方式仍然存在一定争议。
有研究显示,侵袭性肺曲霉病患者采用伏立康唑序贯疗法能提高安全性,有效率为96.97%[11]。姚奇等[12]研采用伏立康唑序贯疗法治疗肺曲霉病临床疗效为92.70%。本研究中,治疗后研究组总有效率为92.06%,与上述研究基本一致,提示伏立康唑序贯疗法在治疗PA方面具有显著优势。序贯疗法中,通过静脉给药能维持较高的血药浓度,且半衰期较长;而口服药物代谢较速度快,起效迅速,两种方式联合能优化抗菌机制,进而提高治疗效果。在安全性方面,两组不良反应发生率比较无显著差异,可能与样本量较小有关,但研究组略低于常规组。提示伏立康唑序贯疗法具有一定的安全性。
曲霉菌感染会导致机体代谢功能失调,使炎症介质TNF-α、CRP、IL-8、ESR异常表达,激发炎症反应,且炎症介质表达程度与感染程度密切相关。炎症反应损伤正常组织,会导致免疫功能发生变化,机体免疫功能不仅与机体感染程度密切相关,且能反映患者预后[13]。免疫球蛋白是免疫功能重要组分,在机体免疫监视、免疫防御、免疫自稳中均能发挥重要作用[14]。其中IgA通过介导改善细胞黏膜吞噬功能;IgG通过血管间隙改善机体免疫功能;IgM能激活补体,可介导补体促进吞噬作用。本研究显示,治疗后,研究组炎症介质水平、免疫功能均优于常规组,研究组Cdyn高于常规组,Fres、RAW、PIP低于常规组。提示伏立康唑序贯疗法能有效降低机体炎症反应程度,减轻正常组织损伤,改善患者免疫功能,进而促进肺功能的改善。
综上所述,TB并发PA患者采用伏立康唑序贯疗法能有效控制炎症反应,改善患者机体免疫功能及肺功能,提高临床疗效,且有较高的安全性。

