地西他滨联合小剂量IA方案治疗老年急性髓系白血病患者的临床疗效
齐海燕 王文松 蓝建平
急性髓系白血病是造血干细胞克隆性恶性血液肿瘤,治愈率低,病死率高,是严重威胁人类健康的恶性疾病。随着人口老龄化、环境污染加重,年龄≥60岁的急性髓系白血病发生率逐年上升。有数据显示,老年白血病的发病中位年龄接近70岁[1-2],5年生存率仅5%~10%。老年白血病耐药率高、染色体核型复杂,常由骨髓增生异常综合征、骨髓增殖性肿瘤转变而来,发病缓,症状不典型,诊断时多已存在多脏器功能衰退以及免疫功能差等特点,总体治疗效果差,治疗方案选择受限,对化疗的耐受性差,化疗相关病死率也较高。因此,针对老年白血病患者,临床需采取科学有效的治疗方案,在给药剂量上作出合理的调整,以减轻患者不良反应,改善预后。IA方案(去甲氧柔红霉素+阿糖胞苷)是目前国际上公认的治疗急性髓系白血病疗效较好的标准诱导方案。去甲氧柔红霉素是柔红霉素的衍生物,结构上的改变使得肿瘤细胞对药物的摄取增加,提高细胞毒作用,因而具有疗效高,心脏毒性低的特点。DNA甲基化异常在急性髓系白血病的发生、发展中起重要的作用[3]。去甲基化药物地西他滨是一种特异性的DNA甲基化转移酶抑制剂,可抑制肿瘤细胞的增殖,高浓度时具有细胞毒作用,低浓度时具有去甲基化作用。基于此,本研究探讨地西他滨联合小剂量IA方案治疗老年急性髓系白血病患者的临床疗效,现报道如下。
1 对象和方法
1.1 对象 选取2016年10月至2020年7月浙江省人民医院收治的老年急性髓系白血病患者72例。根据骨髓涂片细胞分类计数、骨髓流式免疫分型分析、高分辨染色体核型分析等实验室检查结果明确诊断为急性髓系白血病患者(急性早幼粒细胞白血病除外)。其中38例患者采用地西他滨联合小剂量IA方案治疗,为观察组;另34例采用小剂量IA方案治疗,为对照组。两组患者性别、年龄、美国东部肿瘤协作组(Eastern Co-operative Oncology Group,ECOG)体能状况评分、骨髓涂片中原始细胞比例、细胞遗传学和分子遗传学异常进行的预后分层等基线资料比较差异均无统计学意义(均P>0.05),见表 1。
1.2 方法 对照组患者采用IA方案(去甲氧柔红霉素+阿糖胞苷)治疗,去甲氧柔红霉素[商品名:善唯达,辉瑞制药(无锡)有限公司,药品注册证号:H20150313]静脉滴注 8 mg/m2,d1~3;阿糖胞苷(商品名:赛德萨,辉瑞制药有限公司,药品注册证号:H20160403)静脉滴注75 mg 1次/12 h,d1~7。观察组患者采用地西他滨联合小剂量IA方案治疗。地西他滨(正大天晴药业集团股份有限公司,国药准字:H20120067)静脉滴注 10 mg d1~5;去甲氧柔红霉素静脉滴注5 mg/m2,d6~8;阿糖胞苷静脉滴注75 mg 1 次/12 h,d6~12。
两组患者在治疗期间,依据病情及耐受情况,予以止吐、水化、碱化等对症处理。无法进食患者加强静脉高营养、维持水电解质及酸碱平衡等支持治疗,积极预防化疗不良反应和潜在感染风险。患者接受1个疗程治疗后如完全缓解,继续予该方案治疗4~6个疗程巩固治疗;若获得部分缓解,继续使用原方案1个疗程诱导治疗,评估患者缓解情况;若患者未得到缓解,调整治疗方案或参与临床试验。
1.3 观察指标 观察并比较两组患者治疗效果和不良反应发生情况。完全缓解:(1)临床无白血病细胞浸润所致的症状和体征,生活正常或接近正常;(2)Hb≥100 g/L(男)或≥90 g/L(女及儿童),中性粒细胞绝对值≥1.5×109/L,PLT≥100×109/L,外周血白细胞分类中无白血病细胞;(3)骨髓原粒细胞(Ⅰ型+Ⅱ型)比例<5%。部分缓解:骨髓原粒细胞(Ⅰ型+Ⅱ型)比例5%~20%,临床或血象中一项未达到标准。未缓解:骨髓原粒细胞(Ⅰ型+Ⅱ型)比例>20%、血象、症状、体征未达到标准。总有效率=(完全缓解+部分缓解)/总例数×100%。不良反应包括骨髓抑制、感染、恶心、呕吐、肝肾功能损害等。
1.4 随访 随访时间截至2020年11月16日。总生存期定义为从患者接受化疗开始至因任何原因死亡之日或最后随访的时间。无进展生存期为接受化疗到疾病进展或任何原因治疗失败死亡的时间。

2 结果
2.1 两组患者治疗效果比较 治疗1个疗程后,观察组患者治疗总有效率高于对照组(P<0.05);治疗4~6个疗程后,观察组患者治疗总有效率亦高于对照组(P<0.05),见表 2。
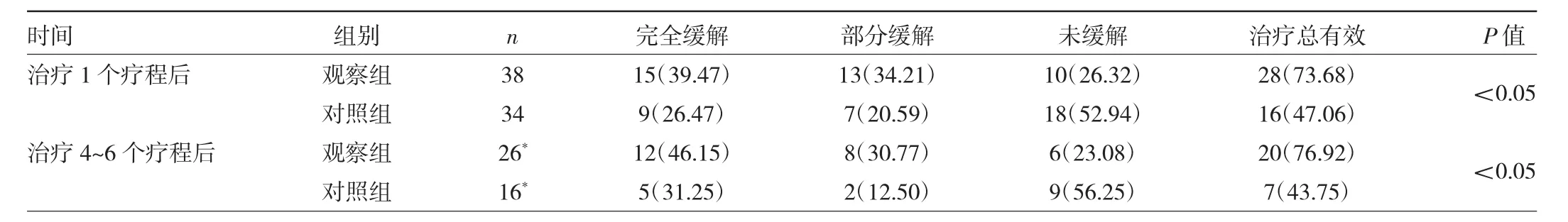
表2 两组老年急性髓系白血病患者治疗效果比较[例(%)]
2.2 两组患者不良反应发生情况比较 两组患者发生Ⅲ~Ⅳ级非血液学不良反应主要是感染。观察组患者肺部感染、骨髓抑制、恶心、呕吐及肝肾功损害等不良反应发生率比较差异均无统计学意义(均P>0.05),见表3。
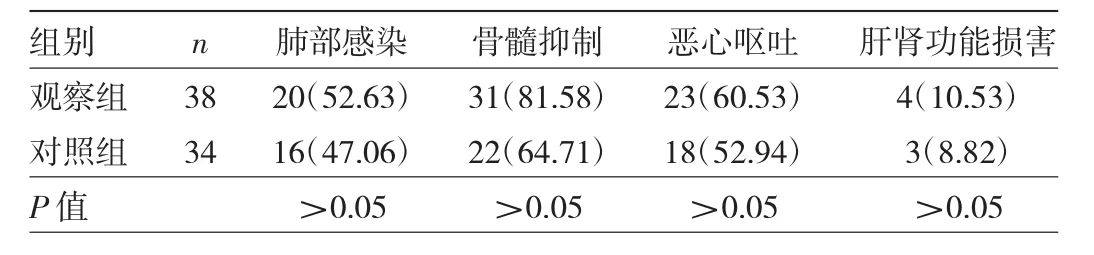
表3 两组老年急性髓系白血病患者不良反应发生情况比较[例(%)]
2.3老年急性髓系白血病患者总生存期影响因素分析Cox回归模型分析显示,患者性别、ECOG体能状况评分与老年急性髓系白血病患者总生存期无关(均P>0.05)。而染色体核型、治疗方案与老年急性髓系白血病患者总生存期有关(均P<0.05),见表4。
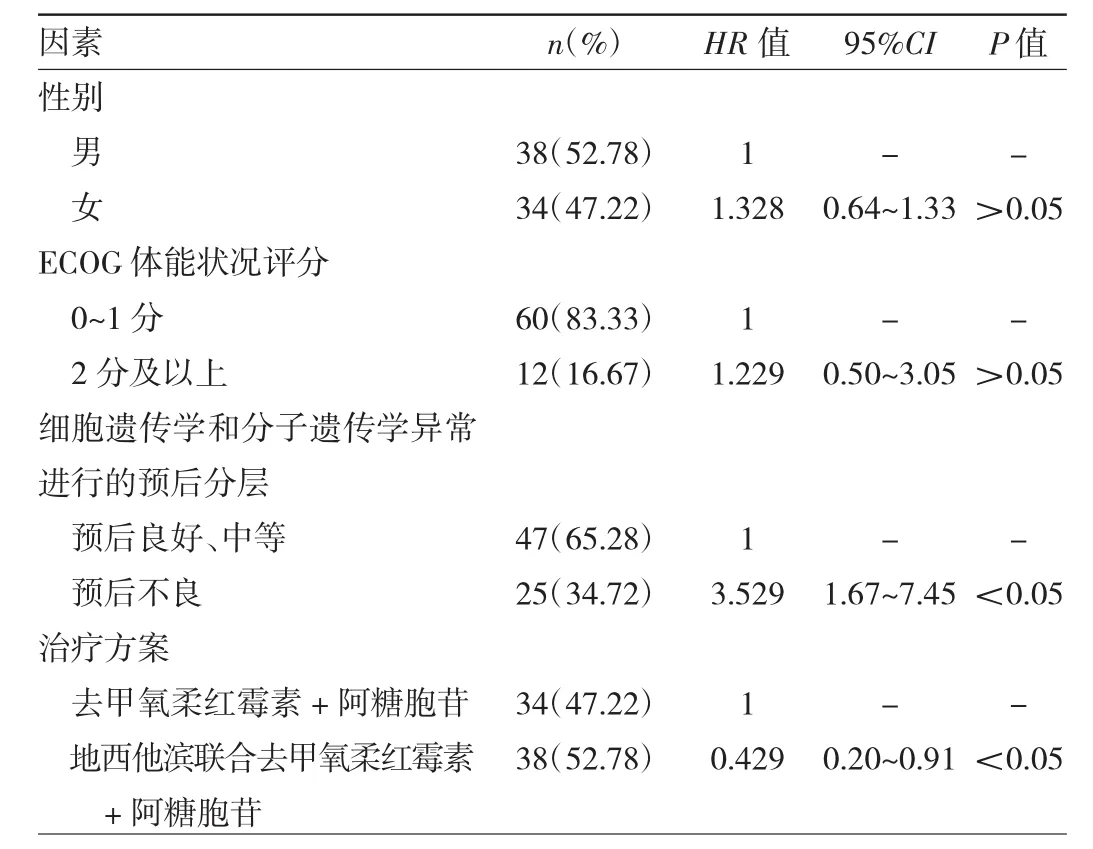
表4 老年急性髓系白血病患者总生存期影响因素分析
2.4 两组患者生存情况比较 72例患者中位随访时间11.5个月,观察组患者存活23例,死亡15例,累计病死率 39.47%,中位总生存期 15个月(95%CI:19.87~20.12),中位无进展生存期 9.61 个月(95%CI:8.39~15.61);对照组患者存活20例,死亡16例,累计病死率47.06%,中位总生存期 10 个月(95%CI:8.40~11.60),中位无进展生存期 6.06个月(95%CI:6.36~9.64)。与对照组相比,观察组患者中位总生存期、中位无进展生存期均明显改善(均 P<0.05)。见图 1、2。

图1 两组老年急性髓系白血病患者总生存曲线比较
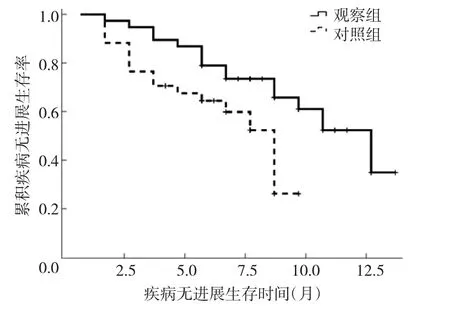
图2 两组老年急性髓系白血病患者疾病无进展生存曲线比较
3 讨论
急性髓系白血病是一种常见的血液恶性肿瘤。确诊为髓系白血病的人群中60岁以上患者占大部分,这部分患者机体抵抗力较差、化疗后骨髓抑制时间较长,免疫系统功能受损,患者更易受到病原体侵袭而发生严重感染性病变[4]。IA方案应用于老年白血病已取得较好的疗效,但仍需根据患者年龄、ECOG体能状况评分、基础疾病、分子遗传学等选择治疗方案及调整化疗药物剂量,达到远期获益。地西他滨是一种特异性的DNA甲基化转移酶抑制剂,其通过抑制DNA甲基化转移酶,改变DNA甲基化状态,启动抑癌基因,诱发抗肿瘤的作用。研究表明,DNA甲基化参与了急性髓系白血病的发生、发展,而地西他滨能够抑制DNA甲基化,活化沉默的抑癌基因,发挥抗肿瘤作用[5]。地西他滨在治疗骨髓增生异常综合征中已取得了比较确切的疗效。地西他滨已被欧洲药品管理局正式批准用于年龄>65岁的不适宜强烈化疗的老年急性髓系白血病患者[6]。研究表明,老年急性髓系白血病患者应用地西他滨的血液学不良反应较小,患者的耐受性较好[7];加用地西他滨,15.7%的患者可以获得完全缓解[8]。有学者采用地西他滨联合CAG方案(阿糖胞苷+阿克拉霉素+粒细胞集落刺激因子)和HAG方案(高三尖杉酯碱+阿克拉霉素+粒细胞集落刺激因子)治疗,完全缓解率达42.1%,1年生存率为67.5%,优于单用地西他滨治疗[9]。
本研究结果显示,地西他滨联合小剂量IA方案治疗能提高不适合强化诱导化疗方案和异基因造血干细胞移植的老年急性髓系白血病患者的缓解率,且近期疗效显著。观察组患者骨髓抑制、肺部感染、恶心、呕吐、肝肾功能损害等不良反应发生率与对照组相当,无统计学差异;而治疗1个疗程后,观察组患者治疗总有效率高于对照组;治疗4~6个疗程后,观察组患者治疗总有效率亦高于对照组。急性髓系白血病患者根据细胞遗传学和分子遗传学异常进行的预后分层以及治疗方案的选择与患者总生存期有关。
综上所述,去甲基化药物地西他滨联合小剂量IA方案治疗老年急性髓系白血病患者临床效果确切,未增加不良反应发生率,值得临床借鉴。

