液相色谱-原子荧光联用法测定沙丁鱼罐头中甲基汞含量的不确定度评定
◎ 郭倩倩,李 新,康雪梅,李梦雨,贾松涛,李 超,赵雪峰,赵林萍
(1.河南中标检测服务有限公司,河南 郑州 450000;2.郑州大学,河南 郑州 450000)
汞是一种对环境和人体有害的重金属,随着食物链传递和富集,在水生系统中尤其严重。MOHAN等人[1]发现汞的积累潜力沿着食物链增加,在鱼类组织中有较高的汞浓度。朱文慧等人[2]发现鱼体内汞含量可能较生活环境中的汞含量高100万倍。
汞以多种形态广泛存在于环境中,其中甲基汞是具有较强生物有效性和毒性的有机汞形态,在所有汞化合物中毒性最强[3],在我国各种环境介质和生物体组织中都检测到了甲基汞的存在[4]。甲基汞具有高神经毒性、致癌性,且在生物体中造成累积和放大效应,可对人类及食鱼生物的健康造成严重影响[5],PRINCE等人[6]发现甲基汞暴露选择性地靶向脑和小脑皮质,导致神经元发育不良,苏海磊等人[7]发现甲基汞可以对脊椎动物造成神经苏醒、内分泌干扰和生殖毒性等。有研究数据表明,通过食物链的传递作用,鱼类等水生生物可以将水体中ng·L-1级甲基汞富集达10~20万倍[8]。对此,中国、欧盟、美国、日本、韩国及澳大利亚等均对水产品中甲基汞含量做了限制,且中国对甲基汞的限量要求相对偏严[9],因此要求检测人员准确测定水产食品中的甲基汞含量。
本文选取基质较为复杂的沙丁鱼罐头作为研究对象,依据《测量不确定度评定与表示》(JJF 1059.1—2012)[10]和《化学分析中不确定度的评估指南》(CNAS-GL006:2019)[11],对《食品安全国家标准 食品中总汞及有机汞的测定》(GB 5009.17—2014)第二篇中甲基汞测定不确定度进行分析和评定。
1 材料与方法
1.1 仪器与试剂
液相色谱-原子荧光联用仪(北京吉天SA20);高速台式冷冻离心机(安徽嘉文仪器装备有限公司);振荡器(德国IKA);电子天平(上海佑科仪器仪表有限公司);玻璃量器(北京玻璃厂)。
甲基汞溶液标准物质(65.0 μg·g-1,中国计量科学研究院);硝酸(优级纯,苏州晶瑞);甲醇(色谱纯);盐酸(优级纯);其余试剂均为分析纯。
1.2 实验方法
根据《食品安全国家标准 食品中总汞及有机汞的测定》(GB 5009.17—2014)第二篇液相色谱-原子荧光光谱联用法,进行测定。
1.2.1 样品前处理
准确称取样品1.0 g(精确至0.001 g)于50 mL离心管中,加入5 mol·L-1的盐酸溶液10 mL,放置过夜。室温下超声水浴提取60 min,期间数次震摇。4 ℃下以8 000 r·min-1转速离心15 min。准确吸取2.0 mL上清液至5 mL容量瓶中,逐滴加入6 mol·L-1的氢氧化钠溶液,使pH为2~7。加入10 g·L-1的L-半胱氨酸0.1 mL,最后用水定容至刻度。用0.45 μm有机系滤膜过滤,上机进行检测。
1.2.2 标准溶液的配制
准确称取甲基汞溶液标准物质0.384 6 g,用纯水定容至25 mL容量瓶中,摇匀,得到甲基汞标准储备液1 μg·mL-1。用10 mL单标线移液管准确量取10 mL甲基汞标准储备液至100 mL容量瓶中,得到100 μg·L-1甲基汞中间工作液;分别用移液管移取0 mL、0.25 mL、0.5 mL、1.0 mL、1.5 mL、2.0 mL和2.5 mL至25 mL容量瓶中,用水定容至刻度,分别得到浓度为0 μg·L-1、1 μg·L-1、2 μg·L-1、4 μg·L-1、6 μg·L-1、8 μg·L-1和10 μg·L-1的标准溶液。
1.2.3 仪器条件
(1)液相色谱。色谱柱:C18色谱柱(柱长150 mm,内径4.6 mm);流动相:5%甲醇+0.06 mol·L-1乙酸铵+0.1% L-半胱氨酸;流动相洗脱方式:等度洗脱;流动相流速:1.0 mL·min-1;进样体积,100 µL。
(2)原子荧光光度计。负高压:300 V;灯电流:30 mA;载气流速:400 mL·min-1;辅助气流速:400 mL·min-1;载流:10%盐酸溶液;还原剂:2 g·L-1KHB4;氧化剂,2 g·L-1过硫酸钾。
2 结果与分析
2.1 不确定度评定数学模型的建立
根据甲基汞含量计算公式以及测量不确定度的主要影响因素,建立沙丁鱼罐头中甲基汞含量的不确定度评定数学模型(1):

式(1)中,X为试样中甲基汞的含量,mg·kg-1;C为经标准曲线得到的测定液中甲基汞的浓度,μg·L-1;C0为经标准曲线得到的空白溶液中甲基汞的浓度,μg·L-1;V为加入提取试剂的体积,mL;m为试样称样量,g;f为稀释因子;1 000为换算系数。
2.2 不确定度来源与分析
从样品前处理过程、测量过程和数学模型分析,用液相色谱-原子荧光联用法测定沙丁鱼罐头中甲基汞不确定度来源,主要有以下几个方面:样品测量重复性引入的不确定度、样品称量引入的不确定度、样品前处理及定容过程引入的不确定度、标准物质及配制引入的不确定度、标准曲线拟合引入的不确定度。
2.2.1 样品测量重复性引入的相对标准不确定度urel(rep)
在重复性条件下,对同一样本重复测量10次,测得样品中甲基汞的含量分别为0.17 mg·kg-1、0.17 mg·kg-1、0.18 mg·kg-1、0.19 mg·kg-1、0.16 mg·kg-1、0.18 mg·kg-1、0.20 mg·kg-1、0.17 mg·kg-1、0.18 mg·kg-1和0.20 mg·kg-1,其平均值为0.18 mg·kg-1。
测量重复性以标准偏差表示,10次测量的标准偏差按贝塞尔公式计算为:

以两次测量的平均值作为最终测定结果,则本次测量的标准偏差为:

本次测定两个结果分别为X1=0.18 mg·kg-1,X2=0.19 mg·kg-1,其平均值为0.18 mg·kg-1,则测量重复性引入的相对标准不确定度为:

2.2.2 样品称量引入的相对标准不确定度urel(m)
根据万分之一电子天平校准证书,其最大允许误差为±0.000 5 g,称量两次,第1次空烧杯,第2次空烧杯加样品,因为每一次称量均为独立的观测结果,两者的现行影响间是不相关的[11]。按照矩形分布其标准不确定度为:
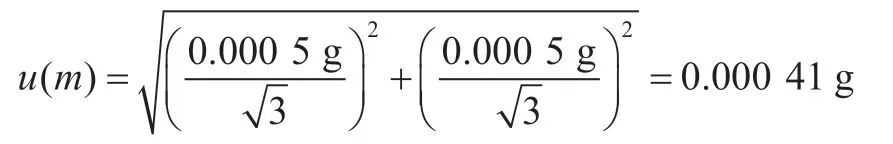
根据方法要求,称取混合均匀的样品1.0 g,则样品称量引入的相对标准不确定度为:
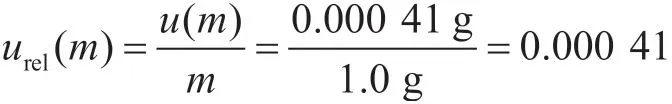
2.2.3 样品前处理及定容过程引入的相对标准不确定度urel(V)
样品前处理及定容过程中不确定度由玻璃量器引入。根据《常用玻璃量器》(JJG 196—2006)[12]要求的容量允差,假设其为矩形分布则可计算各量器由体积引入的标准不确定度u(a),u(a)=容量允差由实验室温度在(20±5)℃,得ΔT=5 ℃,水在20 ℃的膨胀系数为2.1×10-4℃-1,按照矩形分布计算温度引入的标准不确定度u(b),结 合 体 积 和 温度引入的不确定度,各玻璃量器引入的标准不确定度为,其相对标准不确定度为样品前处理及定容过程,玻璃量器引入的不确定度具体计算见表1。

表1 样品前处理及定容过程玻璃量器引入的不确定度表
样品前处理及定容过程中,10 mL分度移液管、2 mL分度移液管、5 mL容量瓶各用到一次,综上计算,则相对标准不确定度为:

2.2.4 标准物质及配制引入的相对标准不确定度urel(c)
由标准物质及配制引入的不确定度主要包括:标准物质纯度引入的不确定度、标准储备液配制引入的不确定度(包括标准物质称量及标准物质定容)、标准中间工作液配制引入的不确定度以及标准曲线系列配制过程中引入的不确定度。
(1)标准物质纯度引入的相对标准不确定度urel(c1)。甲基汞标准物质证书给出的浓度为(65.0±2.5)μg·g-1,k=2,则标准不确定度为:相对标准不确定度为
(2)标准储备液配制引入的相对标准不确定度urel(c2)。①标准物质称量引入的相对标准不确定度urel(c´2)。根据十万分之一天平校准证书,其最大允许误差为±0.5 mg,按照均匀分布则标准不确定度为:

称取标准物质0.384 6 g,则产生的相对标准不确定度为:

②标准物质定容引入的相对标准不确定度urel(c´2)。标准物质定容引入的不确定度由单标线容量瓶的容量允差带入。按矩形分布其相对标准不确定度计算见表2。

表2 标准物质定容过程玻璃量器引入的不确定度表
则由标准储备液配制引入的相对标准不确定度为:

(3)标准中间工作液配制引入的相对标准不确定度urel(c3)。标准中间工作液配制引入的不确定度由移液管和容量瓶的容量允差带入,假设其为矩形分布其相对标准不确定度计算见表3。

表3 标准中间工作液配制过程玻璃量器引入的不确定度表
则标准中间工作液配制引入的相对标准不确定度为:

(4)标准曲线配制过程中引入的相对标准不确定度urel(c4)。标准曲线配制引入的不确定度由容量瓶和移液管容量允差带入,假设其为矩形分布则标准曲线配制过程中25 mL容量瓶引入的不确定度计算同表2,其相对标准不确定度为0.000 92,分度移液管引入的不确定度计算见表4。

表4 标准曲线配制过程分度移液管引入的不确定度表
在甲基汞标准溶液配制过程中,25 mL容量瓶用到7次,则标准曲线配制过程中引入的相对标准不确定度为:

由此得出标准物质及配制引入的相对标准不确定度为:

2.2.5 标准曲线拟合引入的相对标准不确定度urel(q)
标准曲线是采用最小二乘法对甲基汞标准溶液浓度X与其对应的峰面积Y进行线性回归,得到甲基汞标准曲线Y=bX+a,本实验对7个浓度水平的标准工作液分别重复3次测定,根据其平均值拟合所得标准曲线为Y=10 882X-891.2(R²=0.999 0),标准溶液浓度与峰面积见表5。
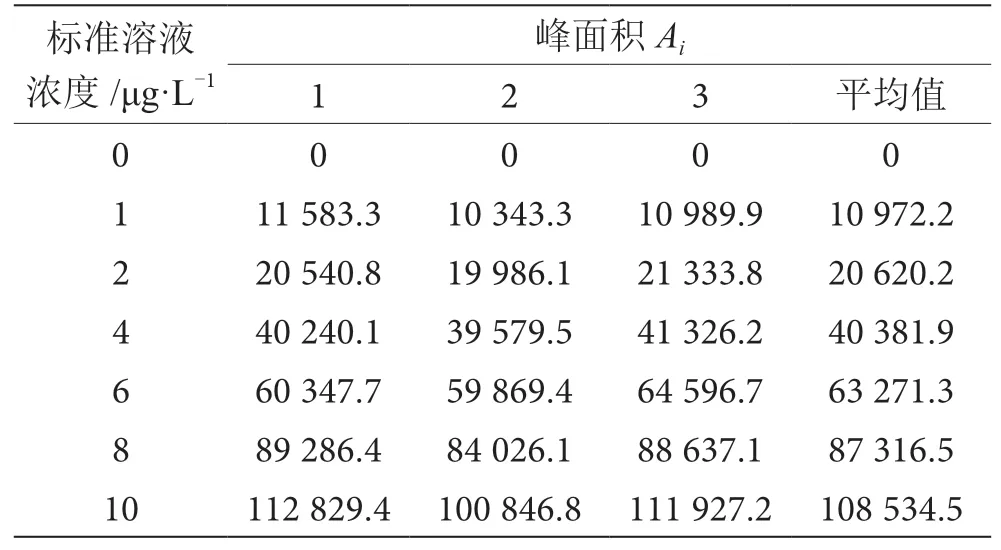
表5 标准曲线的测定结果表
标准曲线标准差计算公式为:

标准曲线拟合引入的标准不确定度计算公式为:

其中Ai为建立工作曲线用标准系列溶液中甲基汞的质量浓度对应的峰面积;b为拟合曲线的斜率,b=10 882;a为拟合曲线的截距,a=-891.2;n为标准溶液总测试次数,n=21;p为样品的测试次数,p=2;c0为实测样品的平均测试浓度,c0=7.505 7 μg·L-1;ci为标准溶液各校准点的浓度,μg·L-1;为标准曲线各校准点的平均浓度,c-=4.428 6 μg·L-1;i为浓度水平序号。
在不确定度的评定过程中,本次实验对样品进行两次测定,平均测试浓度为c0=7.505 7 μg·L-1,从上述数据和公式,可得S=720.92,u(q)=0.054 μg·L-1。
标准曲线的拟合引入的相对标准不确定度为:

2.3 合成不确定度
各个相对标准不确定度分量及量值,汇总见表6。

表6 各个相对标准不确定度来源分量及量值表
对表中各分量进行合成,得到合成相对标准不确定度为:

本次实验,沙丁鱼罐头中甲基汞含量测定的平均值为0.18 mg·kg-1,则合成标准不确定度为:
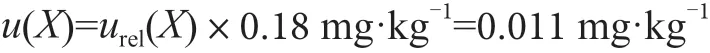
2.4 扩展不确定度及不确定度结果报告
在95%的置信区间下,取包含因子k=2,扩展不确定度为U(X)=k×u(X)=0.022 mg·kg-1。
沙丁鱼罐头中甲基汞含量结果表示为(0.18±0.03)mg·kg-1。
3 结论
按照GB 5009.17—2014的检测方法,对液相色谱-原子荧光联用仪测定丁鱼罐头中甲基汞含量进行不确定度分析,不确定度结果表示为:X=(0.18±0.03)mg·kg-1,k=2。
从不确定度评定过程来看,影响实验最终结果的因素主要有样品测量的重复性、标准物质及配制、标准曲线的拟合,这就要求检测人员在今后的检测工作中,增加平行样的检测频次、使用精度较高的计量器具、规范操作要求等,以降低不确定度带来的影响,提高数据的准确性,为保障食品安全提供强有力的数据支撑,为食品安全保驾护航。

