内镜切除术治疗早期食管鳞状细胞癌短期疗效的回顾性研究
杨叶琴,孙 斌,汪胡根,蔡 轶,冯 慧,王亚雷
中国食管癌以食管鳞状细胞癌为主,占食管癌的90%以上。食管切除加淋巴结清扫是食管癌的标准治疗方法。虽然外科手术可以对淋巴结进行清扫,但是手术过程中很难对每一处淋巴结进行全面彻底清扫,因此术后仍会有淋巴结转移的风险,而且外科手术通常并不能防止远处转移的发生。同时外科手术的创伤性较大,40%的患者出现严重并发症,病死率高达10%,大大降低了患者的生活质量。目前内镜切除术为治疗早期食管鳞状细胞癌提供了一种新的选择,尤其是内镜黏膜下剥离术(endoscopic submucosal dissection,ESD)可以对较大的病变进行整块切除,保证了病变的完整性,因此可以对标本进行准确的组织病理学评估。但内镜切除术后患者的预后如何,ESD术后是否需要追加治疗,各项研究结论并不相同。因此,该研究回顾性分析了ESD治疗早期食管鳞状细胞癌患者的资料,旨在通过评估患者的疗效和短期预后来判断ESD治疗食管鳞状细胞癌的有效性和安全性,并通过分析淋巴血管浸润(lymphovascular invasion,LVI)的危险因素为术后患者的随访监测提供指导作用。
1 材料与方法
1.1 病例资料
收集2018年1月—2019年11月在安徽医科大学第一附属医院因早期食管鳞状细胞癌拟行内镜切除的患者,纳入标准:① 经内镜检查及组织病理学诊断考虑为早期食管鳞状细胞癌;② 术前经CT、EUS等检查证实无淋巴结或远处转移。排除标准:① 既往行食管ESD者;② 术前行辅助治疗者;③ 病理结果为腺癌的患者;④ 未行ESD治疗的患者;⑤ 病理结果不详细的患者。最终纳入完成食管ESD治疗的患者289例(328个病灶)。1.2 ESD手术过程
二氧化碳供气,气管插管麻醉。首先使用奥林巴斯GIF-H260Z放大内窥镜观察病灶,然后使用Lugol碘液进行染色,以确定病变边界及浸润深度。然后使用GIF-Q260J治疗内镜,Q260J置先端帽,使用Dual-Knife刀沿病灶周边约0.5 cm处标记,黏膜下注射玻璃酸钠+生理盐水+肾上腺素+靛胭脂混合液抬举病变,Dual刀沿标记点以外做环周切开,进行黏膜下剥离,直至病灶被完整剥离,创面用热活检钳充分止血,随后取出切除的标本,完成手术。1.3 组织病理学检查与评估
使用不锈钢细针将ESD标本整块固定于泡沫塑料板上,充分暴露黏膜面的病变,标记口侧及肛侧,标本再行碘液染色。然后,将标本固定在福尔马林溶液中,将固定后的标本切成2 mm的切片,石蜡包埋,将包埋后的组织切成5 μm的切片,由病理学家对标本进行病理评估。根据巴黎分型标准,对肿瘤浸润深度进行分期:M1指病变局限于黏膜上皮层; M2指病变浸润至黏膜固有层; M3指病变浸润至黏膜肌层但未突破黏膜肌层;肿瘤浸润至黏膜下层的上、中、下1/3 者分别称为SM1、SM2及SM3,其中将病变浸润至黏膜下层但距黏膜肌层200 μm以内者称为SM1。
1.4 病变治愈性评估
完全切除/R0切除:病变已整块切除,且内镜下切除标本的水平切缘和垂直切缘无肿瘤残留。治愈性切除指内镜下完全治愈:① R0切除;② 黏膜内癌或黏膜下层浸润深度不超过200 μm(SM1)的黏膜下癌;③ 无脉管浸润;④ 组织学类型为高、中分化。
病变复发定义为术后在原切除部位及周围1 cm内发现新的肿瘤病灶。术后1年内在其他部位发现新的病灶定义为同时性癌,术后1年以后发现新的病灶定义为异时性癌。
除了上述指标,采用第11版的日本食管癌分类对内镜切除术后病理情况进行了治愈性评估分组,分为A、B、C 3组,具体标准见表1。

表1 内镜切除的治愈性评估标准
1.5 随访
患者通常在术后3、6、12个月及以后每年一次进行内窥镜检查,每6~12个月做一次CT检查淋巴结和远处转移情况。通过收集患者的临床资料以及电话进行随访,收集相关指标。对于ESD术后患者是否出现并发症、复发、进一步治疗、是否发生淋巴结转移等情况进行随访,并对随访结果进行详细记录。
2 结果
2.1 患者基本资料
共收集了289例患者328个病灶,年龄为45~87(65.02±7.97)岁,男性219例,女性70例。有多个病灶的患者以浸润深度最深的进行分析,具体见表2。
表2 患者基本资料
2.2 ESD患者LVI的临床特征分析
对患者的LVI情况进行分析发现有6例患者术后病理显示LVI阳性。有无LVI的两组患者比较,发现病变大小、病变周长、浸润深度和HM在有无LVI的患者中的差异有统计学意义(P
<0.05)。见表3。
表3 ESD患者LVI的临床特征分析[n(%)]
2.3 LVI的危险因素分析
单因素分析结果显示病变大小、病变周长、浸润深度和HM与LVI相关。然而,在多因素分析中发现只有病变周长(OR
=19.18,95%CI
1.64~224.61;P
=0.019)和浸润深度(OR
=9.66,95%CI
1.40~66.90;P
=0.022)是影响LVI发生的独立危险因素。病变周长≥3/4或浸润至黏膜下层的患者发生LVI的风险更高。见表4。
表4 LVI危险因素的单因素和多因素分析
2.4 临床疗效分析
病灶整块切除率为100.00%(328/328),完全切除率为94.51%(310/328),治愈性切除率为89.33%(293/328)。对于不完全切除的18个病灶,其中水平切缘阳性的病灶有15个(83.33%),垂直切缘阳性的病灶有3个(16.67%),垂直切缘阳性的病灶均浸润至黏膜下层深层。研究分析发现切缘阳性与否与病变浸润深度有关,随着浸润深度的增加,切缘阳性的数量也呈逐渐增加的趋势(P
=0.006)。切缘阳性基于不同浸润深度的分布情况分别为:M1 0.00%(0/37),M2 3.98%(9/226),M3 10.00%(4/40),SM1 16.67%(1/6),SM2以上21.05%(4/19)。术后迟发性出血率为0.75%(2/267),狭窄率4.49%(12/267),无术中及术后迟发穿孔。术中出血及术后迟发性出血均经电热活检钳或止血钳成功止血。狭窄患者经数次球囊扩张术后症状均缓解。
2.5 短期预后
对ESD术后的患者进行了随访,中位随访期为16个月(7~28个月),共随访到267例患者。在随访过程中,发现有1例患者死亡,死亡原因与食管鳞状细胞癌无关。总体复发率为0.75%(2/267),其中1例(0.37%,1/267)患者为肿瘤残留,1例发生了淋巴结和远处转移(0.37%,1/267)。发生淋巴结和远处转移患者在ESD术后追加了放疗,复发后进行了外科手术和化疗,另1例复发患者(M2,pR1)还在跟踪随访中。7例(2.62%,7/267)患者发生了同时性癌,3例(1.12%,3/267)患者发生了异时性癌,其中有9例患者进行了二次ESD术治疗,1例M2患者选择了手术治疗,术后病理显示浸润深度最深为M2,无淋巴血管浸润,且均为R0切除。共有23例(8.61%,23/267)患者在术后追加了手术或辅助治疗,其中8例追加了手术治疗,15例追加了放疗。根据第11版日本食管癌分类将随访到的患者分为A(pCur A),B(pCur B),C(pCur C)三组,分析发现A组术后没有追加任何治疗,B组追加治疗主要以放疗为主,有1例患者追加了手术治疗,但术后病理并未检出癌组织及阳性淋巴结。C组追加治疗主要以外科手术为主,其中1例术后追加放疗的患者最终发生了淋巴结和远处转移。C组中剩余18例患者进行跟踪随访过程中,内镜检查或CT检查目前尚未发现食管新发病变及阳性淋巴结或远处转移。见表5。
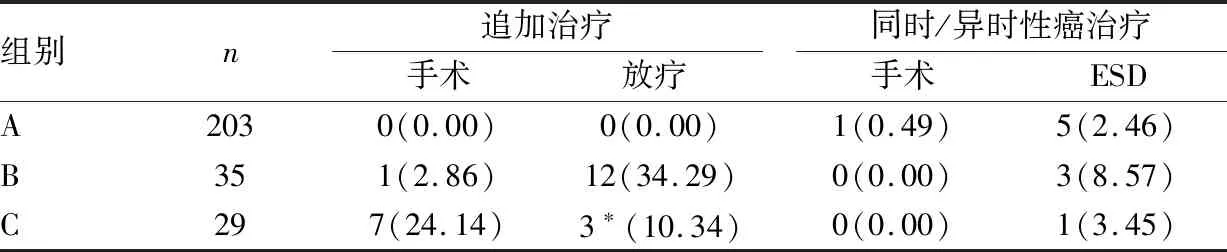
表5 随访期间ESD术后患者的进一步治疗情况[n(%)]
追加手术患者的病理结果见表6,有1例ESD术后病理报告浸润深度为SM2以上的患者在追加手术后发现了残留的肿瘤(患者5),手术后病理为T1bN0。

表6 追加手术治疗患者的病理结果
3 讨论
本研究纳入的患者基本为术前经内镜评估考虑符合内镜治疗绝对适应证的患者(少数为内镜诊断考虑相对适应证,但患者及家属要求先行内镜治疗以确定诊断)。从患者的基本资料发现,患者多为老年男性,病变形态多呈浅表平坦型和浅表凹陷型,病变多位于中下段。对于病变的范围,由于内镜切除后形成狭窄的风险较高,指南不建议对病变周长≥3/4的早期食管鳞状细胞癌进行内镜切除治疗,本研究中接受ESD治疗的患者的病变周长也以<3/4为主。术后病理提示病变浸润深度多局限于黏膜层和黏膜下层浅层(93.43%),符合ESD的适应证,说明目前通过放大内镜、超声内镜以及CT等术前检查对于浸润深度的综合评估准确性良好。在本研究中,ESD手术并发症发生率较低,因此对于符合内镜治疗适应证的早期食管鳞状细胞癌患者而言,ESD是安全、有效的治疗方式。
术后淋巴结转移的风险是判断患者预后的关键因素。既往许多研究认为病变是否存在LVI是预测淋巴结转移的重要危险因素之一。LVI是指淋巴管和血管管腔内存在癌细胞,被认为是肿瘤扩散的重要步骤。Hsu et al对食管鳞状细胞癌患者的LVI进行分析后发现,无论患者术前是否接受新辅助治疗,LVI阳性患者的5年总生存率和中位生存期均显著低于LVI阴性患者,LVI阳性与肿瘤分化差、T分期晚期、N分期晚期和切缘阳性有关。其他研究也得出了相似的结论,认为LVI不仅是生存的重要预后因素,并且LVI的存在会导致更高的复发率。虽然这些研究是根据食管切除术后的病理进行分析的,但是LVI在判断患者生存和复发中的重要作用毋庸置疑。对于进行内镜治疗的患者而言,虽然不能进行淋巴结的清扫,但是术后标本病理可以提供LVI的情况。所以,在内镜治疗相关的指南中建议,如果病理证实切除的标本中存在LVI,则需要追加外科手术或放化疗。在本研究中,单因素分析表明病变大小、周长、浸润深度和切缘阳性是LVI的危险因素,而多因素分析表明病变周长和浸润深度是LVI的独立危险因素。本研究与Hsu et al的研究类似。所以对于病变周长≥3/4或浸润深度更深的患者需要警惕LVI的发生,对于这类患者在术前评估和术后追加治疗方案的选择上需要考虑得更加全面。
目前,eCura评分系统在早期胃癌内镜治疗治愈性评估中得到广泛应用,但在早期食管鳞状细胞癌的评估中并没有类似的评分系统来评估治愈情况,指导后续随访或治疗方案的选择。本研究根据日本第11版食管鳞状细胞癌分类指南中的内镜切除的治愈性评估标准对纳入患者的术后病理情况进行了分析,发现pCurA和pCurB组的患者可以不追加手术治疗,而pCurC的患者肿瘤残留及淋巴结转移发生的可能性较大,因此内镜切除术后仍建议追加手术或者辅助治疗。
综上所述,通过回顾性研究发现,对于浸润深度不超过SM1且无淋巴结转移的早期食管鳞状细胞癌患者,ESD安全、有效,可以作为首选治疗方法。病变周长≥3/4或浸润深度较深的患者是发生LVI的独立危险因素,在术前评估中应加以重视。在术后评估中,对于pCur A或pCur B的患者应密切随访,而pCur C的患者应积极追加手术或者辅助治疗。

