超声造影对肝硬化合并小肝癌的早期诊断价值
王瑞霞
(莘县第二人民医院超声诊疗科 山东 聊城 252423)
超声对肝硬化、肝癌有较高的诊断率,在临床上得到广泛应用。然而,在肝硬化合并小肝癌的状况下,早期诊断有时相对困难,主要原因是小肝癌的超声图像不明显,肝脏形态和回声异常。目前,我国大部分临床诊断方式主要为电子计算机断层扫描(computed tomography, CT)、核磁共振(magnetic resonance imaging, MRI)、血管造影以及其他成像方法,但这些方法对1 cm以下小病变的定性检出率有很大的局限性。本文的主要内容是分析超声的灌注时间,改善方法以及对肿瘤的诊断速度。观察超声造影对肝硬化合并小肝癌的早期诊断价值[1-2]。
1 资料与方法
1.1 一般资料
对本院2019年11月—2020年11月收治的所有肝脏占位性病变患者140例进行超声造影检查。通过手术和病理学明确诊断出45例肝硬化合并小肝细胞癌患者。男性35例,年龄34~80岁,女性10例,年龄27~76岁,平均年龄(56.51±9.7)岁,共45例,均小于3 cm。病灶的大小范围为0.8~1.0 cm 2个、1.1~1.5 cm 9个、1.6~2.0 cm 15个、2.1~3.0 cm 24个,平均大小(2.51±0.68)cm;甲胎蛋白增加17例,占38.6%,其中大于400 ng/mL的有10例。在增强超声检查的上半个月至下半个月之间,有45例小肝癌患者接受了CT检查。共有4位经验丰富的放射科医生以及病理学家采用了双盲诊断。
1.2 选择仪器和方法
采用Bracco公司的新型脂质膜包裹六氟化硫(sulphur hexafluoride, SF6)形成的第二代超声微泡造影剂SonoVue,微泡直径(粒径)1~10μm,平均2.5μm,其中<8μm的微泡占90%,pH值在4.5~7.5之间。使用前,用5 mL生理盐水溶解造影剂冻干粉[3]。摇匀混匀后,从肘浅静脉进行注射2.4 mL,并在两秒钟内检查注射液。超声仪器:此次研究里选用的仪器为超高端多普勒成像系统TechnosDU6,DU8和Real-time CnTL。造影方法:借助常规二维超声对纳入的患者进行肝脏扫描,针对扫描结果,分析患者的主要病灶位置、数量、直径以及主要的回声特点,针对性做好登记记录,对于造影前,进行实施初步诊断;通过扫描患者的肝肿瘤,进而通过最大程序上仔细找到多个结节的主要位置,在此基础上采用CnTL,由于每位病人个体因素存在差异,需要结合具体的胖瘦以及主要的病灶深浅,进而针对性调试仪器的功率,满足机械指数状态。患者主要部位病变的灌注和回声强度不同。应动态观察这种情况;记录靶区主病灶的每一期,以保证完整性,注意不要捉漏,然后观察主要病变附近的病变灌注情况,并作详细报告,在拍摄过程中,为确保可以捕捉到小病变的时相,必须固定探头并指导患者检查呼吸程度;还有另一个不可忽视的因素,即肋间扫描,绕开肋骨干扰的可能性,在整个扫描完成后,可以获得具有诊断意义的时相记录。应迅速检查,可能发现造影剂已从弱回声的新病变中撤出,回声较弱,假如成像不足或必须观察不同部位,可以每隔10 min再实施造影[3]。用高清录像带记录的约7 min的成像过程来判断每个时相,使用磁光盘对单帧静止图像进行有效定位;可以为观察记录的每个目标选择1~3个典型病变;四位具有十多年工作经验的医师在进行对比之前先进行超声和对比分析,并进行记录参照图像数据详细说明所有灌注和回归的时期; 然后他们至少两次仔细地观看视频,实施统计以及数据分析,然后予以全部血管造影评分以及诊断,超声能够清晰地观察到增强以及消除肝动脉,门静脉与肝实质的全过程。在将造影剂注射到忠诚的人体内之后,造影剂增强的超声可以具有与螺旋CT或MRI相同的评估效果;从肝动脉时起主要有6种肝动脉期和门静脉期的开始即为肝静脉及其二级分支开始显像,此后肝实质逐渐强化,即进入实质期。超声造影比CT稍早,尤其是在实质期[4]。
1.3 评价方法
根据肿瘤的二维超声图像回声形态和晕环,以及彩色多普勒超声的诊断经验来检测肿瘤的供血状态[5],合理结合造影剂灌注期的特点,患者造影前后超声诊断得分,确认良性为1分,可疑良性为2分,不确定为3分。疑似恶性为4分,明确恶性为5分,血管造影后改善2分以上者为有效,提高诊断率。对于不能确诊的患者,需要再次进行超声造影或选择18G粗针进行穿刺活检。
1.4 统计学方法
本次研究的全部数据皆选用SPSS 10.0软件统计处理,计量资料比较采用F检验,计数资料采用χ2检验以及Fisher精确检验法。
2 结果
患者分别于术前半个月和术后半个月行超声造影:二维超声CT检查,严格扫描病灶,并采用穿刺活检等方法,共确诊小肝癌45例,其中癌灶占44.5%,发现S7.S8区膈下2 cm以下小肿瘤4例,1例合并胸腔积液。腹水患者,这些经超声造影后能准确反映,其余3例因患者酒精性肝及背回声明显衰减而漏诊。根据本次扫描结果,超声造影检出小肝癌的概率高达95.64%(40/45)。
2.1 45例小肝癌超声造影时间表
行超声造影后小肝癌灶开始增强、高峰、消退的各个时间,见表1。
表1 45例小肝癌超声造影时间(,s)

表1 45例小肝癌超声造影时间(,s)
病理诊断 灶数 开始增强时间 增强峰值时间 开始消退时间中-低分化癌 37 14.13±5.25 22.13±7.48 60.01±45.91高分化癌 5 14.82±3.05 25.01±9.35 263.±152.71透明细胞癌 3 25.66±8.95 30.32±9.49 133.6±65.98
2.2 小肝癌造影增强模式,见表2。

表2 45例小肝癌超声造影增强模式
2.3 45例小肝癌超声造影前后超声诊断评分结果
大多数小肝肿瘤的动脉期迅速明显增加,即表现出“快进”的特征,当迅速清除肿瘤中的造影剂时,正常肝实质增强,回声强度升高。肿瘤明显低于周围肝组织,表现出典型的“快速退出”现象,占病变的83.5%(37/45)。手术和疾病后,病灶37被确认为低分化癌,1个病灶为2.2 cm透明细胞癌。5个分化良好的肝细胞癌,影像学检查后出现“快进”放疗后肿瘤回声增加13~21,然后实质性肿瘤和肝脏以相同回声同时穿孔,在103~291 s内2个灶开始轻度减少,其余2个灶直至380 s和495 s开始逐渐消失,显示出微弱的回声结节,边界不清晰,在三个清晰的细胞肿瘤病变中,两个肿瘤病灶,在成像前5 cm未见明显血管异常,成像后呈21~38度轻度。超声增强,在60~193 s的薄壁组织中仅出现少量,显示出模糊的回声结节,边界不清晰,显示出“慢进慢出”模式。这组病例中45个病灶,造影前超声图像显示仅27个非典型灶病作出明确的诊断或恶性倾向的诊断8个病灶(56.0%);对比后2到4个评分中有14个病变(29.0%)得分增加,19个病变仅增加1分,对比之前和之后45个病变的超声诊断评分,见表3。
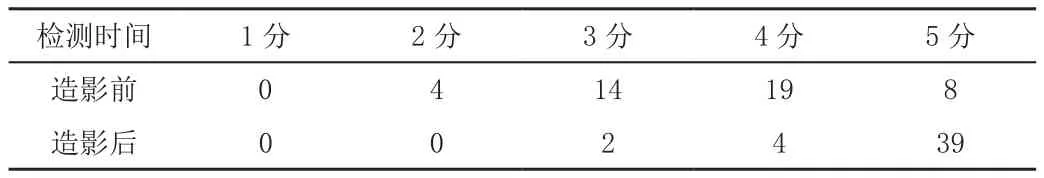
表3 45小肝癌超声造影前后超声诊断评分结果(个)
3 讨论
3.1 灌注时相与回声变化的特点
这项研究表明,以肝硬化为基础,小肝癌增强时相以及灌注的方式,最为典型的是动脉和实质期,门脉期和穿插更常见。对于肿瘤灌注而言,很可能和动脉期出现类似现象,从而对不断增强进行有效反应,另一种原因可能和实质期的回声有类似现象,因此在动脉期和实质期的灌注模式对于观察和鉴别更为有用。
3.2 对微小病灶的诊断
在这项研究中,有51.18%的病例因肝硬化而有小于2 cm的小病变,大多数超声检查并不典型,不足以证实或漏诊,对于这些未得到明确的病例,总共出现20个病灶难以确定,可以出现增生结节现象。采用的超声造影,容易引起增强和消退现象,这一特点不仅提高了小病变的检出率,而且为定性诊断提供了更加准确可靠的依据。在24个小病变中,一次被诊断出22个病变,疑似为恶性2个,在血管造影指导下的18G活检尚不清楚并明确诊断,在三个新发现的病变中,大小仅为0.8~1 cm。超声造影形成的小病变有助于提高肝肿瘤的早期发现率。

