单倍体造血干细胞移植治疗伴阵发性睡眠性血红蛋白尿克隆的重型再生障碍性贫血的临床效果
刘珍珍,卢润青,谢新生,姜中兴,何飞,樊冀鑫,赵海秋,郭荣
(郑州大学第一附属医院 血液内科,河南 郑州 450052)
阵发性睡眠性血红蛋白尿(paroxysmal nocturnal hemoglobinuria,PNH)与再生障碍性贫血(aplastic anemia,AA)关系密切,有研究报道PNH克隆可见于50%以上的初诊AA患者,部分起病时PNH克隆阴性的AA患者接受免疫抑制治疗(immunosuppressive therapy,IST)后PNH克隆转阳[1-2]。临床上伴PNH克隆的AA不易与PNH鉴别,表现为骨髓造血衰竭的PNH更难与AA等疾病鉴别。PNH患者荧光标记的嗜水气单胞菌溶素变异体(fluorescent aerolysin,FlAER)试验缺失率多高于20%,而伴PNH克隆的AA患者FLAER试验缺失率多低于20%[3]。但仍有部分AA患者初诊时PNH克隆可达60%~90%[1,4]。根据溶血和血栓形成风险,将PNH克隆>50%定义为大克隆,10%~50%为中克隆,<10%为小克隆[5-6],PNH克隆大小与AA患者血管内溶血风险呈线性相关[7],而PNH克隆大小及演变对AA患者移植疗效的影响尚不清楚。重型再生障碍性贫血(severe aplastic anemia,SAA)起病急、进展快,IST起效慢,复发率高,且易克隆演变为急性白血病,首选人类白细胞抗原(human leucocyte antigen,HLA)全相合同胞供者异基因移植,而对于缺乏全相合供者的SAA患者,已有研究证实单倍体造血干细胞移植(haploid hematopoietic stem cell transplantation,haplo-HSCT)是一种安全有效的治疗方案[8]。而PNH克隆大小对SAA患者haplo-HSCT疗效的影响报道较少,且多为单中心小样本研究[9]。本研究回顾性分析5例接受haplo-HSCT的伴PNH克隆的SAA患者的临床资料,探讨PNH克隆对haplo-HSCT疗效的影响。
1 资料与方法
1.1 一般资料回顾性分析2018年2月至2020年3月于郑州大学第一附属医院接受haplo-HSCT治疗的5例伴PNH克隆(4例大克隆,1例中克隆)的SAA患者的临床资料。5例患者均为男性,年龄19~35岁,中位年龄21岁。诊断标准参照《再生障碍性贫血诊断与治疗中国专家共识(2017年版)》[10]并经FlAER流式细胞术检测外周血 CD55/CD59 阴性红细胞、粒细胞、单核细胞(>5%定义为PNH克隆阳性)。初诊时PNH克隆大小为42.48%~74.74%,中位数为57.33%,无溶血等临床表现,酸化血清溶血试验、糖水试验、蛇毒因子溶血试验及尿含铁血黄素试验等均为阴性。诊断至移植时间为3~9个月,中位时间4个月,移植前治疗包括环孢素A、成分输血、雄激素及细胞生长因子等,血象、骨髓增生程度等未见明显好转,移植前复查PNH克隆大小为22.49%~62.62%,中位数为61.34%。供者选择按照郑州大学第一附属医院常规顺序(HLA相合同胞供者、HLA相合无关供者、HLA单倍体相同供者)确定,本研究中5例患者均为HLA单倍体供者,其中同胞单倍体供者4例,父亲供者1例。HLA位点相合度为5/10~7/10。所有患者均在移植前签署知情同意书。见表1。
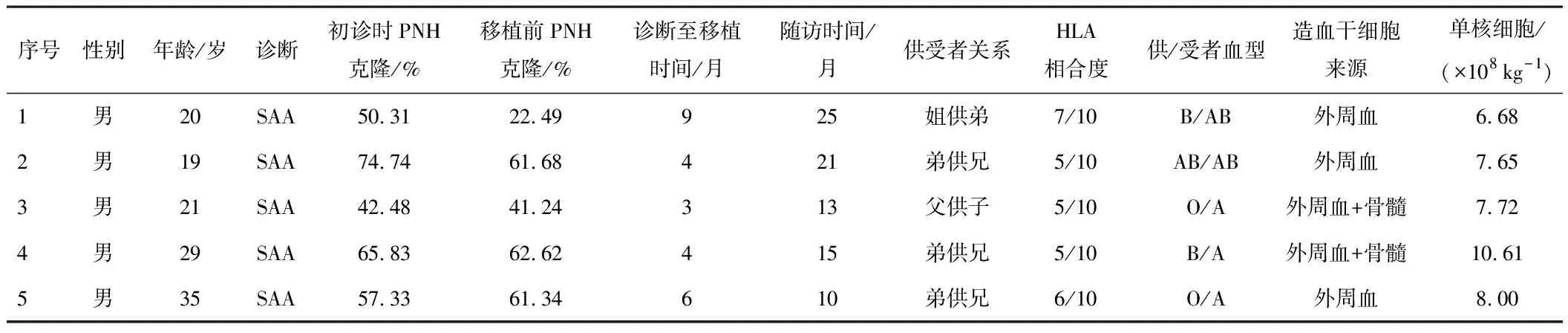
表1 5例伴PNH克隆的SAA患者的一般临床资料及供者情况
1.2 预处理方案采用BU+ FC+ATG方案预处理,具体如下:白消安(Otsuka Pharmaceutical Co.,Ltd.,国药准字H20150289)静脉滴注,3.2 mg·kg-1·d-1,2 d;氟达拉滨(重庆莱美药业股份有限公司,国药准字H20059418)静脉滴注,30 mg·m-2·d-1,4 d;环磷酰胺(Baxter Oncology GmbH,国药准字H20060467)静脉滴注,40 mg·kg-1·d-1,4 d;兔抗人胸腺细胞免疫球蛋白(Genzyme Polyclonals S.A.S,批准文号S20150036)静脉滴注,2.5 mg·kg-1·d-1,4 d。预处理期间给予保肝、护胃、水化、碱化、利尿及静脉滴注美司钠(江苏恒瑞医药股份有限公司,国药准字H10950007)解救等对症支持治疗。
1.3 移植物抗宿主病(graft versus host disease, GVHD)预防口服环孢素A(国药集团川抗制药有限公司,国药准字H10940044)和霉酚酸酯(国药集团川抗制药有限公司,国药准字H20080724)、静脉滴注甲氨蝶呤[Pfizer(Perth)Pty Limited,国药准字H20140205]预防GVHD,全血环孢素A谷浓度控制在150~250 μg·L-1。例3患者由于移植前使用环孢素A出现肝功能损伤,将环孢素A改为西罗莫司(华北制药股份有限公司,国药准字H20100079)口服治疗,全血西罗莫司谷浓度控制在5~10 ng·L-1。
1.4 造血干细胞采集与回输供者经粒细胞集落刺激因子10 μg·kg-1·d-1动员后,于第5天采集外周血造血干细胞,其中例3、例4供者采集外周血造血干细胞前在局麻下于髂后上棘采集骨髓液300~400 mL。回输的单核细胞数为(6.68~10.16)×108kg-1,中位数为7.72×108kg-1,CD34+细胞数为(5.50~11.47)×106kg-1,中位数为6.40×106kg-1。
1.5 造血重建及植入评价粒细胞植入定义为中性粒细胞绝对计数持续3 d>0.5×109L-1,血小板植入定义为无血小板输注情况下血小板持续7 d>20×109L-1,首日分别为粒细胞和血小板植入时间。采用性染色体荧光原位杂交、DNA短串联重复序列、血型检测等作为受者植入指标。
1.6 其他并发症的预防移植前9 d至移植后30 d持续静脉滴注低剂量肝素钠(齐鲁制药有限公司,国药准字H20030428)(血小板<20×109L-1时停用)、熊去氧胆酸(Bruschettini S.r.l,国药准字H20150398)、前列腺素E1(北京泰德制药股份有限公司,国药准字H10980023)预防肝静脉闭塞病。移植前2~9 d静脉滴注喷昔洛韦(浙江尖峰药业有限公司,国药准字H20070186)或阿糖腺苷(大同五洲通制药有限公司,国药准字H20084023)预防巨细胞病毒感染,之后改为阿昔洛韦片口服。移植后每周检测外周血巨细胞病毒DNA拷贝量,阳性者给予更昔洛韦(浙江亚太药业股份有限公司,国药准字H20045825)或膦甲酸钠(正大天晴药业集团股份有限公司,国药准字H20000442)静脉滴注治疗。静脉滴注卡泊芬净(Merck Sharp & Dohme Ltd.,国药准字H20171218)或伏立康唑(丽珠集团丽珠制药厂,国药准字H20064493)预防真菌感染。口服复方磺胺甲噁唑(山东新华制药股份有限公司,国药准字H37020649)预防肺孢子虫病。
1.7 随访采用住院检查、门诊及电话联系对所有患者进行随访。随访截止日期为2021年1月1日,随访时间为10~25个月,中位随访时间为15个月。
2 结果
2.1 造血重建及植入评价5例患者移植后均快速获得造血重建,粒细胞及血小板中位植入时间分别为14、16 d。造血重建后经短串联重复序列、性染色体荧光原位杂交及血型检测均证实为完全植入。其中1例患者(例3)于移植后48 d出现继发性植入功能不良,给予艾曲波帕口服、造血生长因子(粒细胞集落刺激因子、血小板生成素)皮下注射及输注血制品等治疗,未见明显效果。后皮下注射阿扎胞苷(Baxter Oncology GmbH,国药准字H20170238),每日100 mg,使用3 d,28 d为1个疗程,共应用4个疗程,第1个疗程结束14 d后复查血常规,中性粒细胞、血红蛋白及血小板较前明显回升,4个疗程后血常规恢复正常。在随访期内,5例患者血常规均正常,嵌合率均为100%。
2.2 GVHD及其他移植并发症GVHD:1例患者(例3)于移植后9个月发生慢性GVHD(皮肤3分),给予糖皮质激素治疗,西罗莫司改为他克莫司,症状未见明显好转,后给予间充质干细胞治疗,症状逐渐好转,未再发生GVHD相关表现;其余4例患者均未发生急性及慢性GVHD。感染性并发症:1例患者(例2)出现巨细胞病毒血症,给予抗病毒治疗后巨细胞病毒DNA定量逐渐降至正常;1例患者(例4)出现口腔黏膜炎,病原菌为多耐药铜绿假单胞菌,根据药敏试验结果,抗感染治疗后逐渐好转。其他并发症:1例患者(例2)于移植后98 d经PET-CT及组织活检明确诊断为巨细胞病毒相关移植后淋巴组织增殖性疾病(肝、结肠),环孢素A减量至停药,同时给予抗病毒治疗及静脉输注丙种球蛋白,并依次给予R-COP方案(利妥昔单抗+环磷酰胺+长春地辛+泼尼松)化疗2个疗程,利妥昔单抗(Roche Pharma AG,批准文号S20170002)单药治疗2个疗程,治疗结束后复查PET-CT提示肝内多发低密度结节消失,结肠回盲部周围软组织体积较前明显缩小,代谢活性降低,最大摄取标准值约1.5,现随访至移植后23个月,未见移植后淋巴组织增殖性疾病复发表现;1例患者(例3)出现出血性膀胱炎(Ⅲ度),给予水化、碱化、膀胱冲洗、抗病毒等治疗后好转。截至随访结束,5例患者均未发生疾病复发、肝静脉闭塞病、移植相关血栓性微血管病及血栓等并发症。
2.3 移植后PNH克隆演变及WT1基因表达PNH克隆:5例患者移植后1个月FlAER流式细胞术检测外周血PNH克隆均转阴。随访期内多次复查PNH克隆均为阴性,均未转化为临床型PNH。未出现血栓事件、溶血,多次查胆红素、乳酸脱氢酶、酸化血清溶血试验、糖水试验等均未见异常。WT1基因表达:2例患者(例3、例4)为鉴别骨髓增生异常综合征等疾病,采用聚合酶链式反应技术检测WT1基因,结果提示其表达升高(10.2/100~12.8/100),移植后1个月复查WT1基因,结果提示其降至正常范围(正常范围为<0.5/100),移植后定期检测WT1表达水平,波动于0/100~0.76/100。
3 讨论
PNH是一种罕见的获得性造血干细胞基因突变引起的克隆性疾病[11],即使给予最佳的支持治疗,其5 a病死率高达35%[12]。而PNH克隆不仅存在于PNH患者,也可见于AA等疾病。FlAER试验是检测PNH克隆的新方法,具有更高的特异度和灵敏度[13]。60%的AA患者伴有PNH克隆,其中10%~25%可能表现出克隆扩增并进展为临床PNH[11]。临床上伴PNH克隆的AA等不易与PNH鉴别,表现为骨髓造血衰竭的PNH更难与伴PNH克隆的AA等疾病鉴别。研究表明,经典型PNH患者PNH克隆明显大于伴PNH克隆的AA患者[6],伴PNH克隆的AA患者FlAER试验缺失率多低于20%[3],但仍有部分AA患者伴有PNH大克隆。PNH患者中可出现WT1基因表达升高,PNH患者的异常克隆细胞在敲除WT1基因后增殖能力减弱,提示WT1的过表达可能参与PNH患者异常克隆的优势增殖过程[14]。Shichishima等[15]发现PNH患者WT1mRNA表达水平与PNH克隆有关,且其表达水平高于AA组和正常对照组。可通过检测WT1基因定量初步鉴别伴PNH克隆的AA与PNH等疾病。然而,伴PNH克隆的AA患者WT1基因表达情况目前尚不清楚,本研究中有2例患者移植前检测了WT1基因,结果提示其表达均升高,移植后PNH克隆消失,WT1基因也转阴,提示伴PNH克隆的AA患者WT1基因表达水平升高,但需要扩大样本量后进一步研究证实。伴PNH克隆的AA与PNH等疾病的鉴别诊断仍然是临床工作的难点及重点,尤其是少数合并中/大克隆的AA患者,需全面考虑患者的病史、血管内溶血等临床表现及PNH克隆大小、WT1基因表达情况等指标。
SAA是一种严重的骨髓造血衰竭性疾病,根据再生障碍性贫血诊断与治疗中国专家共识(2017年版)[10],对于年龄≤35岁的SAA患者,首选HLA相合同胞供者异基因造血干细胞移植,其造血重建快,克隆性疾病发生率低,长期生存率高。无同胞全相合供者的SAA首选免疫抑制剂治疗。而对于伴PNH克隆的SAA患者,PNH克隆大小及其演变对预后的影响尚不明确。关于PNH克隆对接受IST的SAA患者的影响,已有研究报道了相互矛盾的结果[7,16-17]。目前相对一致的观点是,AA患者初诊时PNH克隆多为小克隆(<10%)且较稳定,部分患者PNH小克隆可消失,故初诊时伴PNH小克隆的AA患者,可按照AA给予规范性治疗,定期随访观察,检测PNH克隆变化即可。对于PNH克隆较大的AA患者,有研究发现PNH克隆大小与血管内溶血的发展呈线性关系[7],转化为临床PNH的可能性较大。然而抗胸腺细胞球蛋白、环孢素等免疫抑制剂起效较慢,治疗中易出现PNH克隆的扩增[18]。Lian等[5]对133例伴PNH克隆的AA患者进行免疫抑制剂治疗,其中34例(25.6%)PNH克隆较大,患者在中位随访时间11个月内出现血管内溶血,而异基因造血干细胞移植造血重建快。Lee等[19]对33例PNH或AA-PNH综合征患者行异基因造血干细胞移植,结果显示PNH克隆约在移植后2个月内转阴。刘立民等[20]报道了40例接受异基因造血干细胞移植(单倍型移植25例,全相合同胞移植15例)的PNH患者,对36例移植后存活的患者多次随访发现PNH克隆均为阴性。然而,目前关于异基因造血干细胞移植在伴PNH大克隆的SAA患者中研究较少。本研究中5例伴PNH克隆的SAA患者,4例为大克隆(PNH克隆>50%),1例为中克隆(PNH克隆为42.48%),均具有移植适应证,且缺乏HLA相合同胞供者,综合评估并结合患者意愿后行haplo-HSCT,PNH克隆均在移植后1个月转阴,未出现移植相关死亡,初步证实单倍体移植对伴PNH克隆的SAA患者可能具有一定的疗效。
异基因造血干细胞移植仍是SAA患者的一线治疗方案,对于伴PNH克隆的SAA也是如此[9]。移植供者的选择顺序通常是HLA相合同胞供者、HLA相合无关供者、单倍型供者。然而只有25%~30%的患者可找到全相合同胞供者[21-22],而查找无关供者耗时较长,可能会延误大部分SAA患者的治疗时机。haplo-HSCT作为重要的替代供者移植类型,几乎所有患者均可找到单倍体供者,且等待时间较短,供者依从性高。研究证实haplo-HSCT在SAA、PNH及AA-PNH综合征等疾病中显示出很好的疗效[8,20,23]。但GVHD、感染及植入失败/延迟植入等仍是SAA患者移植失败的主要原因。随着预处理方案、GVHD预防方案及感染防治的进展,单倍体移植在SAA中已取得与全相合移植类似的疗效。尽管PNH克隆常见于SAA患者,但是关于SAA移植疗效的报道很少考虑到PNH克隆的存在[21]。Gavriilaki等[9]对3例伴PNH大克隆(61%~82%)的SAA患者行造血干细胞移植,2例死于移植后早期急性GVHD及血栓相关多器官功能障碍综合征。但新的治疗方案可能会改善伴PNH大克隆的SAA患者的预后。有研究报道,对于PNH克隆较大的患者,移植前应用C5抑制剂Eculizumab桥接移植,或可减少血栓形成的风险,对于单倍体及无关供者移植同样有效[24]。也有研究认为移植后给予Eculizumab维持治疗,可预防移植后血栓形成,且不增加感染、植入失败等风险[25],尽管如此,预处理过程中仍可能会出现补体激活,从而增加血管内溶血的风险,异基因造血干细胞治疗伴PNH克隆的SAA患者仍有诸多挑战,移植前后需定期检测患者PNH克隆大小及演变,预防血栓、血管内溶血的发生。本研究对5例伴PNH克隆的SAA患者行单倍体移植,其中1例出现继发性植入不良,1例出现慢性GVHD,1例出现移植后淋巴组织增殖性疾病,均在治疗后好转,在随访时间内无移植后死亡病例,未发生PNH转化及PNH克隆相关溶血、血栓事件,可能与诊断至移植时间较短有关,且PNH克隆在移植后1个月内转阴,但本研究病例较少,随访时间较短,仍需进一步研究证实。
总之,haplo-HSCT对于有移植指征的伴PNH克隆的SAA患者,可能具有一定的疗效,但仍需关注GVHD、植入不良、血栓等并发症,随着移植技术的进步及补体抑制剂的应用,其移植疗效将进一步改善。

