二花脸猪linc-NORFA核心启动子鉴定与转录调控分析
杜星,曾强,刘禄,李琦琦,杨柳,潘增祥,李齐发
二花脸猪linc-核心启动子鉴定与转录调控分析
杜星,曾强,刘禄,李琦琦,杨柳,潘增祥,李齐发
南京农业大学动物科技学院,南京 210095
【】前期研究证实linc-作为母猪繁殖性状候选基因参与调控卵泡闭锁与卵泡颗粒细胞凋亡过程,进一步鉴定二花脸猪linc-核心启动子并分析其转录调控机制,为解析linc-介导猪卵泡闭锁的分子机制奠定理论基础并提供新的研究思路。采集二花脸猪耳组织样品并提取基因组DNA,利用PCR扩增和测序技术获得二花脸猪linc-5′调控区序列;通过构建缺失表达荧光报告载体并利用荧光素酶活性试验鉴定二花脸猪linc-核心启动子;利用生物信息学分析二花脸猪linc-核心启动子区序列特征与潜在的转录因子结合位点;构建猪真核生物表达载体并进一步采用Western blot、qRT-PCR以及荧光素酶活性试验分析转录因子FOXO1过表达对二花脸猪linc-转录的影响;利用染色质免疫沉淀(ChIP)技术鉴定转录因子FOXO1与二花脸猪linc-核心启动子区的结合能力。通过克隆测序与序列拼接共获得二花脸猪linc-5′调控区序列1 734 bp,其中包含两个潜在的CpG岛;利用荧光素酶活性试验证实linc-核心启动子位于-988 — -684 bp(转录起始位点作为+1),生物信息学分析表明二花脸猪linc-核心启动子上包含多个转录因子的结合元件,例如ESR2、FOXO1、E2F1、BRCA1以及NFIC等;另外,ChIP试验还证实在猪卵巢颗粒细胞中FOXO1作为转录因子直接靶向结合在linc-的核心启动子区;进一步通过试验证实FOXO1过表达可显著下调linc-核心启动子区活性(<0.01),同时显著抑制体外培养的猪卵巢颗粒细胞中linc-的表达(<0.01)。鉴定了二花脸猪linc-核心启动子区,同时证实FOXO1作为转录因子能够与linc-核心启动子区特异性结合,进而抑制后者的转录活性与表达。研究结果对探究linc-在猪卵泡闭锁过程中显著下调的分子机制具有重要意义。
二花脸猪;卵巢颗粒细胞;Linc-;核心启动子;转录调控
0 引言
【研究意义】卵泡的正常发育与排卵对于维持雌性哺乳动物繁殖过程至关重要[1],而卵泡闭锁作为雌性哺乳动物卵巢中一种普遍的生理现象,过度的卵泡闭锁严重制约了雌性哺乳动物繁殖力的发挥[2]。因此,探究卵泡闭锁的分子机制对于减少卵泡闭锁、提高排卵率以及维持雌性哺乳动物正常的繁殖过程具有重大意义。本研究为鉴定linc-的核心启动子区及其转录调控机制提供理论基础,同时对解析二花脸猪高繁殖力性状的形成机制具有一定意义。【前人研究进展】长链非编码RNA(long non-coding RNA,lncRNA)是一类长度大于200 nt且缺乏开放阅读框(open reading frame,ORF)或编码蛋白能力的内源性RNA分子[3-4]。前人研究通过生物信息学分析与高通量测序技术在哺乳动物体内鉴定了数以千计的lncRNAs,然而仅有极少数lncRNAs经过系统的研究并具有完备的功能注释,绝大多数lncRNAs的生物学功能、作用机制及表达调控模式仍不清楚[5-6]。现阶段研究指出lncRNAs的表达丰度较低、进化保守性与稳定性较差、且具有严格的组织特异性表达模式,这些特点也成为了研究lncRNAs过程中的难点[7]。近年来,相关研究表明lncRNAs广泛参与调控生物体内多种重要的生理与病理过程[8],同时鉴定了若干与雌性哺乳动物繁殖过程相关的lncRNAs。例如,通过构建基因敲除小鼠模型证实与对于雌性小鼠卵巢中黄体形成、附植准备以及类固醇激素合成等生理过程起到至关重要的作用[9-10];而在对多囊卵巢综合征患者的研究中发现linc-能够通过促进KIP1降解进而抑制卵巢颗粒细胞生长[11];另外,Li等通过研究证实能够通过抑制P21介导的ERK/MAPK信号通路促进人卵巢颗粒细胞增殖水平[12]。目前lncRNAs对于雌性哺乳动物卵巢功能与繁殖过程的影响程度尚不清楚,并且其对猪等大型家畜卵巢发育与功能的调控还未见报道。【本研究切入点】笔者前期鉴定了一个与二花脸猪高繁殖力相关的基因间长链非编码RNA(long intergenic non-coding RNA,lincRNA)即linc-。进一步分析发现二花脸猪卵巢颗粒细胞中linc-的表达水平显著高于西方猪种(如大白猪),且在闭锁卵泡中表达下调[13],表明其表达水平与猪繁殖力和卵泡发育命运相关。但目前关于linc-的转录调控鲜有报道。【拟解决的关键问题】以二花脸猪linc-为研究对象,通过多种分子生物学手段鉴定其核心启动子区,并对其序列特征进行分析;预测其转录因子结合位点,同时分析转录因子对二花脸猪linc-转录的影响。研究结果对揭示猪卵巢中linc-转录调控机制、解析二花脸猪高繁殖力性状的形成机制具有一定意义。
1 材料与方法
1.1 材料
1.1.1 实验动物 二花脸母猪耳组织样品来源于江苏焦溪二花脸核心育种场。取耳组织样品放置于液氮中长期保存,并用于后续提取二花脸猪基因组DNA;采集18月龄发情商品母猪双侧新鲜卵巢,置于37℃含有庆大霉素的生理盐水中,并于2 h内带回实验室,用于后续卵巢颗粒细胞的体外培养。
1.1.2 试验试剂 2×Vazyme LAmp Master Mix、AceQ QPCR SYBR Green Master Mix(南京诺唯赞生物科技有限公司)。PrimeScriptTMRT Master Mix反转录试剂盒(大连宝生物工程公司)。Trizol、Lipofectamine 3000转染试剂(Invitrogen公司)。荧光素酶活性检测试剂盒(Promega公司)2 kb DNA marker、Agarose粉末、10×TBE buffer、2.5 mol·L-1甘氨酸、5 mol·L-1氯化钠和pMD19-T载体(南京擎科生物科技有限公司)。37%多聚甲醛(南京晚晴生物有限公司)。DMEM/F12培养基、胎牛血清、青链霉素和PBS溶液(Gibico公司)。限制性内切酶I与I、T4连接酶(赛默飞世尔科技有限公司)。RIPA裂解液、BCA蛋白定量试剂盒(上海碧云天生物技术有限公司)。DEPC水、ECL化学发光液、Protein A+G beads与IgG抗体(Bioworld生物公司)。FOXO1一抗和蛋白酶抑制剂(CST公司)。GAPDH一抗、山羊抗兔二抗(上海生工生物有限公司)。氯仿、无水乙醇、异丙醇、异戊醇、氯化钠、EDTA等均为国产分析纯试剂。
1.1.3 试验地点 本试验于2020年2—6月在南京农业大学动物科技学院分子数量遗传学实验室完成。
1.2 试验方法
1.2.1 基因组DNA提取 采用氯仿-异戊醇法从二花脸猪耳样品中抽提基因组DNA,通过1.0%的琼脂糖凝胶电泳检测基因组DNA的质量与完整性(电压130V,电泳25 min),同时使用NanoDrop 3000核酸定量系统对DNA浓度进行检测。纯化后的二花脸猪基因组DNA置于-20℃环境中保存并用于后续试验。
1.2.2 引物设计与合成、PCR扩增与测序 根据NCBI GenBank数据库中猪linc-序列(MK879596.1)设计特异性引物扩增二花脸猪linc-5′调控区序列,引物由南京擎科生物科技有限公司合成,具体序列见表1。PCR扩增体系(50 μL)如下:上、下游引物各2.5 μL、二花脸猪基因组DNA 2.5 μL、2×Vazyme LAmp Master Mix酶25 μL、加双蒸水至50 μL。PCR反应程序为:95℃预变性2 min;95℃变性10 s,60℃退火15 s,72℃延伸40 s,共30个循环;最后72℃延伸5 min;4℃保存。PCR产物经1.5%琼脂糖凝胶电泳鉴定后,切取目的条带经纯化克隆入pMD19-T载体上,随后经转化后挑取单克隆送至上海生工生物有限公司进行测序。
1.2.3 生物信息学分析 采用Promoter 2.0 PredictionServer在线软件(http://www.cbs.dtu.dk/services/Promoter/)与BDGP数据库(https://fruitfly.org/seq_tools/promoter. html)对二花脸猪linc-的潜在核心启动子区进行初步预测。利用BioEdit v7.0软件对二花脸猪linc-核心启动子区碱基组成进行分析。进一步采用JASPAR在线公共数据库(http://jaspar.genereg. net/)分析二花脸猪linc-基因核心启动子区上潜在的转录因子结合位点,具体使用方法参考文献[14]。利用EMBOSS Cpgplot与MethPrimer在线分析系统对二花脸猪linc-基因5′调控区上潜在的CpG岛进行预测。
1.2.4 载体构建与荧光素酶活性试验 本研究采用双酶切法进行载体构建,具体过程如下:设计带有酶切位点的特异性引物扩增不同长度的二花脸猪linc-5′调控区片段,引物信息详见表1。利用限制性内切酶I与I将纯化后的扩增片段置于37℃金属浴中进行酶切反应1 h,随后与带有相同黏性末端的pGL3-Basic线性载体进行连接(16℃过夜),连接产物经转化、挑取单克隆、测序最终获得相应的阳性重组质粒。将无内毒重组质粒瞬时转染进入体外培养的颗粒细胞24 h后,采用荧光素酶活性检测试剂盒对每个样品的萤火虫荧光与海肾荧光进行检测,具体操作详见说明书,相对荧光活性为萤火虫荧光与海肾荧光的比值。
1.2.5 猪卵巢颗粒细胞体外培养与转染 将新鲜采集的健康母猪卵巢用含有庆大霉素的生理盐水和体积分数为75%的酒精溶液反复清洗数次。颗粒细胞的分离培养方法参考文献[15]进行,简述如下:利用无菌医用注射器吸取有腔卵泡(直径为3—5 mm)中的颗粒细胞,将分离的颗粒细胞利用PBS清洗两次后均匀置于细胞培养板中进行培养,培养基的主要成分如下:DMEM/F12基础培养基、体积分数为15%胎牛血清以及体积分数为1%的青链霉素。细胞放置于37℃、5% CO2的湿度培养箱中进行培养。采用Lipofectamine 3000转染试剂将本试验构建的重组质粒瞬时转染进入体外培养的颗粒细胞,具体操作详见使用说明。
1.2.6 RNA提取与qRT-PCR检测 采用TRIzol提取颗粒细胞总RNA,具体操作步骤按参考文献[16]进行。纯化后的RNA采用PrimeScriptTMRT Master Mix反转录试剂盒进行反转录,反应体系为:500 ng总RNA,反转录酶2 μL,加入去离子水至10 μL;反应条件为:37℃反应15 min,85℃反应5 s,反转录产物置于-20℃保存。根据猪linc-、(NM_214014.3)以及序列(NM_001206359.1)设计定量引物(表1),并采用qRT-PCR方法对上述3个基因表达水平进行检测。qRT-PCR反应体系如下:上、下游引物各0.2 μL,ROX II 0.2 μL,cDNA模板0.6 μL,AceQ QPCR SYBR Green Master Mix酶5 μL,加水至10 μL;反应程序如下:预变性95℃ 5 min,循环反应95℃ 10 s、60℃ 30 s、40个循环,溶解曲线95℃ 15 s、60℃ 60 s、95℃ 15 s。以作为内参基因,使用2-∆∆CT法计算目的基因的相对表达水平。
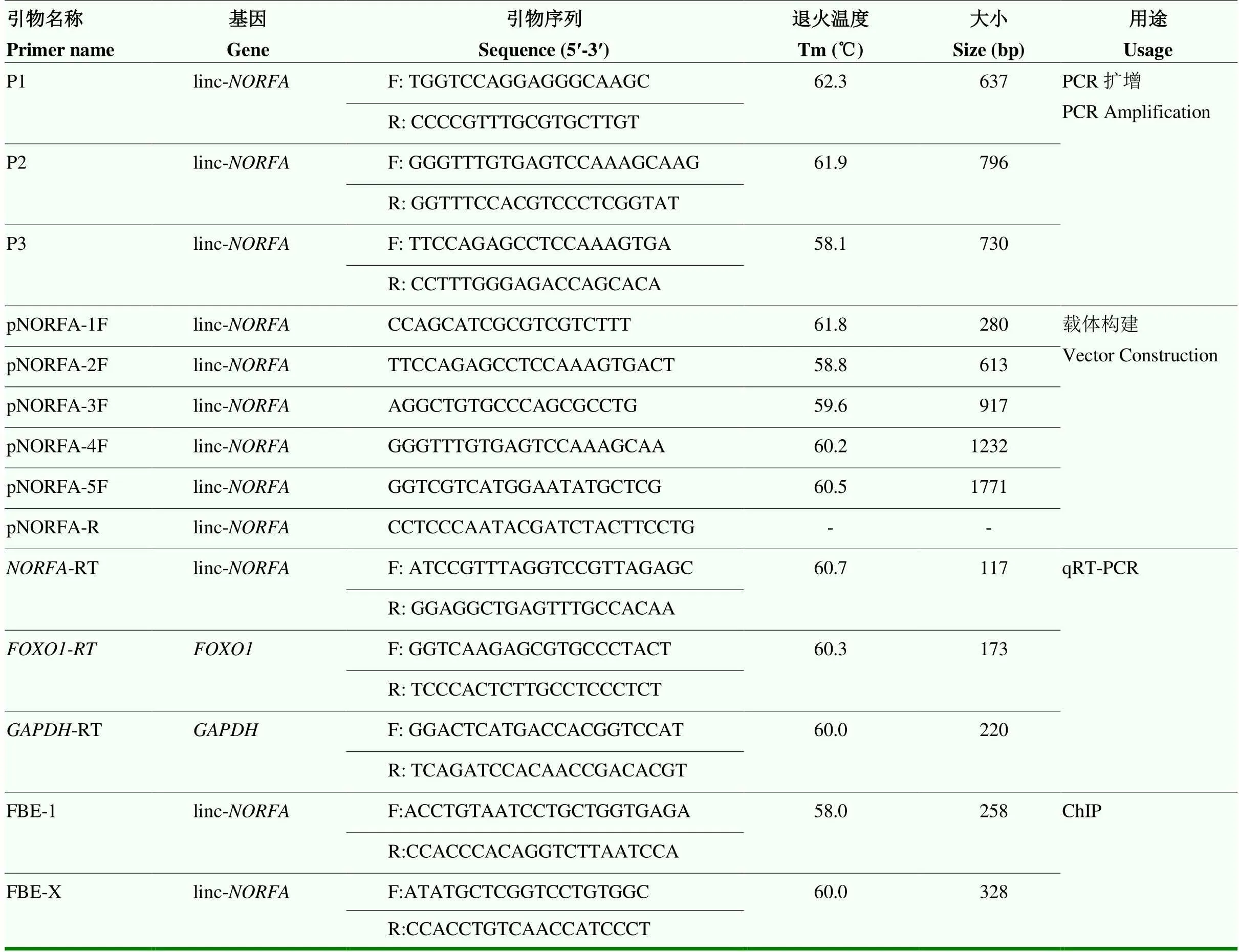
表1 本试验所用引物
1.2.7 Western blot试验 体外培养的颗粒细胞转染48 h后, 使用RIPA裂解液提取并收集颗粒细胞中总蛋白,利用BCA法对蛋白浓度进行检测。通过蛋白免疫印迹法(Western blot)对转染FOXO1过表达载体后猪卵巢颗粒细胞中FOXO1的蛋白水平进行检测,具体操作方法和步骤参见文献[16]。本试验中使用的抗体采用体积分数为0.25%的牛血清蛋白溶液进行稀释(1﹕1000)。蛋白条带在暗室中使用ECL化学发光液进行显色并曝光,利用Image J对蛋白灰度值进行分析,以GAPDH蛋白表达水平作为标准进行内部对照。
1.2.8 染色质免疫沉淀(ChIP)试验 将卵巢颗粒细胞体外培养于10 cm细胞培养皿48 h后, 在培养基中依次加入37%多聚甲醛135 μL、2.5 mol·L-1甘氨酸220 μL,并置于37℃水平摇床上110 r/min混摇10 min,促使蛋白质与染色质交联。收集细胞并利用超声波破碎仪将染色质碎片化,超声波破碎仪参数设置如下:40%输出功率,30个循环,每个循环打开破碎5 s、关闭冷却15 s。随后,在该体系中依次添加蛋白酶抑制剂和预先配置好的Protein A+G beads与FOXO1一抗混合物,并置于4℃环境下混摇孵育过夜,充分调取FOXO1-DNA复合物。最后利用5 mol·L-1氯化钠溶液反交联与洗脱过程获得卵巢颗粒细胞中FOXO1富集的DNA片段。在本试验中IgG一抗添加组作为阴性对照组,而基因组DNA作为阳性对照组的底物。设计引物FBE-X(FOXO1 binding element-X)扩增不含有FOXO1结合位点的DNA片段用于检验FOXO1的非特异性结合情况。根据二花脸猪linc-核心启动子区上FOXO1的结合位点位置信息设计检测引物FBE-1,引物信息详见表1。
1.3 统计分析
利用SPSS Statistics v20.0和GraphPad Prism v6软件进行差异显著性分析。试验结果以平均值±标准误(mean±SEM)的形式表示,两组不同处理间显著性采用双尾检验进行分析。*表示差异显著(≤0.05),**表示差异极显著(≤0.01)。
2 结果
2.1 二花脸猪linc-NORFA5′调控区扩增与克隆测序
设计3对特异性引物P1—P3(表1)扩增二花脸猪linc-5′调控区,均能在最适退火温度下得到单一清晰、且符合预期大小的电泳条带(图1-A)。将目的条带分别进行切胶回收、纯化、克隆测序与序列拼接最终获得二花脸猪linc-5′调控区序列,且序列长度为1 734 bp(图1-B)。
2.2 二花脸猪linc-NORFA5′调控区序列分析
利用BioEdit v7.0生物信息学分析软件对上述试验获得的二花脸猪linc-5′调控区序列核苷酸序列的碱基构成进行分析,其中包含A碱基284个、T碱基317个、C碱基489个以及G碱基644个(图2-A),AT碱基含量(34.7%)明显低于CG含量(65.3%)(图2-B)。随后利用EMBOSS Cpgplot与MethPrimer在线分析系统并以CpG island size>100、CG%>50%以及Obs/Exp>0.6为标准发现二花脸猪linc-基因5′调控区上存在两个潜在的CpG岛,分别命名为Island 1(-1 327 — -1 021)与Island 2(-653— -547),且两个CpG岛的长度分别为307 bp与107 bp(图2-C)。
2.3 二花脸猪linc-NORFA核心启动子区鉴定
根据上述试验获得的二花脸猪linc-5′调控区序列与生物信息学分析结果,设计了5对特异性引物(表1)扩增不同片段长度的linc-5′调控区片段,并成功构建相应的缺失表达荧光报告载体(图3-A)。随后分别将重组质粒转染进入体外培养的猪卵巢颗粒细胞中,荧光素酶活性试验结果显示pNORFA-1与pNORFA-2的荧光活性无显著差异,pNORFA-3的荧光活性显著高于pNORFA-2(<0.01,图3-B),表明二花脸猪linc-基因核心启动子区位于-988 bp — -684 bp(转录起始位点作为+1)。
2.4 二花脸猪linc-NORFA核心启动子区序列特征分析
通过序列分析发现二花脸猪linc-核心启动子区由305个碱基组成,其中A碱基为38个(12.5%),T碱基为74个(24.3%),C碱基个数为72个(23.6%),G碱基个数为121个(39.6%),嘧啶碱基(GC)含量(63.2%)明显高于嘌呤碱基(AT)含量(36.8%)且与linc-5′调控区核苷酸序列碱基构成基本一致。进一步分析发现linc-核心启动子区包含10个潜在的甲基化位点(CG位点),暗示其转录可能受到DNA甲基化的影响(图4-A)。利用生物信息学分析发现二花脸猪linc-核心启动子区上包含多个转录因子的潜在结合位点,例如ESR2、FOXO1、BRCA1、E2F1、KLF4和NFIC等。进一步通过生物信息学分析上述潜在转录因子与二花脸猪linc-核心启动子区结合位点的定位、相似度以及评价得分,结果如图4-B所示。
2.5 二花脸猪转录因子FOXO1真核表达载体构建
通过生物信息学分析发现转录因子FOXO1与二花脸猪linc-启动子区具有较高结合能力,同时FOXO1作为促凋亡因子在哺乳动物卵泡闭锁过程中发挥重要功能[17],因此我们选择了转录因子FOXO1进行后续研究。首先将二花脸猪编码区全序列扩增克隆进入真核生物表达载体pcDNA3.1上,并将该重组质粒命名为pcDNA3.1-(图5-A)。随后又将重组质粒pcDNA3.1-瞬时转染进入体外培养的猪卵巢颗粒细胞中,qRT-PCR和Western blot结果显示FOXO1过表达能够显著上调颗粒细胞中mRNA(图5-B,<0.01)与蛋白表达水平(图5-C,<0.01),表明二花脸猪转录因子FOXO1真核生物表达载体构建成功。
2.6 转录因子FOXO1对猪卵泡颗粒细胞中linc- NORFA转录的影响
为了进一步探究转录因子FOXO1对二花脸猪linc-转录的影响,我们将上述构建的猪真核生物表达载体pcDNA3.1-瞬时转染体外培养的猪卵巢颗粒细胞中。qRT-PCR结果显示FOXO1过表达后颗粒细胞中linc-的表达水平显著下调(图6-A,<0.01)。另外,通过荧光素酶活性试验证实FOXO1过表达能够显著抑制linc-核心启动子区转录活性(图6-B,<0.01)。随后,通过ChIP试验证实在猪卵巢颗粒细胞中,FOXO1作为转录因子能够与linc-核心启动子区特异性结合(图6-C)。最后利用双氧水诱导颗粒细胞氧化应激模型证实氧化应激能够显著诱导体外培养的猪卵巢颗粒细胞中的表达(图6-D,<0.01),同时显著抑制linc-的表达水平(图6-E,<0.05)。上述结果表明在猪卵巢颗粒细胞中,转录因子FOXO1能够通过与linc-核心启动子结合进而下调其转录活性并显著抑制其表达。

(A)M:2 kb DNA marker;P1-P3:PCR扩增产物;(B)二花脸猪linc-NORFA基因5′调控区序列
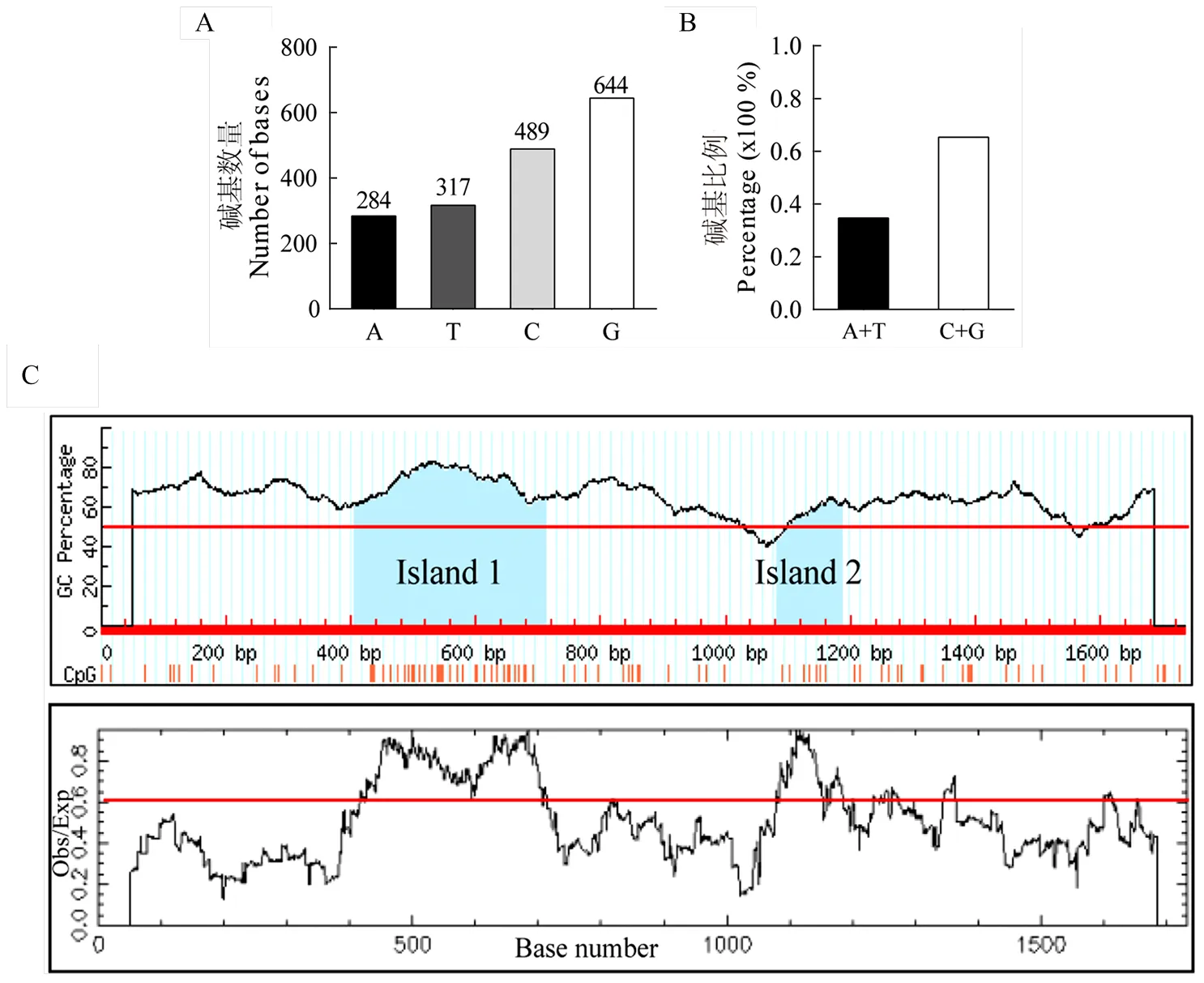
(A)核苷酸组成;(B)核苷酸比例;(C)CpG岛分析
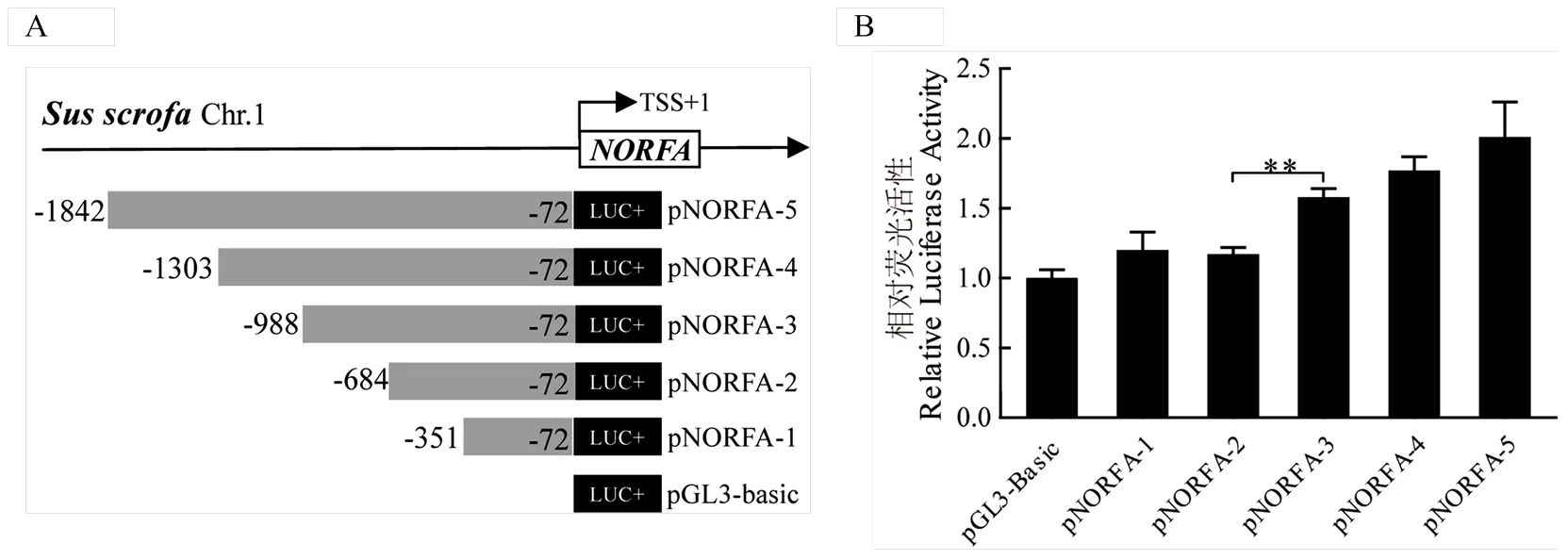
(A)载体构建示意图;(B)荧光素酶活性试验(A) Plasmids construction; (B) Luciferase activity assays
3 讨论
雌性哺乳动物原始卵泡库中卵泡数量巨大,但仅有极少数卵泡能够最终发育成熟并排卵,绝大多数卵泡在发育的各个阶段发生闭锁并退化[18]。现阶段研究普遍认为卵巢颗粒细胞凋亡是引起卵泡闭锁的主要诱因[19],而卵巢颗粒细胞凋亡则受到一个由多种体内外因素组成的复杂调控网络的影响,包括类固醇激素[16]、应激[20]、有毒物质与药品[21]、细胞因子[22]以及表观遗传学因子等,其中三类表观遗传学因子现已证实参与调控母猪等雌性哺乳动物卵巢颗粒细胞凋亡过程,即miRNAs(miR-425、miR-10b)[23-24]、circRNAs(circINHA)[25]以及lncRNAs(linc-)[13]。并且,越来越多的证据表明lncRNAs在维持雌性哺乳动物卵泡正常发育与排卵过程中扮演着重要的角色,本研究团队通过RNA-seq也证实卵泡闭锁过程中卵巢颗粒细胞内一系列lncRNAs发生差异表达,但目前关于lncRNAs的转录调控机制尚未完全明晰。在基因结构上lncRNAs与mRNAs相似,均通过聚合酶II来介导转录起始,且绝大多数lncRNAs也具有稳定的启动子并在转录后形成典型的5′帽子结构(5′-capped)和多聚腺苷酸结构(poly-A)[26-27];进一步分析发现lncRNAs在基因组上转录区域的染色质特征与mRNAs也极其相似,两者的转录起始位点均具有高水平H3K4me3组蛋白甲基化修饰特征,而在转录区域内均含有较高水平H3K36me3甲基化修饰标记[28];同时根据现有报道指出lncRNAs与mRNAs的转录均可受到转录因子的调控[29]。本研究通过鉴定并分析二花脸猪linc-的核心启动子发现多个潜在转录因子结合位点,同时进一步证实转录因子FOXO1能够通过下调二花脸猪linc-核心启动子区转录活性进而抑制其表达。
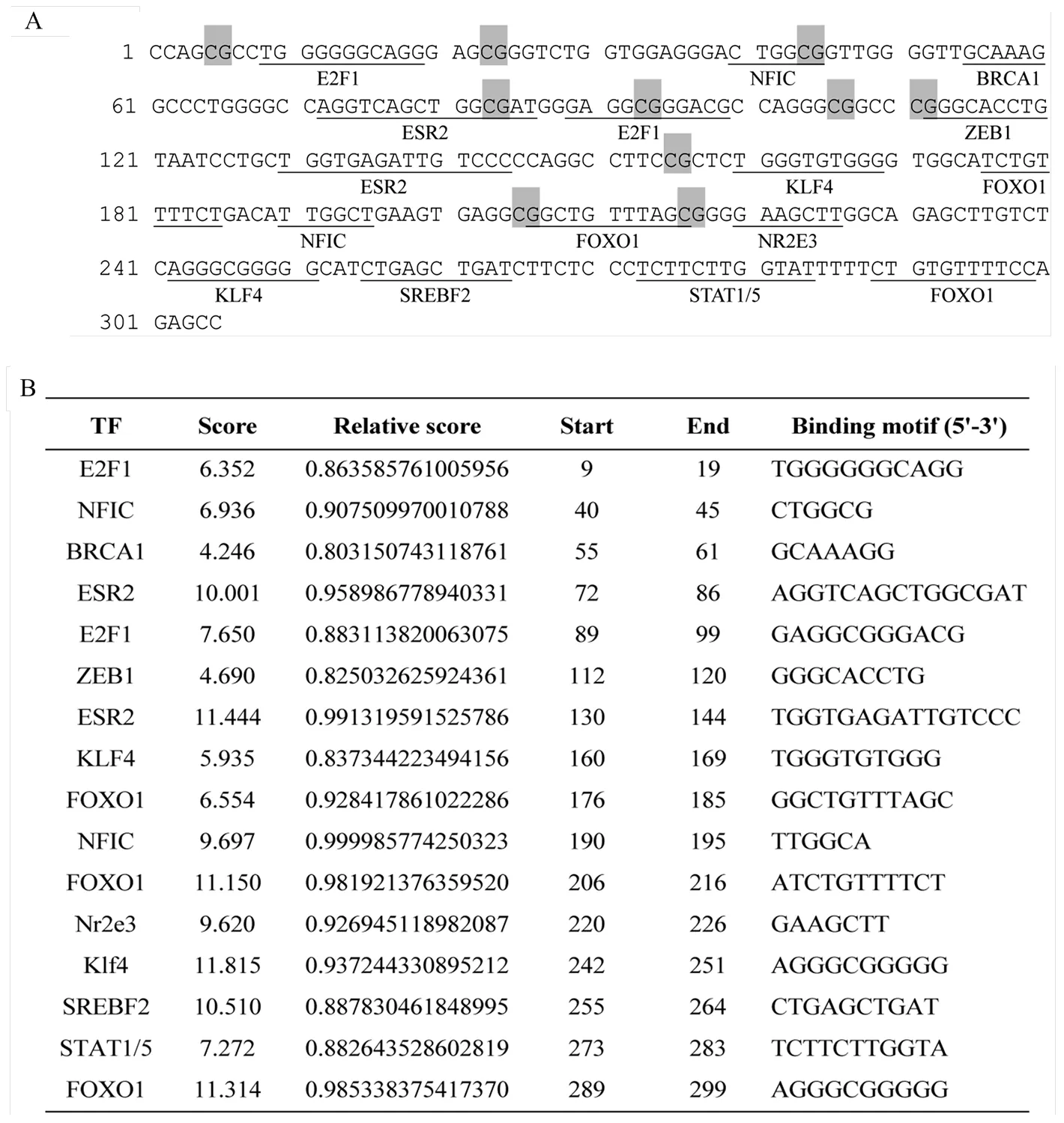
(A)灰色底纹代表甲基化位点,下划线标注代表转录因子结合位点;(B)潜在转录因子结合位点生物信息学分析
除此之外,我们在二花脸猪linc-核心启动子区上还发现了多个与哺乳动物卵泡发育与颗粒细胞状态和功能调控相关转录因子的结合位点,例如ESR2、BRCA1、E2F1以及KLF4等。雌二醇(E2)主要由卵巢颗粒细胞合成与分泌,卵泡液中低水平E2是猪卵泡闭锁的重要特征之一,同时雌二醇-雌激素受体系统(E2-ESR2)对于维持雌性生殖系统健康与功能至关重要[30-31]。通过对不同雌性哺乳动物进行研究发现E2能够促进卵巢颗粒细胞增殖,同时抑制颗粒细胞凋亡,而E2缺乏或E2-ESR2系统功能丧失则会产生相反的结果[32-33]。近年来,通过高通量测序技术证实E2能够诱导不同类型细胞中lncRNAs表达文库发生剧烈变化[34-35]。而的表达上调与猪卵巢颗粒细胞氧化应激介导的细胞凋亡以及基因组的不稳定性密切相关[36];另外,KLF4过表达能够显著促进大鼠颗粒细胞凋亡,同时显著抑制细胞增殖[37],随后相关试验证实KLF4能够促进氧化应激介导的颗粒细胞凋亡过程[38]。根据上述研究成果与本研究结果我们提出如下假设,即猪卵泡闭锁发生过程中伴随着大量转录因子发生显著变化,而这些功能差异转录因子的动态变化进一步影响了它们与linc-核心启动子区的结合,从而改变linc-的转录调控模式。上述猜想或可部分解释二花脸猪linc-在卵泡闭锁过程中显著下调的分子机制,后续研究将着重探讨转录因子的动态变化对猪卵泡闭锁过程中linc-表达调控的影响。
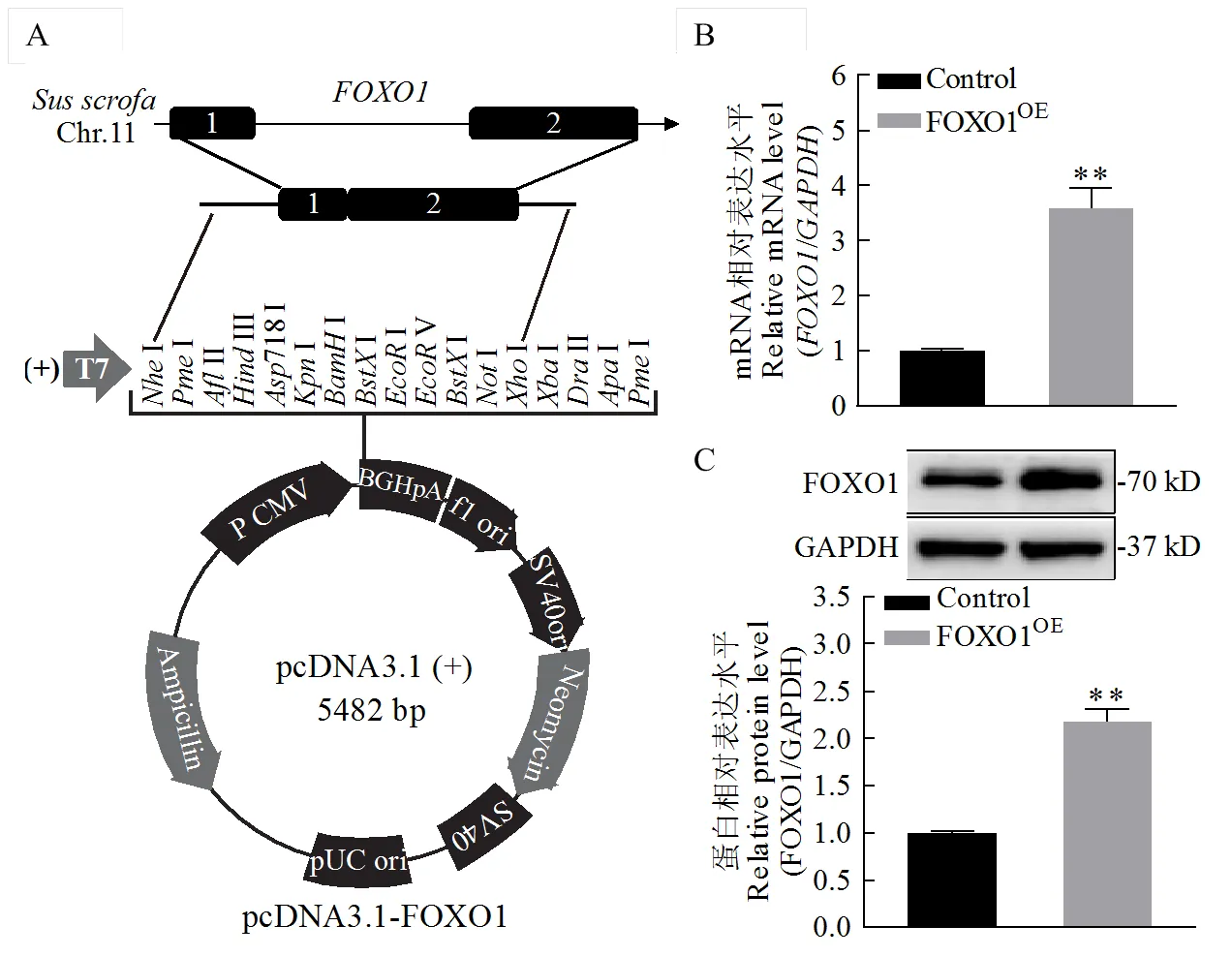
(A)pcDNA3.1-FOXO1构建示意图 Diagram showing the construction of pcDNA3.1-FOXO1;
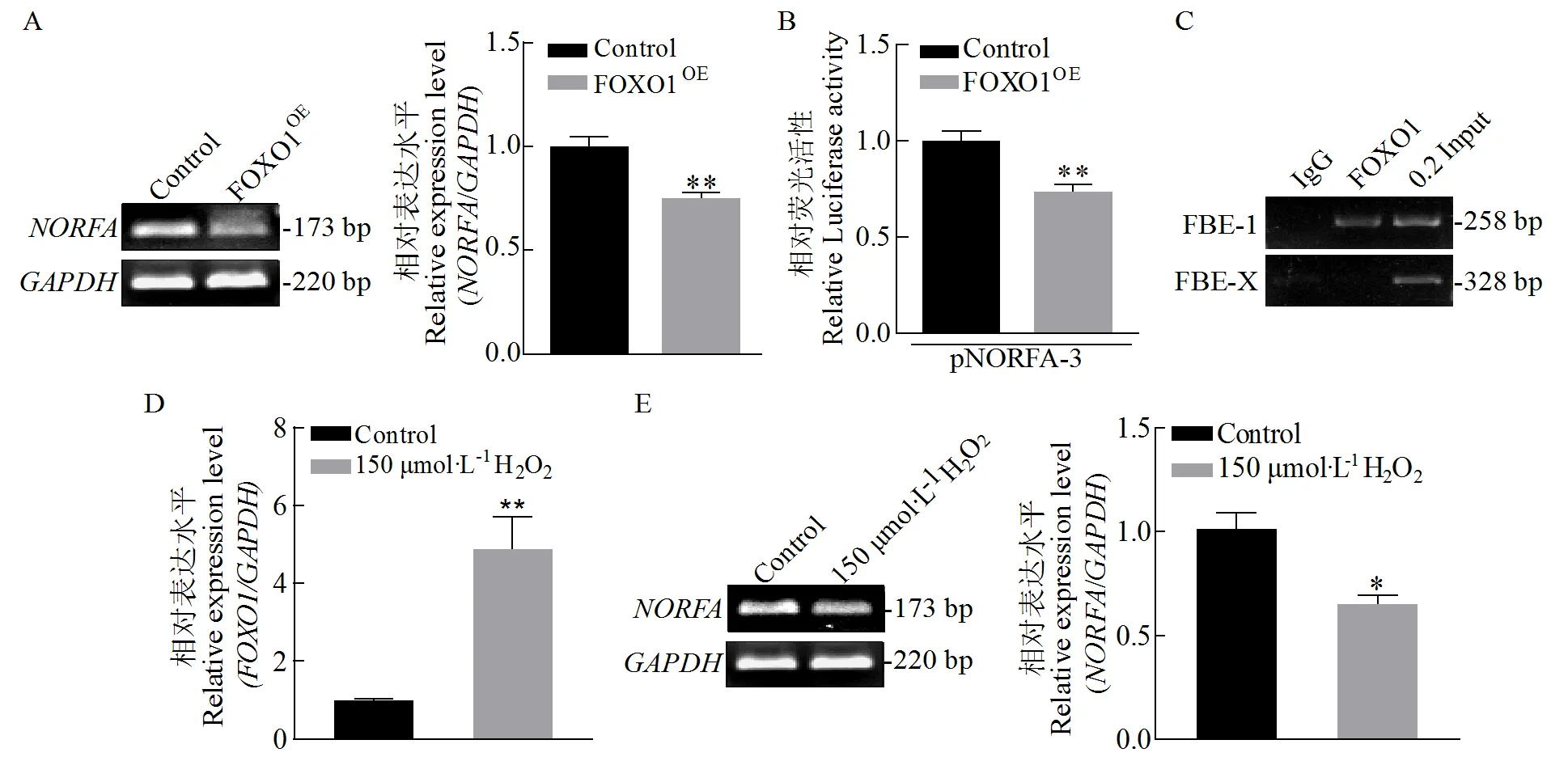
(A)过表达FOXO1对linc-NORFA表达水平的影响;(B)过表达FOXO1对linc-NORFA核心启动子活性的影响;(C)通过ChIP试验鉴定FOXO1与linc-NORFA核心启动子的结合丰度;(D)双氧水诱导氧化应激对FOXO1表达水平的影响;(E)双氧水诱导氧化应激对linc-NORFA表达水平的影响
笔者前期研究证实在猪卵巢颗粒细胞中linc-能够通过miR-126/TGFBR2轴上调TGF-β信号通路活性,进而抑制猪卵巢颗粒细胞凋亡过程[13]。结合本研究结果,可以猜想FOXO1可能通过linc-/miR-126/TGFBR2轴调控猪卵巢颗粒细胞中TGF-β信号通路活性以及颗粒细胞状态。现阶段研究表明FOXO1与TGF-β信号通路互作广泛存在于哺乳动物各个组织、器官以及细胞中,并且介导了多种重要细胞生理过程的发生。例如,TGF-β信号通路通过影响FOXO1的表达与活性从而调控肝糖异生[39]、肾纤维化[40]以及巨噬细胞极化[41]等过程;而FOXO1的异常表达则能够影响TGF-β信号通路活性或成员表达,进而调控胶质母细胞瘤增殖[42]、疤痕修复[43]以及软骨分化[44]等过程。然而,在雌性哺乳动物卵巢发育与功能发挥过程中FOXO1与TGF-β信号通路互作的研究尚未见报道。综合本研究结果,我们在猪卵巢颗粒细胞中发现FOXO1与TGF-β信号通路可能存在互作关系,且该互作可能由一个不同类型RNA分子组成的新调控轴介导,即linc-/miR-126/TGFBR2轴,并最终参与调控猪卵泡闭锁与卵巢颗粒细胞凋亡过程。
4 结论
本研究通过生物信息学分析与多种分子生物学实验技术鉴定了二花脸猪linc-的核心启动子区(-988 — -684 bp),并在其核心启动子区上发现多个与基因转录调控相关的作用元件,包括甲基化位点与转录因子结合位点等;构建猪真核生物表达载体并证实转录因子FOXO1通过与二花脸猪linc-核心启动子区结合,进而显著抑制后者在猪卵巢颗粒细胞中的表达。上述发现为解析二花脸猪linc-在猪卵泡闭锁过程中显著下调的分子机制提供了理论依据,同时为进一步揭示猪卵泡闭锁的调控网络拓展了新的方向。
[1] VOLLENHOVEN B, HUNT S. Ovarian ageing and the impact on female fertilityF1000Research, 2018, 7: 1835.
[2] SHEN M, JIANG Y, GUAN Z, CAO Y, LI L, LIU H, SUN S C. Protective mechanism of FSH against oxidative damage in mouse ovarian granulosa cells by repressing autophagyAutophagy, 2017, 13(8): 1364-1385.
[3] LEE S, KOPP F, CHANG T C, SATALURI A, CHEN B, SIVAKUMAR S, YU H, XIE Y, MENDELL J T. Noncoding RNA NORAD regulates genomic stability by sequestering PUMILIO proteins. Cell, 2016, 164(1/2): 69-80.
[4] AGIRRE X, MEYDAN C, JIANG Y, GARATE L, DOANE A S, LI Z, VERMA A, PAIVA B, MARTIN-SUBERO J I, ELEMENTO O, MASON C E, PROSPER F, MELNICK A. Long non-coding RNAs discriminate the stages and gene regulatory states of human humoral immune response. Nature Communications, 2019, 10(1): 821.
[5] STOJIC L, LUN A T L, MASCALCHI P, ERNST C, REDMOND A M, MANGEI J, BARR A R, BOUSGOUNI V, BAKAL C, MARIONI J C, ODOM D T, GERGELY F. A high-content RNAi screen reveals multiple roles for long noncoding RNAs in cell division. Nature Communications, 2020, 11(1): 1851.
[6] QIN W, LI X, XIE L, LI S, LIU J, JIA L, DONG X, REN X, XIAO J, YANG C, ZHOU Y, CHEN Z. A long non-coding RNA, APOA4-AS, regulates APOA4 expression depending on HuR in mice. Nucleic Acids Research, 2016, 44(13): 6423-6433.
[7] YOU B H, YOON S H, NAM J W. High-confidence coding and noncoding transcriptome maps. Genome Research, 2017, 27(6): 1050-1062.
[8] GIL N, ULITSKY I. Regulation of gene expression by cis-acting long non-coding RNAsNature Reviews. Genetics, 2020, 21(2): 102-117.
[9] NAKAGAWA S, SHIMADA M, YANAKA K, MITO M, ARAI T, TAKAHASHI E, FUJITA Y, FUJIMORI T, STANDAERT L, MARINE J C, HIROSE T. The lncRNA Neat1 is required for corpus luteum formation and the establishment of pregnancy in a subpopulation of mice. Development, 2014, 141(23): 4618-4627.
[10] CHEN Y, WANG J, FAN Y, QIN C, XIA X, JOHNSON J, KALLEN A N. Absence of the long noncoding RNA H19 results in aberrant ovarian STAR and progesterone production. Molecular and Cellular Endocrinology, 2019, 490: 15-20.
[11] ZHAO J, XU J, WANG W, ZHAO H, LIU H, LIU X, LIU J, SUN Y, DUNAIF A, DU Y, CHEN Z J. Long non-coding RNA LINC-01572:28 inhibits granulosa cell growth via a decrease in p27 (Kip1) degradation in patients with polycystic ovary syndrome. EBioMedicine, 2018, 36: 526-538.
[12] LI Y, LIU Y D, CHEN S L, CHEN X, YE D S, ZHOU X Y, ZHE J, ZHANG J. Down-regulation of long non-coding RNA MALAT1 inhibits granulosa cell proliferation in endometriosis by up-regulating P21 via activation of the ERK/MAPK pathway. Molecular Human Reproduction, 2019, 25(1): 17-29.
[13] DU X, LIU L, LI Q, ZHANG L, PAN Z. NORFA, long intergenic noncoding RNA, maintains sow fertility by inhibiting granulosa cell death. Communications Biology, 2020, 3(1): 131.
[14] FORNES O, CASTRO-MONDRAGON J A, KHAN A, VAN DER LEE R, ZHANG X, RICHMOND P A, MODI B P, CORREARD S, GHEORGHE M, BARANASIC D, SANTANA-GARCIA W, TAN G, CHENEBY J, BALLESTER B, PARCY F, SANDELIN A, LENHARD B, WASSERMAN W W, MATHELIER A. JASPAR 2020: update of the open-access database of transcription factor binding profiles. Nucleic Acids Research, 2020, 48(D1): D87-D92.
[15] DU X, LI Q, YANG L, LIU L, CAO Q. SMAD4 activates Wnt signaling pathway to inhibit granulosa cell apoptosis. Cell Death & Disease, 2020, 11(5): 373.
[16] LI Q, DU X, LIU L, PAN Z, CAO S. MiR-126* is a novel functional target of transcription factor SMAD4 in ovarian granulosa cells. Gene, 2019, 711: 143953.
[17] SHEN M, LIN F, ZHANG J, TANG Y, CHEN W K, LIU H. Involvement of the up-regulated FoxO1 expression in follicular granulosa cell apoptosis induced by oxidative stress. The Journal of Biological Chemistry, 2012, 287(31): 25727-25740.
[18] LIN F, LI R, PAN Z X, ZHOU B, YU D B, WANG X G, MA X S, HAN J, SHEN M, LIU H L. miR-26b promotes granulosa cell apoptosis by targeting ATM during follicular atresia in porcine ovary. PloS One, 2012, 7(6): e38640.
[19] REGAN S L P, KNIGHT P G, YOVICH J L, LEUNG Y, ARFUSO F, DHARMARAJAN A. Granulosa cell apoptosis in the ovarian follicle-a changing view. Frontiers in Endocrinology, 2018, 9: 61.
[20] WANG Y, YANG C, ELSHEIKH N A H, LI C, YANG F, WANG G, LI L. HO-1 reduces heat stress-induced apoptosis in bovine granulosa cells by suppressing oxidative stress. Aging, 2019, 11(15): 5535-5547.
[21] SPEARS N, LOPES F, STEFANSDOTTIR A, ROSSI V, DE FELICI M, ANDERSON R A, KLINGER F G. Ovarian damage from chemotherapy and current approaches to its protection. Human Reproduction Update, 2019, 25(6): 673-693.
[22] CHU Y L, XU Y R, YANG W X, SUN Y. The role of FSH and TGF-beta superfamily in follicle atresia. Aging, 2018, 10(3): 305-321.
[23] LI Q, DU X, PAN Z, ZHANG L. The transcription factor SMAD4 and miR-10b contribute to E2 release and cell apoptosis in ovarian granulosa cells by targeting CYP19A1. Molecular and Cellular Endocrinology, 2018, 476: 84-95.
[24] DU X, PAN Z, LI Q, LIU H. SMAD4 feedback regulates the canonical TGF-beta signaling pathway to control granulosa cell apoptosis. Cell Death & Disease, 2018, 9(2): 151.
[25] GUO T, ZHANG J, YAO W, DU X, LI Q, HUANG L, MA M, LIU H, PAN Z. CircINHA resists granulosa cell apoptosis by upregulating CTGF as a ceRNA of miR-10a-5p in pig ovarian follicles. Biochimica et Biophysica Acta-Gene Regulatory Mechanisms, 2019, 1862(10): 194420.
[26] CABILI M N, TRAPNELL C, GOFF L, KOZIOL M, TAZON-VEGA B, REGEV A, RINN J L. Integrative annotation of human large intergenic noncoding RNAs reveals global properties and specific subclasses. Genes & Development, 2011, 25(18): 1915-1927.
[27] QIAN X, ZHAO J, YEUNG P Y, ZHANG Q C, KWOK C K. Revealing lncRNA structures and interactions by sequencing-based approaches. Trends in Biochemical Sciences, 2019, 44(1): 33-52.
[28] GUTTMAN M, AMIT I, GARBER M, FRENCH C, LIN M F, FELDSER D, HUARTE M, ZUK O, CAREY B W, CASSADY J P, CABILI M N, JAENISCH R, MIKKELSEN T S, JACKS T, HACOHEN N, BERNSTEIN B E, KELLIS M, REGEV A, RINN J L, LANDER E S. Chromatin signature reveals over a thousand highly conserved large non-coding RNAs in mammals. Nature, 2009, 458(7235): 223-227.
[29] MATTIOLI K, VOLDERS P J, GERHARDINGER C, LEE J C, MAASS P G, MELE M, RINN J L. High-throughput functional analysis of lncRNA core promoters elucidates rules governing tissue specificity. Genome Research, 2019, 29(3): 344-355.
[30] LIU Y, YANG Y, LI W, AO H, ZHANG Y, ZHOU R, LI K. Effects of melatonin on the synthesis of estradiol and gene expression in pig granulosa cells. Journal of Pineal Research, 2019, 66(2): e12546.
[31] LIU J, LI X, YAO Y, LI Q, PAN Z. miR-1275 controls granulosa cell apoptosis and estradiol synthesis by impairing LRH-1/CYP19A1 axis. Biochimica et Biophysica Acta-Gene Regulatory Mechanisms, 2018, 1861(3): 246-257.
[32] CASARINI L, RICCETTI L, DE PASCALI F, GILIOLI L, MARINO M, VECCHI E, MORINI D, NICOLI A, LA SALA G B, SIMONI M. Estrogen modulates specific life and death signals induced by LH and hCG in human primary granulosa cells in vitro. International Journal of Molecular Sciences, 2017, 18(5): 926.
[33] QUIRK S M, COWAN R G, HARMAN R M. The susceptibility of granulosa cells to apoptosis is influenced by oestradiol and the cell cycle. The Journal of Endocrinology, 2006, 189(3): 441-453.
[34] VUONG N H, COOK D P, FORREST L A, CARTER L E, ROBINEAU-CHARETTE P, KOFSKY J M, HODGKINSON K M, VANDERHYDEN B C. Single-cell RNA-sequencing reveals transcriptional dynamics of estrogen-induced dysplasia in the ovarian surface epithelium. PLoS Genetics, 2018, 14(11): e1007788.
[35] WEI C, GUO D, LI Y, ZHANG K, LIANG G, MA Y, LIU J. Profiling analysis of 17beta-estradiol-regulated lncRNAs in mouse thymic epithelial cells. Physiological Genomics, 2018, 50(8): 553-562.
[36] LIU X L, WU R Y, SUN X F, CHENG S F, ZHANG R Q, ZHANG T Y, ZHANG X F, ZHAO Y, SHEN W, LI L. Mycotoxin zearalenone exposure impairs genomic stability of swine follicular granulosa cells in vitro. International Journal of Biological Sciences, 2018, 14(3): 294-305.
[37] CHOI H, ROH J. Role of Klf4 in the regulation of apoptosis and cell cycle in rat granulosa cells during the periovulatory period. International Journal of Molecular Sciences, 2018, 20(1): 87.
[38] XU L, SUN H, ZHANG M, JIANG Y, ZHANG C, ZHOU J, DING L, HU Y, YAN G. MicroRNA-145 protects follicular granulosa cells against oxidative stress-induced apoptosis by targeting Kruppel-like factor 4. Molecular and Cellular Endocrinology, 2017, 452: 138-147.
[39] YADAV H, DEVALARAJA S, CHUNG S T, RANE S G. TGF-beta1/Smad3 pathway targets PP2A-AMPK-FoxO1 signaling to regulate hepatic gluconeogenesis. The Journal of Biological Chemistry, 2017, 292(8): 3420-3432.
[40] QIAO X, RAO P, ZHANG Y, LIU L, PANG M, WANG H, HU M, TIAN X, ZHANG J, ZHAO Y, WANG X M, WANG C, YU H, GUO F, CAO Q, WANG Y, WANG Y M, ZHANG G Y, LEE V W, ALEXANDER S I, ZHENG G, HARRIS D C H. Redirecting TGF-beta signaling through the Beta-catenin/Foxo complex prevents kidney fibrosis. Journal of the American Society of Nephrology, 2018, 29(2): 557-570.
[41] LIU F, QIU H, XUE M, ZHANG S, ZHANG X, XU J, CHEN J, YANG Y, XIE J. MSC-secreted TGF-beta regulates lipopolysaccharide- stimulated macrophage M2-like polarization via the Akt/FoxO1 pathway. Stem Cell Research & Therapy, 2019, 10(1): 345.
[42] SEOANE J, LE H V, SHEN L, ANDERSON S A, MASSAGUE J. Integration of Smad and forkhead pathways in the control of neuroepithelial and glioblastoma cell proliferation. Cell, 2004, 117(2): 211-223.
[43] PONUGOTI B, XU F, ZHANG C, TIAN C, PACIOS S, GRAVES D T. FOXO1 promotes wound healing through the up-regulation of TGF-beta1 and prevention of oxidative stress. The Journal of Cell Biology, 2013, 203(2): 327-343.
[44] KURAKAZU I, AKASAKI Y, HAYASHIDA M, TSUSHIMA H, GOTO N, SUEISHI T, TOYA M, KUWAHARA M, OKAZAKI K, DUFFY T, LOTZ M K, NAKASHIMA Y. FOXO1 transcription factor regulates chondrogenic differentiation through transforming growth factor beta1 signaling. The Journal of Biological Chemistry, 2019, 294(46): 17555-17569.
Identification of the Core Promoter of Linc-and Its Transcriptional Regulation in Erhualian Pig
DU Xing, ZENG Qiang, LIU Lu, LI QiQi, YANG Liu, PAN ZengXiang, LI QiFa
College of Animal Science and Technology, Nanjing Agricultural University, Nanjing 210095
【】In our previous study, linc-has been proved as a candidate gene for sow fertility and participated in regulating follicular atresia and granulosa cell apoptosis. The aim of this study is to identify the core promoter of linc-and investigate its transcriptional regulation in Erhualian pig, so as to provide theoretical basis and new ideas for revealing the mechanism of linc-regulation to ovarian follicular atresia.【】Ear samples of Euhualian pig were collected for genomic DNA extraction. PCR amplification and clone sequencing were used to obtain the 5’-flanking sequence of Erhualian pig linc-gene. Reporter vectors construction and luciferase activity assays were performed to identify the core promoter of linc-gene, and bioinformatic methods were conducted to analyze the characterization of linc-core promoter and the potential binding elements of transcription factors (TFs). In addition, piggene eukaryotic expression vector was constructed and Western blot, qRT-PCR, and luciferase activity assays were performed to analyze the effects and regulatory mechanism of FOXO1 overexpression on the transcription of linc-gene. Besides, chromatin immunoprecipitation (ChIP) assay was performed to identify the interaction between FOXO1 and the core promoter of linc-in porcine granulosa cells (GCs).【】A total of 1 734 bp 5’-flanking sequence of Erhualian pig linc-was obtained by PCR amplification and clone sequencing technology, which contained two potential CpG islands. Luciferase activity assay was performed and demonstrated that the core promoter of Erhualian pig linc-was located at -988 — -684 bp (TSS as +1). Multiple potential binding elements of several transcription factors (TFs) were identified within the core promoter of linc-using bioinformatic analyses, including ESR2, FOXO1, E2F1, BRCA1 and NFIC. In addition, results from ChIP assay proved that FOXO1 directly binds to the core promoter of linc-by acting as a transcription factor. Furthermore, It was proved that overexpression of FOXO1 could significantly down-regulate the activity of linc-core promoter (<0.01), and also notably inhibited the expression level of linc-in porcine GCs (<0.01).【】In this study, the core promoter of Erhualian pig linc-was identified, and FOXO1 acts as a transcription factor was proved, which significantly inhibited linc-transcription in porcine GCs through binding and further down-regulating the activity of its core promoter. These findings were of great significance for investigating the molecular mechanism of down-regulation of linc-during follicular atresia.
Erhualian pig; ovarian granulosa cells; linc-; core promoter; transcription regulation

10.3864/j.issn.0578-1752.2021.15.016
2020-06-18;
2020-12-22
江苏省自然科学基金(BK20180524)、国家自然科学基金(31902130)、中国博士后科学基金(2018M632321)
杜星,E-mail:duxing@njau.edu.cn。通信作者李齐发,E-mail:liqifa@njau.edu.cn
(责任编辑 林鉴非)

