氯沙坦对急性肺损伤小鼠肺树突状细胞活化的影响及作用机制研究
赵耀东,魏明
(1.郑州大学第五附属医院风湿免疫科,河南 郑州 450052;2.郑州大学第五附属医院输血科,河南 郑州 450052)
急性肺损伤(ALI)是一类较多见的危急大病,能够进展成为更加危急的急性呼吸窘迫综合征(ARDS)。病因众多,其死亡率能够达到40%[1,2]。当前研究认为其发病的主要因素为不可控制的炎性反应[3]。肾素-血管紧张素系统(RAS)的激活在ALI的发生发展中发挥重要的作用。RAS的主要效应因子血管紧张素Ⅱ(AngⅡ)有显著的促进炎症发生的作用,它是介导ALI肺部炎性反应过程的关键因子[4,5]。作为血管紧张素Ⅱ的1型受体阻断剂,氯沙坦能够显著降低肺部炎症损伤水平[6]。树突状细胞(DC)能够调节肺部免疫反应,并在其中发挥关键性作用。有研究表明,肺部组织感染以及由博来霉素诱发的肺部损伤过程都有肺DC的干预[7,8]。肺部结构RAS能够调节肺DC的作用水平,AngⅡ可促进DC分化成熟[9]。但是,氯沙坦能否依赖于抑制AngⅡ诱发的肺DC的激活从而缓解肺部组织炎性反应这仍有待于深究。此实验应用脂多糖(LPS)来构建ALI小鼠的模型,研究在ALI中,氯沙坦对肺DC的数目和功能的作用,从而深入探究氯沙坦对ALI产生的保护性机理。
1 实验材料和实验方法
1.1 实验动物72只C57BL/6小鼠,雄性,6~8周,体重为18~22 g。由郑州大学实验动物中心供给,许可证号:ZYXK(豫)2016-0289。于无特定病原体(SPF级)条件下常规喂养,标准化颗粒饲料、饮用水、垫料及其他相关物品都经灭菌处理。
1.2 试剂和器材LPS(E.coli 0111:B4)购自Sigma公司,胶原酶V购自Sigma-Aldrich公司。小鼠CD11c、CD11b,组织相容性复合物(MHC II),CD80及同型对照单克隆抗体都购自eBioscience公司。Losartan由Cayman公司提供。小鼠IL-6 ELISA kit购自上海依科赛生物有限公司。流式细胞仪购自美国BD公司(BDFACSCaliburTM)。
1.3 模型制备与分组 将72只SD小鼠按随机数字表法分为正常对照组、ALI模型组和氯沙坦干预组各24只。正常对照组:向小鼠腹腔中注射50μl的PBS,30分钟后向气管中滴加30μl的PBS,ALI模型组[10,11]:向小鼠腹腔中注射50μl的PBS,30分钟之后向气管中滴加2mg/kg的LPS(溶于30μl PBS中),成功构建LPS-ALI模型的标准:肺部组织间质内充血、肿大,肺泡之间的间隙显著增宽,肺部组织间质以及肺泡腔中有弥漫性炎症细胞的包裹、出血,大部分肺泡结构萎缩[11]。氯沙坦干预组:向小鼠腹腔中注射15mg/kg的氯沙坦(溶于50 μl PBS中),30分钟之后构建LPS-ALI模型。注射LPS或 者PBS之 后 的6、12、24小 时 左 右 处 死 标本,留取待检的肺组织。
1.4 标本的采集以及病理研究 于6、12、24小时采用右心室取血的方法处死小鼠(n=6只小鼠/每组/每个时间点)。将右肺部分组织标本大小(约0.5cm×0.5cm,1~2g)进行甲醛固定、石蜡片包埋、再经切片、HE染色,由病理科一名医师专门负责观测其病理改变,并将组织小块按照方法[12]对其进行损伤分级评分。规则如下:⑴肺泡的充血,⑵出血,⑶肺泡腔中或者血管壁上有中性粒细胞的包裹,⑷肺泡壁加厚和(或)有透明质膜的产生四项指标,分别按照病变的严重程度对其评0~4分(0:没有病理改变或极度轻微病变,1:轻微病理改变,2:中等程度病理改变,3:严重病理改变,4:极度重症病理改变)。各部分的评分数之和即为急性肺损伤的总分数。
1.5 肺单细胞悬液制备 在灭菌的情况下拿出肺部组织30mg,将其放于含有Hank's平衡溶液的培养皿之中,把取到的肺部组织用眼科剪裁成1mm×1mm×1mm大小的小块,把装有肺部组织小块的培养皿放于培养箱中,勇胶原酶V溶液对其进行消化1小时(37℃,每隔3分钟轻轻振摇数次),冰浴终止消化,缓缓吸打分离细胞,用200目的不锈钢网格过筛,在EP管中集中收取消化液。再经1000 rpm/min的速度离心10分钟,去上清,于下层沉淀中注入2ml的PBS缓缓吸打,相同的速度离心5分钟,弃上清,于沉淀里加5ml的红细胞裂解液,缓缓吸打使细胞分散开来,冰块上静置10分钟,相同的速度离心10分钟,弃上清,加3ml的PBS混合版均匀,离心5分钟,速度同上。弃上清。用台盼蓝染液对细胞进行染色,细胞计数板涂片,光学显微镜下观测活体细胞数目,之后将细胞的浓度调整到1×106个/ml,冰冻保存备用。
1.6 肺湿重/体重(LW/BW)检测 取肺组织,把肺部组织表层多余的水分用吸水纸吸尽同时清理好血渍之后,称量并算出肺组织LW/BW水平。
1.7 ELISA测定肺部组织IL-6水平 挑选右肺下部组织约10mg,加入2ml生理盐水,用电动匀浆机制备肺组织匀浆,4℃,3000rpm/min离心10分钟,留上清液,-80℃保存。按照试剂盒的说明书进行严格规范操作,450nm处测吸光值,计算IL-6水平。
1.8 流式细胞仪测定肺部DC数目以及CD80、MHC II的表达 在管中滴加0.5μg的抗CD16/CD32单克隆抗体避光反应10分钟,在相对应的管中分别滴加0.25μg的抗CD11c-FITC单抗、0.125 μg的CD11b-PE单抗、0.03μg的抗MHC II-APC单抗以及0.06μg的抗CD80-APC单抗。并将FITC荧光标记的抗亚美尼亚仓鼠IgG、PE荧光标记的抗大鼠IgG2b、APC荧光标记的抗大鼠IgG2b设为同型的阴性对照管(抗体在使用之前应该缓慢摇匀),混和均匀,25℃避光反应20分钟,1200rpm的速度离心5分钟,弃去上层清液,向沉淀中滴加1 ml的含有1% BSA PBS混和均匀,同样的速度离心5分钟,弃去上层清液,滴加1%的多聚甲醛300μl,放于4℃避光存放,24小时之内上机检测,检测之前应该缓慢吸打使细胞混合均匀,本实验重复3次。
1.9 统计学处理 实验中均采用SPSS 16.0统计分析软件对数据资料进行分析。对各组数据进行正态检验和方差齐性检验,如果数据方差齐、满足正态分布,采用单因素方差分析(One-way ANOVA),组间比较采用Dunnett-t法,若不满足方差齐性检验条件,则采用秩和检验。用Mann-Whiteney法对其进行组间比较,P<0.05为差异具有统计学意义。
2 结果
2.1 氯沙坦对小鼠肺部结构病理学变化产生的效果6h各组肺部结构切片进行HE染色,在光学显微镜下观察。正常对照组中小鼠的肺泡间隙均等,肺泡腔中没有明显的渗出以及炎症性包裹,ALI模型组小鼠的肺部组织病理学检查可见其肺泡间隙显著加宽、肺间质内血管有充血、出血同时弥漫的炎症性包裹,氯沙坦干预组中小鼠肺部病理学检查可见肺泡间隔稍稍加宽,产生少部分出血以及炎症性包裹,与ALI模型组相比损伤大大降低,见图1。
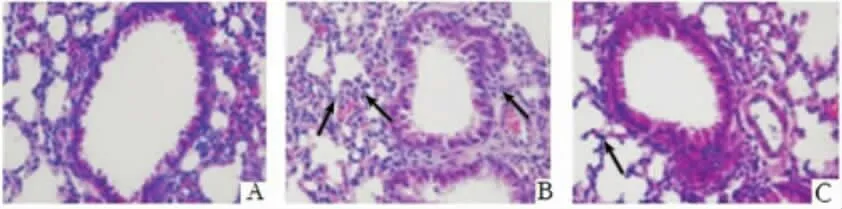
图1 氯沙坦对6 h小鼠肺组织病理变化的影响(HE×400,箭头为中性粒细胞)
2.2 氯沙坦对小鼠肺LW/BW比的影响6h、12h和24h各组小鼠肺LW/BW比较,经方差分析,差异具有统计学意义(F=5.78、5.65和5.51,P=0.006、0.005和0.004);与正常对照组相比,ALI模型组和氯沙坦干预组小鼠肺LW/BW升高(P<0.05);氯沙坦干预组肺LW/BW较ALI模型组降低(P<0.05),见表1。
表1 氯沙坦对小鼠肺LW/BW比的影响(n=8,%,)
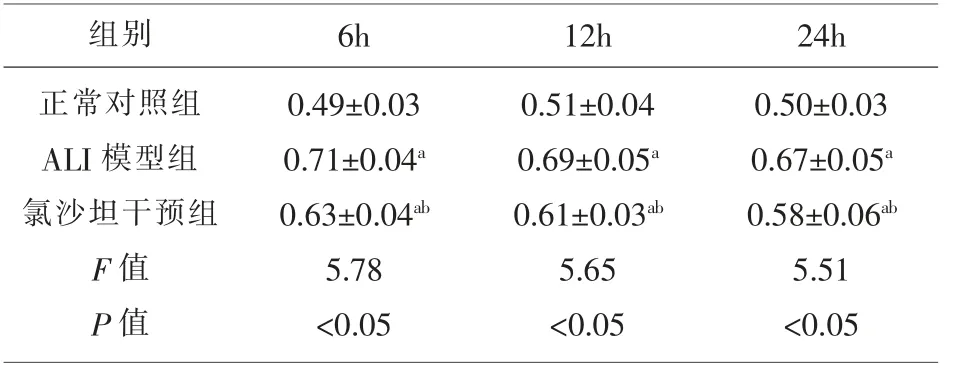
表1 氯沙坦对小鼠肺LW/BW比的影响(n=8,%,)
注:与正常对照组比较:aP<0.05,与ALI模型组比较:bP<0.05
组别 6h正常对照组ALI模型组氯沙坦干预组F值P值0.49±0.03 0.71±0.04a 0.63±0.04ab 5.78<0.05 12h 24h 0.51±0.04 0.69±0.05a 0.61±0.03ab 5.65<0.05 0.50±0.03 0.67±0.05a 0.58±0.06ab 5.51<0.05
2.3 氯沙坦对小鼠肺Smith损伤评分的影响 比较6h、12h和24h各部分小鼠肺部组织病理评分,经方差分析,差异具有统计学意义(F=127.24、118.67和121.38,P=0.002、0.005和0.003),与正常对照组相比,ALI模型组和氯沙坦干预组小鼠肺组织病理切片评分增高(P<0.05);氯沙坦干预组肺损伤评分较ALI模型组明显降低(P<0.05)见表2。
表2 氯沙坦对小鼠肺Smith损伤评分的影响(n=8,分)
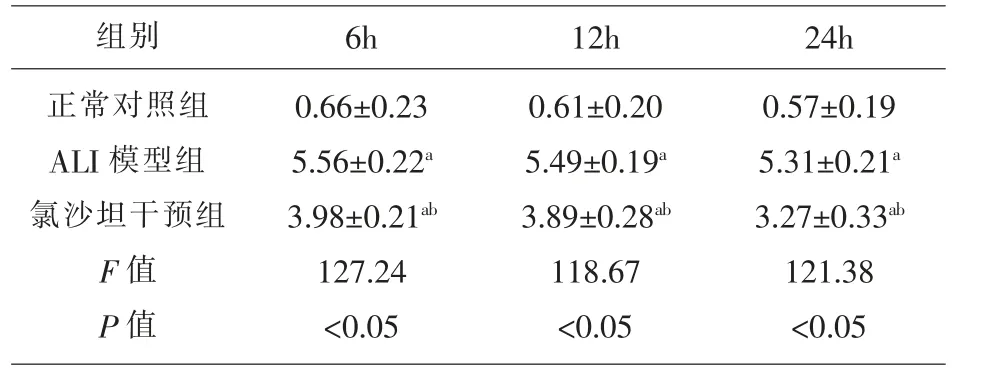
表2 氯沙坦对小鼠肺Smith损伤评分的影响(n=8,分)
注:与正常对照组比较:aP<0.05,与ALI模型组比较:bP<0.05
组别 6h正常对照组ALI模型组氯沙坦干预组F值P值0.66±0.23 5.56±0.22a 3.98±0.21ab 127.24<0.05 12h 24h 0.61±0.20 5.49±0.19a 3.89±0.28ab 118.67<0.05 0.57±0.19 5.31±0.21a 3.27±0.33ab 121.38<0.05
2.4 氯沙坦对小鼠肺组织匀浆IL-6水平的影响比较6h、12h和24h各组小鼠肺组织匀浆IL-6含量,经方差分析,差异具有统计学意义(F=6.84、7.23和8.71,P=0.003、0.003和0.002)。6 h、12 h和24 h ALI模型组小鼠肺组织匀浆中IL-6含量与正常对照组相比,差异具有统计学意义(P<0.05);与ALI模型组比较,氯沙坦干预组IL-6含量降低(P<0.05),见表3。
表3 氯沙坦对小鼠肺IL-6水平的影响(n=8,pg/mg)
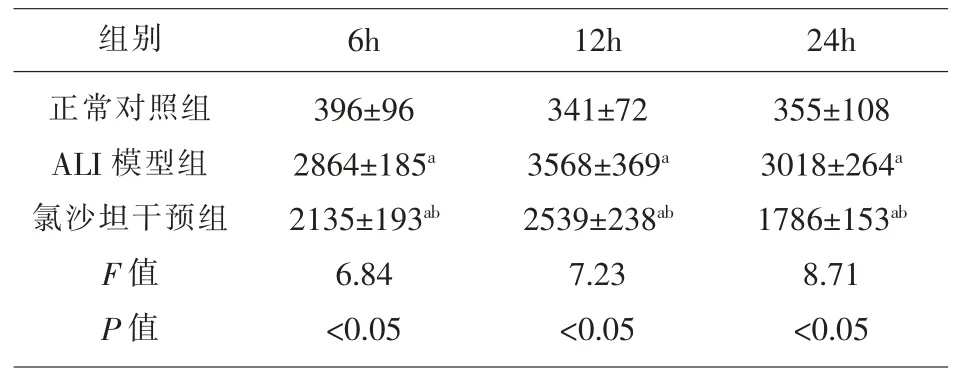
表3 氯沙坦对小鼠肺IL-6水平的影响(n=8,pg/mg)
注:与正常对照组比较:aP<0.05,与ALI模型组比较:bP<0.05
组别 6h正常对照组ALI模型组氯沙坦干预组F值P值396±96 2864±185a 2135±193ab 6.84<0.05 12h 24h 341±72 3568±369a 2539±238ab 7.23<0.05 355±108 3018±264a 1786±153ab 8.71<0.05
2.5 氯沙坦对小鼠肺组织DC数量的影响6h、12h和24h各组小鼠肺组织DC数量比较,经方差分析,差异有统计学意义(F=16.24、13.67和11.38,P=0.005、0.004和0.003);与正常对照组比较,ALI模型组肺组织DC数量和氯沙坦干预组肺组织DC数量均显著升高(P<0.05)。ALI模型组与氯沙坦干预组肺组织DC数量差异无统计学意义(P>0.05),见表4。
表4 氯沙坦对小鼠肺DC数量的影响(n=8,%,)
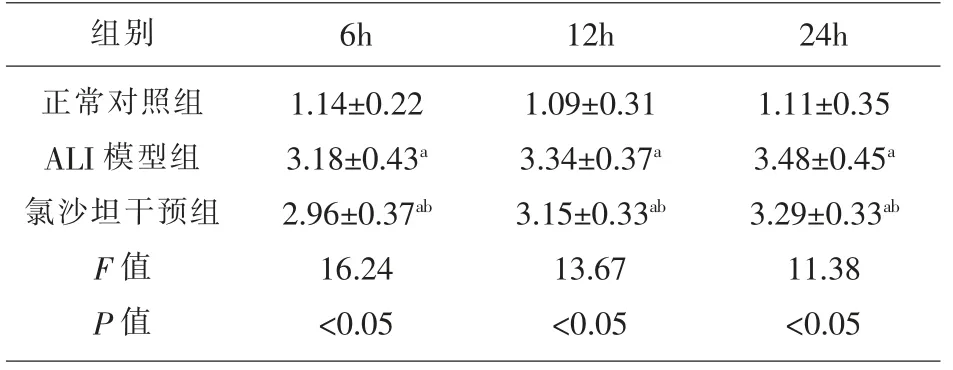
表4 氯沙坦对小鼠肺DC数量的影响(n=8,%,)
注:与正常对照组比较:aP<0.05,与ALI模型组比较:bP>0.05
组别 6h正常对照组ALI模型组氯沙坦干预组F值P值1.14±0.22 3.18±0.43a 2.96±0.37ab 16.24<0.05 12h 24h 1.09±0.31 3.34±0.37a 3.15±0.33ab 13.67<0.05 1.11±0.35 3.48±0.45a 3.29±0.33ab 11.38<0.05
2.6 氯沙坦对小鼠肺部组织DC表达CD80的作用6h、12h和24h各组小鼠肺组织DC表达CD80比较,经方差分析,差异有统计学意义(F=11.78、15.31和19.65,P=0.006、0.004和0.002);与正常对照组比较,ALI模型组和氯沙坦干预组肺DC表达CD80均升高(P<0.05)。ALI模型组肺DC表达CD 80明显高于氯沙坦干预组(P<0.05),见表5和图2。
表5 氯沙坦对小鼠肺DC功能状态的影响(n=8,%,)
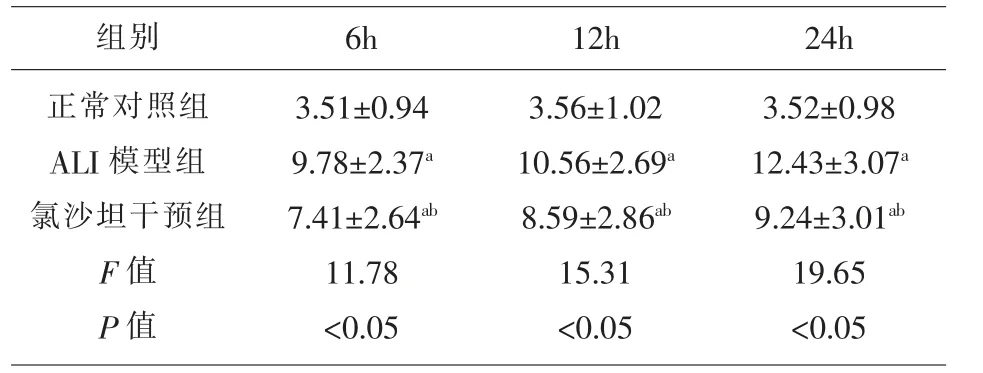
表5 氯沙坦对小鼠肺DC功能状态的影响(n=8,%,)
注:与正常对照组比较:aP<0.05,与ALI模型组比较:bP<0.05
组别 6h正常对照组ALI模型组氯沙坦干预组F值P值3.51±0.94 9.78±2.37a 7.41±2.64ab 11.78<0.05 12h 24h 3.56±1.02 10.56±2.69a 8.59±2.86ab 15.31<0.05 3.52±0.98 12.43±3.07a 9.24±3.01ab 19.65<0.05
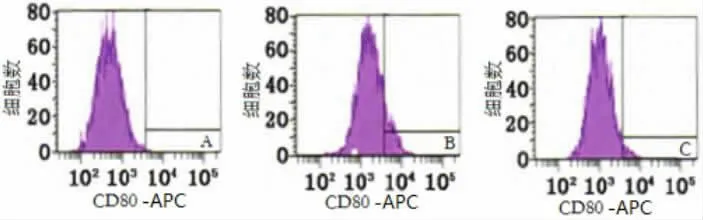
图2 氯沙坦对6 h小鼠肺组织CD80的影响(右框红色部分)
2.7 氯沙坦对小鼠肺组织DC表达MHC II的影响6h、12h和24h各组小鼠肺组织DC表达MHC II比较,经方差分析,差异有统计学意义(F=1.32、1.56和1.24,P=0.065、0.055和0.071);与正常对照组比较,ALI模型组肺DC表达MHC II和氯沙坦干预组肺DC表达MHC II差异无统计学意义(P>0.05),正常对照组和氯沙坦干预组肺DC表达MHC II差异无统计学意义(P>0.05),见表6和图3。
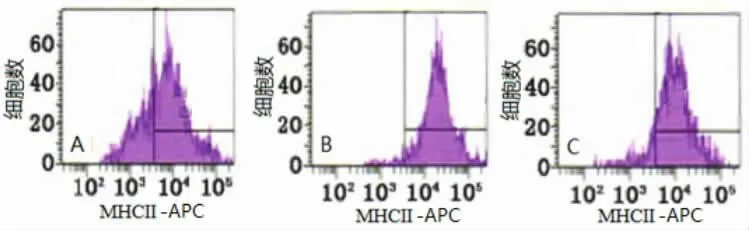
图3 氯沙坦对6 h小鼠肺组织MHCⅡ的影响(右框红色部分)
表6 氯沙坦对小鼠肺DC抗原提呈功能的影响(n=8,%,)
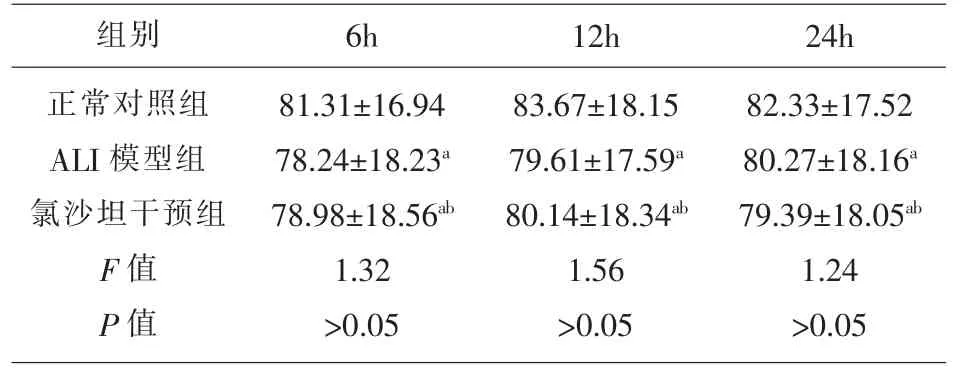
表6 氯沙坦对小鼠肺DC抗原提呈功能的影响(n=8,%,)
注:与正常对照组比较:aP>0.05,与ALI模型组比较:bP>0.05
组别 6h正常对照组ALI模型组氯沙坦干预组F值P值81.31±16.94 78.24±18.23a 78.98±18.56ab 1.32>0.05 12h 24h 83.67±18.15 79.61±17.59a 80.14±18.34ab 1.56>0.05 82.33±17.52 80.27±18.16a 79.39±18.05ab 1.24>0.05
3 讨论
因为炎症感染等多种原因使肺部多种炎症因子激活,从而使肺部组织的免疫反应失去控制是ALI发生的主要原因[13,14]。与此同时,缺少特异性药物的治疗成为影响其病情发展以及预后主要因素之一[15]。有研究[16]显示,肺部RAS系统的活跃状态在整个ALI的免疫紊乱中起到非常关键的作用。也有研究[6]显示,氯沙坦可以显著降低ALI肺部的炎性损伤,这揭示了其在ALI的临床治疗上可能具有重要的应用价值。而探究氯沙坦对ALI肺部免疫紊乱造成的炎性损伤机理有及其重大的意义。
此实验应用向气管内注射LPS复制构建小鼠ALI模型,来重现由于肺部炎症感染所致ALI的整个过程。本实验可见,ALI模型组小鼠肺LW/BW显著升高,肺部切片能够看到肺泡间隙加宽、肺部充血、出血以及弥漫性的炎性细胞的包裹,且IL-6水平也有显著的增高,这都表明ALI模型复制成功[17]。本实验还可见到,与ALI模型组比较,经氯沙坦干预的小组LW/BW降低,肺部组织免疫损伤有所缓解,肺损伤的评分显著降低,并且肺IL-6水平也明显减低,提示氯沙坦能够缓解肺部损伤。此外,本研究还发现,与正常对照组相比,经氯沙坦干预组的小鼠肺部炎症损伤水平依旧较高,提示氯沙坦对ALI产生部分保护的效果。
在肺部免疫系统的防御和保护中,肺DC都起到了非常重要的作用,其数目和功能与免疫效能的发挥有着相当密切的联系[18]。目前已知的肺部感染,慢性阻塞性肺疾病以及支气管哮喘等肺部炎性病变的产生与发展都有肺DC的参与[19]。本次实验结果可见,ALI小鼠的肺DC有广泛积聚现象,其中其表达的CD80水平也显著升高,这些均提示在ALI肺部炎性反应中,都有成熟的肺DC的身影。且在调节ALI肺部免疫损伤这一过程中,肺DC可能成为其重要靶点。此实验还发现,正常对照组与ALI模型组小鼠肺DC表的达MHCⅡ分子水平都相对较高,并且没有显著差异,提示ALI小鼠肺DC的抗原递呈能力没有很大改变。机体内免疫反应的种类以及水平可能是由其DC的数目和功能来决定的。有研究[7]显示,由博来霉素诱发的小鼠肺损伤模型中肺部成熟DC数目有明显升高并且其同时还参与肺部免疫反应,阻碍肺DC的发育成熟能够明显缓解肺部的炎性损伤及其纤维化。
本研究证明,经氯沙坦干预小组对LPS-ALI小鼠肺DC数目没有太大影响,但是表达CD80的肺DC比例显著降低,揭示了氯沙坦能够通过阻碍肺DC成熟缓解ALI肺部免疫损伤水平。本实验还发现,氯沙坦对ALI肺DC表达的MHCⅡ分子不产生显著影响,提示了氯沙坦可能对DC的抗原递呈功能没有明显影响。也有研究[9]发现,氯沙坦能够显著减轻实验性自身免疫性脑脊髓炎小鼠脑以及脊髓中的免疫损伤主要是依赖于对其组织中DC的激活和成熟的抑制。这也更加深入的说明了氯沙坦能够通过阻碍DC成熟从而实现对ALI的免疫调节。
综上所述,氯沙坦能够通过抑制肺DC的发育成熟从而调节ALI肺部免疫损伤,在治疗ALI的临床手段上可能具有非常重要的应用价值。

