介入治疗联合靶向药物阿帕替尼在原发性肝癌治疗中的应用价值分析
翟鹏涛 庞宏涛
(陕西省肿瘤医院,(1.介入科;(2.肿瘤内科,陕西 西安 710061)
原发性肝癌在临床恶性肿瘤中较为常见,患者可出现肝区疼痛、消瘦、腹胀、食欲下降及肝大等临床表现,其中肝区疼痛属于首发症状,并且呈现持续性胀痛、钝痛或刺痛[1]。伴随疾病病程逐渐发展,病患可出现肝性昏迷、癌细胞破裂出血、上消化道出血以及继发感染等并发症,对病患生命安全产生严重威胁[2]。因此,在疾病诊断后及时采取有效措施治疗对改善疾病预后具有积极意义。随着临床对原发性肝癌研究的不断深入,有研究[3]指出对原发性肝癌患者采用介入治疗联合阿帕替尼治疗可获得满意效果。但目前临床对这一说法尚未形成统一结论。为提升临床原发性肝癌治疗效果,本研究采用介入治疗联合阿帕替尼治疗,现报告如下。
1 资料与方法
1.1一般资料 选取2018年9月至2019年9月我院收治的原发性肝癌患者100例,随机分为观察组与对照组,各50例。观察组男27例,女23例;平均(61.37±5.64)岁;肿瘤直径(11.85±1.36)cm;TNM分期:Ⅲ期31例,Ⅳ期19例。对照组男25例,女25例;平均(61.52±5.76)岁;肿瘤直径(11.63±1.52)cm;TNM分期:Ⅲ期30例,Ⅳ期20例。纳入标准:患者基础信息完整,参与整个实验步骤;预计生存期3个月患者;所有研究对象均经病理学确诊为原发性肝癌[4]。排除标准:机体凝血功能存在严重异常者;机体其他系统存在肿瘤或出现转移性肿瘤者;中途因各种原因无法继续接受相关治疗而退出者。经过本院伦理委员会批准,均经过患者知情同意。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2方法 对照组给予介入治疗,选择60 mg多柔比星(浙江海正药业股份有限公司,规格:5 mL:10 mg;批号:国药准字H20041318)、500 mg氟尿嘧啶(天津金耀药业有限公司,规格:10 mL:0.25 g;批号:国药准字H31020593)、100 mg奥沙利铂(江苏恒瑞医药股份有限公司,规格:100 mL:0.1 g;批号:国药准字H20050962),使用近端栓塞剂吸收性明胶海绵、远端栓塞剂碘油作为栓塞剂,直接灌注水剂化疗药氟尿嘧啶,混合碘油及粉剂化疗药,成为悬混液,为患者再灌注,作用缓释。观察组在此基础上给予江苏恒瑞医药股份有限公司提供的阿帕替尼(规格:0.25 g/片;批号:国药准字 H20140103)治疗,每次使用250~850 mg阿帕替尼,1次/d,1个周期共计28 d,用药过程中,对患者病情具体变化情况进行严密监测,若出现药物不良反应,应将患者使用阿帕替尼剂量合理调整,在治疗第2个至第3个周期中调整药物剂量,若患者合并3~4级血液学不良反应、非血液学不良反应,将用药暂停,时间不得超过2周,待患者彻底消失相关症状或者明显缓解,对阿帕替尼用药量进行合理调整。
1.3观察指标 比较每组患者近期治疗效果及疾病控制效果,治疗后病患肿瘤病灶完全消失为效果优异;治疗后病患基线肿瘤病灶直径下降>30.00%为效果尚可;治疗后病患基线肿瘤病灶直径下降≤30.00%或基线肿瘤病灶直径增加≤20.00%为效果一般;治疗后病患基线肿瘤病灶直径增加>20.00%为效果差[5];本次研究将优异、尚可归纳为近期治疗效果;将优异、尚可及一般归纳为疾病控制效果。对两组治疗后不良反应发生率进行对比,常见不良反应有血压过高、腹泻、恶心呕吐、全身乏力等。分别于治疗前后使用生活质量评估量表(SF-36)[6 ]评估每组病患生活质量水平。

2 结 果
2.1近期治疗效果及疾病控制效果 观察组优异25例、尚可19例、一般4例、差2例,近期治疗率88.00%,疾病控制率96.00%;对照组优异15例、尚可20例、一般7例、差8例,近期治疗率70.00%,疾病控制率84.00%。观察组近期治疗率、疾病控制率显著高于对照组(χ2=4.883、4.000,P<0.05)。
2.2不良反应 观察组出现腹泻1例、恶心呕吐1例,不良反应发生率4.00%;对照组出现血压过高3例、腹泻2例、恶心呕吐1例、全身乏力2例,不良反应发生率16.00%。观察组不良反应发生率显著低于对照组(χ2=4.000,P<0.05)。
2.3生活质量 治疗后观察组在SF-36各项评分上均高于对照组(t=5.966、7.360、8.540、7.591、8.247、9.582、8.582、8.725,P<0.05)。见表1。
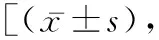
表1 两组治疗前后生活质量评分比较分]
3 讨 论
原发性肝癌主要是指出现在肝内胆管细胞或肝细胞的恶性肿瘤,大部分患者属于肝细胞癌。近年来,原发性肝癌发病率逐渐升高,在我国原发性肝癌在常见恶性肿瘤中居于第四位,并且成为第二大肿瘤致死病因,对人们生命安全及机体健康均产生严重威胁[7]。
对于原发性肝癌患者来说,利用肝动脉药物灌注化疗栓塞处理,可将患者病情有效控制,可将患者生存时间有效延长,因此,在患者治疗过程中,介入治疗占据重要地位[8]。但临床研究[9]表明,单纯介入治疗肿瘤灭活不彻底,术后还会导致栓塞组织细胞缺血缺氧,促进多种生长因子的生长,从而促进肿瘤转移。本次研究结果表明,与对照组近期治疗率、疾病控制率相比,观察组显著较高(P<0.05),与对照组不良反应发生率相比,观察组显著较低(P<0.05),治疗前研究对象在生活质量上无显著差异(P>0.05),治疗后观察组在SF-36各项评分上均高于对照组(P<0.05),分析原因:阿帕替尼是全球第一个在晚期胃癌被证实安全有效的小分子抗血管生成靶向药物,也是晚期胃癌标准化疗失败后,明显延长生存期的单药。可有效提高患者治疗的依从性,并明显降低治疗费用[10]。阿帕替尼可选择性、有效结合患者体内细胞中VEGFR-2ATP 结合位点,属于小分子酪氨酸激酶抑制剂,属于新型药物,可阻断患者下游信号的传导过程,可有效抑制肿瘤组织新生血管,将其应用于原发性肝癌患者治疗过程中,可获得满意成效。阿帕替尼可对多种类型肿瘤存在明显控制作用,抗肿瘤作用较为明显,可对肿瘤侵袭能力及细胞活性起到一定抑制作用,可将患者临床总有效率显著提高,可有效抵抗患者生成肿瘤血管,可对患者静脉血管内皮细胞的增殖、迁移起到一定抑制作用,可对患者肿瘤血管生成起到阻碍作用。
综上所述,在原发性肝癌治疗中给予介入治疗联合靶向药物阿帕替尼后,疗效确切,患者生活质量改善明显,且安全性高,不良反应少,此方法可广泛应用于临床。

