不同剂量奥曲肽治疗重症急性胰腺炎有效性与安全性的Meta分析
林山,肖冰
急性胰腺炎(acute pancreatitis, AP)是指多种病因引起的胰酶过度激活,继以胰腺组织自身消化而导致胰腺水肿、出血和坏死等炎性损伤的疾病,是消化内科常见的急症[1]。重症急性胰腺炎(severe acute pancreatitis, SAP)起病急骤、进展迅速,常表现为全身炎症反应综合征(systemic inflammatory response syndrome, SIRS),严重者可能出现多器官功能障碍[2]。由于人民生活水平的提高以及食物类型和结构的变化等原因,特别是酒精摄入量的增加及大量进食高脂高热量食物,AP的年发病率呈逐渐上升的趋势[3],在过去的30年里,AP的全球年发病率约为13~45/10万,国内的年发病率约为18.6/10万,但各地区发病率存在差异[4]。
以胰腺自身消化学说为基础,生长抑素及其类似物(奥曲肽)可以通过直接抑制胰腺外分泌功能,保护胰腺细胞,避免病情持续进展[5]。研究发现,生长抑素及其类似物对多器官损害具有保护作用,可以降低并发症发生率及病死率[6]。国内多数指南均推荐此类药物在AP治疗中的应用[6-7, 9-10]。当前,奥曲肽在临床上被广泛用于治疗SAP,其疗效也得到了越来越多的认可,但关于奥曲肽的临床应用剂量尚没有统一的标准[8],多数指南推荐的奥曲肽治疗剂量为0.3~0.6 mg/d[9-10],但是临床上也常应用1.2 mg/d的剂量治疗SAP。由于国内多数医疗机构在应用奥曲肽治疗SAP时均采用0.6 mg/d或1.2 mg/d的剂量[8],所以近年来国内相关研究[8,11-20]主要分析探讨上述两种剂量治疗SAP的疗效和安全性。目前,在两种给药剂量的疗效比较方面,尚无系统性的评价研究。本研究对采用0.6 mg/d和1.2mg/d两种不同的奥曲肽给药剂量治疗SAP的临床效果及安全性进行meta分析。以期为临床关于治疗SAP选择合适的奥曲肽用药剂量提供依据。
1 资料与方法
1.1 一般资料
1.1.1 研究类型 以中文或英文发表的关于不同剂量奥曲肽治疗SAP的随机对照试验(randomized controlled trial, RCT)。
1.1.2 研究对象 患者均符合中华医学会消化病学分会胰腺疾病学组编写的《中国急性胰腺炎诊治指南(2019,沈阳)》关于AP的诊断标准[5]:①急性、突发、持续、剧烈的上腹部疼痛,可向背部放射;②血清淀粉酶和(或)脂肪酶活性至少高于正常上限值3倍;③增强CT或MRI呈AP典型影像学改变(胰腺水肿或胰周渗出积液)。临床上符合上述3项标准中的2项,即可诊断为AP,在此基础上伴有持续(>48 h)的器官功能衰竭,即诊断为SAP。。且所有病人均应用奥曲肽进行皮下或者静脉治疗。
1.1.3 干预措施 所有患者均给予AP常规基础治疗,包括禁食、抑酸、止痛、胃肠减压、纠正水电解质酸碱平衡紊乱、营养支持等,并积极防治局部或全身并发症;在此基础上试验组使用大剂量(1.2 mg/d)奥曲肽治疗,对照组使用常规剂量(0.6 mg/d)奥曲肽治疗。
1.1.4 结局指标 ①总有效率;②发热症状消失时间;③腹胀消失时间;④腹痛缓解时间;⑤腹痛消失时间;⑥血淀粉酶复常时间;⑦APCHE Ⅱ评分;⑧住院时间;⑨不良反应发生率;⑩病死率。
1.1.5 疗效判断标准 分为显效、有效和无效3个级别。显效:临床症状及体征完全消失,且辅助检查结果恢复正常;有效:临床症状及体征均改善但未完全消失,且辅助检查结果基本恢复正常;无效:临床症状和体征辅助检查结果无变化,甚至出现加重情况。总有效率=(显效+有效)/n×100%[11]。
1.1.6 排除标准 ①非随机对照试验;②奥曲肽与其他药物联合应用治疗SAP的文献;③重复发表及资料不全影响研究的文献。
1.2 检索策略
检索在国内外生物医学期刊上发表的有关不同剂量奥曲肽治疗SAP的临床随机对照文献。采取主题词与自由词结合的检索方式。以“胰腺炎”、“急性胰腺炎”、“急性重症胰腺炎”、“生长抑素类似物”、“奥曲肽”、“善宁”、“剂量”、“用量”、“量”为中文检索词,分别检索中文期刊全文数据库(CNKI)、维普期刊数据库及万方数据库资源系统。以“acute pancreatitis”、“severe acute pancreatitis”、“SAP”、“somatostatin”、“somatostatin analogues”、“octreotide”、“pancreatitis”、“dose”、“dosage”为英文检索词,检索PubMed。追踪综述类文献的参考文献。检索时间定为自建库起至2021年2月。中文数据库检索策略:#1胰腺炎 OR 急性胰腺炎 OR重症急性胰腺炎;#2奥曲肽 OR 生长抑素类似物 OR 善宁;#3剂量 OR 用量 OR 量;#1 AND #2 AND #3。英文数据库检索策略:#1(”pancreatitis” OR “acute pancreatitis” OR “severe acute pancreatitis” OR “SAP”)AND #2(“octreotide” OR “somatostatin” OR “somatostatin analogues”)AND #3(“dose” OR “dosage”)。
1.3 文献筛选
首先通过阅读文献题目以及摘要对已检出的所有文献初步筛选,将明显与纳入标准不相符的文献剔除;其次,阅读全文确定已检出文献是否完全符合纳入标准;最后,确定文献筛选结果。
1.4 资料提取
对最终确定纳入的文献提取所需的资料,包括:文献一般资料、干预资料以及结局指标资料。文献一般资料包括:文献作者、文献题目、发表时间、文献来源等;干预资料包括:不同剂量奥曲肽治疗分组对应的病例数、年龄、性别、日用药量、用药疗程、疗效判断标准等。结局指标资料包括:总有效率、发热症状消失时间、腹胀消失时间、腹痛缓解时间、腹痛消失时间、血淀粉酶复常时间、APCHE Ⅱ评分、住院时间、不良反应发生率、病死率等。
1.5 质量评价
应用Cochrane协作网提供的偏倚风险评估工具评价纳入研究文献质量,共分为以下6个方面:①随机分配方法是否正确;②是否有分配隐藏方案;③对研究对象是否采用盲法;④结局指标的评估是否采用盲法;⑤是否完整报告结果数据;⑥是否存在选择性报告研究结果。评价级别分为3个等级:是(low risk,低度偏倚)、否(high risk,高度偏倚)、不确定(unclear risk,不确定的偏倚情况)。
1.6 统计方法
从文献中所提取的数据使用Microsoft Excel软件电子表格记录,运用RevMan5.3软件进行meta分析。根据所得出的P值与I2,对所纳入的研究进行统计学异质性分析。当满足P≥0.1且I2≤50%,即说明纳入的研究之间无明显异质性,采用固定效应模型分析;当满足P<0.1且I2>50%,即说明研究之间存在明显的异质性,则采用随机效应模型分析。同时,二分类变量使用相对危险度(RR)及对应的95%CI表示,连续性变量使用标准化均数差(SMD)及对应的95% CI表示,以上两类变量均以P<0.05为差异具有统计学意义。利用漏斗图对主要指标治疗总有效率进行发表偏倚的评价分析。
2 结果
2.1 文献检索结果
初步检索共得到文献262篇,其中中文文献255篇,英文文献7篇,剔除重复文献后剩86篇;通过阅读标题及摘要,排除非临床RCT研究、研究主题不符、研究患者不符、干预措施不符后剩40篇文献;进一步阅读全文,排除对照措施不符、结局指标不符、数据不完整或存疑的文献后,最终共纳入11篇文献,共797例患者。文献检索流程见图1,纳入文献的基本信息见表1。
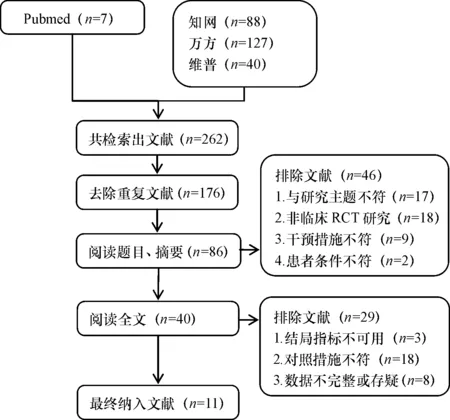
图1 文献筛选流程
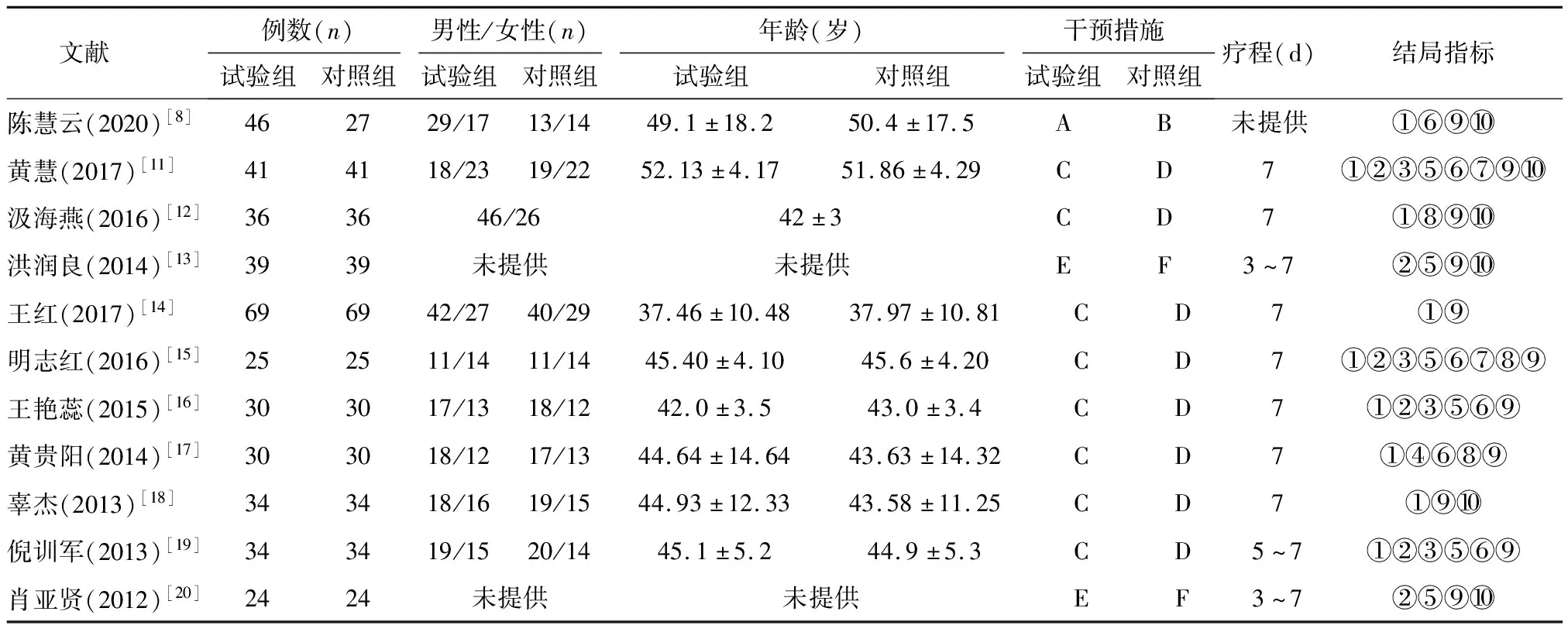
表1 纳入文献基本信息
2.2 纳入文献的质量评价
纳入的11篇文献均为临床随机对照研究,有2篇[12-13]说明采用随机数字表法,2篇[11,13]说明了患者在开始研究前已签署知情同意书,有10篇[8,11-19]说明了所采集的临床数据运用统计学软件SPSS进行统计,所有纳入研究均没有提及是否设计了盲法、分配隐藏及是否存在其他偏倚来源,详细偏倚风险评估见图2、图3。
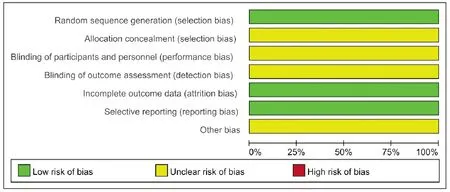
图2 纳入文献风险评估条形图
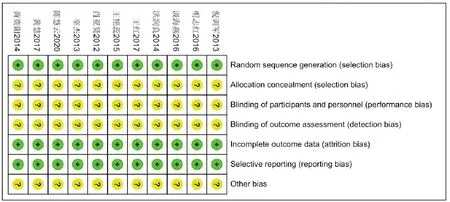
图3 偏倚风险图
2.3 Meta分析结果
2.3.1 总有效率 共有9篇文献[8,11-12,14-19]研究描述了总有效率,各研究之间不存在明显的异质性(P=0.59,I2=0%),故采用固定效应模型,详见图4。结果显示,试验组的总有效率显著高于对照组,差异有统计学意义[RR=1.14,95%CI:1.08~1.34,P<0.0001]。
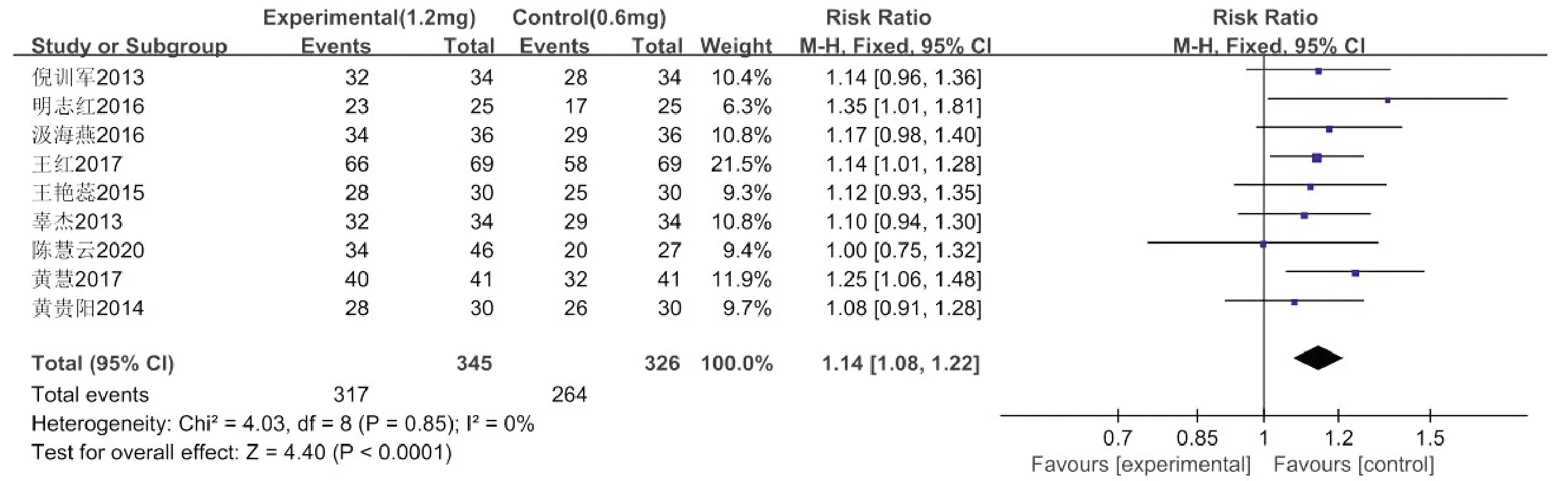
图4 总有效率Meta分析森林图
2.3.2 腹痛消失时间 共有6篇文献[11,13,15-16,19-20]研究描述了腹痛消失时间,各研究之间存在明显的异质性(P<0.00001,I2=81%),故采用随机效应模型,详见图5。结果显示,试验组的腹痛消失时间较对照组明显缩短,差异有统计学意义[SMD=-2.04,95%CI:-2.62~-1.45,P<0.00001]。
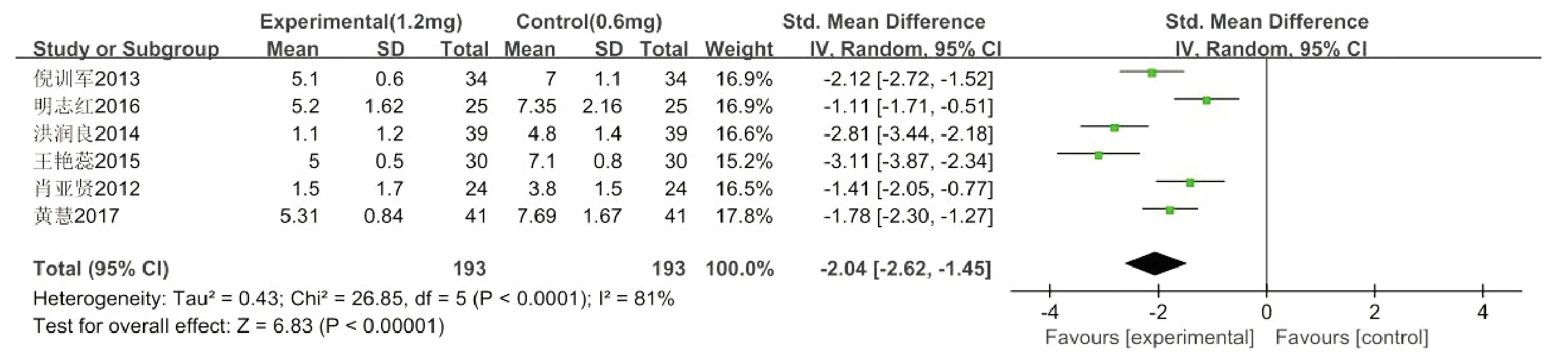
图5 腹痛消失时间Meta分析森林图
2.3.3 发热消失时间 共有6篇文献[11,13,15-16,19-20]研究描述了发热消失时间,各研究之间存在明显的异质性(P<0.00001,I2=89%),故采用随机效应模型,详见图6。结果显示,试验组的发热消失时间较对照组明显缩短,差异有统计学意义[SMD=-1.97,95%CI:-2.73~-1.21,P<0.00001]。
图6 发热消失时间Meta分析森林图
2.3.4 腹胀消失时间 共有3篇文献[11, 16, 19]研究描述了腹胀消失时间,各研究之间存在明显的异质性(P=0.0003,I2=87%),故采用随机效应模型,详见图7。结果显示,试验组的腹胀消失时间较对照组明显缩短,差异有统计学意义[SMD=-3.40,95%CI:-4.64~-2.17,P<0.00001]。

图7 腹胀消失时间Meta分析森林图
2.3.5 血淀粉酶复常时间 共有6篇文献[8,11,15-17,19]研究描述了血淀粉酶复常时间,各研究之间存在异质性(P=0.007,I2=69%),故采用随机效应模型,详见图8。结果显示,试验组的血淀粉酶复常时间较对照组缩短,差异有统计学意义[SMD=-1.51,95%CI:-1.92~-1.10,P<0.00001]。

图8 血淀粉酶复常时间Meta分析森林图
2.3.6 APACHEⅡ评分 共有2篇文献[11, 15]研究描述了APACHEⅡ评分,各研究之间不存在明显的异质性(P=0.74,I2=0%),故采用固定效应模型,详见图9。结果显示,试验组的APACHEⅡ评分较对照组低,差异有统计学意义[SMD=-2.23,95%CI:-2.67~-1.79,P<0.00001]。
2.3.7 不良反应发生率 共有11篇文献[8, 11-20]研究描述了不良反应发生率,各研究之间不存在明显的异质性(P=0.55,I2=0%),故采用固定效应模型,详见图9。结果显示,试验组的不良反应发生率较对照组低,差异有统计学意义[RR=0.68,95%CI:0.49~0.94,P=0.02]。
2.3.8 病死率 共有5篇文献[8,12-13,18,20]研究描述了病死率,各研究之间不存在明显的异质性(P=0.58,I2=0%),故采用固定效应模型,详见图10。结果显示,试验组的不良反应发生率与对照组相比,差异无统计学意义[RR=0.66,95%CI:0.32~1.39,P=0.28]。
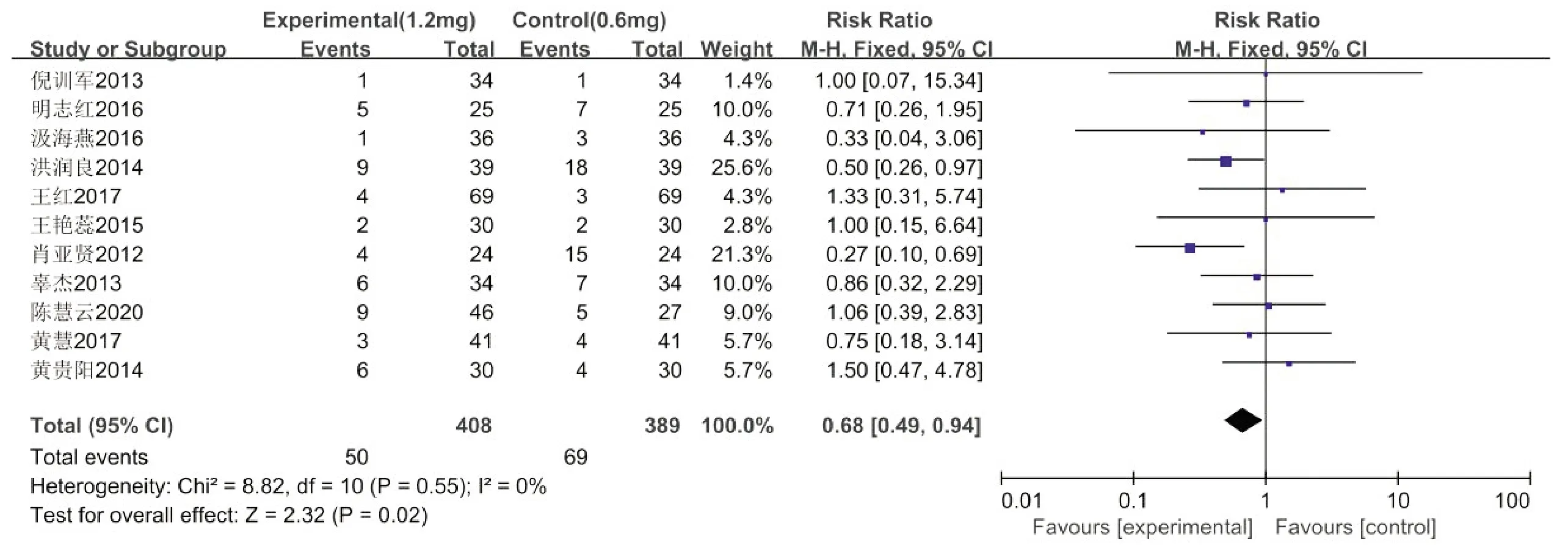
图10 不良反应发生率Meta分析森林图
2.3.9 住院时间 共有3篇文献[12, 15, 17]研究描述了住院时间,各研究之间存在异质性(P<0.00001,I2=97%),故采用随机效应模型,详见图12。结果显示,试验组的住院时间与对照组对比,差异无统计学意义[SMD=-2.04,95%CI:-4.12~0.04,P=0.05]。
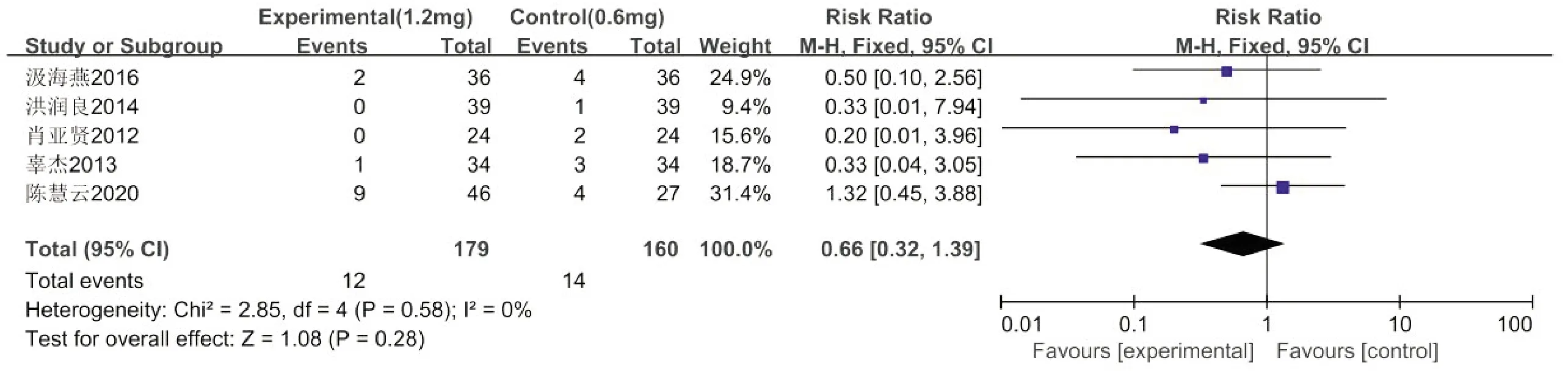
图11 病死率Meta分析森林图
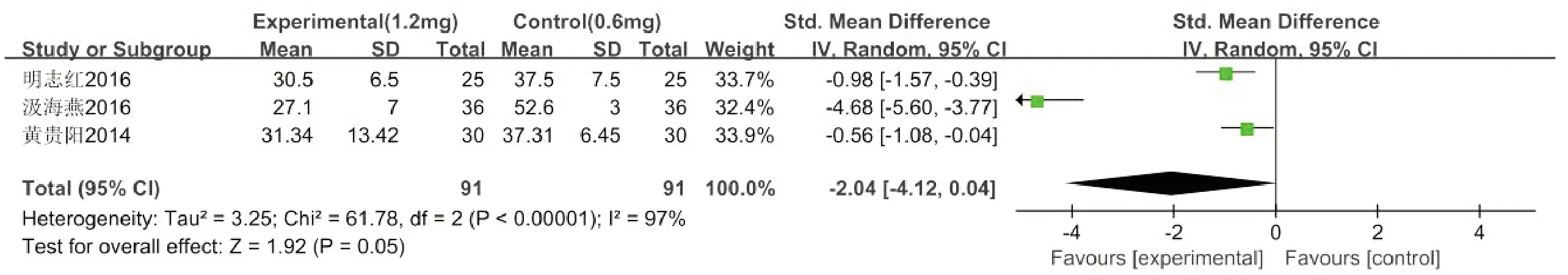
图12 住院时间Meta分析森林图
2.3.10 腹痛缓解时间 仅有1篇文献[17]研究描述了腹痛缓解时间,未行Meta分析。
2.4 发表偏倚分析
将纳入研究的RR值作为横坐标,将RR的对数标准误SE(log[RR])的倒数作为纵坐标,对不同剂量奥曲肽治疗SAP的总有效率进行漏斗图分析,结果(图13)显示,研究散点均落在漏斗图内,且左右基本对称,说明治疗总有效率发表偏倚较小。
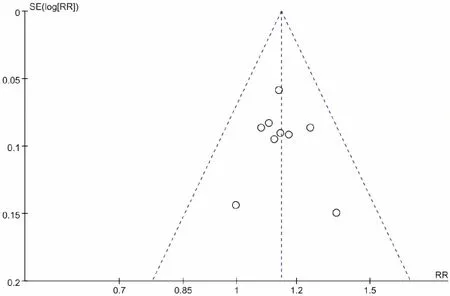
图13 总有效率发表偏倚漏斗图
3 讨论
在正常的生理情况下,人体合成的胰腺消化酶属于没有活性的酶原,酶原颗粒和细胞质是相互隔离的,胰管中的胰蛋白酶抑制物能够将少量的生物活性酶灭活,避免胰腺自身消化[21]。胰酶的异常活化及胰腺的微循环障碍在SAP发生的启动阶段起到重要作用,也是重症急性胰腺炎致多器官功能受损的关键一步[22]。
激活的胰酶破环胰腺组织导致胰腺坏死及出血,同时通过破坏血管内皮屏障和静脉回流进入循环系统并扩散至全身,导致全身血管通透性增加、多脏器出血,而坏死和继发感染可导致各种炎症因子释放并引起瀑布样级联反应[23-24]。
大量炎症因子作用于全身各组织器官,致使胃肠道缺血再灌注,胃肠功能紊乱,胃肠屏障受损和肠道菌群失调、移位,并诱发全身炎症反应,使多器官功能持续恶化、衰竭,最终导致患者死亡[25-26]。
奥曲肽为人工合成的八肽环状化合物,其药理作用与天然内源性生长抑素相类似,可抑制胰酶分泌,减少胰腺自身消化作用;使胃酸、胃泌素、胃蛋白酶释放减少,抑制肠胃运动;松弛Oddi括约肌,促进胰液排出[7, 27]。与内源性生长抑素相比,奥曲肽的半衰期及药效持续时间更长,临床应用也更广[8]。
奥曲肽主要通过抑制胃蠕动及胆囊排空而控制缩胆囊素和促胰液素分泌,从而减少胰酶分泌[21],因此可以抑制AP发生时的胰酶异常活化、分泌,有效地保护胰腺实质细胞,进而治疗AP[28]。
本研究根据制定的纳入及排除标准筛选,共纳入11篇文献,共797例病人,结果显示,1.2 mg/d的奥曲肽应用剂量在SAP的治疗上,较0.6 mg/d的疗效更好,可以更快改善患者的临床症状及体征,具体表现为腹痛、腹胀、发热的持续时间及血淀粉酶恢复正常所需的时间明显缩短,同时不良反应发生率更低,安全性好。此结论具有科学性,为指导临床用药提供证据,但也存在一定局限性:第一,纳入的研究均为国内报道文献,无国外报道文献,可能存在发表偏倚;第二,各纳入的研究中,关于奥曲肽的给药方式、总疗程、效果评价的定量描述均存在细微的不同,可能会增加异质性;第三,纳入的研究中,部分结局指标仅有极个别文献进行了比较分析,数据资料较少,无法进行Meta分析,这可能会对此Meta分析研究结果产生一定的影响。因此,此结论需更多大样本、高质量的RCT作为证据,提高结论的可靠性。

