代谢调控蛋白A调控革兰阳性菌代谢与毒力偶联的研究进展
杨紫瑜,秦娟秀,李 敏,刘 倩
上海交通大学医学院附属仁济医院检验科,上海200127
代谢调控蛋白A(catabolite control protein A,CcpA)是革兰阳性菌重要的全局性转录调控因子,属于LacI/GalR 家族,可直接或间接调控多种基因的转录表达,控制细胞的生理过程。CcpA 可以通过识别并结合至靶基因的特定序列执行其转录调控功能,形成复杂的调控网络。这类结合序列被称为代谢反应元件(catabolite response element,cre)。1991 年在枯草芽孢杆菌中首次证实,ccpA 基因失活可解除碳分解代谢物阻遏效应(carbon catabolite repression,CCR),与细菌次序利用碳源有关[1]。之后研究发现CcpA 存在于多种革兰阳性菌中,包括丙酮丁醇梭菌、艰难梭菌、屎肠球菌、乳酸乳球菌、变异链球菌等,这些革兰阳性菌均编码磷酸转移酶系统(phosphotransferase system,PTS),而CcpA 依赖PTS 调控细菌的代谢和毒力。
1 CcpA介导CCR效应及作用机制
1.1 CCR效应机制
CCR 是细菌中广泛存在的机制,通过控制细菌摄取与利用外界环境中的碳源,使细菌根据自身代谢能力选择利用能源,从而平衡其分解与合成代谢的能力。革兰阳性菌的CCR 主要依赖CcpA 调控,CcpA 则在PTS 的辅助下调控下游靶基因的转录表达[2-4]。PTS 能将糖类从细胞外跨膜主动运输进入细胞,并在此过程中将其磷酸化,被其转运的葡萄糖、甘露糖、果糖等可以直接参与代谢反应。细菌通过CCR 效应优先选择上述糖类作为首要能量来源,维持自身的代谢平衡。在革兰阳性菌中,PTS摄入的碳源经过糖酵解途径形成的中间产物1,6-二磷酸果糖,可促进含组氨酸的磷酸载体蛋白(histidinecontaining phosphocarrier protein,Hpr)第46 位丝氨酸残基被Hpr 激酶(Hpr kinase,HprK)磷酸化,生成Hpr-Ser~P,其可以结合并活化转录调节因子CcpA;该复合物与位于靶基因启动子或编码区的cre 位点结合后,可抑制编码次要碳源转运和代谢所需酶的基因转录[5-6](图1)。
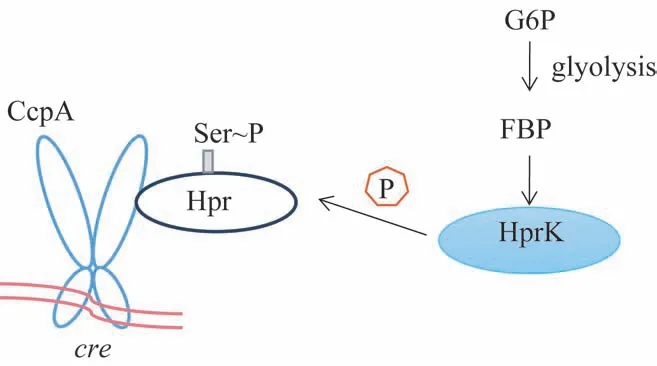
图1 革兰阳性菌CcpA摄取葡萄糖过程Fig 1 Glucose uptake by CcpA in Gram-positive bacteria
枯草芽孢杆菌中存在另一种Hpr 同源蛋白Crh(catabolite repression HPr),其第46 位丝氨酸残基也可被HprK 磷酸化,形成CcpA-(Crh-Ser~P)复合物。但Crh参与完成的PTS调控作用并不能完全替代Hpr[7],目前已知柠檬酸盐转运体基因(citrate transporter,citM)仅依赖Crh-Ser~P 进行PTS 调节。Hpr 与Crh 的区别在于,Hpr-Ser~P 与CcpA 的亲和力高,结合能力更强[8]。除此之外,1,6-二磷酸果糖和6-磷酸果糖等小分子可以作为Hpr-Ser~P 的辅因子,根据细胞对代谢的需求刺激CcpA与DNA结合,但这类小分子不能辅助Crh-Ser~P作用[9]。
1.2 CcpA作用机制
CcpA 通过识别并结合靶基因DNA 序列中不同位置特异性cre 序列发挥功能。当cre 序列位于基因启动子上游时,CcpA 通常具有激活效应;如在枯草芽胞杆菌中,CcpA 可以促进乙酸激酶编码基因(acetate kinase,ackA)、 磷 酸 转 乙 酰 酶 编 码 基 因 (phosphate acetyltransferase,pta)的转录表达[10]。当cre序列位于靶基因的启动子区或编码区时,CcpA 通常产生阻遏效应;如在艰难梭菌中,CcpA 抑制RNA 多聚酶σ 因子(σ factor required for toxin production,tcdR)、乳酸脱氢酶等基因的转录表达[11]。然而,cre 序列的位置与CcpA的效应并不是绝对的;比如枯草芽孢杆菌中CcpA 结合果糖操纵子(levD、levE、levF、levG)的启动子上游区cre序列,却抑制了该操纵子的转录[12]。
1.3 CcpA调节机制
CcpA 可以调控自身的转录表达,戊糖乳杆菌和木糖葡萄球菌中,CcpA 可以结合自身启动子区单个cre 位点,调节ccpA 表达[13-14]。在丙酮丁醇梭菌中发现了一种新的双向自我调控机制,ccpA 基因上存在2 个CcpA 结合位点:分别位于其启动子区(CcpA-creP) 和编码区(CcpA-creORF),CcpA 与CcpA-creP结合能通过募集RNA多聚酶促进ccpA 的表达,而与CcpA-creORF结合则通过阻遏基因转录来抑制基因表达[15]。此外,CcpA本身受细菌生长环境的影响,在肺炎链球菌中,高浓度的甲酸盐能促进谷氨酰胺合成酶转录抑制子GlnR 与ccpA基因上游的cre 序列结合,从而上调ccpA 表达[16]。CcpA 同时也受细菌编码的其他调节蛋白调控。金黄色葡萄球菌中参与中心代谢的丝氨酸/苏氨酸蛋白激酶1 (serine/threonine protein kinase 1,Stk1),可以将CcpA的第18位和第33位苏氨酸磷酸化,使其DNA 结合能力减弱,且CcpA 磷酸化菌株与ccpA 基因敲除株的靶基因表达水平和生物被膜形成能力相似。这进一步证明了Stk1对CcpA 的磷酸化抑制了CcpA 对靶基因的调控[17],代表了一种新的转录因子调节机制。但Stk1对CcpA 的磷酸化调控作用尚未在其他菌属中报道,提示在不同菌属中CcpA 活性的调节具有差异。
2 CcpA在细菌代谢调控中的作用
2.1 CcpA调控糖代谢
糖类是细菌的主要能源物质。微生物在以糖类为主要能源时,CcpA 可以调控代谢相关基因的表达,合理利用碳源[16,18-27]。
枯草芽孢杆菌中,CcpA 促进PTS 转运糖类过程中产生大量3-磷酸甘油醛,抑制中心糖酵解基因调节子结合3-磷酸甘油醛脱氢酶操纵子,间接促进3-磷酸甘油醛脱氢酶的表达,激活糖酵解途径[19-20]。在德氏乳杆菌保加利亚亚种和乳酸乳球菌中,CcpA 能上调las 操纵子(编码乳酸脱氢酶、磷酸果糖激酶和丙酮酸激酶)的表达[21-23],不仅促进糖酵解,还使丙酮酸代谢为L-乳酸,减少进入三羧酸(tricarboxylic acid cycle,TCA)的碳流量。变异链球菌中的磷酸转乙酰酶和乙酸激酶可以促使丙酮酸转化为乙酸,使其自身适应外界压力环境。CcpA 在1,6-二磷酸果糖的作用下结合ackA启动子区域的cre序列,通过高表达乙酸激酶促进丙酮酸转变为乙酸;乙酸等代谢物的堆积导致环境pH 值降低,CcpA 又通过抑制pta 表达,减少乙酸的堆积[24]。同样,在枯草芽孢杆菌中,CcpA和转录因子CodY(transcriptional regulator,GTP and BCAAdependent)协同作用,通过结合ackA 基因编码序列的上游区域,上调ackA 表达,促进丙酮酸代谢为乙酸,使细菌合理利用碳源[25]。金黄色葡萄球菌中,CcpA通过直接结合编码TCA循环的重要酶基因的cre序列,阻遏乌头酸水合酶、异柠檬酸脱氢酶和柠檬酸合酶等转录表达,从而抑制TCA循环[26-27]。
细菌以葡萄糖为首选碳源,但当缺乏葡萄糖时,CcpA 可调节其他糖代谢途径以维持细菌生存。在半乳糖丰富的环境中,细菌利用半乳糖产生多种有机酸,其中丙酮酸甲酸裂解酶(pyruvate formate lyase,PFL)是一种关键酶。PFL 需要丙酮酸甲酸裂解酶活化酶(pyruvate formate-lyase activating enzyme,Pfla)和丙酮酸甲酸裂解酶(pyruvate formate-lyase,Pflb)共同作用而催化半乳糖代谢,CcpA 通过影响PFL 的活性来调节半乳糖代谢途径[16]。在富含半乳糖且氧气缺乏的环境中,肺炎链球菌CcpA 通过上调pflB 的表达,促进细菌发酵半乳糖来获取能量[16]。乳酸乳球菌的半乳糖操纵子,如阿拉伯半乳聚糖 内- β -1,4- 半 乳 聚 糖 酶 编 码 基 因 (putative arabinogalactan endo-β-1,4-galactanase,galA)、半乳糖变旋酶编码基因(galactose-1-epimerase,galM)、半乳糖激酶编码基因(galactokinase,galK)、半乳糖-1-磷酸尿苷 酰 转 移 酶 编 码 基 因 (galactose-1-phosphate uridylyltransferase,galT)、UDP-葡萄糖-4-差向异构酶编码基因(UDP-glucose 4-epimerase,galE),能够编码摄取和转化半乳糖的关键酶;且galA 启动子区存在cre 序列,当半乳糖为唯一碳源时,细菌CcpA 通过调控半乳糖操纵子的表达促使细菌利用半乳糖,促进自身生长[23]。
2.2 CcpA调控蛋白质代谢
CcpA 可以调控细菌摄取及利用氨基酸的能力。艰难梭菌中CcpA 可促进脯氨酸还原酶表达,催化脯氨酸转化为5-氨基戊酸,促进艰难梭菌在肠道中定植[28]。金黄色葡萄球菌利用谷氨酸盐合成精氨酸,而ccpA 突变金黄色葡萄球菌株还可以利用脯氨酸作为底物,通过尿素循环合成精氨酸,提示CcpA 可能通过抑制脯氨酸代谢来调控精氨酸合成[29]。在高浓度葡萄糖环境中,金黄色葡萄球菌CcpA 通过结合氨基酸降解酶(如丙氨酸脱氢酶、乙醛脱氢酶和精氨酸酶)编码区的cre序列[25],阻遏细菌大量利用氨基酸。而当生存环境中葡萄糖受限(如细菌在宿主体内形成脓肿),谷氨酸成为金黄色葡萄球菌的首选能量来源。因此若谷氨酸不足,细菌通过下调ccpA 表达,促进细菌利用脯氨酸、组氨酸、精氨酸来合成谷氨酸,以维持自身生长[30]。
2.3 CcpA调控脂肪酸代谢
细胞膜的脂肪酸组分变化是变异链球菌应对酸性环境的机制之一。酸性环境中,变异链球菌CcpA 可与fabTSm(变异链球菌中脂肪酸代谢合成基因簇成员)编码区上游的cre 序列结合而抑制其转录,进而下调脂肪酸合成基因簇中fabM 的表达,导致长链不饱和脂肪酸与短链饱和脂肪酸比例上调,增强细菌抗酸能力[31]。在葡萄糖丰富的环境中,金黄色葡萄球菌CcpA 抑制甘油摄取蛋白和甘油激酶基因表达,降低外源甘油的利用率,同时抑制乙酰辅酶A 羧化酶,减少脂肪酸合成,从而在一定程度上阻遏脂肪酸代谢[25]。
3 CcpA在细菌毒力调控中的作用
3.1 CcpA影响细菌结构
细菌的荚膜、鞭毛等结构成分与细菌毒力密切相关,在细菌黏附入侵和感染过程中发挥重要作用。通过cDNA表达阵列对高毒力猪链球菌血清2 型的CcpA 功能分析发现,ccpA 突变菌株中共259 个基因表达水平发生变化,其中与荚膜和细胞壁合成相关的18 个基因表达下调;电子显微镜观察发现ccpA 突变菌株的荚膜厚度显著下降;此外,ccpA 突变菌株与猪血浆蛋白的黏附能力增强,抵抗猪中性粒细胞杀伤能力减弱,证明了CcpA 促进猪链球菌的荚膜形成和提高毒力[32]。单核细胞增生李斯特菌的ccpA 缺失菌株无法形成鞭毛,从而减弱了细菌的扩散能力,提示CcpA 参与调控细菌鞭毛的形成过程[33]。血链球菌SK36 的四型菌毛(type Ⅳpili,Tpf)对于细菌的宿主细胞黏附至关重要,而缺乏CcpA 时菌毛相关基因的表达受到明显抑制[34]。
3.2 CcpA影响毒素合成
CcpA 是细菌毒素表达的重要调节因子之一。艰难梭菌毒素的产生受到葡萄糖或其他碳源的抑制,但不受代谢引起的pH 值变化的影响。研究者[35]发现当葡萄糖存在时,ccpA 突变艰难梭菌株中糖基化毒素基因(glycosylating toxin TcdA,tcdA)和tcdB 表达水平下降,证明葡萄糖和转录调控因子CcpA 是抑制毒素基因表达的关键因子。该研究者还发现,CcpA 可以与艰难梭菌毒素基因座中5个cre位点结合,其中,CcpA与tcdR的启动子亲和力最强,可以抑制tcdR 的表达,从而抑制艰难梭菌的主要毒素TcdA 和TcdB 的产生,证明了在艰难梭菌中CcpA 作为代谢调控蛋白能同时调节细菌的毒力因子[11,35]。在咽峡炎链球菌和A 群链球菌中,CcpA 也能通过直接与链球菌溶血素S的启动子结合来抑制溶血素的产生[36-37]。在高糖培养条件下,金黄色葡萄球菌的CcpA 促进其重要毒力因子α溶血素的表达,增强细菌的毒力[38]。
CcpA 可与其他全局转录调控因子相互作用影响细菌毒力,如CcpA 与CodY 可共同调控四型产气荚膜梭菌中ε 毒素的产生;此外,CcpA 能直接与codY 起始密码子上游结合促进codY 基因的转录[39]。艰难梭菌中CodY 在支链氨基酸和GTP的辅助下,可与CcpA共同抑制tcdR的表达和丁酸盐形成,从而抑制毒素产生[40]。产气荚膜梭菌芽胞在肠道中产生的毒素(C. perfringens enterotoxin,Cpe)可导致食物中毒; CcpA 在肠道中促进芽孢产生,进而活化孢子形成特异性聚合酶(RNA polymerase sporulation-specific sigma-29 factor,SigE)、SigK,活化的SigE、SigK 可与cpe基因的启动子区域结合,促进Cpe的合成[41]。
3.3 CcpA调控细菌致病性
细菌代谢变化和毒素表达与细菌的致病性密切相关。动物模型的研究发现,CcpA 通过调控细菌代谢和毒力基因的转录表达,提高细菌的致病性[42-44]。小鼠皮肤脓肿感染模型研究表明,化脓链球菌ccpA 敲除株的毒力较野生菌株显著减弱,具有高DNA 结合力的ccpAT307Y点突变株毒力虽有下降,但细菌定植率明显增高[42]。同样在屎肠球菌中也发现,在心内膜炎感染小鼠模型中,ccpA 基因突变株的生长速度和毒力均显著降低[43]。
肺炎链球菌通过TprA/PhrA 群体感应(quorum sensing,QS)系统调控自身对半乳糖和甘露糖的利用能力、神经氨酸酶活性和大量细胞外毒力因子。CcpA 通过感知外界环境的变化调控QS 系统,如在葡萄糖存在时抑制tprA(多效性调控子的直系同源物)启动子,在半乳糖存在时促进tprA 表达;由于宿主体内不同组织中所含糖的种类与浓度不同,如呼吸道可分泌半乳糖和甘露糖,而血液中葡萄糖浓度更高,CcpA 可根据不同部位糖类的不同促进或阻遏tprA 的表达,有利于细菌在不同组织中的定植与感染[44]。
4 总结
综上所述,CcpA 通过复杂的调控网络参与了细菌的生存及致病过程。CcpA 调控的基因广泛参与革兰阳性菌糖酵解、TCA循环和氨基酸代谢等,同时CcpA也影响细菌致病性,从而将细菌的代谢和毒力偶联。CcpA 还可调控细菌在不同培养环境下的生存能力,但其如何在不同环境中通过特定的功能域调控特异代谢途径从而发挥功能尚未完全阐明。CcpA 调控细菌定植、致病及耐药的分子机制有待于进一步研究。
参·考·文·献
[1] Henkin TM, Grundy FJ, Nicholson WL, et al. Catabolite repression of α amylase gene expression in Bacillus subtilis involves a trans-acting gene product homologous to the Escherichia coli lacl and galR repressors[J].Mol Microbiol,1991,5(3):575-584.
[2] Brückner R, Titgemeyer F. Carbon catabolite repression in bacteria: choice of the carbon source and autoregulatory limitation of sugar utilization[J].FEMS Microbiol Lett,2002,209(2):141-148.
[3] Park H, McGill SL, Arnold AD, et al. Pseudomonad reverse carbon catabolite repression, interspecies metabolite exchange, and consortial division of labor[J]. Cell Mol Life Sci,2020,77(3):395-413.
[4] Grand M, Aubourg M, Pikis A, et al. Characterization of the Gen locus involved in β-1,6-oligosaccharide utilization by Enterococcus faecalis[J].Mol Microbiol,2019,112(6):1744-1756.
[5] Warner JB, Lolkema JS. CcpA-dependent carbon catabolite repression in bacteria[J]. Microbiol Mol Biol Rev,2003,67(4):475-490.
[6] Yang Y,Zhang L,Huang H,et al. A flexible binding site architecture provides new insights into CcpA global regulation in Gram-positive bacteria[J]. mBio,2017,8(1):e02004-16.
[7] Galinier A, Haiech J, Kilhoffer MC, et al. The Bacillus subtilis crh gene encodes a HPr-like protein involved in carbon catabolite repression[J]. Proc Natl Acad Sci USA,1997,94(16):8439-8444.
[8] Schumacher MA, Seidel G, Hillen W, et al. Phosphoprotein Crh-Ser46-P displays altered binding to CcpA to effect carbon catabolite regulation[J]. J Biol Chem,2006,281(10):6793-6800.
[9] Schumacher MA, Seidel G, Hillen W, et al. Structural mechanism for the fine-tuning of CcpA function by the small molecule effectors glucose 6-phosphate and fructose 1,6-bisphosphate[J]. J Mol Biol, 2007, 368(4):1042-1050.
[10] Schumacher MA, Sprehe M, Bartholomae M, et al. Structures of carbon catabolite protein A-(HPr-Ser46-P) bound to diverse catabolite response element sites reveal the basis for high-affinity binding to degenerate DNA operators[J]. Nucleic Acids Res,2011,39(7):2931-2942.
[11] Antunes A, Camiade E, Monot M, et al. Global transcriptional control by glucose and carbon regulator CcpA in Clostridium difficile[J]. Nucleic Acids Res,2012,40(21):10701-10718.
[12] Martin-Verstraete I,Stülke J,Klier A,et al. Two different mechanisms mediate catabolite repression of the Bacillus subtilis levanase operon[J]. J Bacteriol,1995,177(23):6919-6927.
[13] Mahr K, Hillen W, Titgemeyer F. Carbon catabolite repression in Lactobacillus pentosus: analysis of the ccpA region[J]. Appl Environ Microbiol,2000,66(1):277-283.
[14] Egeter O,Brückner R. Catabolite repression mediated by the catabolite control protein CcpA in Staphylococcus xylosus[J]. Mol Microbiol, 1996, 21(4):739-749.
[15] Zhang L, Liu YQ, Yang YP, et al. A novel dual-cre motif enables two-way autoregulation of CcpA in Clostridium acetobutylicum[J]. Appl Environ Microbiol,2018,84(8):e00114-18.
[16] Al-Bayati FAY, Kahya HFH, Damianou A, et al. Pneumococcal galactose catabolism is controlled by multiple regulators acting on pyruvate formate lyase[J]. Sci Rep,2017,7:43587.
[17] Leiba J, Hartmann T, Cluzel ME, et al. A novel mode of regulation of the Staphylococcus aureus catabolite control protein A(CcpA)mediated by Stk1 protein phosphorylation[J]. J Biol Chem,2012,287(52):43607-43619.
[18] Peng Q,Zhao X,Wen J,et al. Transcription in the acetoin catabolic pathway is regulated by AcoR and CcpA in Bacillus thuringiensis[J]. Microbiol Res,2020,235:126438.
[19] Tobisch S, Zühlke D, Bernhardt J, et al. Role of CcpA in regulation of the central pathways of carbon catabolism in Bacillus subtilis[J]. J Bacteriol,1999,181(22):6996-7004.
[20] Ludwig H, Rebhan N, Blencke HM, et al. Control of the glycolytic gapA operon by the catabolite control protein A in Bacillus subtilis: a novel mechanism of CcpA-mediated regulation[J]. Mol Microbiol, 2002, 45(2):543-553.
[21] Zhang GF, Liu LB, Li C. Effects of ccpA gene deficiency in Lactobacillus delbrueckii subsp. bulgaricus under aerobic conditions as assessed by proteomic analysis[J]. Microb Cell Fact,2020,19:9.
[22] Li C, Sun JW, Zhang GF, et al. Effect of the absence of the CcpA gene on growth, metabolic production, and stress tolerance in Lactobacillus delbrueckii ssp. bulgaricus[J]. J Dairy Sci,2016,99(1):104-111.
[23] Luesink EJ, van Herpen RE, Grossiord BP, et al. Transcriptional activation of the glycolytic Las operon and catabolite repression of the gal operon in Lactococcus lactis are mediated by the catabolite control protein CcpA[J].Mol Microbiol,1998,30(4):789-798.
[24] Kim JN, Burne RA. CcpA and CodY coordinate acetate metabolism in Streptococcus mutans[J]. Appl Environ Microbiol,2017,83(7):e03274-16.
[25] Shivers RP, Dineen SS, Sonenshein AL. Positive regulation of Bacillus subtilis ackA by CodY and CcpA: establishing a potential hierarchy in carbon flow[J]. Mol Microbiol,2006,62(3):811-822.
[26] Seidl K,Müller S,François P,et al. Effect of a glucose impulse on the CcpA regulon in Staphylococcus aureus[J]. BMC Microbiol,2009,9:95.
[27] Reed JM, Olson S, Brees DF, et al. Coordinated regulation of transcription by CcpA and the Staphylococcus aureus two-component system HptRS[J].PLoS One,2018,13(12):e0207161.
[28] Fletcher JR, Erwin S, Lanzas C, et al. Shifts in the gut metabolome and Clostridium difficile transcriptome throughout colonization and infection in a mouse model[J]. mSphere,2018,3(2):e00089-18.
[29] Nuxoll AS, Halouska SM, Sadykov MR, et al. CcpA regulates arginine biosynthesis in Staphylococcus aureus through repression of proline catabolism[J]. PLoS Pathog,2012,8(11):e1003033.
[30] Halsey CR, Lei SL, Wax JK, et al. Amino acid catabolism in Staphylococcus aureus and the function of carbon catabolite repression[J].mBio,2017,8(1):e01434-16.
[31] Faustoferri RC, Hubbard CJ, Santiago B, et al. Regulation of fatty acid biosynthesis by the global regulator CcpA and the local regulator FabT in Streptococcus mutans[J]. Mol Oral Microbiol,2015,30(2):128-146.
[32] Willenborg J, Fulde M, de Greeff A, et al. Role of glucose and CcpA in capsule expression and virulence of Streptococcus suis[J]. Microbiology,2011,157(6):1823-1833.
[33] 瞿慧萍. CcpA在单核细胞增生李斯特菌中的功能初探[D]. 武汉:华中师范大学,2014.
[34] Chen YM,Chiang YC,Tseng TY,et al. Molecular and functional analysis of the type Ⅳpilus gene cluster in Streptococcus sanguinis SK36[J]. Appl Environ Microbiol,2019,85(6):e02788-18.
[35] Antunes A, Martin-Verstraete I, Dupuy B. CcpA-mediated repression of Clostridium difficile toxin gene expression[J]. Mol Microbiol, 2011, 79(4):882-899.
[36] Bauer R, Mauerer S, Spellerberg B. Regulation of the β-hemolysin gene cluster of Streptococcus anginosus by CcpA[J]. Sci Rep,2018,8:9028.
[37] Kinkel TL, McIver KS. CcpA-mediated repression of streptolysin S expression and virulence in the group A Streptococcus[J]. Infect Immun,2008,76(8):3451-3463.
[38] Bischoff M, Wonnenberg B, Nippe N, et al. CcpA affects infectivity of Staphylococcus aureus in a hyperglycemic environment[J]. Front Cell Infect Microbiol,2017,7:172.
[39] Li J, Freedman JC, McClane BA. NanI sialidase, CcpA, and CodY work together to regulate epsilon toxin production by Clostridium perfringens type D strain CN3718[J]. J Bacteriol,2015,197(20):3339-3353.
[40] Martin-Verstraete I, Peltier J, Dupuy B. The regulatory networks that control Clostridium difficile toxin synthesis[J]. Toxins (Basel), 2016,8(5):153.
[41] Varga J, Stirewalt VL, Melville SB. The CcpA protein is necessary for efficient sporulation and enterotoxin gene (cpe) regulation in Clostridium perfringens[J]. J Bacteriol,2004,186(16):5221-5229.
[42] Paluscio E, Watson ME, Caparon MG. CcpA coordinates growth/damage balance for Streptococcus pyogenes pathogenesis[J]. Sci Rep, 2018, 8(1):14254.
[43] Somarajan SR, Roh JH, Singh KV, et al. CcpA is important for growth and virulence of Enterococcus faecium[J]. Infect Immun,2014,82(9):3580-3587.
[44] Motib AS, Al-Bayati FAY, Manzoor I, et al. TprA/PhrA quorum sensing system has a major effect on pneumococcal survival in respiratory tract and blood, and its activity is controlled by CcpA and GlnR[J]. Front Cell Infect Microbiol,2019,9:326.

