血清高迁移率族蛋白B1在老年慢性阻塞性肺疾病急性加重病人中的表达及N-乙酰半胱氨酸泡腾片干预效果研究
张立南 刘明 邸红
COPD好发于老年人群,具有气流阻塞特征,严重者可发展为肺心病等[1]。血清高迁移率族蛋白B1(HMGB1)广泛存在于细胞核、细胞质中,被视为多种炎症疾病治疗的潜在靶点[2]。同时,HMGB1能诱导IL-1、IL-8及TNF-α的释放,激活热内皮细胞。N-乙酰半胱氨酸泡腾片主要成分为乙酰半胱氨酸,适用于分泌大量浓稠痰液的COPD、慢性支气管炎(CB)、肺气肿(PE)等慢性呼吸系统感染疾病[3-4],但是药物对老年COPD急性加重(AECOPD)病人HMGB1的影响研究较少。因此,本研究拟探讨HMGB1在老年AECOPD病人中的表达及N-乙酰半胱氨酸泡腾片的干预效果,现报道如下。
1 资料与方法
1.1 临床资料 选取2018年1月至2019年10月老年AECOPD病人82例为AECOPD组,其中男43例,女39例,年龄60~83岁,平均(76.33±5.45)岁;病程1~7 d,平均(3.29±0.61)d。根据GOLD指南对病人病情严重度进行评估,轻度36例,中度30例,重度16例;合并糖尿病8例,高血压12例,高脂血症15例;吸烟43例。选择同期治疗的老年COPD稳定期病人71例为COPD组,男40例,女31例,年龄60~84岁,平均(75.16±5.43)岁;病程1~9个月,平均(3.43±0.69)月;合并糖尿病9例,高血压11例,高脂血症14例;吸烟41例。选择同期健康体检者51例为对照组,男32例,女19例,年龄61~85岁,平均(75.31±5.45)岁。本研究得到医院伦理委员会批准,病人及家属签署知情同意书。
1.2 纳入、排除标准 纳入标准:(1)符合COPD急性加重、稳定期诊断标准;(2)入组病人年龄≥60岁,均能完成HMGB1、TNF-α及肺功能检测;(3)AECOPD病人均符合N-乙酰半胱氨酸泡腾片治疗适应证。
排除标准:(1)合并精神异常、器质性疾病或入院前2周给予抗生素治疗者;(2)合并脓毒症、败血症及类风湿关节炎等全身性疾病者;(3)合并恶性肿瘤、认知功能障碍或伴有自身免疫系统疾病者;(4)对N-乙酰半胱氨酸泡腾片过敏者。脱落标准:(1)病情恶化或死亡者;(2)病例资料不完整或失访者。
1.3 方法
1.3.1 HMGB1、TNF-α检测:AECOPD组、COPD组入院后次日早晨取外周静脉血5 mL,对照组健康体检当天取外周静脉血5 mL,离心后放置在-80 ℃冰箱中,备用。采用ELISA法测定3组HMGB1、TNF-α水平。
1.3.2 治疗方法:AECOPD组根据病人意愿是否使用N-乙酰半胱氨酸泡腾片治疗分为使用组(n=41)和未使用组(n=41)。未使用组入院后给予常规对症支持治疗,使用组在未使用组基础上联合N-乙酰半胱氨酸泡腾片治疗。每次取N-乙酰半胱氨酸泡腾片(浙江金华康恩贝生物制药有限公司,国药准字H20057334,规格:600 mg)600 mg,2次/d,连续治疗1个月。
1.4 观察指标 (1)HMGB1、TNF-α水平:比较入组时3组HMGB1、TNF-α水平;AECOPD组均完成1个月治疗,记录病人治疗前、治疗1个月后HMGB1、TNF-α水平。(2)COPD评估测试评分(CAT):采用CAT量表评估使用组与未使用组病人的疾病严重程度。(3)肺功能水平:使用组与未使用组治疗前、治疗1个月后采用Master screen PET肺功能测定仪测定病人FEV1、FVC、FEV1/FVC水平。(4)安全性:记录使用组与未使用组治疗过程中恶心呕吐、腹泻便秘、血压波动、肝肾异常发生率。
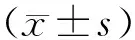
2 结果
2.1 各组HMGB1及TNF-α水平比较 AECOPD组HMGB1、TNF-α水平均高于COPD组和对照组(P<0.05);COPD组HMGB1、TNF-α水平高于对照组(P<0.05);AECOPD组重度病人HMGB1、TNF-α水平高于轻度、中度病人(P<0.05)。见表1。

表1 各组HMGB1、TNF-α水平比较
2.2 AECOPD病人治疗前后HMGB1、TNF-α水平及CAT评分比较 2组治疗前HMGB1及TNF-α水平、CAT评分差异均无统计学意义(P>0.05);2组治疗后HMGB1及TNF-α水平、CAT评分均低于治疗前(P<0.05);使用组治疗后HMGB1及TNF-α水平、CAT评分均低于未使用组(P<0.05)。见表2。
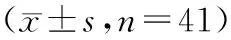
表2 AECOPD病人治疗前后HMGB1、TNF-α水平及CAT评分比较
2.3 AECOPD病人治疗前后肺功能水平比较 AECOPD病人使用组与未使用组干预前肺功能水平差异无统计学意义(P>0.05);干预1个月后,2组肺功能FEV1、FVC及FEV1/FVC水平均得到改善,且使用组改善更显著(P<0.05)。见表3。
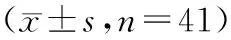
表3 AECOPD病人治疗前后肺功能水平比较
2.4 使用组与未使用组安全性比较 2组治疗过程中恶心呕吐、腹泻便秘、血压波动、肝肾功能异常发生率差异无统计学意义(P>0.05),见表4。
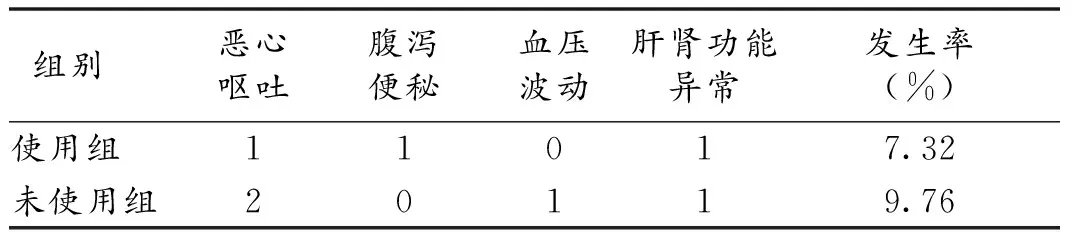
表4 使用组与未使用组安全性比较(n,n=41)
3 讨论
HMGB1最早于20世纪60年代被发现,因其在聚丙烯酰胺凝胶电泳中迁移率较高而得名[5]。国内学者研究表明,HMGB1释放到胞外后能介导机体炎症反应,属于内毒素血症、脓毒症晚期的炎症介质[6]。而机体炎症反应早期释放TNF-α,随着病情的不断加剧,将会刺激晚期炎症介质HMGB1的合成。同时,HMGB1亦可延迟激活单核/巨噬细胞,产生瀑布级联反应,加剧病情发展。因此,HMGB1、TNF-α水平在正常人体中表达水平较低或处于动态平衡状态;而在老年AECOPD病人中HMGB1、TNF-α水平呈上升趋势。本研究中,AECOPD组HMGB1、TNF-α水平均高于COPD组和对照组(P<0.05);COPD组HMGB1、TNF-α水平高于对照组(P<0.05);AECOPD组重度病人HMGB1、TNF-α水平高于轻度、中度病人(P<0.05),说明HMGB1、TNF-α在老年AECOPD病人中呈高表达,其表达水平能反映病人的疾病严重程度,可指导临床治疗。
N-乙酰半胱氨酸泡腾片属于黏痰溶解剂,具有较强的黏液溶解作用,其主要是由于药物分子中含有巯基(-SH),能使痰中糖蛋白多肽链的二硫键断裂,降低痰液的黏滞性,使得痰液更加容易咳出。现代药理结果表明,N-乙酰半胱氨酸泡腾片临床使用能经小肠迅速吸收,并且在用药后1~2 h血药浓度达到峰值。同时,药物进入机体血液循环前多数药物已经发生去乙酰化,部分药物在肝脏内代谢,具有较高的生物利用度[7]。本研究中,AECOPD组N-乙酰半胱氨酸泡腾片治疗1个月后HMGB1、TNF-α水平均低于治疗前(P<0.05),病人肺功能得到明显改善,且优于未使用组(P<0.05);2组治疗过程中恶心呕吐、腹泻便秘、血压波动、肝肾功能异常发生率差异无统计学意义(P>0.05)。说明N-乙酰半胱氨酸泡腾片能降低老年AECOPD病人HMGB1、TNF-α水平,有助于改善病人肺功能,利于病人恢复,且药物使用安全性较高,未增加药物不良反应发生率。但是,由于老年COPD急性加重期病人病情变化较快,应加强HMGB1、TNF-α水平监测,动态了解病人病情变化情况,根据病人恢复情况调整治疗方案,降低临床死亡率。
综上所述,HMGB1在老年AECOPD病人中呈高表达,在常规治疗基础上联合N-乙酰半胱氨酸泡腾片治疗干预能降低病人的HMGB1、TNF-α水平,提高肺功能水平,值得推广应用。

