燃烧条件探究实验的改进
江苏省宜兴市行知实验学校(214262) 薛 昊
1 教材中的实验
教材中的实验是:“在500 mL的烧杯中注入400 mL热水,并放入用硬纸圈圈住的一小块白磷。在烧杯上盖一片薄铜片,铜片上一端放一堆干燥的红磷,另一端放一小块已用滤纸吸取表面上水的白磷”,用导管对准上述烧杯中的白磷,通入少量氧气(或空气)”(见图1)。
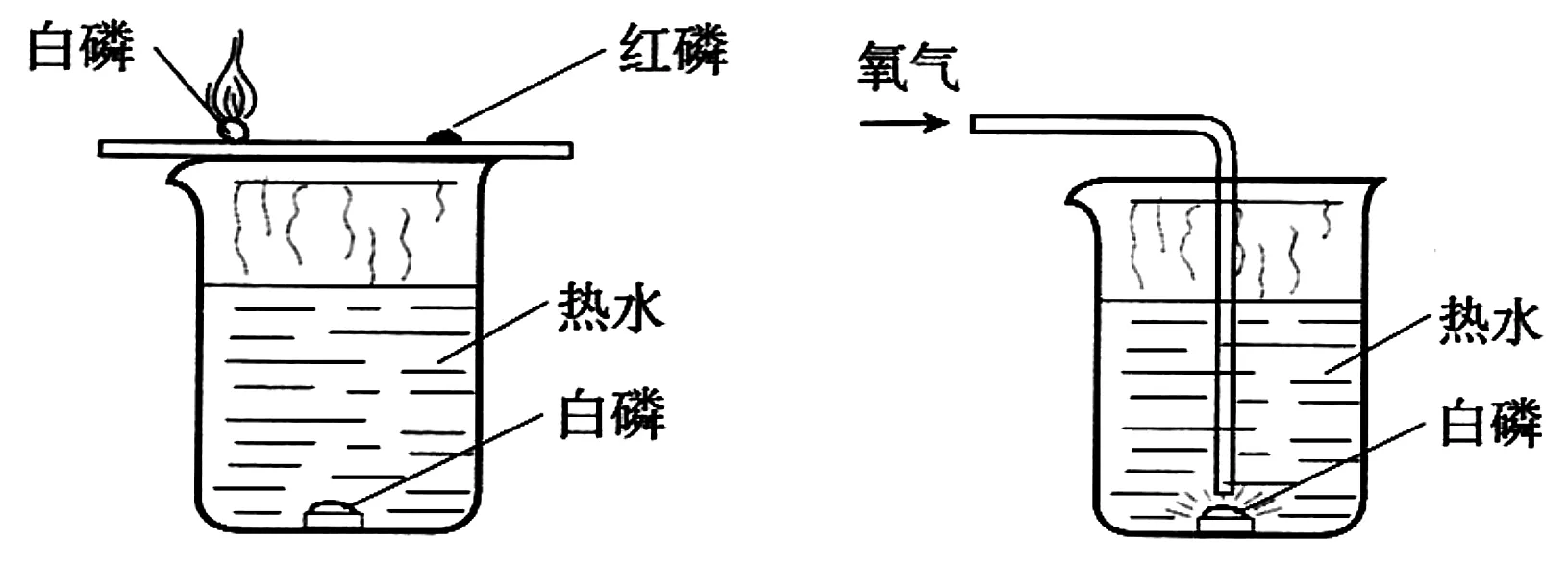
图1 教材中的实验装置
2 教材中实验的不足
2.1 不适于在教室中进行
由于白磷、红磷的燃烧产物对人的呼吸道有强烈的刺激,此实验应在通风橱中或抽风设备下进行,而教室中并没有此类设施,所以在教学中此实验往往由演示实验变为教师口头描述。
2.2 操作不便且现象不明显
用导管对准烧杯中的白磷通入氧气时,白磷易被氧气流吹得到处乱跑,不仅给操作带来不便,而且由于不便对准白磷,使得白磷的燃烧现象不明显。
2.3 不便于处理实验用具和实验残余物,存在安全隐患
白磷具有毒性,且极易燃烧,为安全起见,取用白磷的镊子要在通风厨中用酒精灯灼烧;吸干白磷表面的水的滤纸也要在通风厨中烧掉;实验中用过的水槽要冲洗数遍。按教材上实验的做法,白磷必须在教室中从试剂瓶中取出,则使用的镊子、滤纸和实验后铜片上的残余物不便于处理,从而带来一定的安全隐患。
3 实验改进方案
为了解决这些问题,笔者进行了改进,实验装置图见图2。
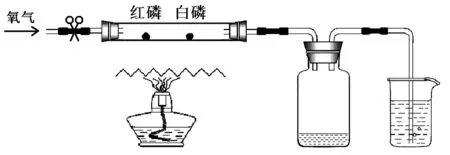
图2 改进实验装置1
实验过程及现象:将白磷和红磷置于硬质玻璃管中(红磷置于通入氧气的一端,避免白磷燃烧产生的热气流引燃红磷),两者相距约5 cm,一端用弹簧夹密封,另一端利用烧杯中的溶液密封。在硬质玻璃管下方距离约1.5 cm处垫一张石棉网,石棉网下用酒精灯加热(酒精灯位于白磷和红磷之间,偏向于红磷,这样可让学生直观地感受到红磷受到的温度高于白磷受到的温度),石棉网上的空气温度升高,再通过受热的空气给硬质玻璃管中的白磷和红磷加热。白磷微微受热便燃烧起来,产生大量白烟;红磷不燃烧。一段时间后,白磷熄灭。打开弹簧夹,向硬质玻璃管中通入氧气,白磷又重新燃烧起来,且燃烧更旺。烧杯中盛放NaOH溶液,以吸收五氧化二磷。为了防止水倒吸,在硬质玻璃管与尾气吸收装置之间放置安全瓶。
笔者用加热高锰酸钾的方法制取氧气,为了多次通入氧气,让白磷重复出现燃烧、熄灭的现象,可将发生装置连一个三通管,一端与硬质玻璃管相通,另一端与大气相通,如图3所示。需向硬质玻璃管内通入氧气时,关闭与大气相通处的弹簧夹,打开与玻璃管相连处的弹簧夹;停止通入氧气时,关闭与玻璃管相通处的弹簧夹,打开与大气相连处的弹簧夹,防止氧气将试管口的橡皮塞冲开。
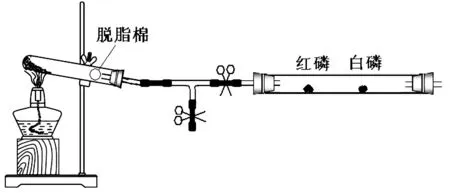
图3 改进实验装置2
4 改进后实验的优点
4.1 适宜在教室中进行,安全环保
将实验装置换成密封装置,并利用尾气处理装置,将五氧化二磷吸收,避免了对人体的危害,使此实验适宜在教室中进行。
4.2 用空气浴加热取代用热水加热,缩短加热时间
由于密封装置为玻璃仪器,而玻璃的导热性远差于铜片,用热水加热引燃白磷所需时间较长,而用空气浴加热缩短了加热时间。
4.3 便于处理实验用具和实验残余物,消除了安全隐患
改用硬质玻璃管作为反应容器,利用装置的密封性,可以事先在实验室中将药品装好,实验后的残余物也可带回实验室处理、清洗。解决了镊子、滤纸等不便处理的问题,消除了安全隐患。
4.4 现象明显,便于学生观察
通过实验可以让学生明确地感知到燃烧的条件是:可燃物、达到着火点、与空气或氧气接触,而且三者缺一不可;也为灭火等知识的学习提供了铺垫。
5 改进后实验装置的温度测定
用空气浴给药品加热,能否使温度达到白磷的着火点而低于红磷的着火点?笔者对实验中的温度进行了测定。
5.1 测定用空气浴加热时硬质玻璃管内的温度
在硬质玻璃管下一定距离垫石棉网,用酒精灯加热,将两支温度计的水银球分别置于酒精灯正上方的A处和距其约4 cm的B处(见图4),实验中药品所处的位置正好在A、B两点之间,所以药品的温度会介于A、B两点的温度之间。
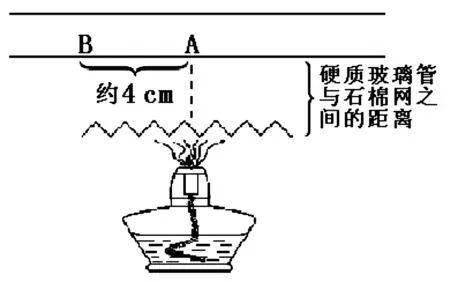
图4 测定用空气浴加热时硬质玻璃管内的温度
(1)实验一:室温22 ℃,硬质玻璃管与石棉网之间的距离1 cm。实验数据见表1。
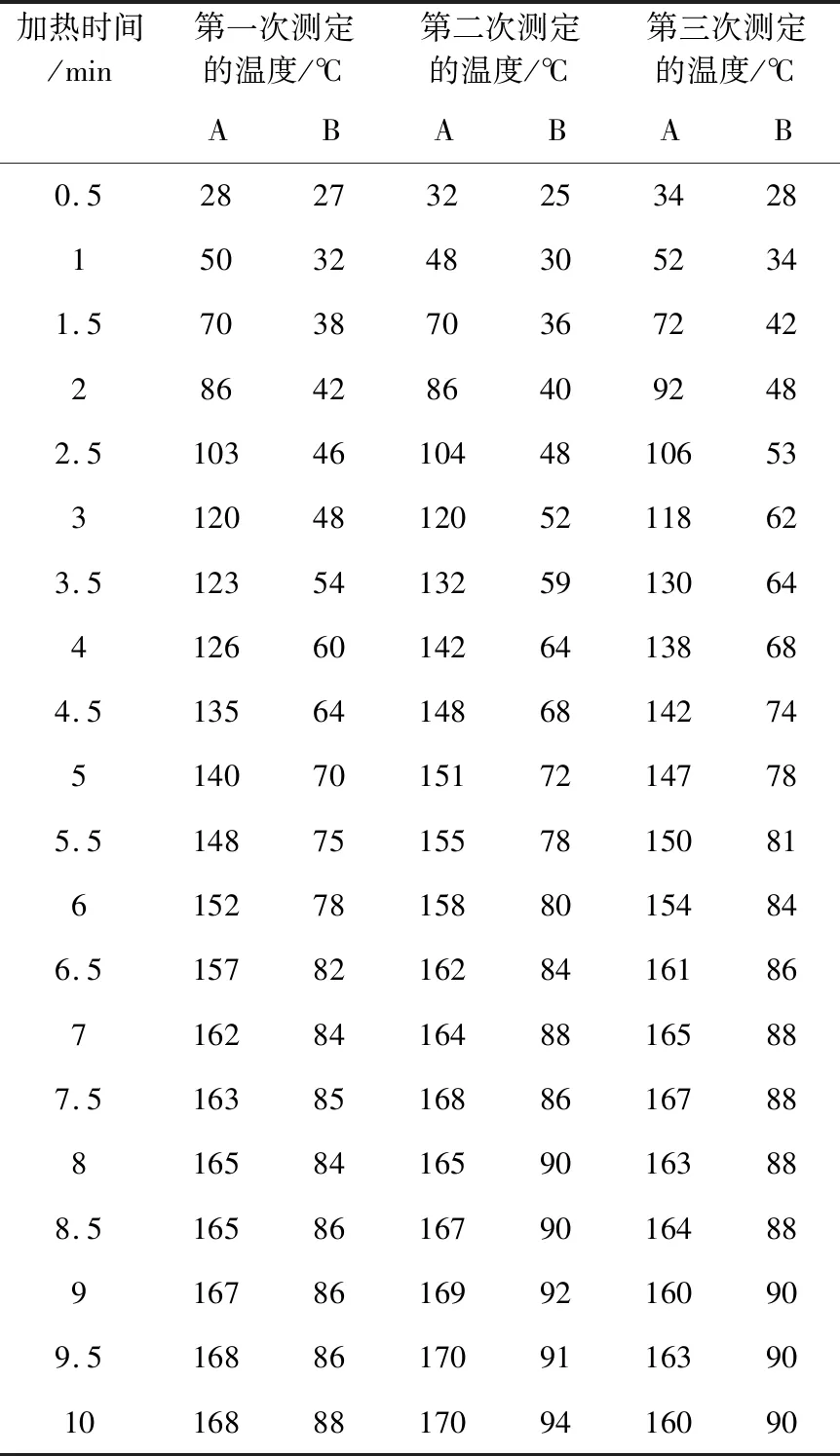
表1 实验一数据
(2)实验二:室温22 ℃,硬质玻璃管与石棉网之间的距离3 cm。实验数据见表2。
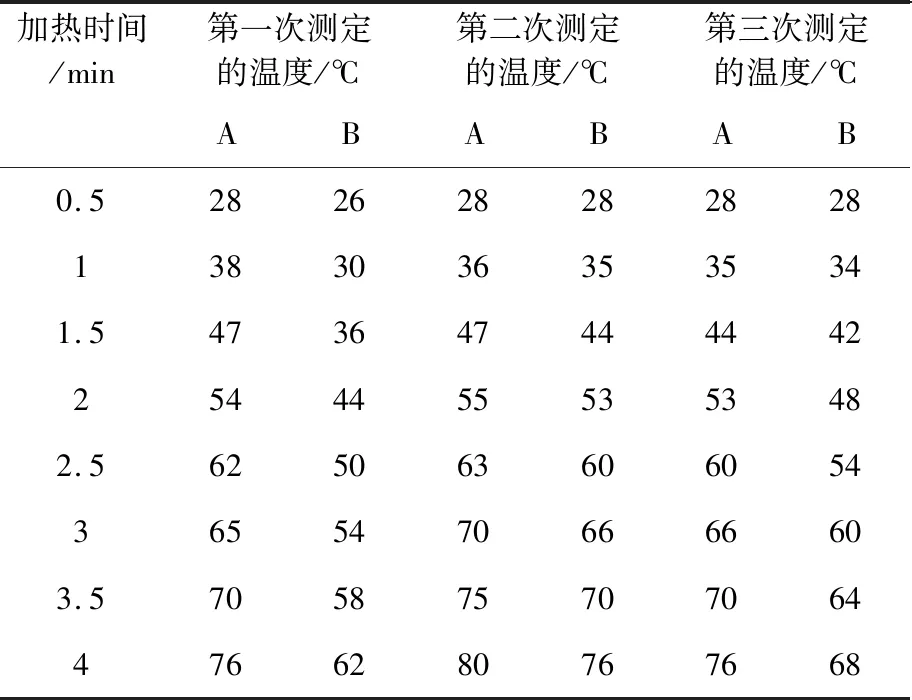
表2 实验二数据
我们知道,红磷的着火点是260 ℃,白磷的着火点是40 ℃。可以看出,用空气浴加热,硬质玻璃管与石棉网之间的距离为1~3 cm时,管内的温度可引燃白磷,却不会引燃红磷。经大量实验发现,当硬质玻璃管与石棉网之间的距离约为1.5 cm时,加热使白磷燃烧的时间较短,又可确保加热效果。
5.2 测定白磷燃烧放出热量与酒精灯共同作用会不会引燃红磷
在硬质玻璃管内的一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸取表面上水的白磷,两者之间相距约5 cm,硬质玻璃管下约1.5 cm处垫一张石棉网,用酒精灯加热,将两支温度计的水银球分别置于白磷与红磷之间的中点A处和红磷下方的B处(见图5)。
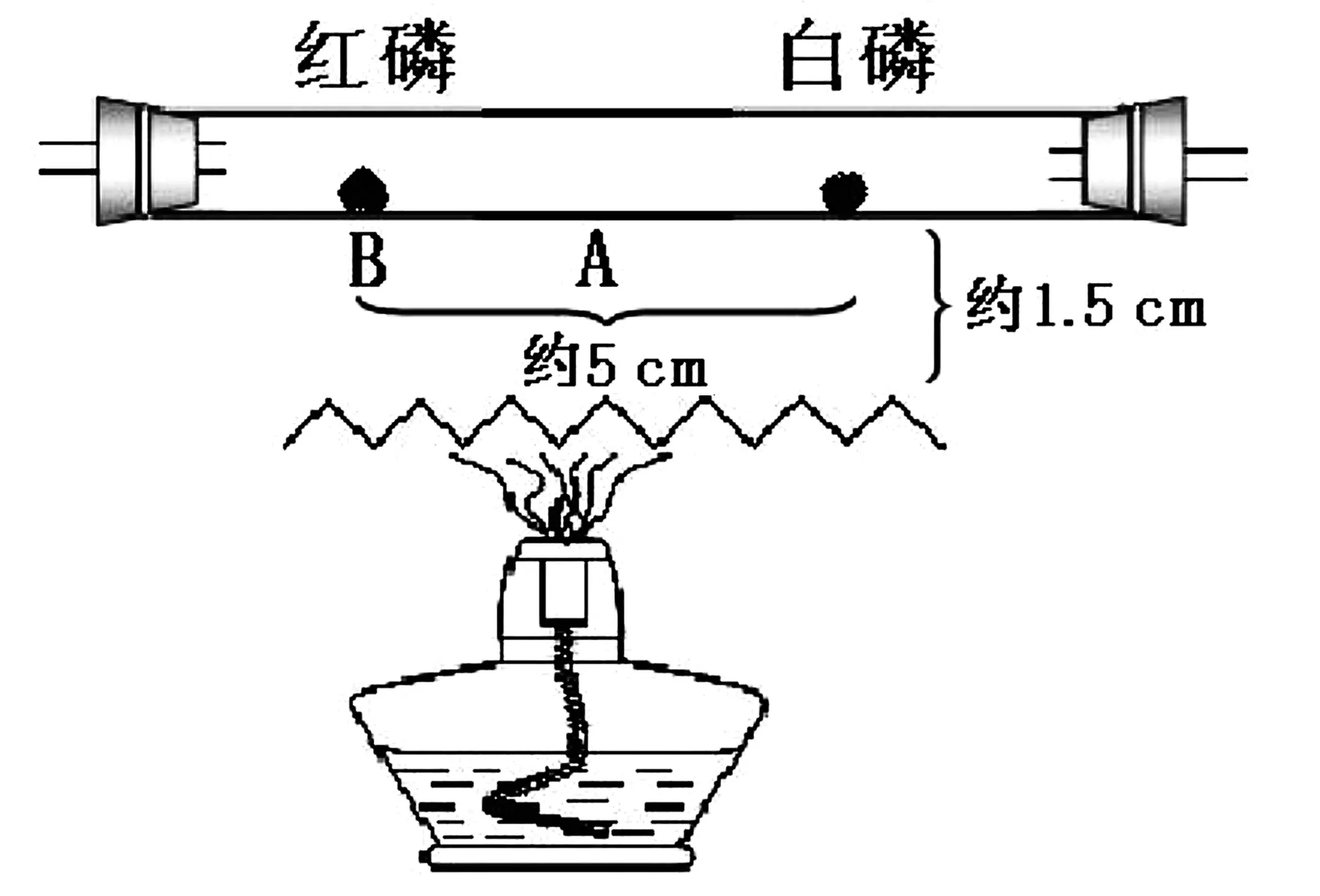
图5 测定白磷燃烧放出热量与酒精灯共同作用会不会引燃红磷
(1)实验三:室温22 ℃,白磷在空气中燃烧。实验数据见表3。
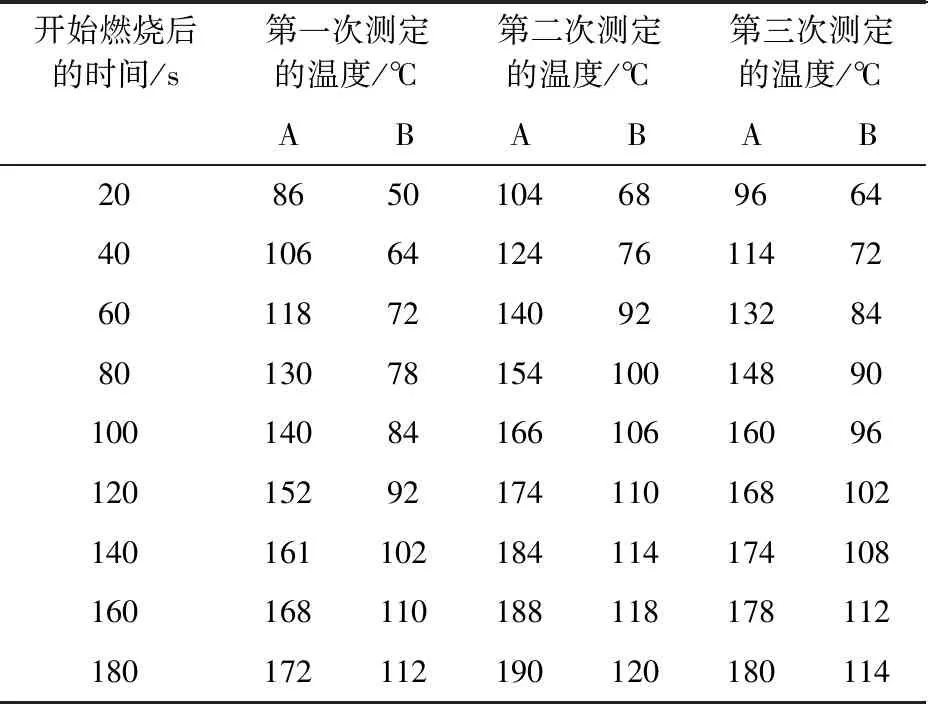
表3 实验三数据
由于氧气被消耗完,白磷燃烧约2 min后熄灭。
(2)实验四:室温22℃,白磷在氧气中燃烧。实验数据见表4。
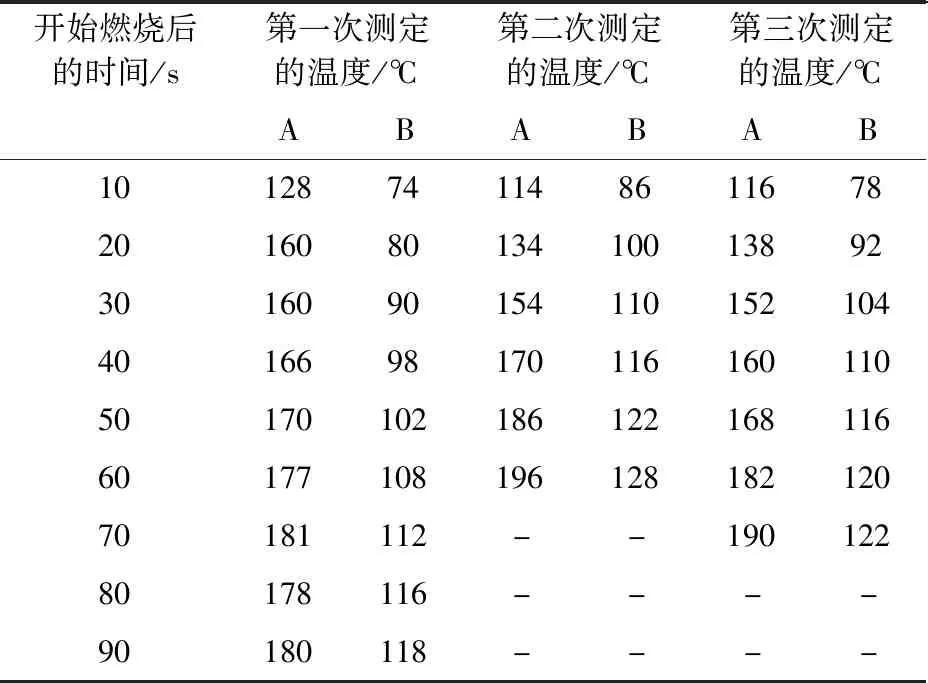
表4 实验四数据
表中空白部分,是由于白磷已燃尽,故没有测定。可以看出即使是处在更靠近酒精灯A处的温度也没有达到红磷的着火点,反应过程中不会将红磷引燃。

