原电池实验探究辅助理解电源电动势
宁夏回族自治区银川一中(750001) 汪路斌
对电源电动势的理解一直是高中物理教学的难点,学生存在很多误解,认为“电动势大的非静电力做功就多”“电动势大的非静电力做功就快”,诸如此类的问题都是学生学习中较常见的问题。学生在化学课中学习过原电池,但很难与物理学中的电动势知识结合起来。本文探究原电池电动势的影响因素,帮助学生将原电池知识与电动势概念相融合。探究溶液浓度对原电池电流的影响,帮助学生理清电流(内阻)与电动势的关系,消除对“化学反应速率越大,电流越大,电动势越大”的误解。最后,通过导体棒切割磁感线实验进一步阐述电动势的概念。
1 探究原电池电动势的影响因素
探究电源电动势的装置如图1所示,直接将电压表接在电极上,测量原电池两端的电压,该路端电压近似可以认为是电源的电动势。

图1 实验装置
1.1 探究两电极之间的距离对电动势的影响
浓度为2 mol/L的稀硫酸,电极为铜和锌,锌板接电压表负接线柱,铜板接电压表正接线柱。控制其他条件不变,只改变两极板间距离,记录电压表读数(见表1)。

表1 探究两电极之间的距离对电动势的影响实验数据
1.2 探究两电极插入溶液的深度对电动势的影响
浓度为2 mol/L的稀硫酸,电极为铜和锌,锌板接电压表负接线柱,铜板接电压表正接线柱。控制其他条件不变,只改变两电极插入溶液的深度,两电极每次插入的深度是相同的,记录电压表读数(见表2)。

表2 探究两电极插入溶液的深度对电动势的影响实验数据
1.3 探究溶液浓度对电动势的影响
纯度为98%的浓硫酸10 mL,逐次加蒸馏水10 mL,改变溶液浓度,电极为铜和锌,锌板接电压表负接线柱,铜板接电压表正接线柱,控制其他条件不变,记录电压表读数(见表3)。
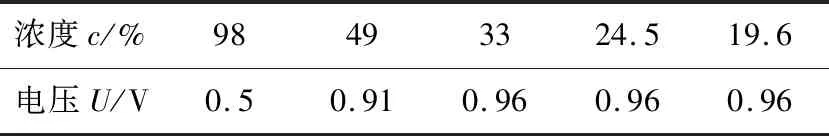
表3 探究溶液浓度对电动势的影响实验数据
1.4 探究电极材料对电动势的影响
浓度为2 mol/L的稀硫酸20 mL,改变电极材料,控制其他条件不变,记录电压表读数(见表4)。
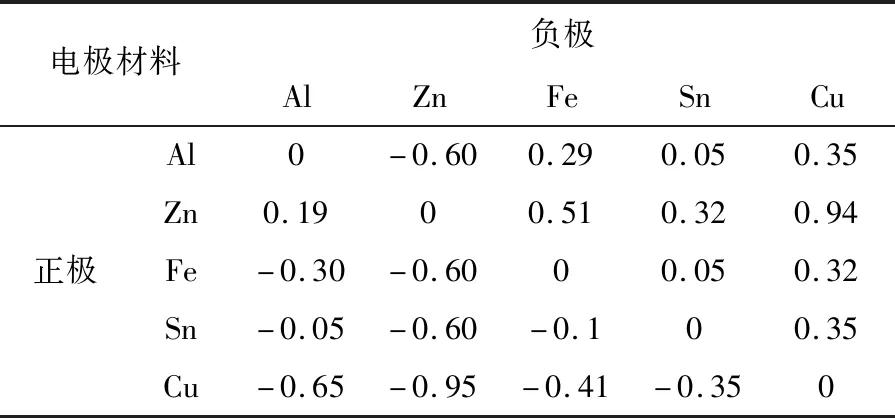
表4 探究电极材料对电动势的影响实验数据(单位:V)
分析表1、2可知,原电池两电极之间的距离,电极在溶液中的深浅(电极与溶液的接触面积)对电源电动势没有影响;从表3中可知,溶液浓度对电动势也几乎没有影响,表3中的第一个数据是由于浓硫酸与金属锌的反应方程式与稀硫酸不同导致;表4反映了电极材料对电源电动势的影响,两电极金属活动性的差异对电动势影响很大。
高中物理课本中电动势反映非静电力做功把其他形式的能转化为电能的本领,等于非静电力把1 C的正电荷从负极移送到正极所做的功。搬运单位电荷非静电力做功越多,表明能量转化本领越大,电动势越大。同一个化学反应,转移一个电子,对应的化学能的变化是相同的,即化学能转化成电能的多少是确定的,即电动势是确定的,与电极间距、电极的深浅(接触面积)、溶液浓度均无关。电极材料不同时,反应方程式不同,化学反应转移一个电子对应的化学能不同,即搬运单位单荷从电源的一极到另一极非静电力做功不同,电动势不同,表3中的第一组数据也是一个很好的佐证,由于锌与浓、稀硫酸的反应方程式不同,导致电动势不同。
化学中用标准电极电势来衡量金属单质在水溶液中失去电子能力大小,即金属活动性。规定标准氢电极的电势为零,其他电极的电势就是该电极与标准氢电极组成原电池的电动势。标准氢电极指将101.3 kPa的氢气通到浸入氢离子浓度为1 mol/L的铂黑上,使铂黑吸附氢气至饱和,这时铂片就好像用氢制成的电极,就是标准氢电极。从金属活动性的衡量标准来看,化学上先用了电动势概念,再有了金属活动性。这也反过来说明了电动势取决于金属活动性。
2 验证原电池内阻的影响因素
水果电池的电极间距增大,电源的内阻增大,相当于增大了金属导体沿电流方向的长度,电极插入水果越深,电源内阻越小,相当于增大了金属导体垂直于电流方向的横截面积。同理,电解质为溶液的原电池间距增大,内阻应该增大,电极浸入溶液越深,内阻应该越小,溶液的浓度越大,自由电荷越多,内阻也应该越小。以下实验进行验证。
2.1 验证两电极之间的距离对电流的影响
溶液为2 mol/L的稀硫酸80 mL,电极材料为锡和铜,将图1的电压表换成电流表,锡板接电流表负接线柱,铜板接电流表正接线柱,改变两极板之间的距离,记录电流表示数(见表5)。
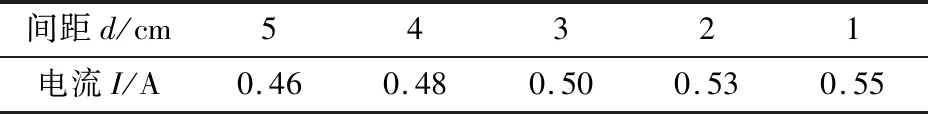
表5 验证两电极之间的距离对电流的影响实验数据
2.2 验证两电极插入溶液的深度对电流的影响
溶液为2 mol/L的稀硫酸80 mL,电极材料为锡和铜,将图1的电压表换成电流表,锡板接电流表负接线柱,铜板接电流表正接线柱,改变两极板插入溶液的深度,记录电流表示数(见表6)。

表6 验证两电极插入溶液的深度对电流的影响实验数据
2.3 验证溶液浓度对电流的影响
纯度为98%的浓硫酸10 mL,逐次加蒸馏水10 mL,改变溶液浓度,电极为铜和锡,将图1的电压表换成电流表,锡板接电流表负接线柱,铜板接电流表正接线柱,控制其他条件不变,记录电流表读数(见表7)。

表7 验证溶液浓度对电流的影响实验数据
表5验证了间距越大,电流越小,内阻越大;表6验证了深度越深,电流越小,内阻越大,也可理解为,深度越深,溶液与金属的接触面积越大,单位时间内发生反应的金属原子数目越多,转移的电子数目越多,即电流越大;表7中电流随浓度减小,先增大后减小,看似反常,其实正常,刚开始两组是锡与浓硫酸的反应,到第3组过渡到与稀硫酸反应,与稀硫酸反应时浓度越小,电流越小,自由电荷越小,内阻越大,也可理解为单位时间内发生反应的金属原子数目随浓度减小而降低,转移的电子数目减少,电流变小。
电动势和内阻是从两个不同角度描述电源的性质。电动势反映的是非静电力将其他形式能转化为电能的本领,搬运1 C正电荷从电源负极到正极做的功,既不是反映电能转化的快慢,也不是反映电能转化的多少。以原电池为例,与化学反应的速率无关,稀硫酸浓度的降低不影响电动势,与能量转化快慢无关;与化学反应的反应物总量无关,溶液的多少,插入的深度都不造成电动势的变化,与能量转化多寡无关,1、5、7号干电池电动势都为1.5 V。
内阻的大小与极板间距有关,间距越大,相当于导体沿电流方向长度增长,内阻越大;稀硫酸溶液浓度越大,反应速率越大,电流越大,相当于增大了电导率,内阻越小;插入溶液深度越深,接触面积越大,单位时间反应物消耗越多,电荷转移越多,电流越大,相当于导体横截面积增大,内阻减小。
3 导体棒切割磁感线实验深层次阐述电动势
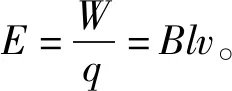
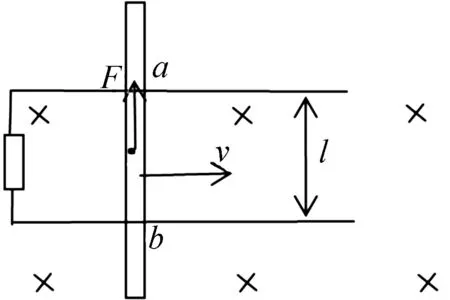
图2 导体棒在磁场中运动

