UHPLC法测定参附注射液中单酯型生物碱含量
袁海英,蔡帮军
(华润三九(雅安)药业有限公司,四川 雅安 625000)
0 引 言
参附注射液是由红参和附子制成的中药复方制剂,源自著名验方参附汤,主要有效成分为人参皂苷、人参三醇类物质和乌头类生物碱[1]。参附注射液临床主要用于阳气暴脱的厥脱症,具有强心、升压、改善微循环等作用,临床用于休克抢救疗效确切[2]。药理研究表明[3-4],参附注射液中的强心成分主要为附子中的生物碱成分,附子中的生物碱包括双酯型生物碱及其水解产物单酯型生物碱,它们既是有效成分又是毒性成分,其中双酯型生物碱有大毒,单酯型生物碱毒性较小。续海训[5]报道参附注射液中,双酯型生物碱基本上全部水解,只含有低毒有效的单酯型生物碱。为进一步评价参附注射液质量,本试验建立了超高效液相色谱(UHPLC)法同时测定参附注射液中单酯型生物碱的含量。
1 仪器与试药
1.1 仪器
Waters 2695超高效液相色谱仪(沃特世)、XPE26电子天平(梅特勒)、UPT-1-40L超纯水器(优普),SC-8L-150数控固相萃取仪(广州智真)。
1.2 试药与试剂
参附注射液(华润三九(雅安)药业有限公司);苯甲酰新乌头原碱(批号:111795—201303)、苯甲酰乌头原碱(批号:111794—201303)、苯甲酰次乌头原碱(批号:111796—201303)对照品均购于中国食品药品检定研究院;甲醇为色谱纯(默克);其余试剂均为分析纯;水为超纯水。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液制备
精密称取苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱对照品适量,加异丙醇-二氯甲烷(1∶1)的混合溶液制 57.56 µg/mL苯甲酰新乌头原碱、55.12 µg/mL 苯甲酰乌头原碱、53.90 µg/mL 苯甲酰次乌头原碱的混合对照品贮备溶液。再精密吸取上述贮备溶液适量,加异丙醇-二氯甲烷(1∶1)的混合溶液稀释制成每1 mL含苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱分别为10.36 µg、9.92 µg、9.70 µg 的混合对照溶液。
2.1.2 供试品溶液制备
精密量取参附注射液10 mL,加于phenomenex Strata-X C18固相萃取小柱(先以15 mL甲醇活化,再以15 mL水平衡),以水5 mL冲洗,再以甲醇1 mL洗脱,用1 mL量瓶收集甲醇洗脱液至刻度,摇匀,作为供试品溶液。另按参附注射液工艺制备缺附子的阴性样品,照供试品处理方法制备成阴性样品溶液。由于参附注射液中生物碱含量较低,需对待测生物碱进行富集,试验考察了氯仿萃取法、固相柱萃取柱法、氧化铝萃取法等,结果表明固相柱萃取法所制备的供试品杂质较少[6-8]。同时比较了不同厂家的C8和C18固相萃取小柱以及不同洗脱方法,最终确定了上述供试品溶液的制备方法。
2.2 色谱条件
采用 Agilent ZORBAX Eclipse Plus C18(2.1 m×100 mm,1.8 µm)色谱柱;以甲醇为流动相A,0.01 mol/L乙酸铵溶液(冰乙酸调pH5.0)为流动相B,等度洗脱(A∶B=39∶61);流量为 0.4 mL/min;柱温为 30 ℃;检测波长为235 nm;理论板数以苯甲酰新乌头原碱峰计算大于20 000,进样量1 µL。
2.3 专属性试验
精密吸取混合对照品溶液、供试品溶液和阴性样品溶液各1 µL,注入超高效液相色谱仪,按“2.2”项下色谱条件测定,结果阴性样品对供试品测定无干扰,见图1,说明本方法专属性良好。
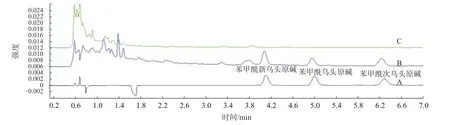
图1 对照品(A)、供试品(B)和阴性样品(C)UHPLC色谱图
2.4 线性范围、检出限和定量限考察
2.4.1 线性范围
取“2.1.1”项下混合对照品贮备溶液,分别稀释2、4、8、16、32、64倍,精密吸取不同浓度的对照品溶液各1 µL注入超高效液相色谱仪,按“2.2”项下色谱条件分别测定,以各色谱峰进样量为横坐标X(ng),峰面积为纵坐标Y,进行线性回归,各成分回归方程及线性范围见表1。结果表明各成分在线性范围内与峰面积有良好的线性关系。
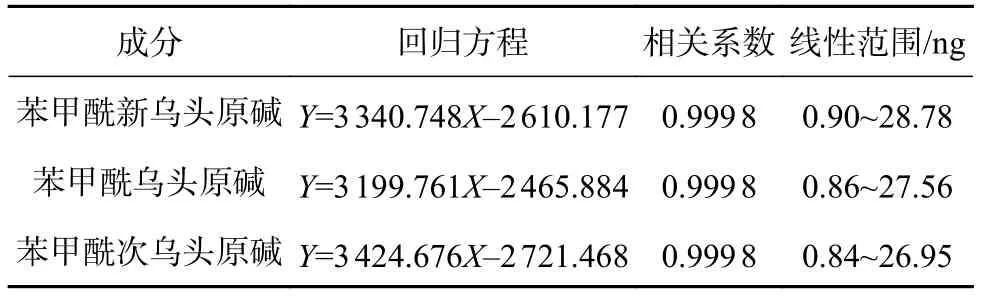
表1 线性关系考察
2.4.2 检测限和定量限
取“2.4.1”项下最小浓度的混合对照品溶液,分别稀释不同倍数后精密吸取1 µL进样检测,考察信噪比(S/N),根据3倍S/N确定检出限、10倍S/N确定定量限,分别计算出各成分的检出限和定量限见表2。结果表明采用UHPLC方法检测时各成分的检出限和定量限均较低。
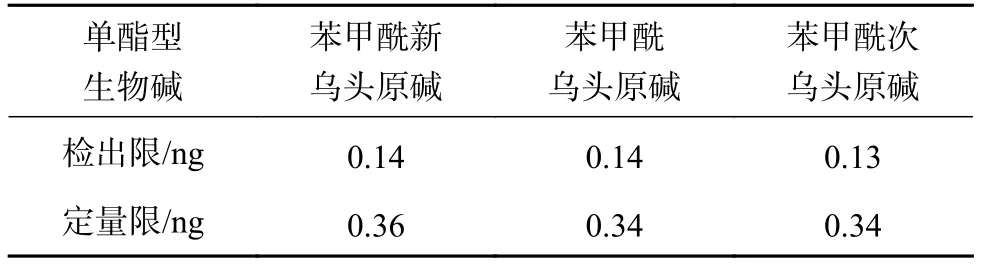
表2 各成分检出限和定量限
2.5 精密度试验
精密吸取“2.1.1”项下混合对照品溶液 1 µL,连续进样6 次,测得苯甲酰新乌头原碱、苯甲酰乌头原碱和苯甲酰次乌头原碱峰面积见表3。RSD分别为1.18%、1.23%、1.07%,表明仪器精密度良好。
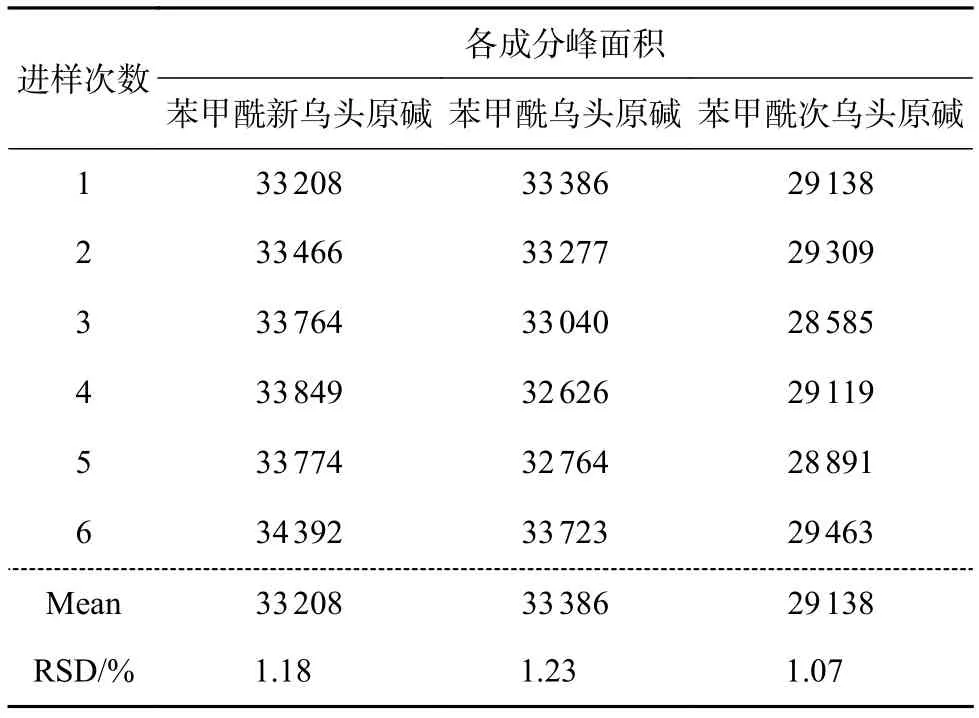
表3 精密度考察
2.6 重复性试验
取同一批参附注射液,按“2.1.2”项下方法,平行制备供试品溶液6份,按“2.2”项下色谱条件测定,结果见表4。6份平行供试品中测得苯甲酰新乌头原碱、苯甲酰次乌头原碱和苯甲酰乌头原碱的含量RSD分别为1.63%、0.91%、1.19%,表明本方法重复性良好。
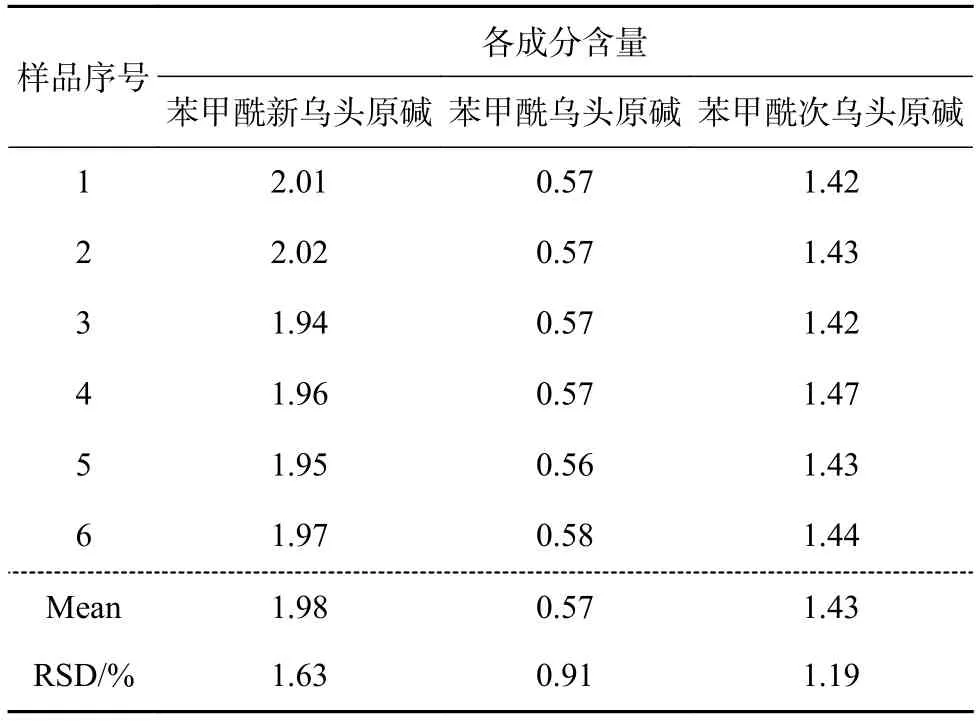
表4 重复性考察 µg/mL
2.7 稳定性试验
取同一供试品溶液室温放置,分别于0,2,4,6,8,12,24 h 按“2.2”项下色谱条件测定,结果见表5。在24 h内苯甲酰新乌头原碱、苯甲酰乌头原碱和苯甲酰次乌头原碱含量的RSD分别为1.79%、0.83%、1.09%,表明供试品溶液在24 h内稳定性较好。
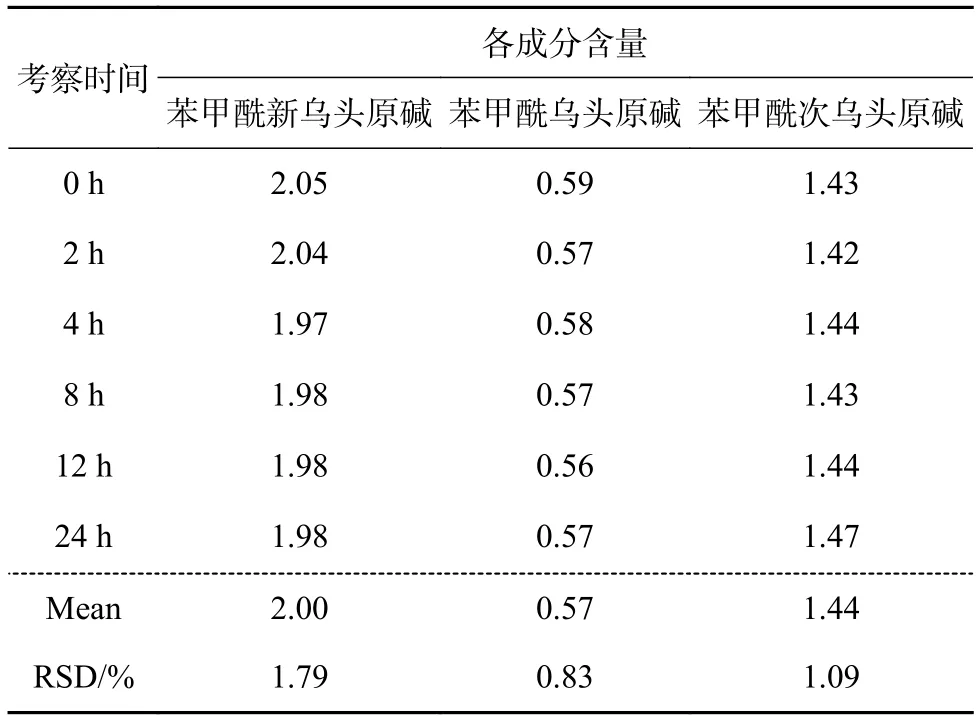
表5 稳定性考察 µg/mL
2.8 加样回收率试验
根据参附注射液中已知苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱的含量,配制相应浓度的混合对照品溶液,分别精密吸取参附注射液共9份,分别精密加入低、中、高3种水平的混合对照品溶液,按“2.1.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件测定,结果见表6。苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱的加样回收率均在97.1%~104.8%之间,RSD均小于2%,表明本方法准确度较好。

表6 加样回收试验结果
2.9 样品测定
取10批参附注射液,按“2.1.2”项方法制备供试品溶液,并按“2.2”项下色谱条件测定,计算10批样品中单酯型生物碱的含量,结果见表7。
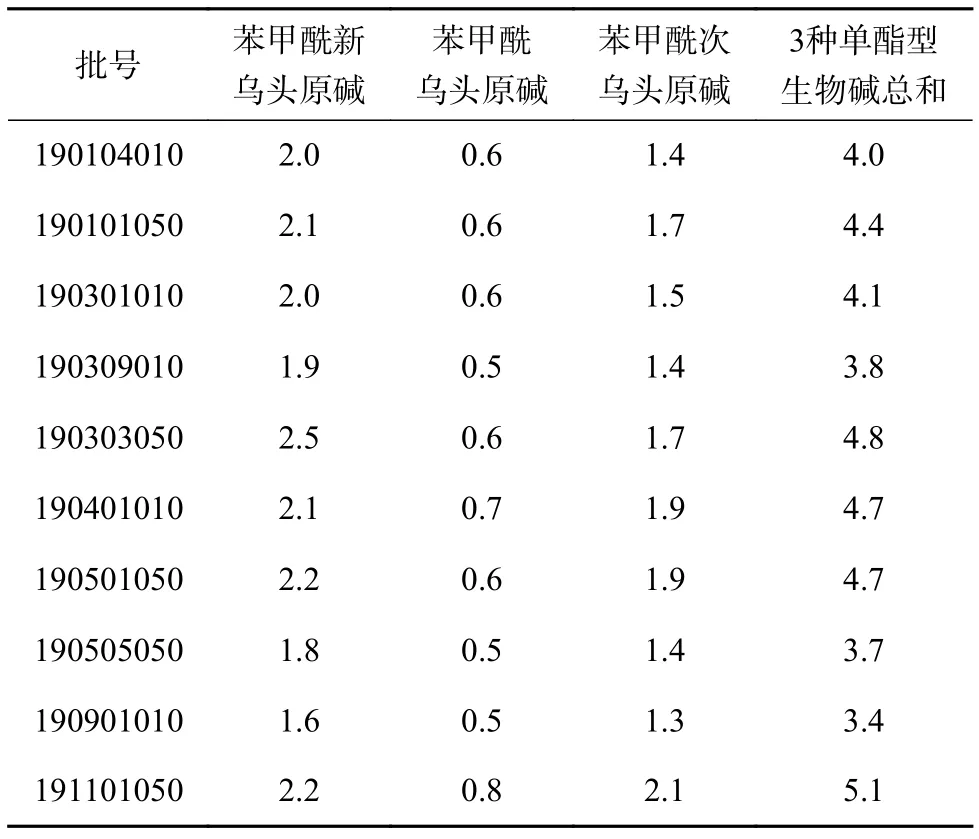
表7 参附注射液3种单酯型生物碱含量测定结果 µg/mL
3 讨 论
3.1 检测方法优选
中成药中乌头类生物碱含量测定方法文献报道较多,主要采用的高效液相色谱法[9-12],而参附注射液中乌头类生物碱含量测定的研究则较少。本试验先采用了一般高效液相色谱法,考察了不同流动相及色谱柱对3种单酯型和3种双酯型乌头类生物碱的分离效果,结果各色谱峰的响应值较低,出峰时间较长,且基线易发生漂移。后采用超高效液相色谱法,可使基线平稳、各色谱峰响应值较高、峰形较好且出峰较快,见图2。
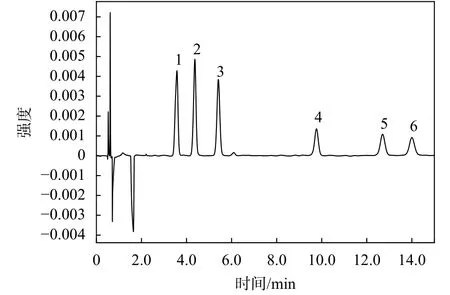
图2 3种单酯型和3种双酯型乌头类生物碱UHPLC色谱图
3.2 参附注射液制备过程酯型生物碱的含量变化情况
参附注射液处方中附子为毒性药材,主要毒性成分为酯型生物碱。研究表明,双酯型乌头碱的毒性为单酯型的50~500倍,为无酯型的2 000倍,而毒性较低的单酯型生物碱被认为是附子的主要药效物质[13]。通过对5批参附注射液制备过程中关键工艺点的酯型生物碱含量进行监测,发现毒性较大的双酯型乌头碱逐步降解,成品中总含量为0(见图3);而毒性较小的单酯型乌头碱也在逐步降解,成品中总含量约为提取液的20%(见图4)。说明参附注射液制备过程是一个减毒过程,而体内动物实验表明,人参配伍附子后可促进单酯型生物碱的吸收[14],起到增强药效的作用。
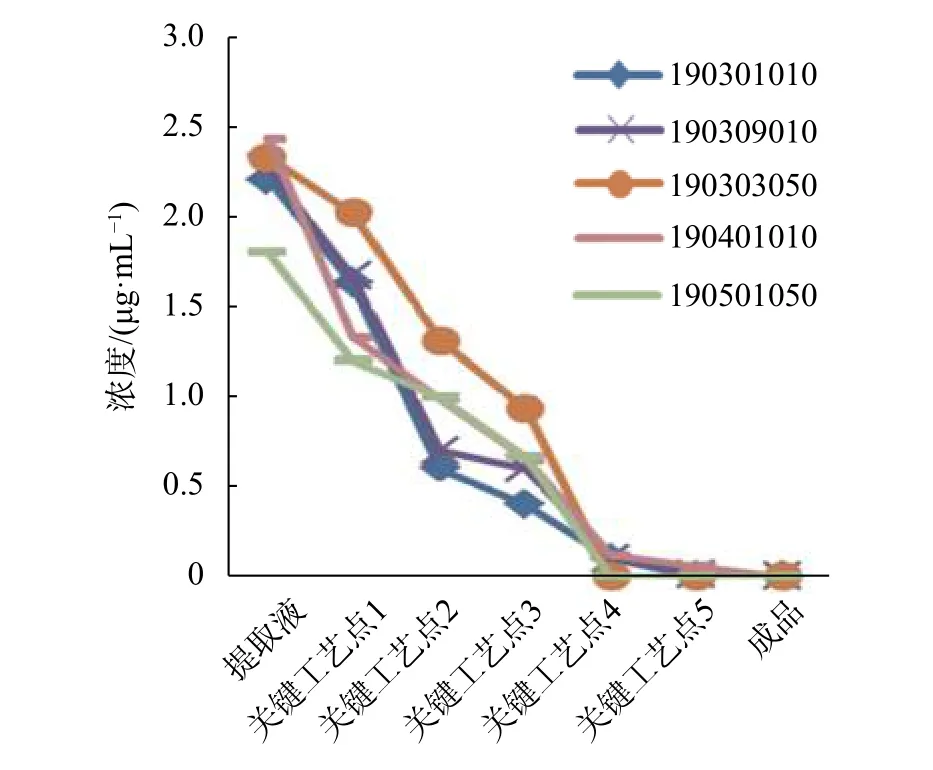
图3 参附注射液制备过程双酯型生物碱含量变化图
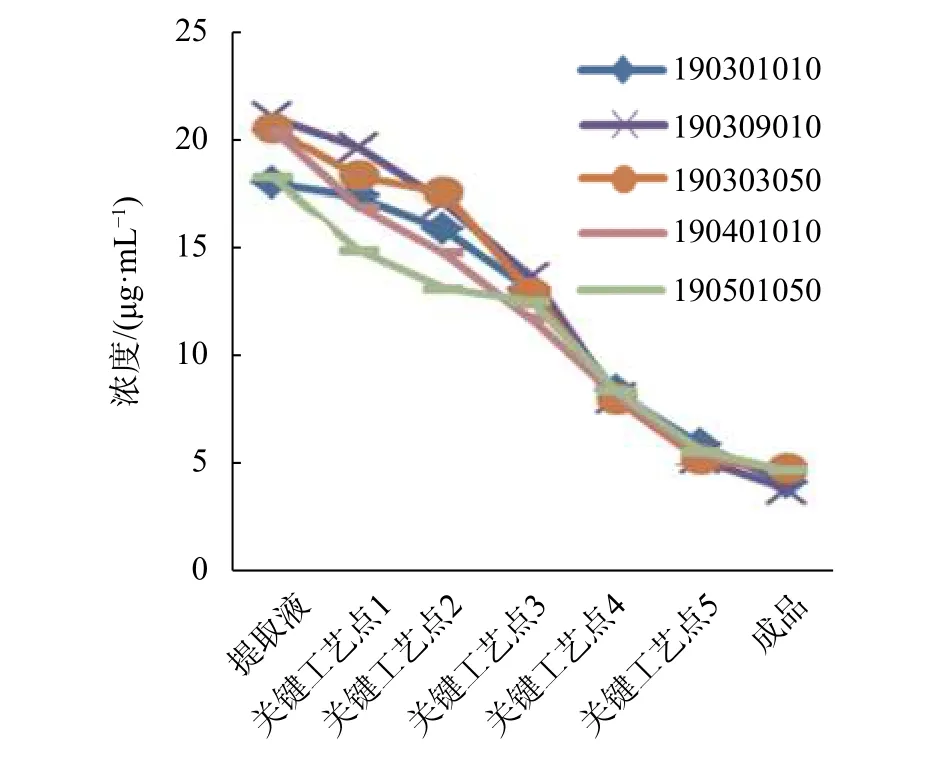
图4 参附注射液制备过程单酯型生物碱含量变化图
4 结束语
综上所述,由于参附注射液中起强心作用的主要药效物质为单酯型生物碱,但由于其仍具有一定的毒性作用,需对其总含量进行控制。从表7结果可知10批参附注射液中3种单酯型生物碱总含量在3.4~5.1 µg/mL 范围内波动,均值为4.3 µg/mL,RSD为13.0%,批间较稳定。因参附注射液现行质量标准已采用薄层色谱法对双酯型生物碱的限量进行了检查,要求供试品色谱中与乌头碱、次乌头碱、新乌头碱对照品色谱相应的位置上出现的斑点应小于对照品斑点或不出现斑点,故建议增加参附注射液中3种单酯型生物碱总含量限度2.5~6.0 µg/mL,以此作为现行质量标准的补充,从而进一步保证临床用药的安全性及有效性。

