依达拉奉加强PC12细胞氧化损伤自噬防护的机制研究
郭道宇 刘昊 李冬

【摘要】 目的:研究依達拉奉防护过氧化氢(H2O2)损伤神经细胞PC12的分子机制,为依达拉奉在脑出血疾病的治疗利用提供理论依据。方法:本研究设置对照组(PC12细胞)、损伤组[PC12细胞+H2O2(600 μmol/L)]和处理组[PC12细胞+H2O2(600 μmol/L)+依达拉奉(0.5 mmol/L)]。观察依达拉奉对PC12细胞氧化损伤防护效果。结果:损伤组PC12细胞繁殖下降,而处理组细胞数量接近对照组。细胞流式实验显示:处理组PC12细胞没有发生明显的凋亡,而损伤组细胞凋亡率稍高。与对照组比较,损伤组细胞内ROS的荧光强度显著升高,损伤组细胞培养上清液中SOD、GSH-Px活性均显著降低,而MDA含量显著升高(P<0.05)。与损伤组比较,处理组细胞内ROS的荧光强度显著降低,处理组细胞培养上清液中SOD、GSH-Px的活性均显著提高,MDA水平显著降低(P<0.05)。Western blot实验分析结果显示:处理组中ATG7表达显著增强,同时,LC3Ⅰ含量减少,而LC3Ⅱ含量增加。结合KEGG富集分析发现:在损伤组和对照组间,有4条信号通路发生了显著性变化,其中mTOR信号通路和Caspase介导的信号通路被激活;在处理组和对照组间,有12条信号通路发生了显著性变化,其中mTOR信号通路和MAPK信号通路被激活,而与细胞凋亡密切相关的Caspase信号通路没有显著增强。结论:依达拉奉通过增强PC12细胞自噬而防护氧损伤。该研究为依达拉奉在氧损伤对神经元细胞保护机制的研究提供了一定的理论参考。
【关键词】 PC12细胞 依达拉奉 H2O2胁迫 自噬 转录组学
Study on the Mechanism of Edaravone Enhancing Autophagy Protection in PC12 Cells from Oxidative Injury/GUO Daoyu, LIU Hao, LI Dong. //Medical Innovation of China, 2021, 18(36): 0-030
[Abstract] Objective: To study the molecular mechanism of Edaravone protecting nerve cell PC12 from hydrogen peroxide (H2O2) injury, so as to provide a theoretical basis for the treatment and utilization of edaravone in intracerebral hemorrhage. Method: In this study, the control group (PC12 cells) and the injury group [PC12 cells + H2O2 (600 μmol/L)] and treatment group [PC12 cells + H2O2 (600 μmol/L) + Edaravone (0.5 mmol/L)]. The protective effect of Edaravone on oxidative damage of PC12 cells was observed. Result: The proliferation of PC12 cells in the injury group decreased, while the number of cells in the treatment group was close to that in the control group. Flow cytometry showed that there was no obvious apoptosis in PC12 cells in the treatment group, but the apoptosis rate in the injury group was slightly higher. Compared with the control group, the fluorescence intensity of ROS in the injured group increased significantly, the activities of SOD and GSH-Px in the cell culture supernatant decreased significantly, and the content of MDA increased significantly (P<0.05). Compared with the injury group, the fluorescence intensity of ROS in the treatment group decreased significantly, the activities of SOD and GSH-Px in the cell culture supernatant in the treatment group increased significantly, and the level of MDA decreased significantly (P<0.05). The results of Western blot analysis showed that the expression of ATG7 was significantly increased in the treatment group, while the content of LC3Ⅰ decreased and the content of LC3Ⅱ increased. Combined with KEGG enrichment analysis, it was found that there were significant changes in four signal pathways between the injury group and the control group, in which mTOR signal pathway and caspase mediated signal pathway were activated; There were significant changes in 12 signal pathways between the treatment group and the control group, in which mTOR signal pathway and MAPK signal pathway were activated, but caspase signal pathway closely related to apoptosis was not significantly enhanced. Conclusion: Edaravone protects PC12 cells from oxygen injury by enhancing autophagy. This study provides a theoretical basis for the action of edaravone protection of neurons from oxygen-induced injury.
[Key words] PC12 cells Edaravone H2O2 stress Autophagy Transcriptomics
First-author’s address: North China University of Science and Technology Affiliated Hospital, Hebei Province, Tangshan 063009, China
doi:10.3969/j.issn.1674-4985.2021.36.007
脑出血(intracerebral hemorrhage,ICH)是由血管壁病变或脑血管导致颅内血液凝结功能障碍或血液动力学改变的一种非创伤性的脑实质出血[1]。脑出血可引起多种类型的神经元损伤,氧化应激损伤是其中之一[2]。大脑细胞中含有丰富的脂质且抗氧化能力较弱,因此很容易成为氧化应激损伤的靶点[3-4],因此,脑出血后神经元细胞凋亡、死亡、自噬等都与氧化应激损伤后过度出现的自由基和ROS有关[5-6],这些自由基和ROS等的过度化打破了神经元细胞抗氧化防御机制的最强能力,从而导致细胞发生损伤[7]。
先前研究表明在氧化应激的状态下,Keap1/Nrf2复合物中解离下的转录因子Nrf2进入细胞核,结合在抗氧化反应元件(ARE)上激活许多抗氧化酶[8-9]。而脑保护剂依达拉奉,一种自由基清除剂[10],可以有效提高Nrf2的表达从而抑制氧化应激对神经元细胞的损伤[8]。但是Nrf2基因是怎样被依达拉奉增强转录的机制尚不清楚,本研究构建脑出血后氧化应激神经细胞模型(H2O2胁迫PC12细胞),通过RNA-seq技术深入解析依达拉奉对神经细胞的保护作用。现报道如下。
1 材料与方法
1.1 试剂与仪器 依达拉奉( Edaravone,Mitsubishi Chemical Corporation,日本),DMEM培养基,胎牛血清(Gibco,美国),超净工作台(苏州净化),CO2培养箱(ESCO),高速低温离心机,全波长酶标仪(SPECTROstar Nano),流式细胞仪(伯乐S6e)等。蛋白提取试剂(碧云天生物科技有限公司),MDA和SOD活性检测试剂盒(北京索莱宝生物科技有限公司)、Western blot抗体(Abcam)、RNA-seq实验(上海生工生物工程有限公司)。
1.2 细胞分组与处理 本实验所用PC12细胞购自中国科学院典型培养物保藏委员会细胞库,然后齐鲁医药学院保存。本实验中将PC12细胞分为对照组、损伤组和处理组,每组5个重复,对照组采用DMEM培养基培养,损伤组在培养基中加入H2O2(终浓度为600 μmol/L)[11],处理组在培养基中加入终浓度为600 μmol/L的H2O2后12 h,加入依达拉奉注射液(终浓度为0.5 mmol/L)[12]。将三组细胞置于37 ℃,5% CO2培养箱孵育24 h。
1.3 细胞存活率检测 将三组PC12细胞以1×103个/孔的细胞量接种于96孔板,37 ℃、5% CO2培养箱中培养24 h,然后每孔加入MTT(5 mg/mL),37 ℃继续孵育4 h。去掉培养基,用PBS缓冲液清洗一次,去掉PBS后再每孔加入100 μL二甲基亚砜(dimethyl sulfoxide,DMSO)溶解甲瓒晶体。待结晶完全溶解后,吸弃DMSO,用PBS缓冲液清洗3遍后,加入100 μL PBS缓冲液,置于酶标仪中测定波长490 nm处吸光值。
1.4 细胞凋亡检测 将三组细胞以1×106个/孔的细胞量接种至6孔板中,37 ℃、5% CO2孵箱中孵育培养72 h,胰酶消化后,用Annexin V-FITC和Propidium Iodide(PI)双染法在流式细胞仪上进行细胞凋亡检测并进行数据分析。
1.5 细胞氧化应激水平检测 PC12细胞被药物处理后,加入0.5%的胰酶消化细胞,收集细胞到15 mL离心管,4 ℃ 1 000 r/min离心沉淀细胞,吸取并保存上清液。将上清液与荧光探针DCFH-DA 1 mmol/L在室温孵育30 min,然后用酶标仪检测荧光强度。根据荧光强度及试剂盒说明书上的计算方法评估细胞上清液中MDA含量和SOD活性。
1.6 Western blot检测细胞自噬相关蛋白 取处理后的细胞样品裂解提取总蛋白,并用Qubit 3.0荧光仪测定蛋白浓度。取20 μg总蛋白进行10%的SDS-PAGE电泳,然后进行转膜至PVDC膜。用5%脱脂牛奶室温封闭蛋白2 h,随后加入一抗(ATG7 1︰500,LC3Ⅱ 1︰1 000,LC3Ⅰ 1︰500,Actin 1︰1 000)置于4 ℃环境进行过夜封闭,第2天加入对应二抗(1︰2 000)室温封闭1 h,最后滴加ECL。以Actin作为内参,在暗室压片曝光分析。
1.7 转录组基因富集分析 取处理后的细胞样品提交给Beyotime生物技术公司进行RNA-seq。使用Qubit™ 3.0荧光仪(Invitrogen)对RNA定量后,上机RNA样品按照QuantSeq 3’mRNA-Seq文庫试剂盒FWD(illumina)说明进行处理,然后使用NextSeq 500测序系统(illumina)进行分析。数据FASTQ文件被上传到随机软件BaseSpace进行分析[13]。使用BaseSpace软件中的Cufflinks Assembly和DE application (Version 2.1.0)对输出文件进行分析,以确定差异表达基因(DEGs),这些差异表达基因用于生成表达热图和FPKM散点图。此外,数据基因的分析还使用ClueGO(2.3.3版)、CluePedia(1.3.3版)、Cytoscape(3.5.1版)等软件。生物过程(BPs)的功能分组是基于Kappa评分进行的。下载基因本体数据进行分析。基因集富集分析(3.0版)用于测定实验组中差异富集的BPs[14]。
1.8 统计学处理 采用SPSS 18.0 (SPSS Inc.,Chicago,IL,USA)软件对所得数据进行统计分析,计量资料用(x±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 依达拉奉对PC12细胞氧化损伤防护效
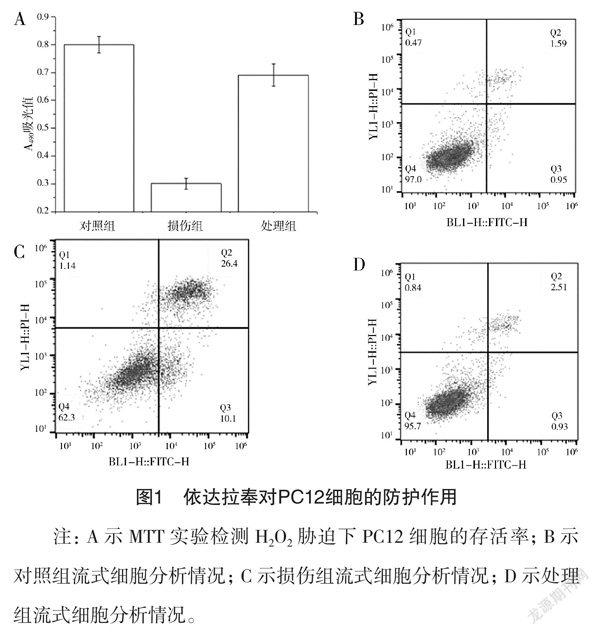
果 对照组吸光值为(0.80±0.03),损伤组吸光值为(0.31±0.02),处理组吸光值为(0.69±0.04)。损伤组PC12细胞繁殖下降,可能是因为H2O2引起细胞死亡或凋亡,而处理组细胞数量接近对照组,见图1A。细胞流式实验显示:处理组PC12细胞没有发生明显的凋亡,而损伤组细胞凋亡率稍高,见图1B、1C、1D。
注:A示MTT实验检测H2O2胁迫下PC12细胞的存活率;B示对照组流式细胞分析情况;C示损伤组流式细胞分析情况;D示处理组流式细胞分析情况。
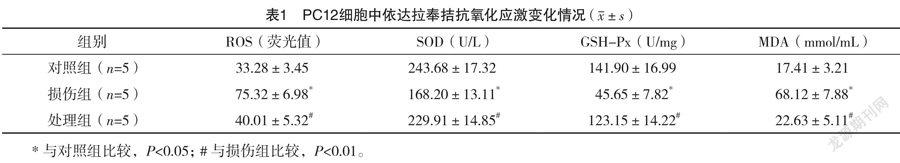
2.2 PC12细胞中依达拉奉拮抗氧化应激变化情况 与对照组比较,损伤组细胞内ROS的荧光强度显著升高,损伤组细胞培养上清液中SOD、GSH-Px活性均显著降低,而MDA含量显著升高(P<0.05)。与损伤组比较,处理组细胞内ROS的荧光强度显著降低,处理组细胞培养上清液中SOD、GSH-Px的活性均显著提高,MDA水平显著降低(P<0.05)。见表1。
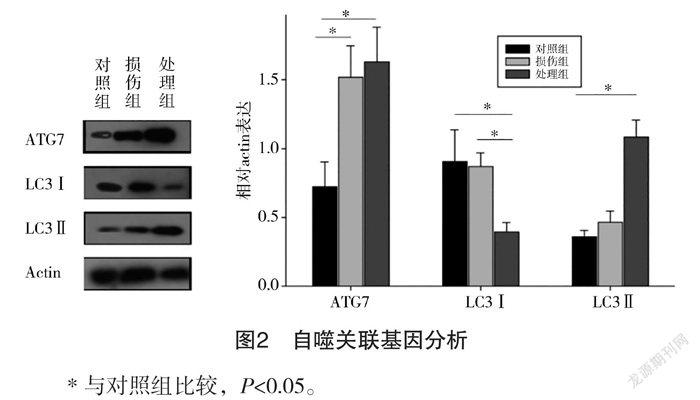
2.3 依达拉奉促进PC12细胞自噬情况 通过Western blot实验分析依达拉奉对PC12细胞的防护作用,对每条条带灰度值采用ImageJ软件分析,以actin蛋白灰度值为基准,计算各蛋白的相对表达,对照组ATG7表达量为(0.72±0.20),损伤组ATG7表达量为(1.52±0.23),处理组ATG7表达量为(1.63±0.25);对照组LC3Ⅰ表达量为(0.93±0.23),损伤组LC3Ⅰ表达量为(0.87±0.10),处理组LC3Ⅰ表达量为(0.39±0.05);对照组LC3Ⅱ表达量为(0.36±0.05),损伤组LC3Ⅱ表达量为(0.46±0.08),处理组LC3Ⅱ表达量为(1.08±0.12)。结果显示:处理组中ATG7表达显著增强,同时,LC3Ⅰ含量减少,而LC3Ⅱ含量增加。见图2。
2.4 依达拉奉激活mTOR信号通路 本研究将RNA-seq结果借助KEGG数据库进行注释和分析,结果表明:损伤组相对于对照组有4条信号通路发生了显著性变化,其中mTOR信号通路和Caspase介导的信号通路被激活(图3A),说明损伤组细胞的凋亡被启动,氧化损伤增加了细胞凋亡;而处理组与对照组相比,有12条信号通路发生了显著性增强,其中mTOR信号通路和MAPK信号通路被激活,而与细胞凋亡密切相关的Caspase信号通路没有显著增强(图3B),说明处理组的依达拉奉降低了细胞凋亡,而增强了细胞自噬。
3 讨论
MAPK/JNK信号通路被激活后会影响应激损伤状态下细胞的存活。先前诸多实验证实细胞自噬以及细胞内MAPK/JNK信号通路活化在缺血性脑卒中等多种神经系统疾病的病理过程中发挥了重要作用[15]。其中mTOR-MAPK信号通路对下游JNK因子有正调控作用。文献[16]显示细胞内氧自由基的增高是影响细胞自噬关键因素之一,而且尤为重要,且氧自由基能调节MAPK/JNK等多种信号转导途径。自由基增高是引起神经细胞凋亡和神经组织水肿的主要原因[17],本研究也观察到了氧化损伤可引起细胞凋亡。
细胞自由基清除剂依达拉奉通过降低细胞内自由基浓度实现抗脑水肿和保护神经系统免受伤害的作用[18]。尽管目前依达拉奉被广泛应用于脑出血的治疗中,但是其抑制脑出血后MAPK/JNK/Caspase-3表达机制尚不清楚,该机制与细胞自噬的发生及疾病的缓解密切相关。
本研究结果显示:损伤组PC12细胞繁殖下降,而处理组细胞数量接近对照组,表明H2O2给PC12神经元细胞造成损伤并抑制了细胞的生长,但是在添加依达拉奉后,细胞的繁殖情况明显变好,说明依达拉奉能够有效保护PC12细胞免受氧化损伤,具有拮抗氧化剂和细胞氧化应激的能力。而后进一步的流式细胞仪实验显示,处理组PC12细胞没有发生明显的凋亡,而损伤组细胞凋亡率稍高,表明H2O2诱发了PC12细胞凋亡,但是添加依达拉奉后观察到细胞的凋亡率很低,接近对照组,猜测可能是依达拉奉降低了氧自由基,同时降低了细胞凋亡。为了深入分析其凋亡降低的机制,采用Western blot分析PC12细胞是否发生了自噬,结果显示:处理组中ATG7表达显著增强,同时,LC3Ⅰ含量减少,而LC3Ⅱ含量增加。在添加依达拉奉后,细胞自噬标记性基因的表达明显上升。说明依达拉奉可能通过诱发细胞自噬启动细胞存活的自我保护机制,避免受到氧损伤而死亡。
为了进一步说明依达拉奉加强了细胞自噬,进行了RNA-seq研究,转录组数据利用生物信息学进行KEGG分析,KEGG是涵盖基因组信息、化学信息和生化系统功能的综合数据库,拥有16个子数据库[19]。结果显示在损伤组中细胞凋亡和自噬等关联信号通路都被激活,而添加依達拉奉后自噬关联信号通路被显著激活而凋亡途径没有显著差异,说明依达拉奉激活了细胞自噬。基于上述实验,笔者认为依达拉奉对氧损伤神经元具有显著防护作用,其通过增强细胞自噬功能而对细胞进行防护。
参考文献
[1] ZHANG C,XIA B J,GE H,et al.Long-Term Mortality Related to Acute Kidney Injury Following Intracerebral Hemorrhage: A 10-Year (2010-2019) Retrospective Study[J].Journal of Stroke and Cerebrovascular Diseases,2021,30(5):105688.
[2] XU X,ZHANG J,YANG K,et al.Prognostic prediction of hypertensive intracerebral hemorrhage using CT radiomics and machine learning[J].Brain and Behavior,2021,11(5):e02085.
[3] Shoamanesh A,Katsanos A H.Combatting Secondary Injury From Intracerebral Hemorrhage With Supplemental Antioxidant Therapy[J].Stroke,2021,52(4).
[4] Salim S.Oxidative Stress and the Central Nervous System[J].
J Pharmacol Exp Ther,2017,360(1):201-205.
[5] Ozkul A,Akyol A,Yenisey C,et al.Oxidative stress in acute ischemic stroke[J].Journal of Clinical Neuroscience,2007,14(11):1062-1066.
[6] Magid-Bernstein J,Beaman C B,Poyraz F C,et al.Impacts of ABO Incompatible Platelet Transfusions on Platelet Recovery and Outcomes after Intracerebral Hemorrhage[J].Blood,2021,137(19):2699-2703.
[7] Sies H.Oxidative stress: oxidants and antioxidants[J].Experimental Physiology,1997,82(2):291-295.
[8] Vries H,Witte M,Hondius D,et al.Nrf2-induced antioxidant protection: a promising target to counteract ROS-mediated damage in neurodegenerative disease?[J].Free Radic Biol Med,2008,45(10):1375-1383.
[9] Wei R,Enaka M,Muragaki Y.Activation of KEAP1/NRF2/P62 signaling alleviates high phosphate-induced calcification of vascular smooth muscle cells by suppressing reactive oxygen species production[J].Sci Rep,2019,9(1):10366.
[10]祝丹丹,夏磊,陈泉,等.依达拉奉对脑出血血肿周围水肿的影响[J].心脑血管病防治,2021,21(1):90-92.
[11]王力波,贝赟,秦东旭,等.依达拉奉通过Nrf2信号分子调节氧化应激减轻脑缺血再灌注诱导的神经损伤[J].中国生物化学与分子生物学报,2020,36(3):328-336.
[12] LIU X,WU Y,ZHOU D,et al.Nlinoleyltyrosine protects PC12 cells against oxidative damage via autophagy: Possibleinvolvement of CB1 receptor regulation[J].International Journal of Molecular Medicine,2020,46(5):1827-1837.
[13]李福记,梁靖梅,段秀萍,等.苦参碱对TGF-β1诱导的人腹膜间皮细胞ETS2表达的影响[J].中国现代医生,2020,58(6):30-33.
[14]于瑜,王钟兴.基于生物信息学途径筛选缺血性脑卒中关键基因及药物预测[J].中山大学学报(医学科学版),2021,42(1):42-50.
[15] Schellino R,Boido M,Vercelli A.JNK Signaling Pathway Involvement in Spinal Cord Neuron Development and Death[J].Cells,2019,8(12):1576.
[16] LI N,LU X Y,SHI W Y,et al.Combined mTOR/MEK inhibition prevents proliferation and induces apoptosis in NF2-mutant tumors[J].Eur Rev Med Pharmacol Sci,2019,23(13):5874-5883.
[17] Paasz A,Segovia Y,Skowronek R,et al.Molecular neurochemistry of the lanthanides[J/OL].Synapse,2019,73(9):e22119.
[18] MIAO H,JIANG Y,GENG J,et al.Edaravone Administration Confers Neuroprotection after Experimental Intracerebral Hemorrhage in Rats via NLRP3 Suppression[J].Journal of Stroke and Cerebrovascular Diseases,2019,29(1):104468.
[19]郭俊愷,赵承磊,赵兴旺,等.通过生物信息学分析鉴定干燥综合征的关键基因[J].中国麻风皮肤病杂志,2021,37(3):131-135,152.
(收稿日期:2021-04-07) (本文编辑:姬思雨)

