铁改性火山岩颗粒对水中低浓度磷吸附性能的研究
赵明杰, 李思晨, 刘晓静, 栗勇田
(1.天津大学环境科学与工程学院,天津 300072;2.秦皇岛天大环保研究院有限公司,河北 秦皇岛 066000;3.河北省河道水质净化及生态修复重点实验室,河北 秦皇岛 066000;4.秦皇岛市水污染监测及治理工程技术研究中心,河北 秦皇岛 066000)
0 引言
磷是生物生长所必需的元素,同时也是水体营养化的重要限制因子[1],控制磷等营养性物质进入水体是解决富营养化问题的根本途径[2]。城镇污水厂处理对象为生活污水和预处理后的工业废水,经二级处理后,污水中的TP 质量浓度通常在2 mg/L 以下。随着污水厂出水排放标准的不断提高,污水厂出水的TP 浓度需要进一步降低,针对低浓度含磷废水的深度处理,吸附法因其操作方便,费用低廉、绿色环保、可重复利用等优点而被广泛应用。目前关于吸附法的研究多集中于粉状吸附材料[3],吸附剂回收困难,容易导致吸附材料流失,限制了吸附除磷技术的应用。此外,单一的硅藻土、活性炭等吸附材料,吸附容量受限,被吸附的磷存在脱逸现象,很难达到理想的除磷效果。
火山岩作为一种储量极大的天然矿石资源,表面疏松多孔,通常用来吸附水体中的重金属[4-6],铁盐作为常见的除磷混凝剂,具有稳定高效的除磷效果[7]。本研究采用FeCl3对天然火山岩进行改性,制得改性火山岩颗粒吸附剂,并用其对低浓度含磷废水进行吸附影响因素和吸附特性研究,以期为开发新型吸附材料处理含磷废水提供参考。
1 实验部分
1.1 材料与设备
天然火山岩颗粒,KH2PO4,FeCl3,硫酸亚铁,钼酸铵,氢氧化钠,酒石酸钾钠,硫酸,盐酸,过硫酸钾,抗坏血酸,均为分析纯;多参数水质分析仪(DGB-401,雷磁);数显恒温磁力搅拌器(HJ-6B,常州金坛晨阳电子仪器厂);X 射线荧光仪 (Supermini200,日本理学株式会社);X 射线衍射仪(Smartlab9,日本理学株式会社);扫描电子显微镜(Maia3,泰思肯贸易有限公司);电热恒温鼓风干燥箱(DHG-9023A,上海笃特科学仪器有限公司);pH 计(pHS-25 型,上海精密科学仪器有限公司)。
1.2 改性火山岩颗粒的制备及表征
将天然火山岩分别过3 和5 mm 筛,控制粒径在3 ~5 mm 之间,用纯水洗净,在105 ℃下烘干,冷却后按1 ∶5 的固液比,将火山岩颗粒置于质量分数为7%的盐酸溶液中浸泡8 h。 用纯水洗净烘干,冷却后按1 ∶5 的固液比,将酸改性后的火山岩颗粒置于17%的FeCl3溶液中浸泡8 h 后,取出置于200 ℃的马弗炉中焙烧2 h,冷却后得到铁改性火山岩颗粒。 通过X 射线荧光仪(XRF)分析确定改性前后的元素组成,X 射线衍射仪(XRD)分析改性前后火山岩的晶体结构变化,扫描电子显微镜(SEM)观察改性前后火山岩表面形貌特征。
1.3 磷吸附影响因素实验
分别取一定量的改性火山岩颗粒加入100 mL由KH2PO4配置的模拟低浓度含磷废水中,置于磁力搅拌器上搅拌一定时间后取出,离心分离,取上清液测定溶液中的TP 浓度,并计算TP 去除率和单位质量吸附剂的磷吸附量。 设置不同吸附剂投加量、溶液pH 值和温度条件,同时严格控制其他条件不变,以确定吸附的最佳条件。 TP 浓度分析方法采用钼酸铵分光光度法 (GB 11893—89),通过绘制TP浓度与吸光度的标准曲线确定TP 浓度,为保证数据的可靠性,每组实验均设重复实验,测量结果取平均值。
TP 去除率(η)和单位质量吸附剂吸附量(Qe)的计算方法分别见式(1)和式(2):

式中:η 为TP 去除率,%;Qe为单位质量吸附剂对TP 的吸附质量浓度,mg/L;V 为处理污水体积,L;C0为废水中TP 的初始质量浓度,mg/L;Ce为吸附后TP的剩余质量浓度,mg/L;m 为吸附剂的质量,g。
2 结果与讨论
2.1 改性火山岩的化学元素组成
利用XRF 对天然火山岩和改性火山岩样品中的化学元素种类及含量进行了分析,结果见表1。
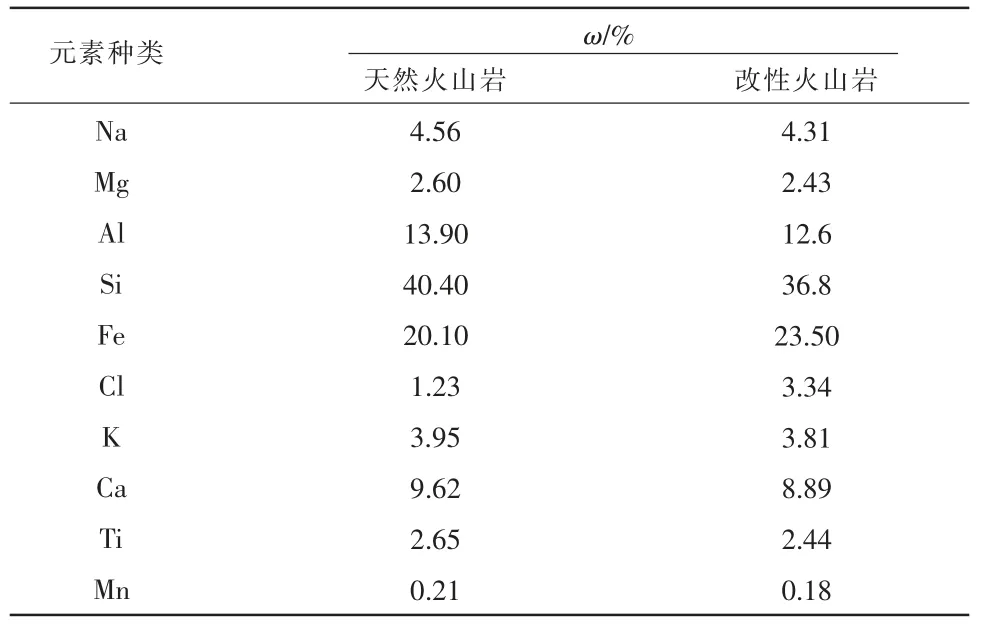
表1 火山岩改性前后的元素组成
由表1 可以看出,改性前后,火山岩的主要化学成分均以Si,Fe,Ca,K,Na 为主。 与天然火山岩相比,改性后的火山岩晶格中Ca,Na,K 等元素含量降低,这说明在盐酸浸渍处理过程中,有效去除了火山岩中的部分金属阳离子氧化物杂质。此外,改性火山岩中ω(Fe)增加了3.50%,ω(Cl)增加了2.11%,表明铁盐可能附着于火山岩表面。
2.2 改性火山岩的XRD 分析
利用XRD 对天然火山岩和改性火山岩进行分析,得到结果见图1。
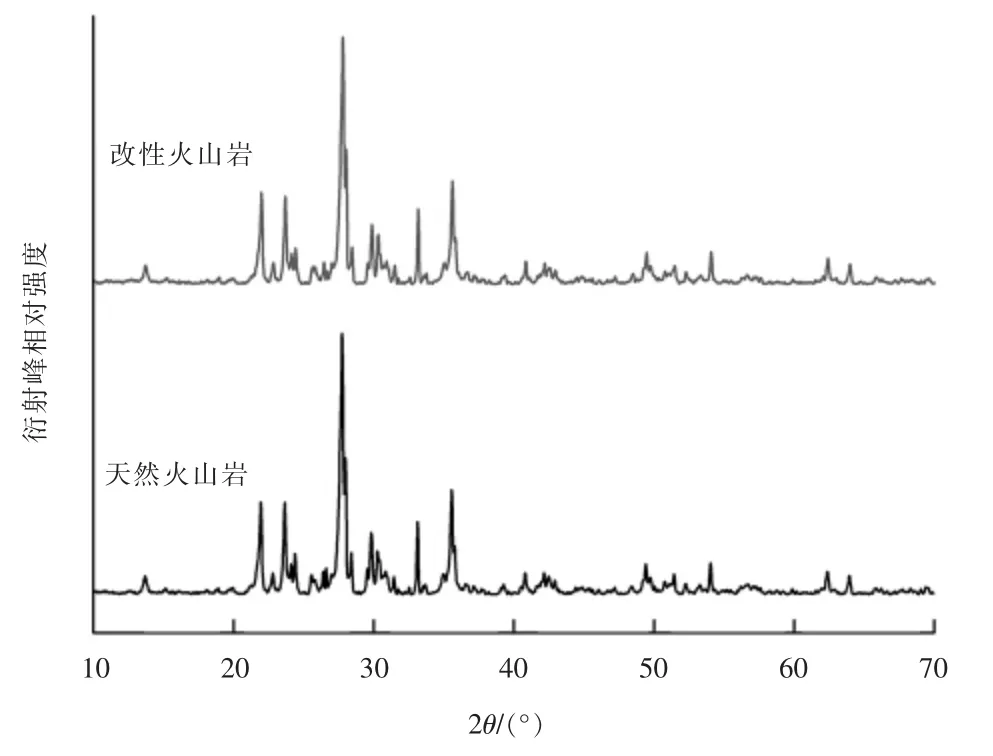
图1 火山岩改性前后的XRD
由图1 可以看出,火山岩中含有以Si,Al,Ca,Fe,O 元素形成的多种化合物,主要为SiO2。 与天然火山岩相比,经过焙烧后的改性火山岩主要特征峰没有发生显著变化,但Fe2O3峰形更加尖锐,结晶度更好,说明附着在火山岩表面的部分FeCl3转化成了Fe2O3,火山岩层间结构没有发生显著的变化。
2.3 改性火山岩的SEM 分析
利用SEM 分别对天然火山岩及铁改性火山岩样品进行分析,结果见图2。

图2 火山岩改性前后的SEM
由图2(a)可以看出,天然火山岩表面粗糙,层状结构较为明显,具有较多的孔隙。 从图2(b)可以看出,经过改性后,火山岩外层附着了大量的椭球体颗粒。 结合相关文献[8-9]及XRD 分析结果,得知改性火山岩表面的附着物可能为α-Fe2O3,这些Fe2O3粘连堆叠在一起,一方面增大了火山岩的比表面积,另一方面也增强了火山岩的化学吸附能力。
2.4 改性火山岩对水中磷吸附的影响因素研究
2.4.1 改性火山岩投加量对磷吸附效果的影响
对水温20 ℃,pH 值=7,TP 质量浓度为2.0 mg/L的模拟废水进行不同投加量实验,吸附时间为12 h,研究铁改性火山岩吸附剂投加量对水中TP 去除率的影响,结果见图3。

图3 不同投加量对改性火山岩吸附除磷效果的影响
由图3 可以看出,随着投加量的增大,改性火山岩对水中TP 的去除率呈现先增大后略微降低的趋势。这是因为投加量过小时,水中磷酸根离子远多于改性火山岩能够提供的吸附点位,剩余TP 浓度较高,随着投加量增大,吸附剂提供的表面吸附点位随之增多,吸附面积增大,使水中更多的磷可以附着在改性火山岩上,所以TP 的去除率升高,当投加质量浓度为5.0 g/L 时,TP 去除率最高达到了79.1%,继续加大吸附剂的投加量,TP 去除率变化较小,过多的吸附剂可能会导致磷酸根从液相向火山岩固相表面的迁移能力降低,阻碍吸附过程的进行。 另外,吸附剂投加量的增大,会导致吸附点位发生相互掩蔽现象[10],存在空余吸附点位,致使单位质量吸附剂的吸附量下降。
2.4.2 溶液pH 值对磷吸附效果的影响
其它试验条件一定时,控制溶液初始pH 值进行改性火山岩对水中磷的吸附实验,结果见图4。

图4 不同pH 值对改性火山岩吸附除磷效果的影响
由图4 可以看出,随着溶液pH 值的增加,TP 的去除率呈现先增大后趋于平缓再减小的趋势,在强酸或强碱条件下,改性火山岩吸附除磷效果较差。这是因为磷酸的一级酸度系数为2.12,当pH 值<2.12时,水中的磷以H3PO4的形式存在,难与Fe3+结合吸附。 随着溶液pH 值的增大,水中PO43-增多,在吸附过程中,HPO42-,H2PO4-与Fe3+结合生成络合物,吸附反应逐渐活跃。 当pH 值为5 ~9 范围内,TP 去除率均达到了75%以上。 而当溶液pH 值过高时,OH-浓度增加导致Fe3+浓度减少,在浓度积一定的情况下,PO43-浓度相应增大,导致除磷效果下降。
2.4.3 温度对磷吸附效果的影响
控制其它试验条件一定,改变溶液温度进行改性火山岩对水中磷的吸附实验,结果见图5。
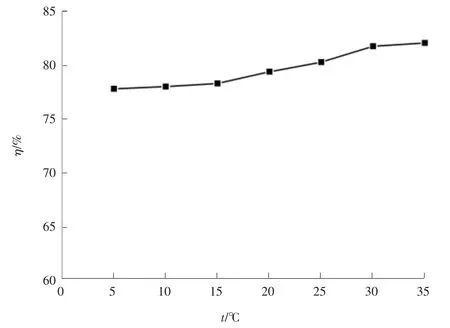
图5 不同温度对改性火山岩吸附除磷效果的影响
由图5 可以看出,随着溶液温度升高,TP 去除率逐渐提升,反映出改性火山岩对水中磷的吸附为吸热反应。这是由于温度的升高,离子之间的碰撞逐渐增多,热运动加剧,与吸附剂之间的碰撞增多,有利于吸附的进行。 在溶液温度为30 ℃时,达到吸附平衡后,TP 去除率为81.8%,此时溶液中剩余TP 质量浓度为0.364 mg/L,达到GB 18918—2002《城镇污水处理厂污染物排放标准》一级A 排放标准。 当温度超过30 ℃后,溶液中TP 去除率基本平稳,同时考虑到实际情况,确定30 ℃为最佳温度。
2.5 吸附动力学研究
动力学模型是对于吸附剂吸附速率的描述。 室温下,当溶液中TP 质量浓度为2 mg/L,pH 值在7 左右,改性火山岩投加质量浓度为5 g/L 时,实测改性火山岩在不同吸附时间下的吸附量,并分别采用非线性拟一级动力学方程(式3)、拟二级动力学方程(式4)和Webber-Morris 方程(式5)对实验数据进行拟合,见图6,相关拟合参数数值见表2。

式中:t 为吸附时间,h;k1为拟一级动力学模型常数;k2为拟二级动力学模型常数;kd为Webber-Morris模型常数;qt为t 时刻的吸附质量分数,mg/g;qe为吸附平衡时的吸附质量分数,mg/g。

图6 不同动力学模型拟合
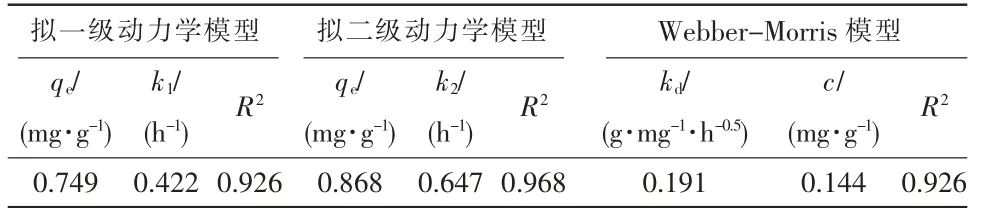
表2 不同动力学模型拟合参数
由图6(a)可以看出,改性火山岩在初期对TP的吸附速率较快,曲线斜率较大,之后趋于平缓。0 ~12 h 中,随着吸附时间的增加,吸附量也在逐渐增加,第12 h 时,对TP 的吸附质量分数达到0.80 mg/g,此后,吸附量趋于饱和稳定。 吸附过程由物理吸附、化学吸附和颗粒内扩散共同控制,由表2 中动力学拟合参数可以看出,拟二级动力学模型中R2为0.968,且所得平衡吸附量与实测值接近,说明反应更符合二级动力学模型。 由图6(b)可以看出,拟合曲线没有经过原点,说明除了颗粒内扩散外,还有其他过程对改性火山岩吸附除磷的反应速率进行控制[11]。在颗粒内扩散的过程中,火山岩的吸附共经历3 个阶段: 第一阶段水中磷酸盐扩散至改性火山岩外表面阶段,这是由于吸附剂表面存在大量的吸附点位,具有较快吸附速率;第二阶段水中的磷酸盐在火山岩颗粒内部扩散阶段,受到改性火山岩和磷酸盐之间的电子共用和转移作用,扩散阻力增大,第三阶段随着磷酸盐浓度的降低,颗粒内部扩散逐渐减弱,直至吸附达到平衡的阶段。
2.6 等温吸附研究
当温度一定时,吸附剂的吸附量随着平衡浓度变化而变化的曲线称为等温吸附曲线,作为吸附剂吸附性能的重要参考依据。 在25 ℃室温下,改性火山岩投加质量浓度为5 g/L,pH 值=7 时,吸附14 h后,水体水中TP 浓度基本不变,达到吸附平衡状态,此时测量不同磷吸附平衡浓度下的吸附数据,采用Laungmuir 模型(式6)和Freundlich(式7)对实验数据进行拟合见图7,拟合参数数值见表3。

式中:Qe为单位质量吸附剂的吸附质量浓度,mg/L;Qm为吸附平衡时,单位质量吸附剂的最大吸附质量浓度,mg/L;KL为Laungmuir 吸附常数;KF为Freundlich吸附常数;Ce为吸附平衡时溶液中的TP 质量浓度,mg/L;1/n 为特征常数。
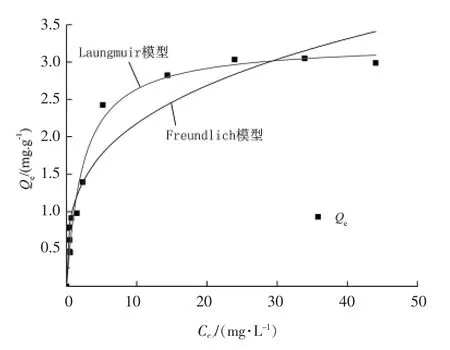
图7 等温吸附曲线模型拟合

表3 等温吸附曲线模型拟合参数
由图7 可以看出,随着TP 吸附平衡浓度的增大,改性火山岩的吸附量先迅速增大,后趋于平缓,这是因为随着污水中磷浓度的增大,水中磷酸根离子浓度与吸附剂表面液膜的浓度差增加,有利于磷酸根向吸附剂表面迁移[12],最终达到单位质量吸附剂的最大吸附量。通过表3 中拟合参数可以看出,改性火山岩吸附剂对水体中TP 的吸附行为更符合Laungmuir 等温吸附模型,说明吸附过程主要是单分子层吸附[13],利用分离因数RL进一步分析Langmuir吸附模型,其值可依照(式8)计算。

式中:C0为初始TP 质量浓度,mg/L。
根据RL的不同数值,可将吸附分为4 类:RL=1时,吸附过程为可逆吸附;RL=0 时,吸附过程为不可逆吸附;0 <RL<1,吸附过程为优势吸附;RL>1时,吸附过程为非优势吸附。 在实验浓度范围内,Langmuir 等温吸附曲线中,RL始终处于0 ~1 的范围中,说明改性火山岩对水体中磷为优势吸附。
3 结论
(1)通过FeCl3对天然火山岩进行改性,制备铁改性火山岩颗粒吸附剂,利用XRF,XRD,SEM 对改性前后火山岩进行表征,显示铁有效附着于火山岩表面,增大了吸附剂比表面积及吸附点位,火山岩晶体结构没有发生显著的变化。
(2)在温度为30 ℃,初始pH 值为7,TP 质量浓度为2 mg/L 的模拟污水中投加质量浓度为5 g/L 改性火山岩颗粒吸附剂,吸附12 h 后达到吸附平衡,此时水中TP 的去除率为81.8%,溶液中剩余TP 质量浓度为0.364 mg/L,达到GB 18918—2002《城镇污水处理厂污染物排放标准》一级A 排放标准。
(3)铁改性火山岩对水中低浓度磷的吸附为单分子层吸附,吸附速度较快,属于优势吸附,并由物理吸附、化学吸附和颗粒内扩散共同控制,其吸附过程更符合拟二级动力学模型及Langmuir 等温吸附模型。

