NaOH改性活性炭的制备及其吸附饮用水中二溴乙腈的性能
丁春生,杨明,霍建祺,余家明,姚俊
(浙江工业大学 土木工程学院,浙江 杭州 310014)
0 引言
饮用水消毒工艺杀灭了大量对人体有害的病原微生物,但同时产生了对人体有毒害作用的消毒副产物(DBPs)[1-3]。研究者目前已发现约 700 多种DBPs[4-6],其中二溴乙腈(DBAN)是一种含氮消毒副产物(N-DBPs),虽然在饮用水中含量极低(ng/L~μg/L),却比含碳消毒副产物(C-DBPs)的毒性更强[7-8]。Muellner等[9]进行7种卤乙腈(HANs)的毒性检测时发现DBAN表现出最强的细胞毒性,并且世界卫生组织已经将DBAN纳入监管(限值为 70 μg/L)[10],因此研究去除DBAN 的有效方法具有实际意义。
活性炭吸附净化是饮用水处理中常用的方法,其比表面积大,孔隙丰富,并且表面官能团易于调控[11]。目前常用的活性炭改性方法有表面氧化改性、表面还原改性、负载改性等,用适当的方法对活性炭进行改性能明显提高其对污染物的吸附能力[12-14]。研究表明,碱改性后的活性炭表面疏水性增强,比表面积增大,有利于活性炭对疏水性有机物的吸附[15-16]。丁春生等[17]研究表明采用NaOH对颗粒活性炭(GAC)改性后,对三氯硝基甲烷(TCNM)的去除率明显提高。本试验用NaOH对GAC进行改性,研究NaOH改性活性炭(NaOH-GAC)对DBAN的去除效果。
1 材料与方法
1.1 试验材料与仪器
试验试剂:DBAN标品:GR;GAC:AR;氢氧化钠溶液:AR;甲基叔丁基醚(MTBE):AR;1,2-二溴丙烷(C3H6Br2):GR;无水硫酸钠(Na2SO4):AR;丙酮:AR;去离子水。
试验仪器:GC-2014型气相色谱仪、A0C-20I,GC-2010型自动进样器;BS223S型电子天平(Sartorius公司);1 000 μL移液枪(dragon);IKS KS 130 basic型恒温往复式摇床(IKS公司);Sension 3型pH测定仪(Hach公司);JW-BK112型比表面及孔径分布测定仪;Nova NanoSEM450型扫描电镜(FEI公司);NEXUS912A型傅立叶红外光谱仪(ThermoNicolet公司)。
1.2 试验方法
1.2.1 氢氧化钠改性活性炭的制备
先用去离子水将GAC洗净,置于质量分数为2%的稀硝酸溶液中处理3 h,随后用去离子水洗至中性。在恒温干燥箱(110℃)中烘干12 h,冷却至室温,保存于储存瓶中。取30 g处理后的GAC放入90 mL 0.1 mol/L NaOH溶液中,浸泡2 h后滤出,于恒温干燥箱(110℃)中烘干12 h,然后冷却至室温,得到氢氧化钠改性活性炭,记为NaOHGAC。
1.2.2 活性炭表面结构的表征方法
本试验采用JW-BK112型比表面及孔径分布测定仪分析GAC和NaOH-GAC的比表面积和孔隙结构的变化;采用Nova NanoSEM450型扫描电镜观察GAC和NaOH-GAC表面形貌的变化;采用NEXUS912A型傅立叶红外光谱仪分析GAC和NaOH-GAC表面官能团的变化。
1.2.3 吸附试验
(1) 反应时间的影响
将100 mL 40 μg/L DBAN溶液加入250 mL的锥形瓶中,然后将浓度为0.7 g/L的GAC和NaOH-GAC分别投加到DBAN溶液中,并置于转速为110 r/min,温度为20℃的摇床中摇晃反应。每隔30 min取样一次,吸附反应时间共4 h。研究反应时间对反应效果的影响。
(2) NaOH-GAC投加量的影响
将100 mL 40 μg/L DBAN溶液加入250 mL的锥形瓶中,然后将浓度为0.3、0.5、0.7、0.9、1.1 g/L的NaOH-GAC分别投加到DBAN溶液中,并置于转速为110 r/min,温度为20℃的摇床中摇晃反应。每隔30 min取样一次,吸附反应时间共4 h。研究NaOH-GAC投加量对反应效果的影响。
(3) DBAN初始浓度的影响
NaOH-GAC投加浓度为0.7 g/L,分别投加到100 mL 不同浓度的DBAN(10、20、40、60、100 μg/L)溶液中,并置于转速为110 r/min,温度为20℃的摇床中摇晃反应。每隔30 min取样一次,吸附反应时间共4 h。研究DBAN初始浓度对反应效果的影响。
1.3 DBAN的分析方法
试验采用气相色谱-电子捕获器(GC-ECD)法对DBAN进行测定。将25 mL待测水样加入棕色瓶中,加入适量无水硫酸钠,迅速摇匀使其完全溶解。再加入2 mL MTBE后震荡5 min,静置5 min使两相分离。取上层萃取液放入GC-ECD进行检测。根据GC-ECD分析得到内标物1,2-二溴丙烷和目标物DBAN的保留时间间隔大,分离效果较好。试验分析得到的标准曲线的R2=0.995 3,具有良好的线性关系。
2 结果与讨论
2.1 表面性质表征结果
2.1.1 BET结果分析
对GAC和NaOH-GAC比表面积和孔隙结构进行分析,结果见图1、图2和表1。
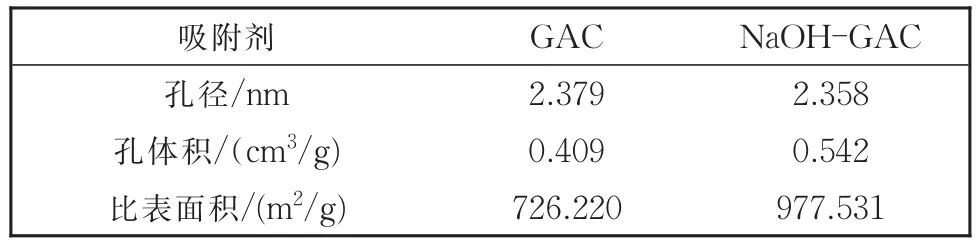
表1 吸附剂比表面积和孔径测定结果Table 1 Specific surface area and pore size measurement results of activated carbon

图1 吸附剂氮气吸附-脱附曲线Fig.1 N2adsorption-desorption curves of activated carbon

图2 吸附剂孔径分布曲线Fig.2 Particle size distribution curves of activated carbon
由图1可知,GAC和NaOH-GAC的吸附等温线趋于I型与Ⅳ等温线的结合形状,相对压力(P/P0)较小时吸附等温线迅速上升,随着P/P0的增大,GAC和NaOH-GAC的吸附量增长速率明显减少,并在P/P0大于0.4后出现了H4型滞后环。这说明GAC和NaOH-GAC具有丰富的孔隙结构。吸附反应刚开始的时候,GAC和NaOH-GAC的吸附以填充微孔为主,随着吸附反应的进行,由于GAC和NaOH-GAC具有一定的介孔,在较高的压力下发生毛细管凝聚现象,从而使吸附等温线出现了H4型滞后环。由图2可知,GAC经过改性后,其孔隙结构更发达,具有更多的微孔和介孔,孔隙分布主要集中在1.6 nm、2.2 nm和3.6 nm处。
由表1可知:GAC经过改性后,比表面积和孔体积分别增大了34.6%和32.5%,这可能是因为NaOH溶液腐蚀了GAC的孔壁,清除了孔内杂质,GAC内部微孔数量增多,使得GAC比表面积和孔体积增大;改性后平均孔径略微减少,这可能是因为GAC经过改性后,表面微孔数量增多,占比增大,使得平均孔径略有减少。
2.1.2 SEM扫描结果分析
SEM扫描结果见图3,由图3可以看出,GAC经过改性后,暴露出更多的微小孔隙,孔径变大。这可能是因为NaOH的腐蚀作用清除了孔隙表面和内部杂质,从而使微小孔隙数量增多,较小孔隙的孔径变大[18]。

图3 吸附剂活性炭的SEM图Fig.3 SEM of activated carbon
2.1.3 FT-IR结果分析
用FT-IR法对GAC和NaOH-GAC的表面官能团进行测定,结果见图4。
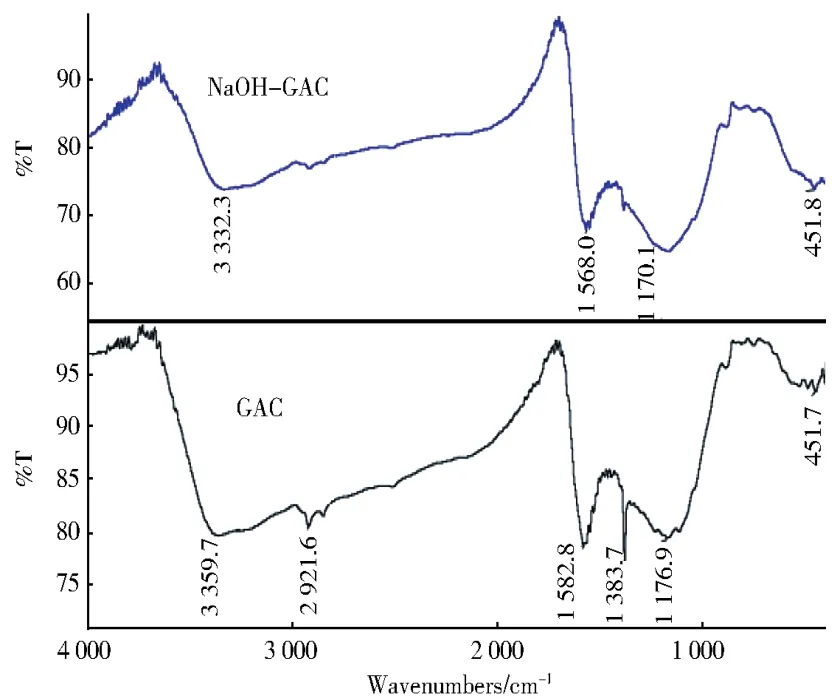
图4 吸附剂活性炭的FT-IR图Fig.4 FT-IR of activated carbon
由图4可知,GAC经过改性后,1 176.9 cm-1和1 383.7 cm-1左右处的吸收峰面积明显减少,GAC在1 176.9 cm-1的吸收峰为C—OH(酚羟基)的伸缩振动吸收峰[19],而在 1 383.7 cm-1左右处的吸收峰为—COOH(羧基)的对称振动峰[20],说明经过改性后,活性炭的C—OH和—COOH含量减少。改性前后的活性炭在1 568.0 cm-1和3 332.3 cm-1左右的吸收峰面积变化不大。1 568.0 cm-1附近的峰为C=O(羧基、酯基或非共轭酮)吸收峰,而3 332.3 cm-1左右的峰是由O—H(羧基或酚羟)引起的[21]。
由以上分析可知,GAC经过改性后,其表面的官能团发生了变化,表面非极性略有增强,因DBAN具有一定的亲水性,故GAC表面官能团的改变不利于对DBAN的吸附。但NaOH-GAC对DBAN的吸附能力是由其表面的物理性质与化学性质共同决定的[22]。本试验中,与化学吸附相比,NaOH-GAC的物理吸附起主导作用,因此GAC经过NaOH改性后,对DBAN的吸附能力得到较明显提升。
2.2 反应时间对吸附效果的影响
将浓度为0.7 g/L GAC和NaOH-GAC分别加入40 μg/L的DBAN溶液中,在pH=7,反应温度为20℃的条件下,反应4 h,结果见图5。
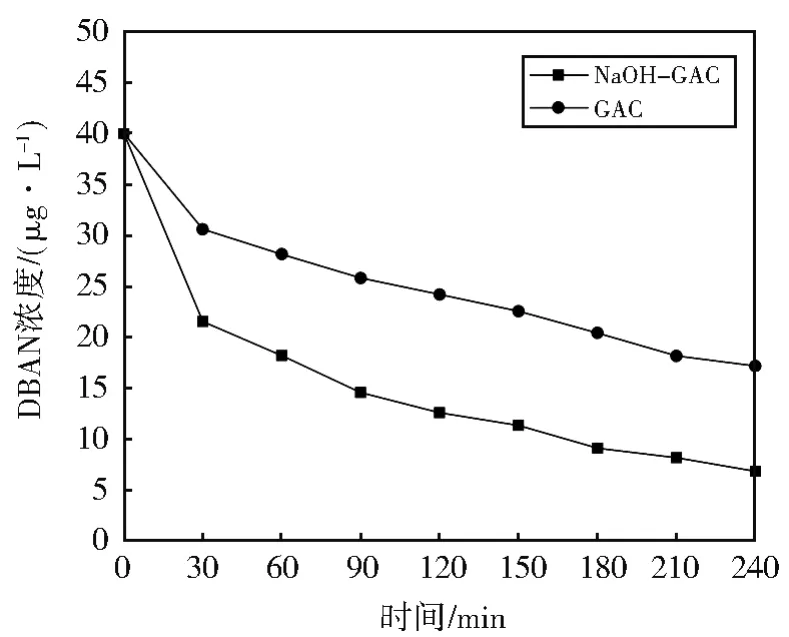
图5 吸附时间与吸附效果的关系Fig.5 Relationship between adsorption time and adsorption performance
由图 5可知:在 0 min~30 min内,GAC 和NaOH-GAC对DBAN吸附速率较快。这可能是因为溶液中DBAN的浓度较高,吸附剂表面的活性点位多,吸附传质动力大[23]。在30 min~180 min内,由于溶液中DBAN的浓度变低,吸附剂表面活性位点减少,使得吸附速率变慢。在180 min~240 min内,由于吸附剂表面活性位点基本饱和,对DBAN的吸附基本达到了平衡状态,使得DBAN的吸附量变化缓慢。此外,吸附时间为4 h时,NaOH-GAC对DBAN的去除率为82.89%,是GAC的1.45倍。这是因为NaOH-GAC具有更大的比表面积,更多的微小孔隙,本试验中物理吸附起主导作用,故NaOH-GAC对DBAN的吸附效果更好[24-25]。
根据图5中NaOH-GAC吸附DBAN的数据,得到DBAN去除率随时间变化趋势,结果见图6。用准二级吸附动力学方程对试验数据进行拟合,结果见图7。
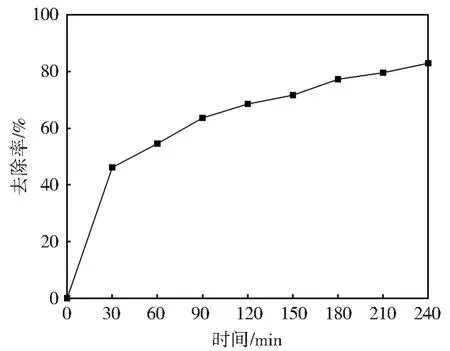
图6 吸附时间与去除率的关系Fig.6 Relationship between adsorption time and removal rate
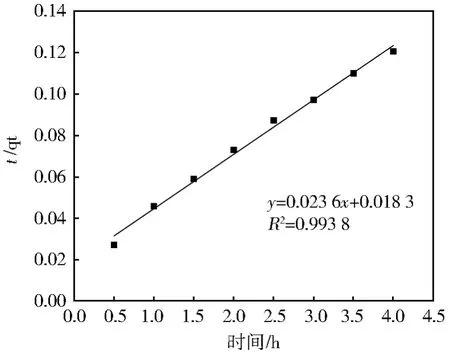
图7 准二级吸附动力学拟合结果Fig.7 Fitting results of quasi-secondary adsorption kinetics
由图 7可知:R2为 0.993 8,NaOH-GAC 对DBAN的吸附反应符合准二级吸附动力学方程。
2.3 NaOH-GAC投加量对吸附效果的影响
在pH=7、反应温度为20℃的条件下,分别将不同浓度NaOH-GAC(0.3、0.5、0.7、0.9、1.1 g/L)加入40 μg/L的DBAN溶液中,反应4 h,结果见图8。
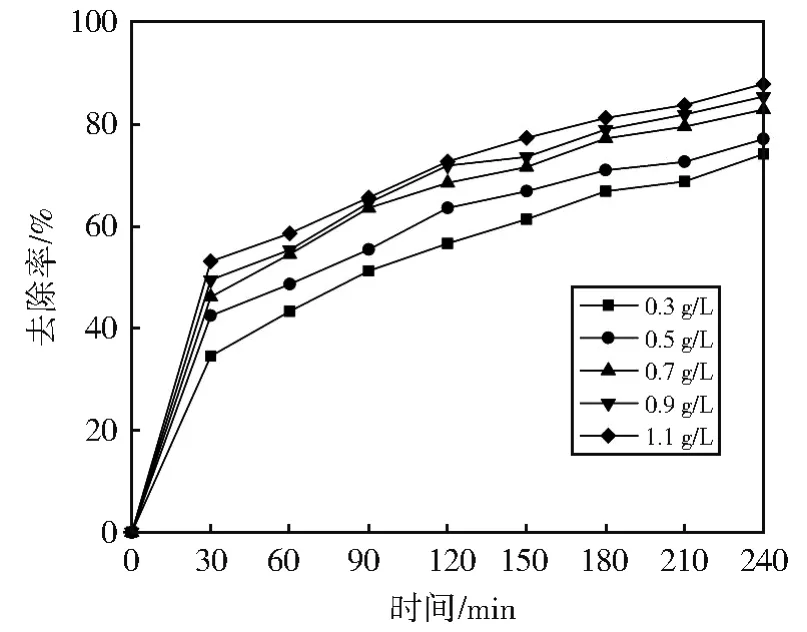
图8 投加量与吸附效果的关系Fig.8 Relationship between dosage and adsorption performance
由图8可知:随着NaOH-GAC的投加量增大,对DBAN的去除率增大。最小投加量和最大投加量相应的去除率分别为74.17%和87.89%。当NaOH-GAC的投加量大于0.7 g/L后,增加投加量难以有效提高去除率。因为吸附剂投加过量,NaOH-GAC表面活性位点过多,大量活性位点不能有效利用。此外,反应进行中DBAN浓度逐渐减小,使得NaOH-GAC和DBAN间传质阻力增大,不利于NaOH-GAC对DBAN的吸附[26]。
2.4 DBAN初始浓度对吸附效果的影响
分别向浓度为10、20、40、60、100 μg/L 的DBAN溶液中加入浓度为0.7 g/L的NaOH-GAC,反应温度为20℃,pH=7,反应4 h,结果见图9。
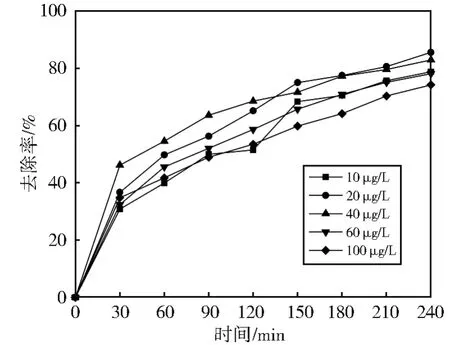
图9 初始浓度与吸附效果的关系Fig.9 Relationship between initial concentration and adsorption performance
由图9可知:当DBAN的初始浓度为20 μg/L时,反应4 h后,NaOH-GAC对DBAN的去除率最大,达到85.51%。DBAN的去除率随着初始浓度的增加,先升后降。这可能是因为溶液中DBAN的初始浓度增大,增大了NaOH-GAC与溶液中DBAN的接触面积,减小了吸附过程中的传质阻力[27],从而使DBAN的去除率上升。而NaOHGAC表面的活性点位是有限的,因此吸附达到平衡后,NaOH-GAC对DBAN吸附作用会逐渐减弱[28],从而使DBAN的去除率降低。
2.5 吸附等温线
用Langmuir和Freundlich两种模型评价NaOH-GAC的吸附性能。根据图9中的试验数据,并画出DBAN的平衡浓度(Ce)和NaOH-GAC对DBAN的吸附容量(qe)关系图(图10)。再用两种吸附等温线对图10数据进行拟合,结果见图11和表2。

图11 Freundlich方程对吸附过程拟合结果Fig.11 Fitting results of adsorption process by Freundlich equation

表2 吸附等温线的拟合结果Table2 Fitting results of adsorption isotherms
由图11和表2可知:NaOH-GAC对DBAN的吸附过程更符合Freundlich方程,R2为0.941 1,表明Freundlich吸附等温线能较好地描述NaOHGAC对DBAN的吸附行为。
3 结论
(1)NaOH-GAC相比于GAC,表面的化学性质发生了变化,非极性略有增强,不利于对DBAN的吸附;但改性后比表面积和孔体积分别增大了34.6%和32.5%,物理吸附容量增加较多。由于本实验中物理吸附起主导作用,因此经过NaOH改性后,活性炭对DBAN的吸附能力得到较明显提升。
(2)在DBAN初始浓度为40 μg/L、pH = 7、温度为20℃的条件下,反应4 h后,0.7 g/L NaOHGAC对DBAN的去除率为82.89%,是相同浓度GAC的1.45倍。
(3)随着DBAN初始浓度的增加,NaOH-GAC对其吸附去除率先升后降。这是因为溶液中DBAN的初始浓度增大,增大了NaOH-GAC与溶液中DBAN的接触面积,减小了吸附过程中的传质阻力,使DBAN的去除率上升。由于NaOH-GAC表面的活性点位是有限的,因此吸附达到平衡后,NaOH-GAC对DBAN吸附作用会逐渐减弱,从而使DBAN的去除率降低。
(4)Freundlich吸附等温线能较好地描述NaOH-GAC对DBAN的吸附行为,其吸附反应符合准二级吸附动力学方程。

