利用化学实验落实“教学做合一”提升化学核心素养
叶永鑫

摘要:以“Fe2+与Fe3+的检验与转化”一课中的教学片段为例,结合陶行知先生“教学做合一”的思想,通过设计教师演示实验和学生小组合作实验的方法让学生参与到课堂中来,让教师在“做中教”,学生在“做中学”,让核心素养的提升落地到“教、学、做”的过程中来。
关键词:化学实验;教学做合一;核心素养
文章编号:1008-0546( 2021)01-0081-02
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2021.01.022
著名教育学家陶行知先生说过:“教学做是一件事,不是三件事。我们要在做上教,在做上学。在做上教的是先生;在做上学的是学生。”“教学做合一,做是学的中心,也是教的中心。”具体到化学学科的课堂教学中,教师在进行教学设计时,要在课堂中积极融人化学实验,让学生从眼、耳、口、手、脑等多个维度行动起来[1]。在《普通高中化学课程标准(2017年版)》中,提出了化学学科核心素养的5个方面。学生核心素养的提升需要教师将教学内容与生产生活实际紧密结合起来,需要教师和学生共同开展高水平的实验活动[2]。下面,笔者將结合自身执教的“Fe2+与Fe3+的检验与转化”一课中的教学片段,谈谈利用化学实验,落实“教学做合一”思想,提升学生的化学核心素养。
一、教师演示实验,激活学生思维
教学片段一:铁肥溶液变黄,引发学生思考
[师]植物缺少铁元素会引起叶片发黄,此时可以使用有效成分为FeSO4的铁肥溶液来给植物补铁。在使用时发现,久置的铁肥溶液由基本无色变为黄色。请大家想一想可能是什么原因?能有方法验证吗?
[生]含Fe2+的溶液显浅绿色,含Fe3+的溶液显黄色,应该是Fe2+被空气氧化成了Fe3+。
[师]依次展示新配置的FeSO4溶液、FeCl,溶液、茶叶水、将一滴FeCl3溶液滴人5mL蒸馏水后形成的溶液,并提问:此时仅靠观察还能说明Fe3+的存在吗?
[生]直接观察颜色的方法有时可靠度较低,可能受到浓度或者其他物质的干扰,可以改用滴加NaOH溶液的方法,如果有Fe3+,则会生成红褐色沉淀。
[演示实验1]向两支洁净的试管中各加入2mL的FeCl3溶液和铁肥溶液,再依次滴人5滴NaOH溶液。盛有FeCl3溶液的试管中出现红褐色沉淀,盛有铁肥溶液的试管中出现灰绿色沉淀。
[师]这个对比实验中铁肥溶液没有出现刚才预计的红褐色沉淀,反而出现了灰绿色沉淀,有可能是什么原因?能证明你的猜想吗?
[生]说明用NaOH溶液检验Fe3+也有局限性,铁肥溶液中有其他离子对Fe3+的检测产生了干扰,有可能是Fe2+遇碱生成了灰绿色沉淀。可以用FeSO4溶液和NaOH溶液验证。
[演示实验2]向一支洁净的试管中加入2mL的FeSO4溶液,再滴人5滴NaOH溶液,试管中出现灰绿色沉淀。
[师]从这个实验中确实说明了Fe2+对Fe3+的检验产生了干扰。老师向大家介绍一个新的试剂:KSCN溶液,它可以用来特征性地检验Fe3+,且不受Fe2+的干扰。
[演示实验3]向三支洁净的试管中各加入2mL的FeCl3溶液、FeSO4溶液和铁肥溶液,再依次滴人2-3滴KSCN溶液。盛有FeC13溶液的试管中溶液变为血红色,盛有FeSO4溶液的试管中溶液不变色,盛有铁肥溶液的试管中溶液变为红色。
[生]久置的铁肥溶液中确实有Fe3+;用KSCN溶液来检验Fe3+灵敏度更高,准确度也更高。
[设计意图]在本环节中,学生虽未真正动手,但是教师通过3个演示实验引导学生观察、思考、表达、聆听,充分调动了学生的眼、耳、口、脑,让学生参与到了对铁肥溶液中是否含有Fe3+这一问题的证明过程中。在这个教学过程中,教师唯一教给学生的是KSCN溶液对Fe3+的特征性检验,而且这一知识的教授是建立在学生参与到课堂中,认识到现有的检验方法存在缺陷时提出的。在3个演示实验中,后一个实验都是对前一个实验不足之处的修正,三种检验方法的相互对比之间,学生不难发现KSCN溶液对Fe3+的检验具有灵敏度高,准确度高的优点。
从发展学生核心素养的角度上来看,学生从溶液的颜色判断所含微粒,是从观察宏观表象到探析微观原因的进步;学生对3个演示实验的观察、分析、对比、推理,是寻找证据证明猜测的过程,是对证据推理能力的提升;学生在此过程中经历了“初步确定方案→实践→未达预期→分析干扰因素并排除→新方案或优化方案……”这一螺旋上升的思维和实践过程,初步建立了对物质检验方案选择的认知模型[3]。
二、小组合作实验,提升核心素养
教学片段二:复现铁肥变黄,加强小组合作
[师]通过刚才的实验,我们已经可以确认久置的铁肥中含有Fe3+。刚才也有同学已经提到应该是Fe2+被空气氧化生成了Fe3+。请大家根据提供的试剂,复现这一过程,并且确认该过程已经发生。
提供试剂:FeS04溶液、FeCl3溶液、KSCN溶液、H2O2溶液、酸性KMnO4溶液、铁粉、铜粉。
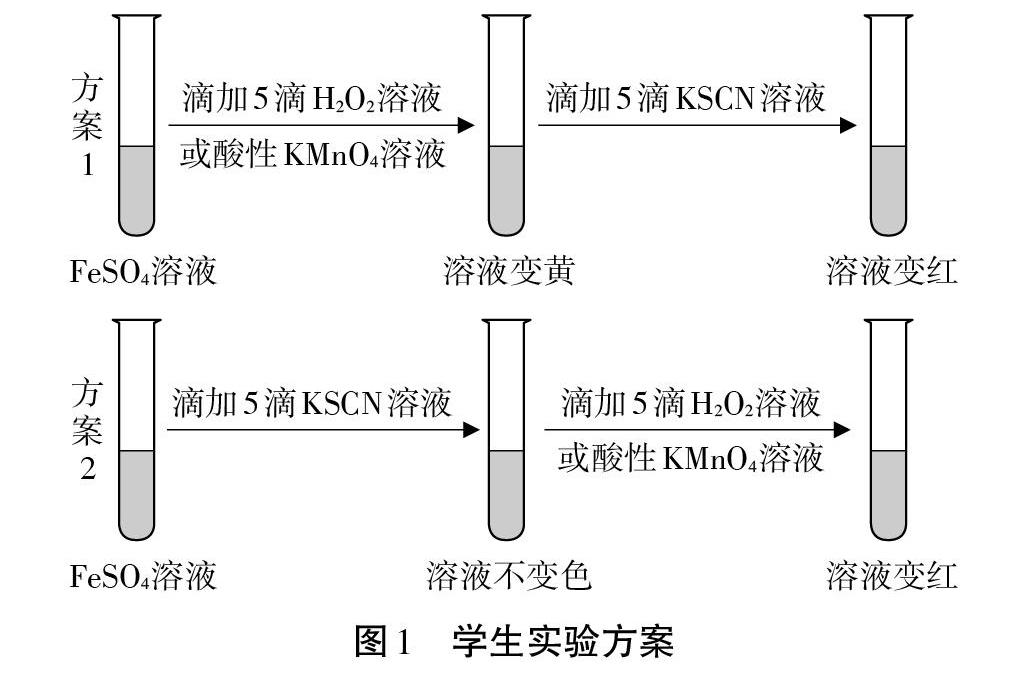
[生]小组讨论,形成方案,合作实验,汇报结论。如图1所示。
[师]这两种方案中都实现了将Fe2+氧化为Fe3+,并且通过KSCN溶液证明了这个过程的发生。我们再仔细对比这两种方案,能否从中得到启示:如果想要证明一份未知溶液中是否含有Fe2+,应该采取哪一种操作方案?为什么?
[生]要先加入KSCN溶液,再加入氧化剂。Fe2+无法直接检测,被氧化为Fe3+可以通过KSCN溶液检出。先加KSCN溶液不仅是为了检出Fe3+,更是为了保证原溶液中不含Fe3+,防止它的干扰。
[师]通过这两组实验,我们知道了Fe2+是非常容易被氧化的,常见的可以将其氧化的氧化剂有:氧气、H2O2溶液、酸性KMnO4溶液等……
[板书]如图2所示
[设计意图]在这个教学片段中,学生通过小组合作的形式复现了铁肥溶液变黄的过程,并通过KSCN溶液验证了Fe3+的产生。这项任务的完成,意味着学生动用了“氧化还原反应”和“物质检验”的相关知识,用已有知识指导自身的实践体验,实现了将“学”应用于“做”。同时,教师引导学生对比两种方案中,哪一种方案更适合检验未知溶液中是否含有Fe2+,从学生的“做”出发,引导学生从实践中总结经验,进一步用于解决实际问题。
通过这组实验,让学生体会到了物质的转化是普遍存在的,转化过程的发生是有条件的,转化过程的图示则是对物质世界高度概括的一种模型。对Fe2+检验方法的探讨则帮助孩子形成化学学科的思想和方法,促进学生形成物质检验过程中所需的缜密思维:不仅需要选对试剂,而且在使用多种试剂时还需考虑试剂添加顺序带来的影响[4]。
三、反思与总结
无论是教师的演示实验,还是学生的小组合作实验,教师在进行教学设计的过程中应当对该实验所起到的效果和最终目的有明确的认识。再小、再简单的演示实验也应当有它存在的目的,也應当启发学生参与到对课堂的思考中来。例如:将1滴FeCl,溶液滴人5mL蒸馏水中,将这份溶液与原本的FeCl溶液作对比,学生即可发现:观察颜色所得结论的可靠性并不十分准确。由此便可顺理成章地引出加碱沉淀法。而对比向FeCl3溶液和铁肥溶液中加入NaOH溶液的现象,也是为了让学生直观地感受到一种检测方法在不同情况下可能准确度有差异。此时学生虽未真正动手做,但教师的操作其实都是在学生给出的方案中进行的。学生真正参与到了课堂中,与教师进行问答沟通,对知识的记忆和掌握也更加牢固。
在学生真正动手做的小组合作实验中,教师应当对实验的过程有所预设,但在学生操作的过程中要给他们一定的自由度。例如在重现铁肥变黄,并验证Fe3+生成的过程中,教师不对学生添加试剂的顺序进行提示。学生使用两种不同方案得到了相同的结果,但只要教师一提问:“如果将FeSO4溶液替换成未知的溶液,如何检验Fe2+?”学生就能想到试剂的添加顺序有时对实验结果有着不同的影响,也就建立了更加完善的事实证据链,对于物质检验的认知水平也得到了提升。
化学科学诞生于生产生活实践,因此学生对化学知识的学习也离不开化学实验。缺少化学实验的课堂学生会觉得无趣,失去了学生注意力的课堂自然也失去了灵魂。化学实验不能只是课堂中的装饰,应当通过实验让学生“动起来”,和教师进行交流。这样才能让学生在“做中学”,让教师在“做中教”,学生核心素养的提升才能得到落实。
参考文献
[1]李秀芝.教、学、做合一在高中化学实验教学中的应用[J].中学化学教学参考,2015(24):53
[2] 中华人民共和国教育部.普通高中化学课程标准(2017年版)[S].北京:人民教育出版社,2018:2,72-74
[3]何建平,在“教学做合一”中优化思维品质提升创新能力——高中化学“乙烯”教学设计[J].化学教与学,2016 (10):73-74,80
[4]任润武.如何通过化学实验落实核心素养[J].中学化学教学参考,2020(4):58-59

