砷及MPST过表达对SH-SY5Y细胞GRP78/CHOP通路的影响
李 成,楼迪栋,齐晓岚,范海琼,朱 卫,潘际刚
(1.贵州医科大学基础医学院生理学教研室,2.贵州中医药大学基础医学院,3.贵州医科大学分子生物学重点实验室,贵州 贵阳 550025)
砷是一种广泛分布于环境中的环境毒物。砷常通过水、食物、空气等途径进入人体后引起人的器官或组织损伤[1]。研究表明,砷具有神经毒性作用,其可以通过血脑屏障直接造成人大脑皮质组织不可逆性损伤,从而引起人认知功能障碍,并造成学习、记忆能力的减弱[2-3]。因此,开展对于砷的神经毒性损伤及其作用机制的研究对于防治砷中毒具有重要现实意义。本课题组前期研究表明,亚砷酸钠对SH-SY5Y神经细胞具有毒性作用,而外源性过表达MPST蛋白可以拮抗砷所致的神经毒性损伤[4]。而本研究以慢病毒转染稳定表达外源MPST的SH-SY5Y细胞为观察对象,检测砷暴露前后GRP78和CHOP蛋白表达水平,进一步探讨内质网应激通路是否参与砷神经损伤以及MPST过表达对砷诱导的内质网应激水平的影响。
1 材料与方法
1.1 材料
1.1.1细胞系 人神经母细胞瘤SH-SY5Y细胞,购自德国DSMZ公司稳定感染慢病毒载体的人的SH-SY5Y细胞(SH-PEB细胞)稳定感染MPST重组慢病毒载体的SH-SY5Y细胞(SH-MPST细胞)
1.1.2试剂 胎牛血清(Gibco),购自以色列BioInd公司(批号:10099141C);青霉素-链霉素,购自美国Gibco公司(批号:15140163);胰蛋白酶,购自美国Gibco公司(批号:25200056);磷酸盐缓冲液(PBS),购自北京索莱宝公司(批号:P1032);DMEM培养基,购自美国Hyclone公司(批号:SH30081);NaAsO2,购自美国Sigma公司(批号:S7400);葡萄糖调节蛋白78蛋白(glucose regulated p rotein,GRP78)抗体(批号:sc-166490)、转录因子C/EBP同源蛋白(C/EBP-homologous protein,CHOP)抗体(批号:sc-365318)、抗小鼠IgG-HRP二抗(批号:P1032),购自美国Santa Cruz公司,牛磺熊去氧胆酸(TUDCA),购自购自美国Sigma公司(批号:sc-2005)。
1.1.3仪器 Model 310细胞恒温CO2培养箱(美国Thermo公司);细胞培养超净台(苏州净化);全波段多功能酶标仪(BioTek公司);Eclipse Ti-s倒置显微镜(日本Nikon公司);FACSCalibur流式细胞仪(美国BD公司);全自动凝胶成像仪(美国SynGene)。
1.2 方法
1.2.1细胞培养 SH-SY5Y细胞培养在高糖DMEM培养基(含10% FBS和1%青霉素-链霉素)中,培养于37 ℃、5% CO2的培养箱中,隔天换液,细胞生长至70%汇合度时进行传代或冻存。
1.2.2慢病毒转染MPST过表达 本实验所用细胞为前期已建立过表达细胞株[5]。通过PCR扩增出MPST目的基因,并将其克隆到慢病毒表达载体pEB-GFP(T2A)PURO上,然后将重组慢病毒表达载体和慢病毒包装质粒系统(pLP/VSVG, pLP1, pLP2)共转染293T细胞48 h后,收集病毒液。当SH-SY5Y细胞在12孔板生长至50%汇合度时进行转染,细胞更换为含10 mg·L-1基因转染增强剂聚凝胺(polybrene)及10% FBS的DMEM培养基,分别于不同孔加入1 mL含MPST和空载体的病毒液,分别设为过表达组和空载对照组,培养箱中继续培养6 h后,更换含10% FBS的DMEM培养基继续培养,细胞生长至90%汇合度以嘌呤霉素进行筛选,最终以蛋白印迹实验验证MPST表达水平。
1.2.3实验分组 实验分6组:MPST慢病毒转染组(SH-MPST过表达组),空载体转染对照组(SH-PEB组),染砷组(NaAsO2组),TUDCA阻断剂组,TUDCA预处理染砷组。
1.2.4蛋白印迹检测 药物处理细胞后,以RIPA细胞裂解液(含1 mmol·L-1PMSF)裂解细胞,冰上裂解10 min,20 627×g离心15 min,取上清液进行BCA蛋白定量,计算并配制上样缓冲液,100 ℃变性5 min,进行12% SDS-PAGE电泳分离蛋白,湿转至PVDF膜,5%的脱脂牛奶封闭2 h,用GRP78、CHOP抗体(1 ∶1 000)或内参抗体GAPDH(1 ∶ 2 000)于4 ℃摇床孵育过夜,PBS洗膜3次,抗小鼠IgG-HRP二抗室温孵育1 h,PBS洗膜3次,PVDF膜以化学发光试剂盒进行显色,凝胶成像仪成像,以Quantity One对蛋白印迹条带进行处理和分析。
2 结果
2.1MPST过表达对细胞GRP78与CHOP蛋白表达的影响如Fig 1所示,蛋白印迹实验发现,未染砷处理的对照组和过表达组细胞内GRP78与CHOP蛋白表达无差异。
2.2 NaAsO2和TUDCA对SH-PEB细胞GRP78与CHOP蛋白表达的影响如Fig 2所示,蛋白印迹实验发现,与未染砷处理的对照组细胞相比,50 μmol·L-1NaAsO2处理的对照组细胞中GRP78与CHOP蛋白明显上调(P<0.01);而预先加入1 mmol·L-1内质网应激阻断剂TUDCA预处理可以逆转砷诱导的GRP78与CHOP的上调现象(P<0.01)。
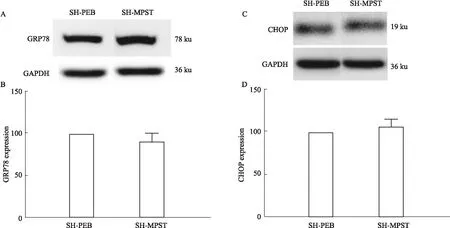
Fig 1 Effect of MPST overexpression on expression of GRP78 (A) and CHOP (B) proteins n=3)

Fig 2 Effect of NaAsO2 and TUDCA on expressions of GRP78 (A) and CHOP (B) proteins in SH-PEB cells
2.3 NaAsO2和TUDCA对SH-MPST细胞GRP78与CHOP蛋白表达的影响如Fig 3所示,蛋白印迹实验发现,与未染砷处理的过表达组细胞相比,50 μmol·L-1NaAsO2处理的过表达组细胞中GRP78与CHOP蛋白明显下调(P<0.01);而预先加入1 mmol·L-1内质网应激阻断剂TUDCA预处理使50 μmol·L-1NaAsO2处理的过表达组细胞中GRP78与CHOP蛋白上调(P<0.01)。

Fig 3 Effect of NaAsO2 and TUDCA on expressions of GRP78 (A) and CHOP (B) proteins in SH-MPST
3 讨论
内质网是一种重要的细胞器,参与并调节蛋白质的合成、折叠、修饰及运输等生命活动。当细胞受到遗传因素或者环境因素影响时,会使错误折叠的蛋白质在内质网中积聚,发生内质网应激。研究表明,内质网应激与神经退行性疾病、糖尿病、代谢综合症和癌症的发生发展密切相关[6]。Sun等[7]通过建立大鼠饮用水染砷模型研究发现,慢性砷暴露处理后大鼠学习记忆能力明显下降且伴随着大鼠海马细胞中GRP78 蛋白、PERK蛋白、ATF4蛋白、CHOP蛋白表达上调。在本实验中,砷暴露处理后的SH-SY5Y细胞内的GRP78与CHOP蛋白表达也明显上调,而给予内质网应激阻断剂TUDCA预处理可以逆转砷诱导的GRP78与CHOP蛋白上调现象。众所皆知,GRP78与CHOP蛋白表达的变化是内质网应激的标志[8]。这些结果共同提示砷的神经毒性作用可能与砷诱导细胞发生内质网应激有关。
近年来,H2S作为一种新型气体信号分子得到广泛关注[9]。在哺乳动物体内,H2S由胱硫醚-γ-裂合酶、胱硫醚-β-合酶和3-巯基丙酮酸硫转移酶(MPST)合成。H2S具有舒张血管、降血压、抗凋亡、抗炎、参与抗氧化应激等多种生物学功能[10]。此外,Li等[11]研究发现,腹腔注射30或100 μmol·kg-1NaHS的生理盐水可以改善由链脲佐菌素诱导的糖尿病大鼠的心肌肥大,使用含NaHS的生理盐水干预的大鼠心肌细胞中GRP78、CHOP和caspase-12蛋白表达降低,这说明H2S通过影响内质网应激发挥心脏保护作用。本课题组前期研究表明,亚砷酸钠对 PC12 细胞的损伤作用与砷下调3MST蛋白的表达有关,外源性过表达MPST可以拮抗亚砷酸钠的毒性损伤作用[4,12]。而本次实验发现,过表达MPST可以逆转砷诱导的GRP78与CHOP蛋白上调,而且使内质网应激水平明显低于正常,这一结果提示外源性过表达MPST可以降低机体对砷刺激后一系列内质网应激反应。进一步使用内质网应激阻断剂TUDCA进行预处理,MPST过表达对砷暴露下内质网应激超低水平的维持效应被逆转。综上所述,GRP78/CHOP内质网应激通路参与了砷诱导的神经毒性损伤;MPST过表达可降低砷诱导的内质网应激水平。然而砷是如何引起GRP78、CHOP蛋白表达的变化从而发挥损伤效应,过表达MPST又是如何在砷暴露下维持超低内质网应激水平,这些机制还有待进一步研究。

