多模态乳腺肿瘤图像特征提取与分级诊断的研究进展
陈继鑫,孔恒
近年来,随着乳腺癌发病率逐年上升,乳腺癌 已经成为女性最常见的恶性肿瘤,严重危害女性健康[1]。及早明确诊断,并予以有效治疗是乳腺癌预防治疗的关键。超声、钼靶、核磁共振成像等影像学检查往往在乳腺肿瘤的诊断中起到关键的作用。使用的单一影像技术存在一定的局限性,从而导致的错误分级诊断结果会给临床带来不良后果。多模态影像技术是通过联合多种成像技术、融合不同模态图像信息的成像技术,以此能够实现信息的交叉互补及相互验证,同时获得机体多方面信息从而提高诊断效率。本文就多模态乳腺肿瘤图像特征提取与分级诊断的研究进展进行综述。
1 影像学联合诊断在乳腺肿瘤诊断中的应用
目前,针对乳腺癌诊断的影像学检查方法主要包括乳腺超声、钼靶摄影、及核核磁共振检查,不同影像学检查方法的诊断效果不尽相同。
超声是诊断乳腺肿瘤的重要影像学方法。超声检查的优势在于可以观察内部结构和准确定位病灶,以及对大部分致密型的乳腺有较为良好的显影。同时超声检查对囊性病变较敏感,可以很好的区分实性和囊性肿块,对纤维腺瘤也有较特征的影像学表现。其具有经济、简便、无创、方向性好、可显示病灶血流等优点。在中国,超声检查在女性乳腺癌筛查中常作为首选手段。超声在女性乳腺癌症检测中起着至关重要的作用[2]。
乳腺钼靶检查是迄今唯一被证实能够降低乳腺癌病死率的筛查方法。钼靶可以清楚显示各层组织,特别是对微小钙化十分敏感,能够发现2 mm以下钙化灶。在国际上,钼靶检查被广泛应用于45 岁或者50 岁以上妇女乳腺癌的筛查手段[3]。但是钼靶组织穿透力有限,乳腺腺体致密程度常常会影响诊断结果,在致密性乳腺中常会呈现假阴性。其空间分辨能力较差,较难发现和定位微小病变组织。同时,乳腺钼靶检查亦具有一定的辐射。尽管如此,钼靶检查仍是诊断乳腺癌中不可或缺的影像学检查方法。
乳腺核磁共振检查在乳腺良恶性肿瘤诊断、对乳腺癌分期、术前评估、治疗随访、及肿瘤血管等方面,相比超声和钼靶,可以提供更多的信息,有着不能替代的作用。因其具有良好的软组织分辨率和无辐射特点,对乳腺检查拥有独到的优势,一直以来作为乳腺癌高危人群筛查的影像学检查方法。在其中一篇文献报告中乳腺增强核磁共振检查表现出的特异性和敏感性分别为72.22%、94.87%,在核磁钼靶超声三个影像学检查中,核磁影像的敏感性是最高的,对恶性病灶的检出率也同样最高。在检测有症状及无症状的乳腺癌高危女性时,核磁共振增强影像已被证明具有高敏感性。但因为核磁共振对钙化显示不敏感,并且良恶性病变重叠率高,以至于其特异性低[4]。
隋广平等[5]在其研究中选取早期乳腺癌患者70 例进行研究,患者分别进行常规超声检查(作为常规组)与超声检查+钼靶+核核磁共振的方式联合检查(作为联合组),并分别与术后病理结果进行比较,对其检测结果的灵敏度、特异度及约登指数进行分析。结果:常规组患者检查的敏感度、特异度、约登指数分别为75.7%、72.7%、48.4%;联合组分别为91.9%、93.9%、85.8%;组间对比差异性均显著(P<0.05)。在另外一个文献报告中,Hongda Shao 等[6]选取了90 名临床怀疑乳腺癌的中国女性患者接受了前瞻性乳腺核磁、超声和钼靶检查。以病理报告为金标准,比较各种影像学方法及其相互间联合诊断的性能。在本队列研究中,单独磁共振影像检查的准确率和敏感度(AUC)明显高于单独使用超声或者钼靶检查(P<0.05)。单独磁共振影像诊断的敏感性为90.91%,钼靶为72.73%,超声为80.0%,联合磁共振+钼靶+超声诊断的敏感性为98.2%(χ2=25.9,P<0.001),联合磁共振+超声诊断敏感性为94.5%(χ2=53.3,P=0.002),联合磁共振+钼靶诊断敏感性为92.9%(χ2=41.9,P<0.001)。可以看出,两种或三种方法的联合诊断显著提高了乳腺癌的诊断敏感性。多影像学技术联合应用可显著提高早期乳腺癌的诊断准确率,在提高乳腺癌诊断率中发挥重要作用。
1.1 超声和钼靶联合诊断
乳腺超声检查和钼靶X 线摄影相结合的潜力是在30年前的“模拟成像时代”首次提出的[7]。结合钼靶和超声联合诊断可以提高乳腺癌检测的准确性,原因来自于这两者具有较好的互补性[2]。在临床中,当出现一下情况时,钼靶X 线检查常常存在一定局限性:小乳房而产生投照困难,患者对X线的放射性不适宜,致密型乳腺等等。同时钼靶对乳腺腋窝乳腺组织及淋巴结易漏诊,对导管内病变诊断较局限,对肿块的大小测量不精确等等。因此,为能够提高乳腺癌诊断准确性,在进行钼靶影像学检查时,建议同时选择超声检查。
林欢等[8]以自查或者体检发现乳腺肿块(最大直径≤2 cm)的患者作为研究对象,纳入分析了9 篇乳腺癌超声钼靶联合诊断的meta 分析文献,结果提示:超声敏感度为0.75,钼靶敏感度为0.66,联合诊断敏感度为0.92。超声特异度为0.75,钼靶特异度为0.83,联合诊断特异度为0.82。综合受试者工作特征曲线下面积中,超声0.7902,钼靶0.8120,联合诊断为0.9496。诊断比值比超声为7.11,钼靶为8.67,联合诊断为60.82。联合诊断的异质性性明显低于超声或钼靶X 线。该研究表明对直径2 cm 以内的乳腺肿块,超声和钼靶联合诊断可以提高乳腺癌诊断的准确性,对乳腺癌的早期诊断及治疗有着重要的作用。
在另外一项对3418 名乳房高密度的女性进行的研究中,研究人员发现,在乳房密度超过50%的妇女的乳房X 光检查中添加ABUS(全自动乳腺超声)后,可以使每1000 例乳腺癌中检测出12.3例乳腺癌,而仅通过乳房X 线检查时,则为4.6 例。敏感性从76.0%增加到97.7%,而特异性从98.2%增加到99.7%。Giuliano 发表了迄今为止最有力的证据支持FFDM(全数字化乳腺摄影)的使用,其次是ABUS 作为筛选工具[9]。
超声和钼靶的联合诊断,因能表现出其各自的诊断优势,可以提高乳腺癌诊断的准确性、特异性和敏感度,有助于提高乳腺癌早期筛查的准确率。钼靶超声联合在乳腺癌诊断的准确性优于单一超声或钼靶诊断,因此,可作为优选诊断方案在临床中更加广泛的使用。
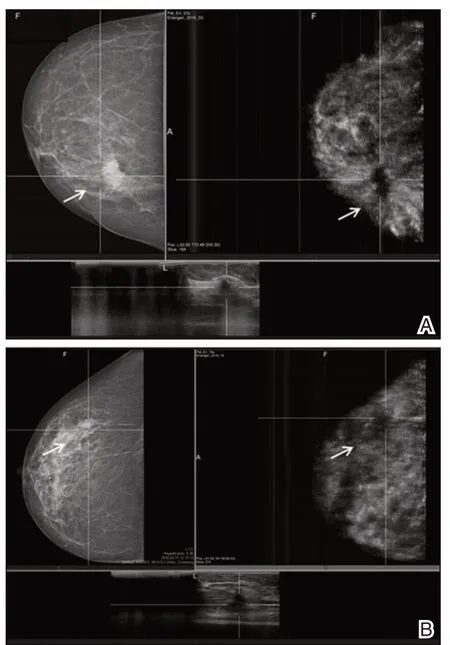
图1 使用超声检查和乳房X 光(钼靶)检查相结合的示例
1.2 超声和核磁共振联合诊断
同超声和钼靶相比,核磁共振成像受到腺体致密程度、病灶大小和位置的影响更少,对小叶癌和小叶原位癌有更高的检出率,同时病灶的大小、形态和边缘,磁共振能够更清晰及准确的显示出来。但磁共振成像对肿块钙化的敏感度低于钼靶及超声的检查,且特异性不足[11]。
超声、MRI 两者联合检查诊断乳腺癌可更有效地提高诊断准确性。将其应用于乳腺癌高危人群的筛查与检测,能够有效的减少漏诊误诊率,并能更早发现及诊断乳腺癌,尽早一步指导患者治疗方案。在一份文献报告中,马财等收集63 例68个结节的彩色多普勒超声和核磁共振影像资料,其中超声诊断敏感度为97.14%,特异度为80%,准确性为83.33%,MR 敏感度为100%,特异度为50%,准确性为83.33%,两者结合可提高诊断的准确性,准确性可达88.88%。研究表明,彩色多普勒超声与核磁共振增强扫描联合应用能提高乳腺良恶性病变的检出率,超声和MRI 联合应用在诊断乳腺结节方面具有更大优势[12,13]。QIAOHONG PAN 和JIANWU JI 在一篇文献中分析了超声结合核磁共振在乳腺癌T、N 和M 分期中的诊断价值,得出结论时超声结合核磁共振对乳腺癌的诊断具有较高的敏感性和特异性,对各个阶段的肿瘤识别准确率更高[14]。
临床中常常使用超声和磁共振来对乳腺癌进行诊断,这两种影像学检查都具有很高的价值,相比超声,磁共振在早期乳腺癌的发现及良恶性鉴别中表现出更高的准确率及敏感性,两者联合诊断则拥有更高的价值。
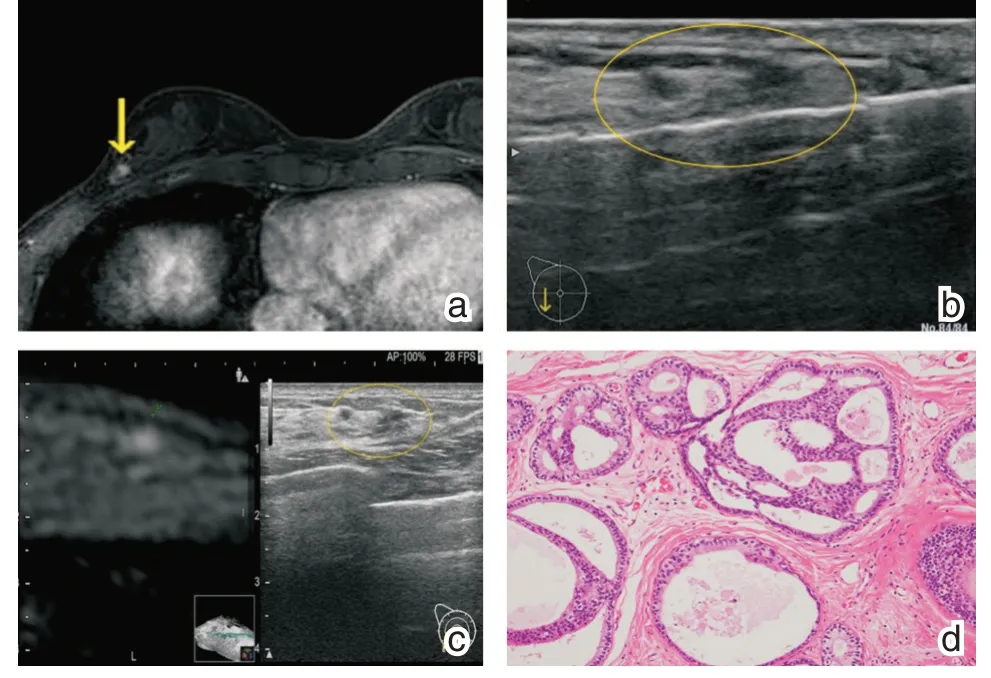
图2 患者57,左乳房增生性纤维囊性变[15] a 增强MRI 显示右乳房有局灶性非肿块强化(箭头);b 在MRI/US 融合图像上识别出MRI 检测到的病变;c 超声引导下进行活检;d 活检标本显示低度恶性导管原位癌
1.3 钼靶和核磁共振联合诊断
钼靶检查能很好的观察到乳腺细小钙化灶以及淋巴结转移的情况,但同时也容易受到腺体密度和肿块位置的影响。而核磁共振对细小钙化灶显影不敏感,但其不受腺体密度和体位以及肿块位置的影响,软组织分辨率高,能显示清楚乳腺肿块血流情况,病变的定位更准确[16]。因此钼靶和核磁共振能很好的形成优势互补,联合诊断能使得检出率得到提高。
核磁共振和钼靶的联合诊断在早期乳腺癌患者中的诊断准确率高于核磁共振和钼靶的单独检查[6]。联合这两项技术在诊断早期乳腺癌应用价值高。
雷焦等[17]检索2005~2015年有关比较核磁共振和钼靶对乳腺癌诊断的研究,纳入13 篇文献进行meta 分析得出,核磁共振、钼靶和核磁共振+钼靶各自的敏感性分别为69%、87%、94%,特异性分别为81%、84%、81%,AUC 分别为80.61%、93.12%、96.11%。得出结论:核磁共振、钼靶对乳腺癌有较高诊断价值,两者联合诊断可以提高诊断正确率。该Meta 分析结果提示核磁共振和钼靶的联合在乳腺癌的诊断中敏感性是最高的,但因其特异性不高,仍具有一定的假阳性。核磁共振的敏感性和特异性比钼靶高,这与其对乳腺软组织分辨率高有一定的相关性。
中国女性乳腺相比西方女性体积较小,脂肪含量较低,这些特征给超声检查提供了有利的条件。超声检查在鉴别囊实性病变、病灶定性诊断方面具有重要价值。核磁共振在乳腺癌筛查、乳腺疾病鉴别诊断、术前分期、疗效评估等方面均具有重要的意义。钼靶摄影在检测乳腺钙化方面有着无可替代的价值。综上,单一影像技术存在一定的局限性,多影像技术联合诊断能大大提高诊断的敏感性、特异性,对诊断正确率也有可观的提升。超声、钼靶、核磁共振联合诊断,能够实现信息的交叉互补及相互验证,同时获得机体多方面信息从而提高诊断效率。
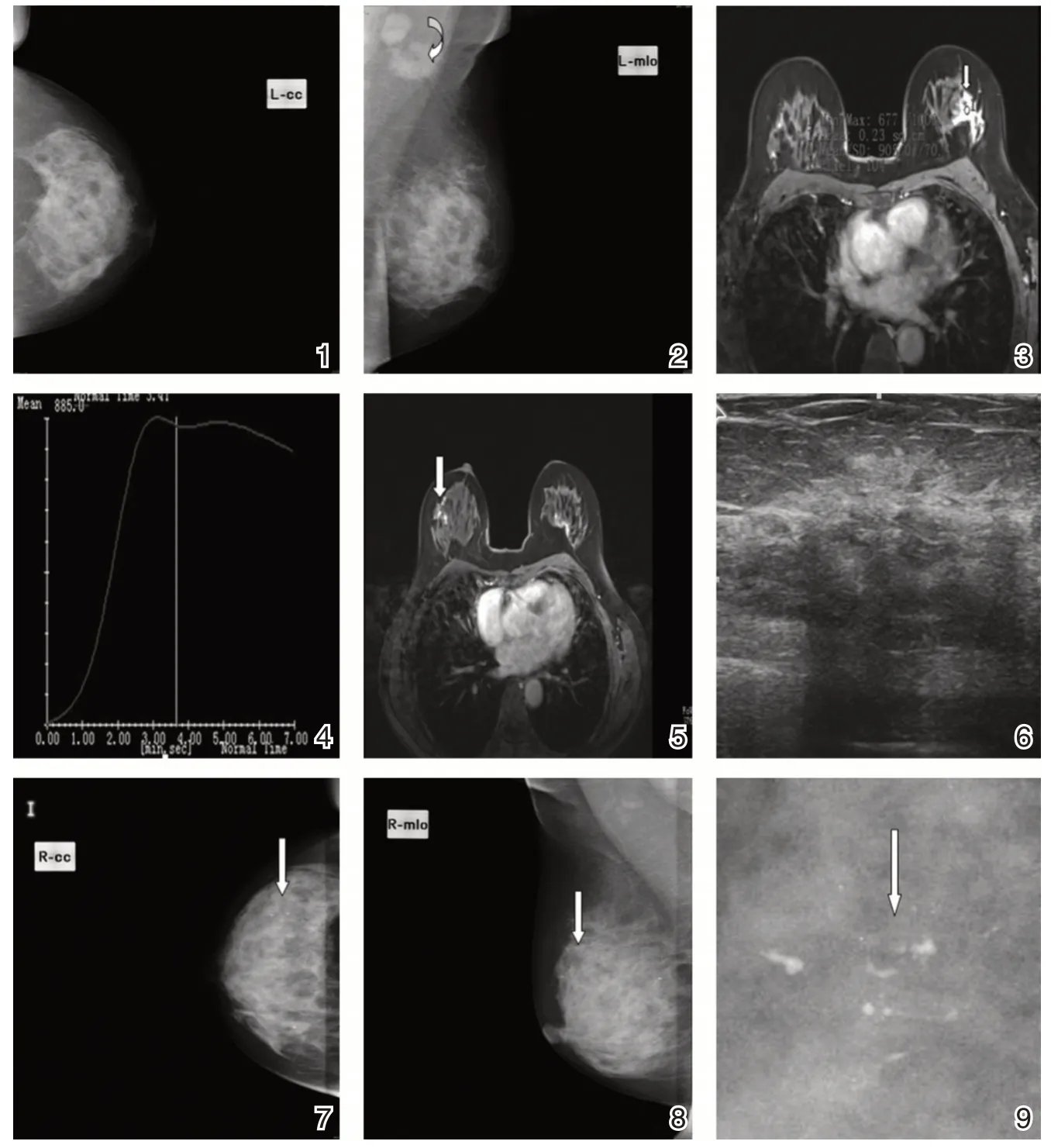
图3 [18] 患者52 岁,女性,右乳房为DCIS,左乳房为IDC 左乳ACR 密度为3 级的头尾①和内侧斜②片,除腋窝淋巴结肿大(弯曲箭头)外,均未见肿块或异常钙化;轴位T1 加权增强MRI③显示左乳房有不规则形状的肿块,呈3 型动态增强④,恶性嫌疑大(BI-RADS5 级);MRI 轴位T1WI 增强扫描可见右乳房点状强化,但未见肿块⑤,故MRI 诊断为BI-RADS 1 级。超声未见异常发现⑥;右乳头尾⑦、内侧斜⑧及其斑点扩大⑨X 线片示多形性钙化簇状(直箭头)。钼靶诊断为BI-RADS 4c 类
2 多模态乳腺肿瘤图像特征提取
计算机辅助诊断(computer aided diagnosis,CAD)是1966年首次被Ledley 所提出[19]。通过医学影像学、图像处理技术以及其他方法对医学图像进行分析诊断,即为CAD。其前期主要包括图像的收集、预先处理、感兴趣区域(region of interest)的分割、特征提取和分类识别等,之后再进行计算机相关程序分析,辅助发现病灶,提高诊断的准确性[19]。2010年Gillies 等[20]提出了影像组学的概念,2012年Lambin等对其进一步进行了完善[21]。他们使用计算机相关处理方法从核磁、超声、钼靶影像中通过自动高通量提取大量(通常超过200 多幅)医学图像的定量特征来改善图像分析,通过给定成像方式的自动或半自动软件对医学图像进行数据的定量分析,从而进一步获取图像相关联的诊断、分级、治疗等方面信息。最后通过定量分析医学影像所包含的数据信息,从而对病灶进行相关的疾病诊断、分级、治疗等评估。
近年来,随着医疗设备(硬件)的创新、成像剂的创新和影像分析的创新,使得人工智能在诊断乳腺癌的应用中有了很大的进展。要从超声、MRI、钼靶等图像中提取特征,首要条件是获取高质量标准化的影像图像。要获得高质量的分析结果,第一步是对医学图像进行感兴趣区识别,即在影像图像中找到肿瘤或可疑肿瘤的相关区域。下一步为图像分割,将进一步缩小相关区域范围,使用自动、半自动或人工手动的方法确定感兴趣区域的大致轮廓;其中图像分割是提取特征的关键,直接影响所得图像的准确性。目前后两种方法(即半自动或手动方式确定图像区域的方式)应用较多,并且当前仍无理想的分割方法。其主要原因是在核磁钼靶超声等检查获取的图像中,许多肿瘤的边界是不清楚的,实际进行图像分割时分割结果的重现性不好,而且暂时没有检验论证分割结果是否准确的统一标准。当下,图像分割操作中使用较多的方法仍是先由计算机辅助确定感兴趣区域的大致轮廓,然后再由有经验的影像医师分割出精确的病灶边缘[22],最后通过计算机算法从所选择的感兴趣区中提取相关影像学特征,这些特征包括统计学特征、形态学特征、区域特征以及基于模型特征等4 类[23]。将医学影像中肉眼难以观察到但实际存在的病变信息转化为相关的量化数据,从所提取的大量图像病变特征中进一步去除多余信息,最终构建一个准确可靠的影像组学模型。所以提取乳腺图像肿瘤最典型的判别特征,是一套乳腺肿瘤诊断影像系统实现高诊断精度的保障。因此,研发高效准确的诊断系统最关键的一步就是进行特征提取。
医学图像的分割方法包括图像切割法、水平设置法、半自动分割法、区域增长法、动态轮廓(蛇形)算法、livewires 法和基于容量CT的分割法等[24]。
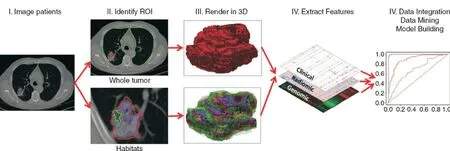
图4 [22] 流程图显示了放射组学的过程和放射组学在决策支持中的使用 患者检查需要将来自不同来源的信息组合成一个连
特征提取方法主要基于统计学的特征、滤波特征和形态特征三大类。此外,还有基于灰度尺寸区域矩阵的特征,Minkowski 函数以及其他方法[25]。关于病灶特征提取,Melendez 等[26]提出了2 种方法,第一种是通过相邻的区域再现功能最大值,以达到特征最大化;第二种方法是局部特征选择,即在图像分割选定区域中结合病变位置进行相关联的不同特征选择。这2 种方法可以联合或者单独使用,当2 种方法同时应用时可获得最好的结果,平均每幅图像的假阳性数为1 时,敏感度从0.628提高到0.734。在其中一篇文献中,谢轶峰对乳腺肿瘤的肿瘤的几何特征、乳腺的纹理特征、肿瘤后回声特征等几个重要特征,作了简单的描述,根据Stavros 标准,提出了运用支持向量机SVM 来对提取的影像特征进行良性肿瘤和恶性肿瘤的判定分类。以此研制出的计算机图像辅助诊断系统,可以使乳腺肿瘤的诊断更加可靠,因为其一定程度上避免人为的主观因素导致的误差。文献[27]根据Stavros 标准,用常规超声成像诊断仪器所获取的乳腺图像肿瘤特征,主要包括以下5 种:乳腺图像纹理、边缘锋锐程度、肿瘤几何形状、声波回声特性和肿瘤图像亮度特征;其中肿瘤图像亮度特征和声波回声特性是使用新的超声弹性成像技术才能检测到的特征,它主要能反映肿瘤的钙化特性,以及外界压力而改变是否影响肿瘤形状[27]。在Liwen Zhang 等[21]的研究中,高维影像学特征被提取来描述肿瘤表征类型。在该研究中,特征分为四组:临床认知特征、图像强度特征、纹理特征和小波特征。第一组的主要目的是描述肿瘤表型,例如圆度和毛刺的形状,面积,体积和紧密度;第二组描述了灰色直方图的肿瘤区域和体素的灰色分布;第三组揭示了肿瘤内结构的同质性或异质性;最后一组通过解析原始图像来获取图像强度和纹理。
一套完善可用乳腺癌诊断和分级建议的工具,需要计算模型的设计与高级机器学习算法开发,而乳腺肿瘤特征提取则是这些模型与算法建立的根本。目前因为影像组学研究方法存在较大差异并缺少结果验证标准,所以尚无关于乳腺肿瘤特定影像特征提取分析的文献报道。通过从不同影像学检查所获得的多个图像的组合数据,相关的机器学习技术也在飞快发展。总之,随着影像学领域的成熟,最终有望能开发出基于人工智能的乳腺肿瘤影像自动诊断系统。
3 总 结
影像学检查是一种非侵入性医学成像方式,它具有以非侵入性方式捕获肿瘤内异质性的能力。利用影像学的多模态图像,同时设计一套标准化的图像特征提取和诊断系统便可进行定性分析。这是一个基于人工智能技术的乳腺肿瘤诊断自动化软件所需的关键步骤。综上所述,影像学的联合诊断能帮助临床医生提高整体诊断效率,降低漏诊误诊率。预计到2040年,乳腺癌发病率将增加2 倍[28]。随着人口老龄化、乳腺癌或肿瘤的低龄化,及我国筛查普及等各种因素,研发一套准确而高效的乳腺肿瘤自动诊断系统研究具有重要临床应用价值。

