TiO2改性的Co-Mo耐硫变换脱氧催化剂常压性能研究
孙倩,张新堂,赵国明,刘珊珊,尹爽,刘营春
(山东科技大学 化学与生物工程学院,山东 青岛 266590)

TiO2属于一种典型的强金属-载体相互作用类型的载体[4-5],并在光催化领域得到了一定的应用[6-8],但是直接用作催化剂载体具有一定的局限性[9]。本实验选择加入TiO2作为镁铝尖晶石载体改性剂,充分利用镁铝尖晶石和TiO2两种载体的优点,探究对催化剂性能的影响。
1 实验部分
1.1 材料与仪器
AlOOH·nH2O、MgO、TiO(OH)2、C6H8O7·H2O、Co(NO3)2·6H2O、Ni(NO3)2·6H2O、Ce(NO3)3·6H2O、Fe(NO3)3·9H2O、氨水、C2H8N2、(NH4)6·Mo7O24·H2O、K2CO3均为分析纯;田菁粉,工业级。
DJ-40型单螺杆挤条机;101-1型鼓风干燥箱;SX24-10型马弗炉;常压微反装置,自制;DLIII-500智能颗粒强度测定仪;麦克ASAP2460比表面积测定仪;Rigaku Utima IV型X射线衍射仪;SP6800A气相色谱仪。
1.2 耐硫变换脱氧催化剂的制备
将一定量的拟薄水铝石、MgO、偏钛酸混合,配以一定比例的造孔剂、助挤剂混捏挤成条状,经100 ℃干燥24 h、550 ℃焙烧3 h得到载体。其中Al2O3/MgO摩尔比为1∶1,制备一系列不同TiO2含量的载体。将硝酸钴、钼酸铵、碳酸钾、硝酸镍配制成浸渍液,浸渍于载体,100 ℃干燥24 h,500 ℃焙烧3 h制得成品耐硫变换脱氧催化剂。
1.3 强度稳定性测试
随机抽取20 g试样,用颗粒强度测试仪测试不同TiO2含量载体的径向破碎强度。并考察载体经过水煮处理和水热处理后,强度的变化。
1.4 BET分析
将所需样品研磨至无明显颗粒感,预处理样品抽真空4 h,BJH分析模版进行分析测试。
1.5 XRD表征
采用X射线衍射仪对催化剂进行晶相结构测定。工作电压40 kV,工作电流100 mA,波长λ=0.154 06 nm,对样品在 2θ为 10~80 °范围进行扫描,扫描步长为0.02(°)/s,扫描速率为 8(°)/min。
1.6 O2/CO含量分析方法
使用气相色谱仪对原料气及尾气中的O2、CO含量进行分析,5A分子筛填充柱检测产物中的O2、CO,氦气作为载气,采用热导池检测,外标法进行定量分析。色谱条件:柱箱温度为45 ℃,汽化室温度为100 ℃,检测器温度为100 ℃,桥流100 mA,衰减1。
1.7 评价装置及方法
在常压微反装置上进行催化剂硫化及活性评价,以脱氧前后气体中O2、CO含量的变化来评价脱氧/变换活性的好坏。
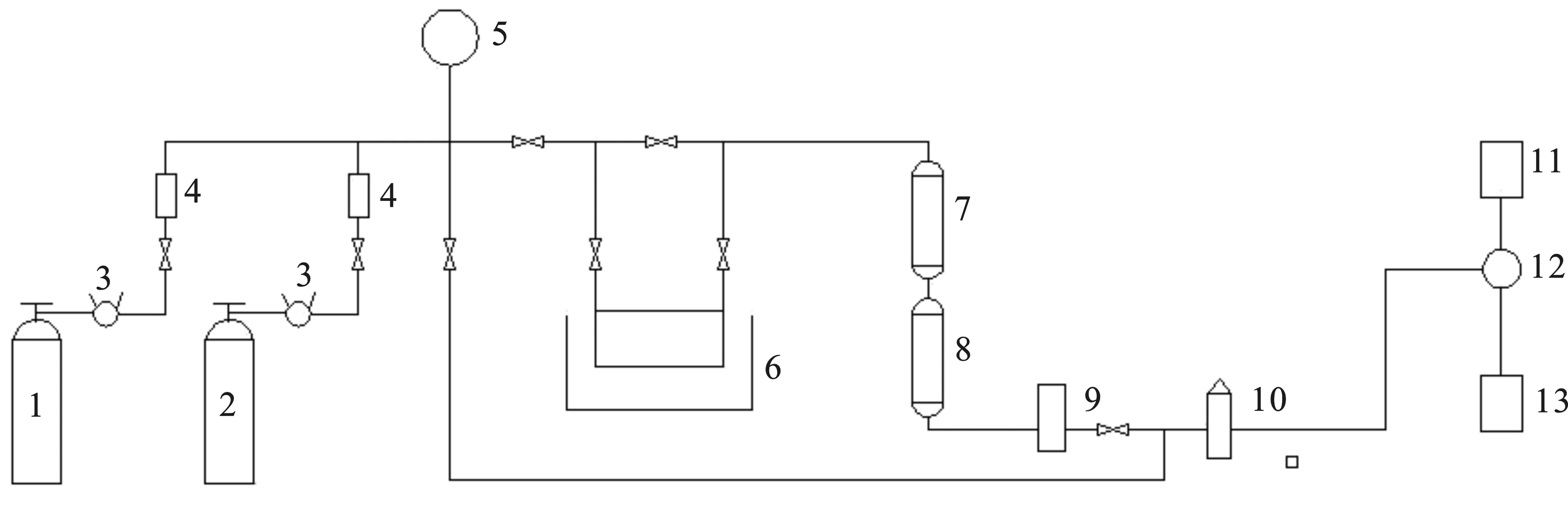
图1 催化剂产品评价装置流程图Fig.1 Flow chart of catalyst product evaluation device1.原料气钢瓶;2.高纯氮气钢瓶;3.稳压阀;4.转子流量计;5.压力表;6.水浴饱和器;7.微反装置预热器;8.微反装置反应器;9.冷凝器;10.气体干燥塔;11.气相色谱分析系统;12.采样六通阀;13.气体放空
常压脱氧剂评价条件:脱氧剂装填量1 mL,空速3 000 h-1;原料气组成:CO 45%,O20.5%,H2S 0.5%,其余为H2;硫化温度280 ℃,硫化时间2 h,在210,230,250,270,290 ℃五个温度下测定催化剂活性,先对干气反应(水气比:0)进行讨论,最后与湿气反应(水汽比:0.88)对比。脱氧率(%)和CO变换率(%)的计算公式如下:
(1)
(2)
其中,XO2为O2转化率;XCO为CO变化率;yO2·in为反应前原料气中O2百分含量;yO2·out为反应后尾气中O2百分含量;yCO·in为反应前原料气的CO百分含量;yCO·out为反应后尾气中的CO百分含量。
2 结果与讨论
2.1 Ti对载体强度及吸水率的影响
考察了改性剂TiO2添加量对镁铝尖晶石载体及其水煮处理和水热处理后强度和吸水率的变化,结果见表1。

表1 不同TiO2含量的载体强度及吸水率Table 1 Support strength and water absorption of different TiO2 content
由表1可知,当TiO2含量为20%时,载体吸水率呈现出最大值,载体中加入少量的TiO2强度明显下降,随着TiO2含量的增加,载体的强度呈先上升后下降至趋于平稳,当达15%时,强度值出现最大值。当TiO2含量为75%时强度又突然增大,这是因为此载体主要相转变为Ti的晶型,尖晶石结构发生变化时,强度突然增大。在水热水煮处理过程中,载体物相发生变化,强度均得到明显的提升。
2.2 载体XRD表征
对含有15%TiO2的载体在不同温度下(450~850 ℃)焙烧处理后进行XRD表征,结果见图2。
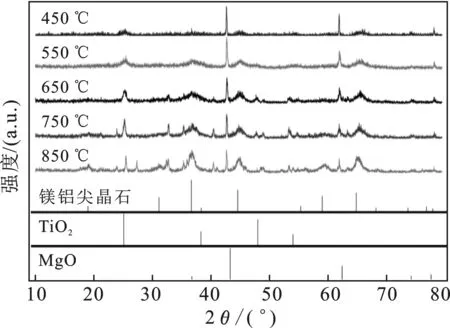
图2 不同焙烧温度的催化剂载体XRD图(含15%TiO2)Fig.2 XRD patterns of catalyst support at different calcination temperatures(containing 15% TiO2)
通过与标准物的XRD图对比分析,随着焙烧温度的增大,镁铝尖晶石峰越来越多,且峰强度越来越大,说明高温条件下有利于镁铝尖晶石的生成。其中2θ为43.5,62.8,78.1 °处出现衍射峰归属于MgO,随着焙烧温度不断增大,MgO衍射峰峰强度逐渐减弱,这说明温度升高使得游离态的MgO减少,从而促进镁铝尖晶石的形成,且25.2,54.3 °处的TiO2衍射峰也峰逐渐增强,谱线变得尖锐,TiO2的结晶度增加,物相趋于一相。
2.3 载体BET测试
对2.2节中不同温度焙烧后的载体进行BET测试,结果见表2。
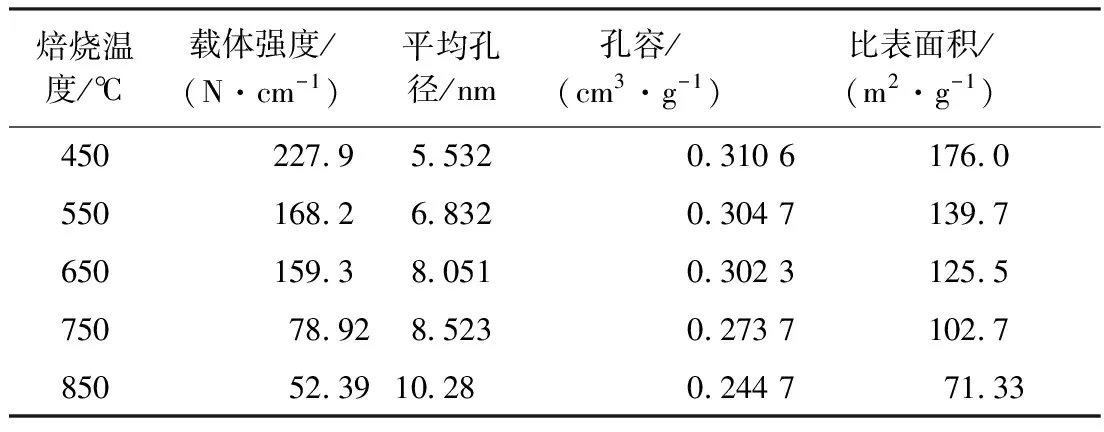
表2 不同焙烧温度对载体强度及孔分布的影响Table 2 Effect of different firing temperatures on the strength and pore distribution of the support
由表2可知,随着焙烧温度的增大,载体强度呈下降趋势,比表面积和孔容减小,平均孔径增大。450~750 ℃焙烧时,平均孔径<10 nm,以小孔为主。在焙烧的过程中,TiO2-Al2O3-MgO三元复合物颗粒表面发生粘结、表面扩散和晶格扩散,使粒子变大,比表面积和孔容随着焙烧温度的升高而减小,高温焙烧使得孔壁崩塌[10],一些小的孔径逐渐消失,形成了更大的孔径,呈现出小孔所占的比例逐渐减少,大孔比例呈增长的趋势。这种三元复合型载体既保证了镁铝尖晶石载体高强度、热稳定性好、大比表面积和适宜的孔径分布特点,又具有TiO2结构稳定性。
2.4 Ti对催化剂脱氧性能的影响
在2.1节的载体上分别浸渍相同活性组分,进行脱氧实验,结果见图3。

图3 TiO2含量对催化剂脱氧活性的影响Fig.3 Effect of TiO2 content on catalyst deoxidation activity
由图3可知,加入TiO2对催化剂的脱氧活性有明显的促进作用,当TiO2含量为15%时,脱氧活性呈现出最大值64.75%,随着TiO2含量的继续增加,脱氧活性下降至58%呈稳定趋势。TiO2作为一种载体改性剂,可促进Mo还原成具有活性的低价Mo5+[11]。TiO2具有很强的Lewis酸性,当MoS2负载于TiO2改性的载体上,催化剂中MoS2的堆积层数和晶粒长度均趋于很小的范围,催化剂表面的晶格缺陷或活性组分的结构都可能发生变化,从而影响催化剂的脱氧性能[12-13]。TiO2促使MoO3在镁铝尖晶石表面分散,使MoO3在经TiO2调变的复合载体TiO2-Al2O3-MgO上的分散阈值较镁铝尖晶石表面上大,而且TiO2的存在还有利于MoO3的深度还原,使活性组分Mo的还原态显示出较高的催化活性[14]。综合催化剂载体强度、吸水率及脱氧性能测试结果得出,当TiO2含量为15%时,脱氧率最高。
2.5 不同TiO2含量催化剂的XRD表征
对具有不同含量TiO2的镁铝尖晶石催化剂进行XRD表征分析,结果见图4。

图4 不同TiO2含量催化剂XRD图Fig.4 XRD patterns of different TiO2 content catalysts
由图4可知,发现42.9,62,78.3 °处均出现NiTi峰,43.1,62.1,78.6 °处出现CoTi衍射峰,这些衍射峰强度随着TiO2含量的增加而减弱,镁铝尖晶石峰强度基本不受TiO2含量的影响。催化剂中均未观察到明显的Mo、K的衍射峰,由此得出催化剂活性组分在载体中未发生团聚,较为分散,且TiO2含量对催化剂物相的形成有一定影响。
2.6 Ce、Fe、Ni对催化剂活性的影响
此脱氧催化剂以Mo作为主要活性组分,Co在此催化剂体系中必不可少,当Co和Mo同时存在时,Co2+可以抑制Mo6+物种过度还原,促进“oxysulfo-Mo5+”相的生成,其中MoS2纳米层和位于其边缘的Co2+构成活性相Co-Mo-S,对脱氧反应起到活化促进作用,所以Co-Mo同时存在产生的协同作用更有利于脱氧过程进行[15]。
据专利CN201510316306.2报道[16],添加Ce、Fe、Ni为活性助剂对脱氧活性有影响,研究了在Co-Mo-K的基础上添加Ce、Fe、Ni助剂对催化剂脱氧活性的影响,结果见表3。

表3 添加Fe、Ce、Ni对催化剂脱氧活性的影响Table 3 Effect of Fe,Ce,Ni addition on catalyst deoxidation activity
由表3可知,添加Ce、Fe在低温条件下均有助于提高脱氧活性,且Ce的作用强于Fe,加入Ni的催化剂活性最高,脱氧率可达57.44%。210 ℃时,Fe对催化剂的脱氧性能具有促进作用且脱氧率较高,此状态下的催化剂处于刚硫化完状态,硫化形态较好,表现出的活性较高,随着反应温度的升高,Fe的加入反而减弱脱氧性能。氧气存在时,硫化铁在100~400 ℃之间处于加速氧化期,硫化铁表面的活性中心吸附氧气分子,表面氧气浓度迅速增加,使硫化铁向深度氧化阶段进行,催化剂活性中心减少,温度越高,催化剂脱氧活性越低[17-18]。综上,Ni在提高催化剂脱氧活性方面较为优势。
2.7 助剂Ni对催化剂活性的影响
常压下,考察了NiO含量对催化剂活性的影响,结果见图5。


图5 不同Ni含量对催化剂活性的影响Fig.5 Effect of different Ni content on catalyst activitya.脱氧活性;b.变换活性
由图5可知,加入Ni对催化剂的脱氧活性有促进作用,当NiO含量达到0.2%时,各个温度点催化剂均表现出较高的脱氧活性;当NiO含量超过0.2%时,各温度点催化剂脱氧活性均降低。这是因为当加入少量NiO时,对载体中镁铝尖晶石的覆盖削弱了活性组分Mo和镁铝尖晶石的相互作用,增大了Mo的浓度,协同TiO2的相互作用更加促进Mo的分散,使结构发生变化,有利于H2和O2的反应[19],且由2.2节中催化剂载体XRD表征结果得出,载体中存在少量MgO,MgO可提高NiO的分散度[20],从而提高催化剂活性。当继续增大NiO的含量时,负载的NiO会在载体表面发生聚集,从而弱化部分镍相与载体之间的相互作用,导致催化剂脱氧活性降低[21]。催化剂均具有变换活性,随着温度的升高,变换活性不断增大,加入Ni的变换活性略微有所提高。
由表4加NiO和不加NiO的BET测试结果表明,NiO对催化剂样品的比表面积和孔分布影响不大,Ni不是通过改变催化剂的几何结构而提高催化剂活性的。

表4 加Ni和不加Ni催化剂的物性比较Table 4 Comparison of physical properties with and without Ni catalyst
2.8 K对催化剂脱氧活性的影响
据文献报道Co-Mo系催化剂中添加碱金属可以会促使Mo5+更稳定的存在,有效提高催化活性[22-23]。以K2CO3作为K源,对不同含量的K2O对催化剂活性的影响进行研究,实验结果见图6。


图6 不同K含量对催化剂活性的影响Fig.6 Effect of different K content on catalyst activitya.脱氧活性;b.变换活性
由图6可知,加入K对催化剂的脱氧活性有明显的促进作用,且当反应温度为270 ℃时,催化剂脱氧活性最高。K2O含量到达9%时,脱氧活性表现出最大值。继续增加K2O的含量,催化剂脱氧活性明显降低,且K2O含量在9%时,催化剂变换活性最高,变换活性随着温度的升高而增大。纵秋云等[24]研究发现,K含量对Co-Mo系催化剂的孔分布和比表面积影响不大,所以K并不是通过改变催化剂的几何因素促进催化剂脱氧活性升高。K同时促使Mo转向低价态,活性中心Mo(V)数量增加,活化态的氧分子、氢分子和活性组分Mo之间的电子转移加快,从而加速脱氧反应的进行,有利于气体的吸附脱附[25]。同时K与TiO2在影响催化剂脱氧活性方面具有协同作用,提高催化剂的“捕硫”能力,增加催化剂表面硫浓度,降低失硫速率,能够保持较高的耐硫脱氧活性。但K2O含量过高,易使脱氧剂活性中心覆盖过剩的游离态的K,从而活性中心减少,达不到真正的脱氧目的。
3 硫化及工艺条件对催化剂活性的影响
3.1 干湿气硫化对催化剂活性的影响
干湿气硫化会对催化剂活性产生影响。由图7可知,干气硫化后的催化剂无论是脱氧活性还是变换活性均高于湿气硫化的催化剂,说明在原料气中配入水蒸气影响催化剂的硫化程度,降低催化剂活性。当反应温度低于250 ℃时,湿法硫化的催化剂脱氧率呈下降趋势,随后又升高,说明湿法硫化后的催化剂不稳定。水能够加速催化剂中K流失速率和反硫化反应,同时还可以加速催化剂中小颗粒融结和长大,催化剂中的Co-Mo-S活性相和“缺陷”面积急剧减少[26],导致硫化效果低。

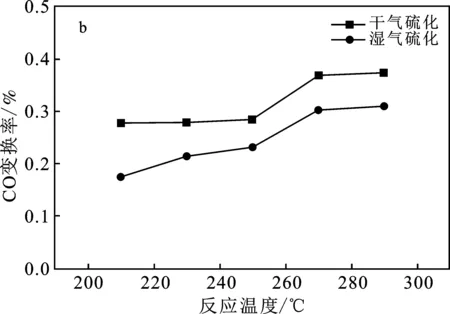
图7 干湿气硫化对催化剂活性的影响Fig.7 Effect of dry and wet gas sulfuration on catalyst activitya.脱氧活性;b.变换活性
3.2 硫化时间对催化剂活性的影响
硫化时间对催化剂活性产生影响见图8。
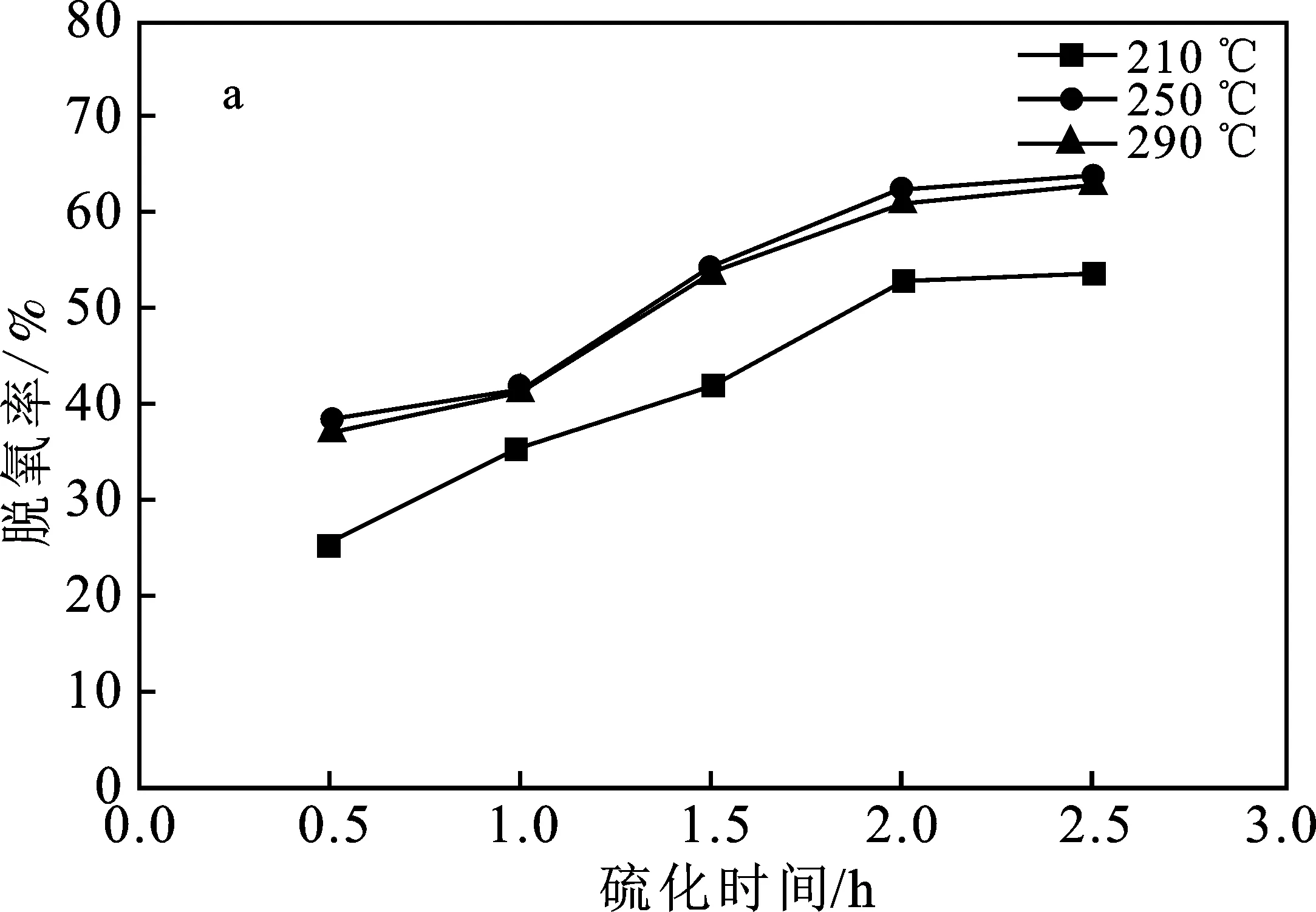
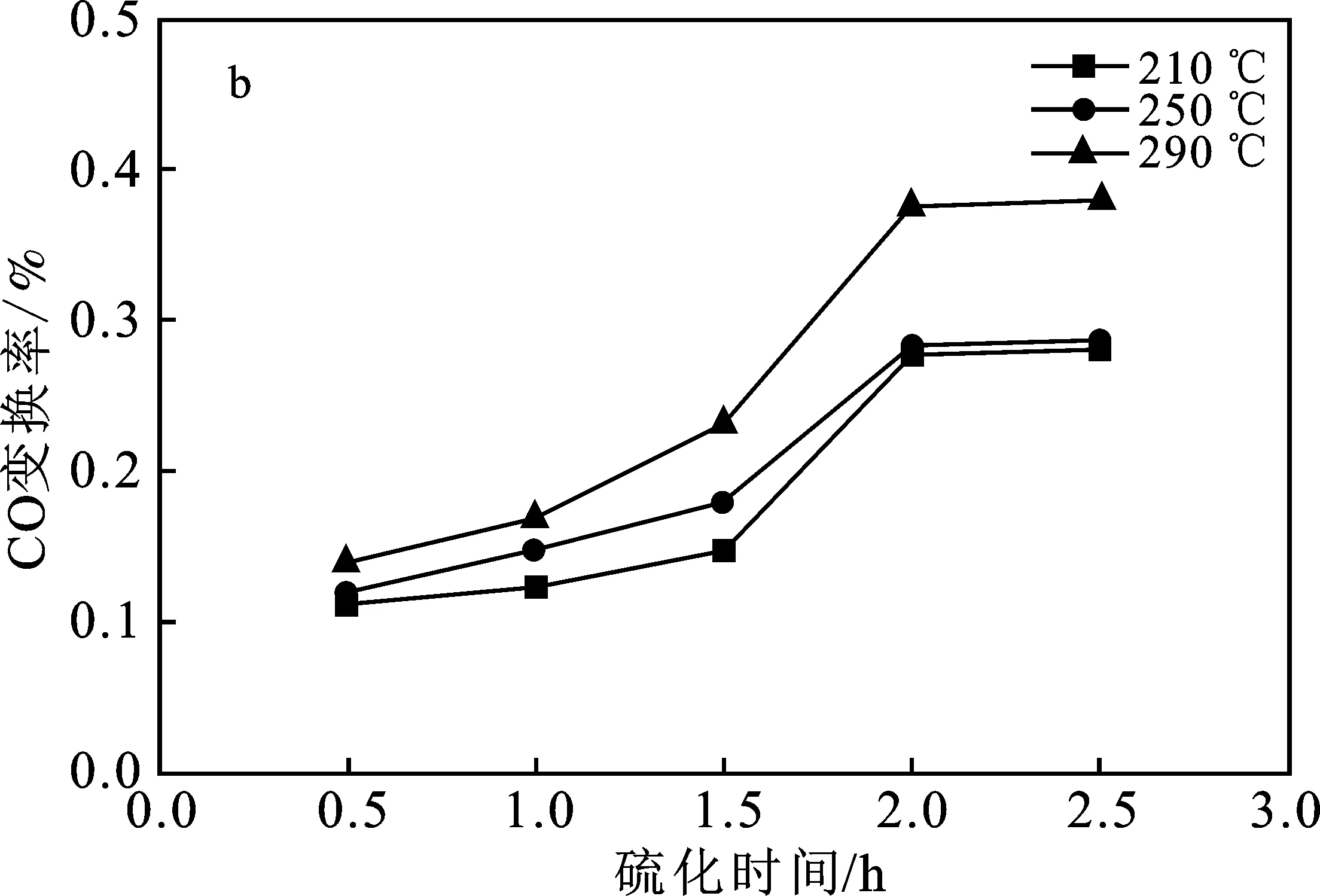
图8 硫化时间对催化剂活性的影响Fig.8 Effect of vulcanization time on catalyst activitya.脱氧活性;b.变换活性
由图8可知,随着硫化时间的延长,催化剂的脱氧、变换活性均呈递增趋势。当硫化时间低于2 h时,催化剂的脱氧、变换活性提升较快,到达2 h后,延长硫化时间催化剂的脱氧率、变换率趋于平缓。这是因为硫化时间越短导致氧化态的催化剂硫化不充分,生成的硫化态活性中心不足。随着硫化时间的延长,催化剂硫化度增加,每个温度条件下都存在一个平衡值,当达到此平衡值后,硫化时间延长,硫化度不会再提高,催化剂活性趋于稳定[27]。
3.3 反应空速对催化剂活性的影响



图9 空速对催化剂活性的影响Fig.9 Effect of space velocity on catalyst activitya.脱氧活性;b.变换活性
由图9可知,在空速低于5 000 h-1时,提高空速,催化剂的脱氧活性增大。在此范围内提高空速有助于扩散阻力的消除,从而提高脱氧活性。但是提高空速的同时,催化剂的变换活性下降,这是因为提高空速,催化剂床层中反应气的停留时间变短,并且本实验只使用了1 mL的催化剂,在反应器中能转化的CO气体随着空速的增加减少,导致催化剂变换活性降低。
3.4 干湿气反应活性对比

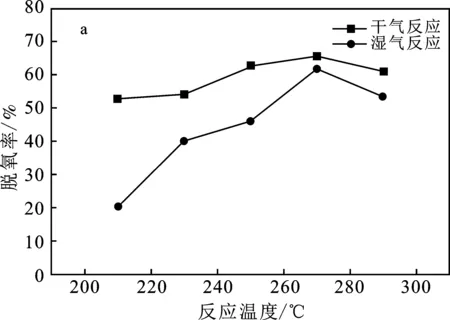
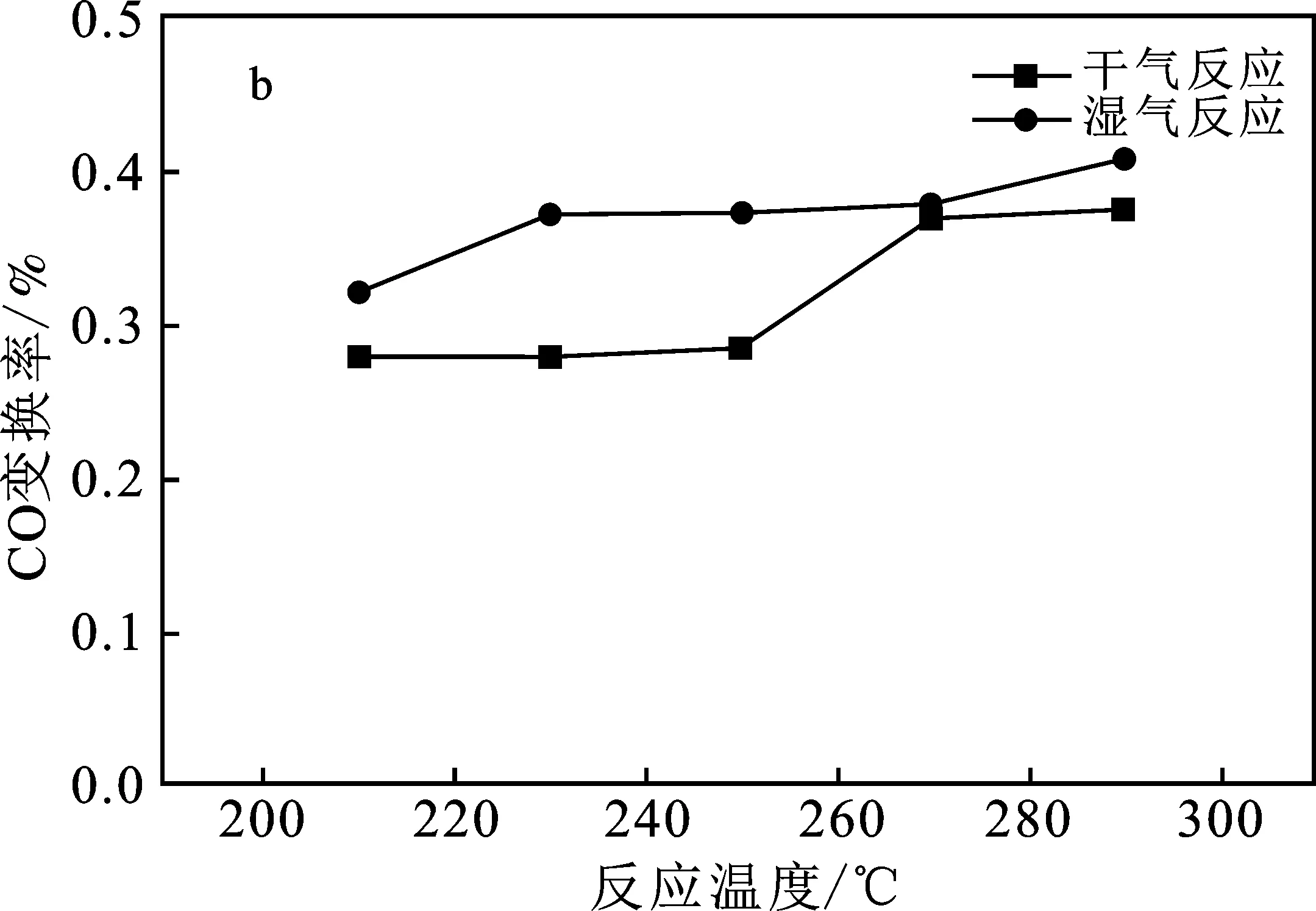
图10 干湿气反应对催化剂活性的影响Fig.10 Effect of dry and wet reaction on catalyst activitya.脱氧活性;b.变换活性
3.5 催化剂热稳定性探究
正常测试不同温度下催化剂的脱氧活性之后,切断原料气,通入高纯氮气,提升反应器温度至500 ℃,在此条件下热冲击5 h。再将催化剂重新硫化,测试不同温度下的催化剂活性,结果见图11。

图11 催化剂热稳定性比较Fig.11 Comparison of catalyst thermal stability
由图11可知,催化剂经长时间热冲击后,脱氧活性变化不大,说明此催化剂具有较好的热稳定性。
4 结论
(1)载体加Ti改性有助于提升催化剂脱氧活性,当含量在15%的时候,活性最高,载体强度稳定性最好。且Ti的加入影响载体的强度、吸水率和活性组分Mo的分布从而影响催化剂活性,且TiO2含量影响催化剂物相的形成。
(2)焙烧温度越高镁铝尖晶石晶型越多,TiO2晶型越稳定。
(3)对比Ce、Fe、Ni3种活性助剂对脱氧活性的影响,加入Ni的催化作用较好,其中NiO含量在0.2%时,能够保持较高的脱氧活性。
(4)助剂K的加入大大提高了脱氧活性,当 K2O 的含量在9%时,表现出较高脱氧活性和变换活性。
(5)硫化过程中使用干气比湿气硫化效果好,且经过2 h,催化剂硫化度达到稳定,在5 000 h-1空速以内,提高空速有助于脱氧活性提升,干气脱氧效果比湿气脱氧好,湿气条件有助于催化剂变换作用,催化剂具有较好的热稳定性。

