胰胆管汇合异常的诊治进展
刘宇虹,邓 刚,陈俊宗 综述 汤 地 审校
(中山大学附属第七医院普通外科,广东 深圳 518107)
胰胆管汇合异常 (pancreaticobiliary maljunction,PBM)是一种先天性畸形,表现为胰管和胆管在十二指肠壁外汇合。通常形成较长的共同通道,使Oddi括约肌失去对胰胆汇合部的正常约束作用,发生胰液与胆汁的单向或双向逆流,最终导致胆胰系统的一系列病理生理改变(见图1)。临床上一些不明原因或反复发作的胆道结石、急慢性胰腺炎、胆囊炎、梗阻性黄疸、胆囊穿孔等胆胰疾病,可能与PBM密切相关。此外,PBM还是胆道癌发生的高危因素[1]。
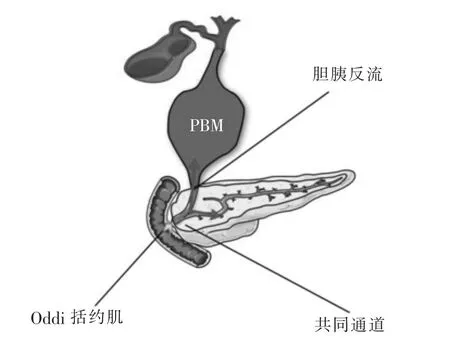
图1 PBM的病理生理学
1906年,首例PBM在欧洲报道。亚洲是PBM的高发地区,患病率比其他地区高100~1 000倍[1]。女性比男性易发生PBM,男女之比为 1∶3[2]。
有学者粗略统计了我国的PBM发病情况,25家医院近年报道了1 482例PBM病人。近年来,随着内镜技术以及影像学技术的发展,此病检出率有所上升,国内学者对PBM的研究愈发重视。本文归纳总结国内、外PBM诊断和治疗的研究进展。
胚胎学发生机制
PBM的发病机制仍有争议。尽管已报道一些家族性病例,但尚不清楚PBM是否为遗传性疾病。多数学者认为PBM的发生与胚胎时期的异常发育有关。正常妊娠第4周初,胚胎前肠腹侧形成固态肝憩室,其头部发育成肝脏和肝外胆道,尾部上芽发育成胆囊和胆囊管,下芽发育成左侧和右侧腹胰。第5周,肝憩室近端伸长形成胆总管(common bile duct,CBD),前肠背侧形成胰背芽。随着前肠旋转和十二指肠形成,腹侧胰芽和胆管绕十二指肠旋转180°,以连接背侧胰芽。第6周CBD再通,腹胰管连接CBD,并通过大乳头排入十二指肠。当腹背胰芽融合,其导管也在胰颈区域融合。背胰管近端通常退化,留下腹胰管,最终成为主胰管[3]。在此过程中,包括胚基发生、再通、旋转、退化等任一阶段发育异常,均有可能导致PBM发生。
分 类
形态学上将PBM分为胆管扩张型和胆管未扩张型。CBD直径通常与年龄密切相关。更多临床及影像医师主张根据年龄组的CBD直径进行诊断。
解剖学上根据胰胆管的不同汇合趋势分为3种类型,Ⅰ型为胰管型,CBD垂直汇入主胰管(B-P型);Ⅱ型为胆管型,主胰管呈锐角汇入CBD(P-B型);Ⅲ型为复杂型。
共同通道的扩张和副胰管的存在,可能与PBM病人并发复发性胰腺炎和胆道癌相关。Komi在解剖学分类的基础上进行细化,提出Komi分类:Ⅰ型、Ⅱ型(a和b两个亚型)、Ⅲ型(a、b和c三个亚型)。a型共同通道无扩张,b型共同通道有扩张,c型具有副胰管(即Santorini管)的复杂结构。
2015年,日本PBM研究小组 (Japanese Study Group on Pancreaticobiliary Maljunction,JSGPM)提出基于胰胆汇合部形成的 PBM分类[4],分为4种类型:①狭窄型,具有狭窄的远端CBD连接到共同通道;②非狭窄型,无狭窄的远端CBD连接到共同通道;③扩张管道型,共同通道扩张;④复杂型,胰胆汇合部形成复杂结构(见图2)。该分型是对Komi分型的概括和简化,为新Koni分型。2019年,Yoshimoto等[5]调查168例PBM成年病人新分型与临床特征的关系。结果表明,新的分类方法简单,并与临床特征有较好的相关性。
目前国内专家主张采用新Komi分型进行小儿PBM分类,并根据分型采取下一步治疗手段[6],而成人的分类标准尚未规范一致。
临床表现
不同的解剖学分型和年龄阶段PBM的临床表现不同,包括腹痛、呕吐、黄疸、发热、腹部包块和背部疼痛。
伴先天性胆道扩张PBM病人典型三联征是腹痛、黄疸和腹部包块。B-P型易出现黄疸和腹部包块,新生儿和婴儿多见。P-B型则主要表现为腹痛,儿童早期多见。不伴先天性胆道扩张的病人,很少在儿童时期出现症状,多于成人后出现反复发作的胆管炎或胰腺炎,主要表现为轻微、自限性复发性腹痛。此类病人常因症状轻微、确诊较晚而延误治疗,增加胆道肿瘤的风险。部分病人可能原发疾病症状轻微而主要以CBD结石、胆源性胰腺炎或胆道恶性肿瘤为主要临床表现。
诊 断
PBM诊断标准:通过内镜逆行胰胆管造影(endoscopic retrograde cholangio-pancreatography,ERCP)、经皮经肝胆道造影、术中胆道造影、磁共振胰胆管成像(magnetic resonance cholangiopancreatography,MRCP)等影像学检查,观察到胆胰系统以下任一现象即可诊断:①具有异常长的胰胆管合流的共同通道;②合流的形态异常。
关于胰胆共同通道长度异常的判定尚有争议。有学者指出,小儿>5 mm,成人>9 mm,可初步认为异常[7]。
一、影像学检查
(一)超声检查
普通超声检查作为非侵入性方式,主要用于PBM的筛查。超声检查可显示肝外或肝内胆管扩张,是筛查伴有先天性胆道扩张PBM的最佳方法。多中心研究确定超声测量人群肝外胆管的最大内径,肝外胆管的最大内径与年龄呈正相关,可根据该内径初步判定先天性胆道扩张。小儿CBD内径的上限为,<1岁 3.0 mm,5岁 3.9 mm,10岁 4.5 mm,15岁5.0 mm。 成人上限为,20~29岁 5.9 mm,30~39岁 6.3 mm,40~49岁 6.7 mm,50~59岁 7.2 mm,60~69岁 7.7 mm,70岁以上为8.5 mm[8]。在不伴先天性胆道扩张的PBM病例中,胰胆反流引起胆囊黏膜细胞增生可表现为胆囊壁增厚,提供诊断线索。但超声检查对CBD远端及共同通道的成像较差,不能独立诊断PBM。
(二)CT 检查
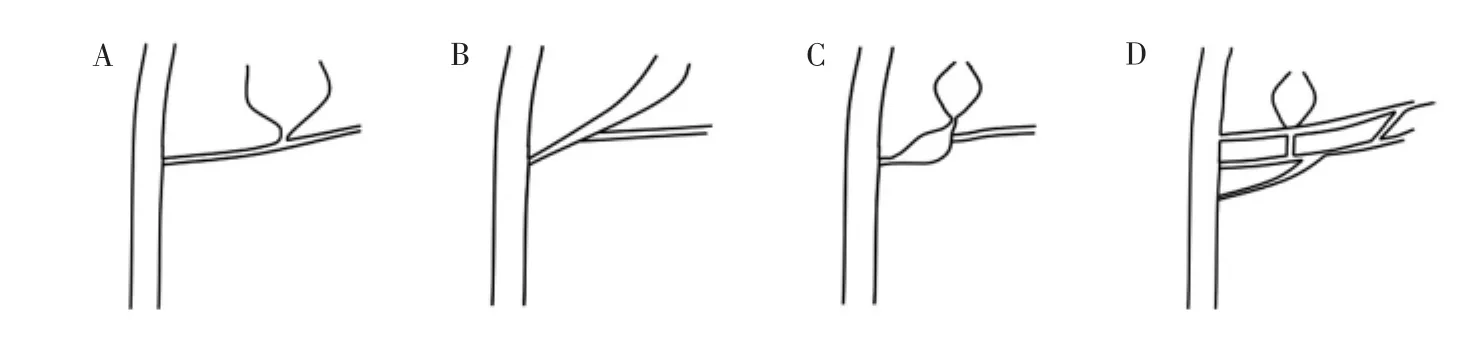
图2 JSGPM提出的PBM分类
多层螺旋高分辨率CT检查可提供胆胰系统多平面重建图像并显示胆胰汇合部。静脉滴注法CT胆系造影术可描绘胰胆管解剖结构的细节并测定胰胆反流,有助于诊断PBM。滴注胆道造影有一定侵入性,并有辐射及过敏风险,因此,目前仅作为PBM的二线诊断方式。此外,增强CT检查可见胆道肿瘤的不规则结节强化,在诊治和术后随访中对癌变的筛查和监测有一定价值。
(三)MRCP 检查
MRCP具有无创、无需注射造影剂且成像效果较好等优势,目前是PBM的首选检查方式。结构上,MRCP清晰显示胆管系统和胆胰汇合部的立体图像;功能上,促胰液素刺激的动态MRCP可用于可视化胰胆反流测定。但对于共同通道较短如婴幼儿的PBM显像,普通MRCP检查效果不及ERCP检查,并有运动伪影等图像质量缺点(见图3)。
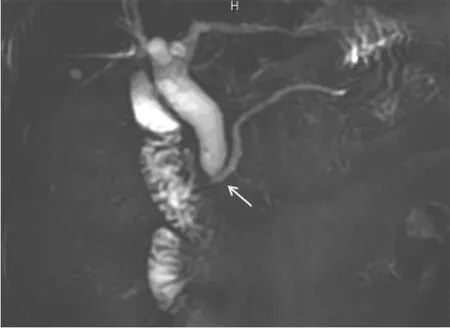
图3 PBM的MRCP表现
(四)ERCP 检查
ERCP是侵入检查方式,可清晰反映Oddi括约肌的结构与功能,并细致描绘胆胰汇合部的解剖学结构。此外,ERCP可同时进行诊断和治疗,在采集胆汁和组织取样的同时进行乳头括约肌切开、CBD取石、鼻胆管引流等治疗。但ERCP有一定的并发症发生风险,包括胰腺炎、胆道炎、出血和感染等[9]。对于PBM,一般不进行诊断性ERCP操作。若MRCP检查表现不典型,可考虑作ERCP。应权衡操作的难度以及并发症发生的风险。
(五)超声内镜检查
超声内镜检查也属于侵入性方式的一种,但其侵入性小于ERCP[10]。超声内镜检查不仅显示胆管系统,还可探及实质脏器的具体结构,具有较高的空间分辨率。超声内镜检查通过显示胆胰汇合部与十二指肠壁位置关系,可确诊PBM。此外,超声内镜检查也可用于PBM并发症以及胆道癌的诊断。超声内镜检查具有一定的应用前景,尤其是门诊检查,但对操作者的专业水平要求较高。
(六)术中胆道造影
术中胆道造影可直观了解胆道系统的解剖,尤其适用于判断胆道狭窄、结石、蛋白质栓塞,可指导手术。术中胆道造影结合术前MRCP检查可减少大型囊肿的图像遮挡,有利于切除PBM病人的胆总管近端狭窄[11]。
(七)三维重建虚拟胆道、胰管和肝血管显像技术
数字医学技术利用现代成像和计算机虚拟技术,可重建体内胆道、胰管和肝血管的立体仿真结构,有助于精准定位和个性化治疗。
各种影像学检查方法诊断PBM的效果比较见表1。
二、实验室检查
胆汁淀粉酶升高对PBM的诊断有辅助意义,特别是显著升高>1 000 U。儿童PBM病人常出现高胰淀粉酶血症。成年PBM病人在有症状时也可发生一过性血生化改变[17]。血生化检查胰淀粉酶同工酶升高有一定提示价值。
并发症
一、胆道穿孔
PBM是导致自发性胆道穿孔的主要原因。日本的调查显示,317例PBM患儿胆道穿孔的发生率达5.9%,共同通道扩张型PBM更高发(14.3%)[18]。胆道穿孔的可能病理机制包括胰液反流及胰酶破坏,蛋白质栓塞导致导管内压力升高以及炎症感染等[19]。发生穿孔的PBM病人,需立即行胆汁引流,稳定后考虑手术治疗。
二、高胰淀粉酶血症和胰腺炎
PBM病人易发生急性胰腺炎,但一般情况下多为轻度。儿童(30%)比成人(9%)更易发生[20]。由蛋白质栓塞引起的胆汁压力升高会引起胆管静脉回流,胆汁反流的淀粉酶通过胆汁静脉回流入血液,引发高胰淀粉酶血症。胆汁排入十二指肠受阻而反流至胰腺,可引起症状较明显的胰腺炎[21]。部分病人还会出现复发性胰腺炎,可能与胆胰汇合部及胰腺的复杂畸变有关[22]。
三、胆道结石
PBM与胆囊炎、胆石病关系密切。伴先天性胆道扩张的病人比不伴先天性胆道扩张的更易患胆道结石[23]。由于胰胆反流,胆汁中活化的胰酶可能会使卵磷脂分解出脂肪酸,结合胆汁中游离钙离子,产生脂肪酸钙结石。此外,Oddi括约肌功能不全、胆汁淤滞、肠液反流等也可导致结石发生。胆道结石不仅发生在术前,术后也可能产生,在复查和随访中应注意。
四、胆道癌变
关于PBM病人发生癌变的原因,有多种解释。经典的认为胰液胆汁持续反流,破坏胆道上皮,病理上发生“增生-不典型增生-癌”序贯变化。分子层面表现为细胞增殖激活因子(如COX-2)、突变型K-ras、细胞周期蛋白D1和P53等多种因子的异常表达[24]。研究显示,PBM病人发生胆道癌变的概率是无PBM人群的200多倍,其中伴胆管扩张病人的胆道癌变发生率为21.6%、无胆管扩张为 42.4%[25]。
治 疗
PBM与多种胆胰系统疾病存在因果关系,远期可合并胆道癌变,明确诊断后应及时手术治疗。术前先控制感染或黄疸。不能通过保守治疗控制的严重病人,可先行经皮或内镜胆道引流。PBM病人实施手术后,需终身随访。
一、手术方法
(一)PBM的手术方式
对于胆管扩张型PBM,目前胆囊切除术、肝外胆管切除术和肝管-空肠Roux-en-Y式重建术是标准的手术方式。术后也可能发生新的并发症,如吻合口狭窄、反流性胆管炎、肝内结石和胆管肿瘤等。原因可能是胆道密闭性被破坏、Oddi括约肌丧失功能、肠液反流入胆道、菌群移位等[26]。为减少术后并发症的发生,胆管切除近端应包括肝门相对狭窄的胆管,远端胰腺段部分应尽量贴近胆胰管汇合部上方[27]。
对于胆管未扩张型PBM,应行预防性胆囊切除,但对预防性肝外胆管切除存在争议。因此,长期随访和动态监测很有必要,一旦发生癌变等应手术治疗。
(二)腹腔镜治疗
对伴先天性胆道扩张的PBM,行完全切除和Roux-en-Y肝空肠吻合术,目前可通过腹腔镜进行。国外已有团队建立成熟的技术流程包括腹腔镜扩张胆管、远端CBD结扎、肝内胆管和共同通道蛋白质栓塞清除和定制Roux-en-Y环的长度。研究认为,通过规范的操作,腹腔镜胆管切除术和Roux-en-Y肝空肠吻合术是可行和安全的。与开放性手术相比,具有术后并发症发生率低和术中出血量少等优势[28]。

表1 不同影像学检查方法诊断PBM的效果比较[12-16]
(三)内镜治疗
近年来,介入内镜检查已被越来越多地用于治疗PBM。多用于胆道引流,包括胆管引流和胆囊引流,结石和蛋白质栓塞去除,胰周液和胆汁收集。即主要用于缓解临床症状及PBM并发症的治疗。
杨玉龙[26]提出,ERCP下乳头括约肌切开(endoscopic sphincterotomy,EST)缩短胆胰流出道可改善PBM的胰胆反流问题。通过EST分流胰胆管,调节流出道压力,可改善反流并促进排出。通过对53例病人的回顾性分析,该团队证实,对于低位胆胰管汇合异常或合流过长,此种方法具有一定效果,胆汁中淀粉酶明显下降,但对于胰胆管汇合位置过高则效果不明显[29]。相比于标准化手术方式,ERCP内镜技术具有创伤小、并发症发生少的特点,但其应用于PBM的治疗效果及适应证选择仍需进一步的长期临床研究证实。
二、术中并发症发生的预防和处理
(一)术中蛋白质栓塞
蛋白质栓塞大多在PBM治疗后自行消失。若因狭窄或栓塞过大、长期嵌顿导致病情复杂时,需在术前行引流或灌洗术。
(二)肝内胆管狭窄
先天性胆道扩张中胆管先天性狭窄并不罕见,是术后胆管炎、肝内结石和癌症发生的危险因素。值得注意的是,发现肝门处或肝内胆管狭窄时一定要在首次手术时彻底切除或重建胆管,以最大程度降低长期并发症的发生风险[30]。可选择的术式包括从肝总管切开端仔细探查并切除狭窄、广泛的肝门肝管空肠吻合术,以及当肝门狭窄过长或由于严重粘连而无法到达肝门时进行部分肝切除术。
(三)术中出血
PBM病人术前可并发胆道胰腺炎症,炎症刺激导致血管增生或囊壁黏连,在切除时易引发出血,需在术前控制炎症。此外,术中门静脉、肝动脉等大血管损伤则可能导致大出血,术前需借助影像学检查探明血管与囊肿的位置关系。
(四)胰管损伤
部分病例的胆管狭窄部分显示模糊,会增加术中胰管损伤的风险。可应用金属夹定位切除部位或行术中胆道造影指导手术。分支胰管损伤可不处理,主胰管损伤则需放置胰管支架。
(五)术后肝内胆管结石
肝内结石是PBM病人术后较多见的长期并发症之一。一旦发生肝内结石,可经皮肝穿内镜清除结石。
(六)残余胆管癌
标准术后残留的胆管癌变在长期随访后的报道逐渐增多。研究显示,胆囊切除术后病人0.7%~6.5%发生胆管癌[31]。首先需避免囊肿切除不足,其次胆肠吻合术本身是胆管癌的危险因素,即使将囊肿完全切除,也需长期随访[32]。
目前认为,PBM一旦诊断明确,需尽快手术,无论是否合并胆管扩张,都需手术。日本一项回顾性研究显示,512例诊断PBM且未胆管扩张的的病人胆管系统恶性肿瘤的发生率为42.2%,明确诊断为恶性肿瘤的病人中,胆囊癌占88.1%,因此,胆囊切除术可考虑作为预防性手术用以减少恶性肿瘤的发生,但对于是否行预防性肝外胆管切除术,存在许多争议[33]。Kusano等[34]研究发现,对于不伴胆管扩张的PBM,单纯行胆囊切除术,术后长期观察未发现胆管恶性肿瘤的发生。随着内镜技术的不断发展,国内、外对于PBM不伴胆管扩张的病人开始应用内镜治疗。杨玉龙[26]认为,胆管结石及胆道系统肿瘤发生的共同之处在于胰液反流,解决胆胰反流是关键所在,通过EST,使胰液排出通畅,减少反流,降低恶性肿瘤及结石发生的风险。对于不愿接受预防性胆管切除手术的病人是一个很好的选择。
对于胆管扩张的PBM病人,公认标准的手术方式是胆囊切除术加肝外胆管切除术,进行胆胰分流以预防胰腺炎和胆囊及胆管恶性肿瘤的发生。
预后和随访
通常认为伴先天性胆道扩张的PBM病人预后好于不伴先天性胆道扩张的PBM病人。后者常因症状隐匿、延误治疗而出现恶变。对于无症状或症状轻微的不伴先天性胆道扩张的PBM病人,行常规超声筛查。若发现胆囊壁增厚等可能征象,应尽早行 MRCP检查。
CBD囊肿切除术后,需长期随访以监测并发症和癌变的发生。随访包括血生化肿瘤标志物(如CEA和CA19-9)和影像学检查(如腹部US和CT)等。
结 语
总之,PBM的临床特征通常不具特异性,常被其他胆胰疾病所掩盖,“治标不治本”的手术方式可能贻误病情并导致反复胰腺炎、胆管炎以及胆道系统癌变等严重后果。因此,早期诊断PBM是目前临床诊治的首要目标,临床医师需重视本病。影像学技术、内镜技术的发展及标准诊断流程的建立有助于提高诊断准确率。关于PBM致癌作用,目前已发现多步骤致癌过程。胆胰分流手术大幅降低胆道肿瘤的发生率,但仍有部分残留导管癌发生,其发生机制以及癌变的预防,可成为新的研究方向。

