碳酸钠溶液中滴入盐酸的图象探析
◇ 湖北 鲁方征
Na2CO3是一种典型的强碱二元弱酸盐,溶于水后由于水解溶液显碱性.向Na2CO3溶液中滴入盐酸,先发生反应全部转化为后,再发生反应:H2O+CO2↑,高考中常考查的图象有以下形式.
1 溶液的p H和盐酸体积图象
例1常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL相同浓度的Na2CO3溶液,滴定曲线如图1所示(饱和H2CO3溶液p H=5.6).回答下列问题:
(1)H2CO3的Ka2=________.
(2)b点溶液中离子浓度由大到小顺序为:________.
(3)c点处溶液中c(Na+)=________.
(4)a、c两点水电离的c(OH-)之比为______.

图1
分析(1)a点,c()≈c(OH-)=10-2.4水解平衡常数

(2)b点Na2CO3+HCl=Na HCO3+Na Cl,溶液显碱性,离子浓度由大到小顺序为:c(Na+)>c(Cl-)>c()>c(OH-)>c(H+)>c().
(3)c点溶液的p H=7,c(OH-)=c(H+),根据电荷守恒:

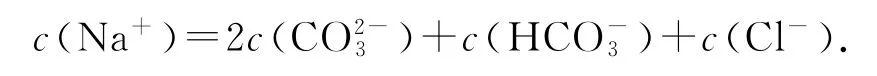
(4)a点溶液为碳酸钠,促进水的电离,水电离的c(OH-)=10-2.4mol·L-1,c点为中性溶液,对水的平衡无影响,水电离的c(OH-)=10-7mol·L-1,a、c两点水电离的c(OH-)之比为104.6.
2 溶液中含碳微粒物质的量分数和溶液的p H图象
例2常温下,在0.1 mol·L-1的10 mL Na2CO3溶液中逐滴加入0.1 mol·L-1盐酸,溶液中含碳微粒的物质的量分数变化如图2所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),回答下列问题:
(1)在0.1 mol·L-1Na2CO3溶液中,根据质子守恒,c(OH-)=________.
(2)常温下,水解常数Kh(CO23-)的数量级为________.
(3)当溶液呈中性时,溶液的总体积________(填“大于”“小于”或 “等于”)20 mL.

图2
分析(1)0.1 mol·L-1Na2CO3溶液中,由质子守恒可知,

(2)由图中信息可知,A点,则水解常数

A点对应的p H为11>p H>10,则10-4mol·L-1<c(OH-)<10-3mol·L-1,所以,水解常数的数量级为10-4.
(3)0.1 mol·L-1Na2CO3溶液中加入10 mL 0.1 mol·L-1HCl生成碳酸氢钠,此时溶液仍呈碱性,所以当溶液是中性时,溶液的总体积大于20 mL.
总之,往Na2CO3溶液中滴入盐酸,不管是哪一种曲线,都要明确反应的先后顺序,离子浓度大小关系则要用物料守恒、电荷守恒、质子守恒判断,电离常数或水解常数的计算则要找题干中的关键点,特别是酸分子和酸根离子浓度的数量关系.

